胰腺癌术后辅助治疗的昨天、今天和明天
 |
近年来随着各种诊疗技术的进步,癌症的治愈率和生存率较以往有了较大的改善,可是,有一种肿瘤仍被冠以“早期诊断率低、预后极差、远期生存率最低、在所有肿瘤中治愈率最低……”,它就是――胰腺癌。
作为消化道常见肿瘤之一,胰腺癌近年来的发病率不断上升,并且发病年龄逐渐趋于年轻化,引起了广泛关注。美国癌症学会(ACS)在2007年进行的一项统计表明,胰腺癌在美国癌症相关死亡原因中占第4位。胰腺癌起病隐匿,就诊时大部分患者已为晚期,首次诊断时50%以上已经有转移,30%为局部晚期,20%为局限性疾病,而且仅有10%可以接受根治性切除。胰腺癌的预后极差,转移性胰腺癌的中位生存期仅6个月,局部晚期者为9个月。胰腺癌患者在手术后仍有很高的复发率,即使接受根治手术者的生存期也仅为15~19个月,5年生存率约为20%。
为了降低胰腺癌术后复发风险,研究人员一直在积极探索更有效的综合治疗模式,其中术后放化疗和术后单纯辅助化疗是研究得最多的模式。下面与您一同回顾胰腺癌术后辅助治疗二十余年来的进展。
, 百拇医药
~1987年 GITSG研究
美国因此将放化疗作为胰腺癌术后标准治疗,但该研究存在明显缺陷,结果有待进一步验证
胰腺癌对化疗非常抗拒,在吉西他滨出现以前唯一公认有效的化疗药物是5-氟尿嘧啶(5-FU)。1985年,卡尔泽(Kalser)等公布的胃肠道肿瘤研究组(GITSG)研究,第一次表明了胰腺癌手术切除后辅助治疗的益处。美国14个研究中心参加了该研究,研究方案为静脉推注5-FU(500 mg/m2,每个放疗疗程开始后前3天)联合分割放疗(总量40 Gy,分2个疗程进行),并在同步放化疗结束后给予静脉推注5-FU(500 mg/m2,每周1次)维持治疗2年。21例患者接受辅助放化疗,22例仅予观察,两组的中位生存期分别为20和11个月,2年生存率分别为43%和18%(P<0.03)。
1987年,GITSG研究结果被更新,放化疗组增加入组了30人,最终结果与前期报告相似。因此美国将这一治疗方式作为胰腺癌术后的标准治疗。
, 百拇医药
然而,GITSG研究也存在明显缺陷:入组周期太长,最终入组病例数太少(8年仅仅入组了43例患者),结论缺乏说服力,质量控制较差,实际入选的患者仅仅来自2个癌症中心,24%的患者没有按研究限定时间开始辅助治疗,只有9%的患者接受了为时2年的化疗,32%的患者没有按规定放疗,这些都引起了质疑。此外,静脉推注5-FU维持治疗是否有必要也备受争议。因此,GITSG研究结果非常需要得到大规模前瞻性随机对照研究的验证。
1999年 EORTC研究
证实术后放化疗没有益处,欧洲因此并不推荐胰腺癌术后进行辅助放化疗
欧洲29个研究中心随后进行的欧洲癌症研究与治疗组织(EORTC)研究进一步观察了胰腺癌术后辅助放化疗的效果。该研究方案不同于GITSG研究,方案为5-FU持续静脉滴注联合分割放疗(总量40 Gy),但不再给予5-FU维持治疗,给药方式由静脉推注改为持续静脉滴注。
, http://www.100md.com
研究最初入组了114例胰头癌和93例壶腹癌患者,将其随机分入放化疗组(104例)和观察组(103例),两组的中位生存期分别为24.5和19.0个月,2年生存率分别为51%和41%,P=0.208。去除壶腹癌,进行胰头癌的亚组分析,放化疗组和观察组的中位生存期分别为17.1和12.6个月,2年生存率分别为37%和23%,P=0.099。欧洲因此并不推荐胰腺癌术后辅助放化疗。
EORTC研究的质量控制和患者依从性明显好于GITSG研究。但应该注意的是,由于该研究入组了相当数量的壶腹癌,导致真正的胰腺癌入组数量不太充分。亚组分析中,胰头癌同步放化疗组似乎有改善生存的趋势,但增加病例数能否显示有显著性差异尚不可知,这也成为一些同步放化疗支持者认为该研究存在潜在阳性结果的理由。尽管存在一些缺陷,但EORTC研究目前的结果显示同步放化疗不仅没有显著改善生存,而且也没有改变胰腺癌自然进程,因为治疗组和观察组分别有65%和66%患者最终复发,并且首次复发部位和远处转移部位也非常相似。
, http://www.100md.com
2001年 ESPAC-1研究
证实术后单纯化疗的益处,欧洲因此将单纯化疗作为胰腺癌术后标准治疗
2001年,《柳叶刀》(Lancet)公布了欧洲胰腺癌研究组1(ESPAC-1)研究的结果。该研究是11个国家66家研究中心共同开展的一项大规模前瞻性随机对照研究,共入组541例胰腺癌术后患者,进行三种随机分组。第一种随机分组既含同步放化疗又含化疗,285例患者按2×2交叉分析随机分为4组:同步放化疗组为静脉推注5-FU联合分割放疗(40 Gy),化疗组为静脉推注5-FU,联合组为同步放化疗后继续化疗,其余为观察组。第二种随机分组将另外68例患者分为放化疗组和观察组。剩余188例患者接受第三种随机分组,即分为化疗组和观察组。
对全部患者进行分析发现,同步放化疗组和非同步放化疗组的中位生存期无显著性差异(15.5对16.1个月,P=0.24),而化疗组相对于非化疗组的中位生存期则有显著性差异(19.7对14.0个月,P=0.0005)。
, 百拇医药
2004年的研究中,仅对第一种随机分组人群(289例)进行分析发现,非同步放化疗组无论是中位生存期还是2年生存率均优于同步放化疗组(17.9对15.9个月,P=0.05;41%对29%),而化疗组无论是中位生存期还是2年生存率均优于非化疗组(20.1对15.5个月,P=0.009;40%对30%)。
ESPAC-1研究是第一项证实胰腺癌术后单纯辅助化疗有益的大规模前瞻性随机对照研究。基于此,欧洲将单纯化疗作为胰腺癌术后标准治疗,同步放化疗则被认为有害无益。但该研究的放疗质量控制存在一定缺陷,一些研究中心缺乏先进的放疗设备,而且尽管大部分患者的放疗总剂量为40 Gy,但仍有些剂量达到60 Gy。虽然如此,该研究与EORTC研究结果一样,证实术后辅助同步放化疗不能改善胰腺癌患者生存。
2006年 RTOG 9704研究
进一步确认了与5-FU相比,吉西他滨在胰腺癌辅助治疗中的优势
, http://www.100md.com
由于胰腺癌术后5-FU同步放化疗的Ⅲ期临床研究结果不一致,研究人员开始探讨吉西他滨同步放化疗的疗效。1997年,已经有研究证实吉西他滨是胰腺癌的有效化疗药物,并有望取代5-FU成为新的标准化疗药物。
2006年美国临床肿瘤学会(ASCO)年会上公布的美国放射治疗肿瘤学协作组(RTOG)9704研究比较了5-FU和吉西他滨联合放疗在胰腺癌辅助治疗中的疗效。5-FU组为在5-FU同步放化疗前后分别5-FU静脉滴注3周和3个月。吉西他滨组为在5-FU同步放化疗前后分别静脉推注吉西他滨3周和3个月。共入组442例患者,对全组患者的分析显示两组生存无差异。但亚组分析显示,对于胰头癌患者(380例),吉西他滨组生存显著优于5-FU组(中位生存期为20.6对16.9个月;3年生存率为32%对21%,P=0.003)。
该研究确认了吉西他滨相对5-FU在胰腺癌辅助治疗中的优势,但并不能进一步证明副作用较大的同步放化疗能成为标准治疗模式,寻找更安全和副作用小的治疗模式成为继续探索的方向。
, http://www.100md.com
2007年~ CONKO-001研究
吉西他滨具有疗效优势,被接受为胰腺癌术后推荐辅助治疗
2007年厄特勒(Oettle)等公布了一项多中心Ⅲ期随机对照研究――CONKO-001研究(1998-2004年)的结果,该研究观察了吉西他滨6个月辅助化疗对胰腺癌的疗效。吉西他滨组179例,观察组175例。结果两组的无病生存(DFS)期分别为13.4个月和6.9个月(P<0.001),中位生存期分别为22.1个月和20.2个月(P=0.06),吉西他滨辅助化疗显示出明显的优势。
2008年ASCO会议上,CONKO-001更新后的数据显示,吉西他滨组和观察组的中位生存期分别为22.8个月和20.2个月,5年生存率分别为21%和9%,均有显著性差异。至此,吉西他滨辅助化疗已经被接受为胰腺癌术后推荐辅助治疗。
CONKO-001研究是第一项将吉西他滨与单纯观察组进行对比的大规模Ⅲ期随机研究,在RTOG 9704研究基础上进一步确认了吉西他滨在胰腺癌术后辅助治疗中的地位。
, http://www.100md.com
吉西他滨系列研究
吉西他滨单药逐渐成为胰腺癌术后辅助化疗的标准对照,多项研究对此进行了探讨
正是基于上述研究结果,越来越多的研究人员将单药吉西他滨辅助化疗作为胰腺癌术后辅助化疗的标准对照组。
2008年,日本研究者良富(Yoshitomi)报告了一项Ⅱ期研究的结果。研究将100例接受了根治手术的胰腺癌患者随机分为两组,一组给予吉西他滨1.0 g/m2,每周1次,连续3周,休息1周,另一组除了吉西他滨外还给予尿嘧啶/替加氟(UFT)200 mg/d,持续口服。中位随访21个月,联合组的1年和3年DFS率分别为50.0%和17.7%,单药吉西他滨组则分别为49.0%和21.6%,没有显著性差异。该研究表明,到目前为止,尚无任何联合辅助化疗方案疗效优于单药吉西他滨。
其他正在进行中的一系列研究也将吉西他滨单药辅助化疗作为胰腺癌术后辅助化疗的标准对照,如ESPAC-3、EORTC 40013-22012和日本胰腺癌辅助治疗研究组(JASPAC)-01研究等。
, 百拇医药
ESPAC-3研究将吉西他滨单药与5-FU直接进行了比较。研究将胰腺癌术后患者随机分为5-FU+亚叶酸钙组、吉西他滨单药组和对照组。其中吉西他滨组给药6个月。研究的主要终点为2年生存率,次要终点为毒性、生活质量和5年生存率。入组标准为经组织学确诊的初治患者,无恶性腹水,无肝、腹部其他器官、腹膜和腹外转移,未接受过新辅助化疗或其他辅助化疗。
EORTC 40013-22012研究是一项Ⅱ/Ⅲ期辅助治疗试验,最初比较的是吉西他滨联合同步放疗(50.4 Gy)组和对照组对胰十二指肠切除术后胰头癌患者的疗效,后根据2004年发表在《新英格兰医学杂志》(N Engl J Med)上的ESPAC研究结果将吉西他滨单药作为标准对照组。研究的主要终点是耐受性和总生存期,次要终点是DFS、复发部位、毒性和生活质量。入组标准是没有壶腹周围癌,先前未接受过化疗或放疗。
随着对胰腺癌辅助治疗研究的深入,相信今后会产生新的更有效的辅助化疗方案,而放疗在胰腺癌术后辅助治疗中的作用和地位也将在吉西他滨辅助化疗时代接受重新评估。
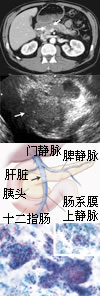
图1 轴位增强CT示胰腺头颈部的低密度团块(箭头)
图2 超声内镜检查示一个低回声团块,直径2.3 cm,位于胰头部
图3 胰腺与肠系膜上静脉、门静脉(易受胰腺癌侵犯)的解剖关系(箭头)
图4 穿刺获得的胰腺细胞学标本(巴氏染色),可见大量腺细胞形成,有典型癌细胞特征,即核增大、不规则和深染,核-质比例增加,旁边插图示伴黏蛋白的肿瘤细胞, http://www.100md.com