脑缺血大鼠γ-氨基丁酸和P物质对纹状体多巴胺代谢的调控作用
作者:李庆有 江德华 张瑞珠 张卫华
单位:300052天津市神经病学研究所神经化学研究室
关键词:脑缺血;多巴胺;P物质;γ-氨基丁酸
中华医学杂志931113 摘要 于纹状体内注射荷包丹碱(Bic)及黑质内注射P物质(SP)拮抗剂后结扎大鼠右侧大脑中动脉(MCA)造成局灶性脑缺血模型,采用放射免疫分析及高效液相色谱电化学检测方法对纹状体多巴胺(DA)的代谢进行观察。结果:纹状体内注射Bic 80nmol,黑质的SP水平无明显变化,纹状体的DA和高香草酸(HVA)变化亦不明显,而3-4二羟苯乙酸(DOPAC)的水平升高。若在给予Bic后结扎MCA,则黑质SP的含量明显升高,纹状体的DOPAC升高更为显著,而DA、HVA变化仍不明显,黑质内注射5nmol的SP拮抗剂,能够逆转上述Bic对纹状体DA、DOPAC及HVA的作用。表明纹状体GABA对DA代谢的调控主要是以黑质的SP为介导;GABA及SP调控纹状体DA及其代谢产物的作用在大脑中动脉闭塞引起纹状体缺血的状态下仍起作用。
, 百拇医药
近年来的实验业已证明,脑缺血导致多巴胺(DA)、γ-氨基丁酸(GABA)及P物质(SP)的代谢异常〔1,2〕,各递质间的调节失控,引起或加重神经组织结构破坏和功能障碍,因此,研究阐明缺血递质间的调控变化极为必要。正常情况下,GABA、DA、SP相互调控形成纹状体-黑质-纹状体在功能上的调节回路〔3〕。但三者间的调控在大脑中动脉闭塞引起纹状体缺血时是否还起作用?如何起作用?目前还知之甚少,本研究对此做了初步探讨。
材料与方法
1.脑缺血动物模型:雄性SD成年大鼠,体重250~350g。按Tamura等〔4〕及Bederson等〔5〕方法,结扎大鼠右侧大脑中动脉(MCAO),但手术步骤略有改变,经病理切片证实此方法可以造成大鼠颞区皮层及纹状体外三分之二区域组织坏死,此为缺血的中心区域,脑梗死发生率达100%。
, 百拇医药
2.药物注射:纹状体内注射荷包牡丹碱(Bicuculline,Bic)及黑质内注射SP拮抗剂〔D-Arg1,D-Phe5,D-Trp7,9,Leu11〕-SP。将大鼠麻醉,固定于立体定位仪上,根据Pellegrino鼠脑立体定位图谱,以坐标为L=3.5mm,A-P=1.6mm、D-V=5.5mm行右侧纹状体前外侧注射Bic 80nmol,以坐标为L=2.5mm、A-P=-3.2MM、D-V=8.5MM行右侧黑质注射SP拮抗剂5nmol,经验证上述注射部位均准确无误。注入药物均以生理盐水配制,洲入量为1μl,注入时间不得短于1分钟。注药对照组注入同容量的生理盐水。
3.标本选取:将大鼠断头处死后,迅速剖出鼠脑置于冰皿上,取右侧半球,自嗅结节前缘始作冠状切片,其厚度依次为1.5及2.0mm,在2.0mm厚脑片上取外2/3纹状体为测定标本。黑质区的标本自中脑大脑脚首端始作冠状切片,其厚度为1.6mm,然后在脑片上剖出所需黑质区域为测定标本。
, http://www.100md.com
4.标本处理:将所取标本称重,按1∶20(w/v)加入0.17mol/L过氯酸(PCA),在冰浴下超声粉碎制成匀浆,取20μl留测蛋白,余在4℃下离心(12000r/min)20分钟,取上清液250μl移至另一管中,再离心(4℃,12000r/min)10分钟,取上清液备高效液相色谱测定用。从标本处理至样品测定完毕全过程均在6小时内完成。测定SP的标本与上述步骤基本相同,但以1mol/L乙酸代替0.17mol/L PCA,此外,离心前还需经过加热过程,将提取的上清液贮存于-20℃待 。
5.高效液相色谱测定条件:采用Kim法〔6〕。流动相为:32mmol/L柠檬酸,1.25mmol/L Na2HPO4,0.1lmmol/L辛烷基磺酸钠,0.5mmol/L Na2EDTA,14%甲醇(V/V)。C18反相层析柱,室温下测定,流速1.2ml/mm,氧化电压+0.8V,检测器灵敏度5nA(AuFs).
6.SP放射免疫测定:参照Powell等〔7〕的方法略有改进。
, 百拇医药
结 果
1.于非缺血的正常状态,纹状体内注射Bic后黑质SP含量变化不明显,纹状体DA、高香草酸(HVA)的含量亦无明显变化,而3-4二羟苯乙酸(DOPAC)却明显高于对照组(P<0.05);而于缺血状态下,黑质SP含量明显高于对照组,纹状体的DA代谢产物DOPAC亦明显高于对照组(P<0.01),而DA及HVA的变化则不明显(表1)。
表1 不同状态下Bic对黑质SP、纹状体DA、DOPAC、HVA(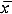 ±S)的作用 组别
±S)的作用 组别
SP
DA
DOPAC
HVA
, 百拇医药
(pmol/mg蛋白)
(nmol/mg蛋白)
(nmol/mg蛋白)
(nmol/mg蛋白)
对照组
8.0±2.0
24.2±5.2
2.8±0.9
2.6±1.0
(6)
(5)
(5)
, http://www.100md.com
(5)
Bic组
8.9±1.4
25.5±3.2
5.6±2.2
3.8±1.0
(8)
(8)
(8)
(8)
Bic
11.5±3.1*
, http://www.100md.com 27.3±4.1
7.0±2.7**
3.6±1.2
MCAO组
(7)
(7)
(7)
(7)
注:括号内为动物数;与对照组比较*P<0.05**P<0.01
2.事先向黑质内注射SP拮抗剂5nmol,则发现,DA及其酸性代谢产物均明显降低,DOPAC恢复至盐水注射对照组水平,DA达盐水注射对照组水平以下(表2)。从而清楚地表明,SP拮抗剂不仅能完全逆转Bic促进DA更新的作用,而且通过其自身拮抗SP受体的作用抑制DA在纹状体的释放。
, http://www.100md.com
表2 SP拮抗剂黑质内注射逆转Bic对纹状体DA、DOPAC、HVA(nmol/mg蛋白,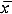 ±S)的作用 组别
±S)的作用 组别
DA
DOPAC
HVA
Bic+MCAO
27.3±4.1
7.0±2.7
3.4±1.2
(7)
(70
, http://www.100md.com
(70
黑质SP拮抗剂+
17.2±1.9
2.8±0.9
2.2±0.4
Bic+MCAO
(5)
(5)
(5)
注:括号内为动物数;两组比较▲P<0.001
讨 论
脑缺血后递质的代谢异常,导致神经元的损伤及神经功能障碍,越来越受到研究者的重视。我室以前的实验已初步证明了脑缺血后DA、GABA及SP等神经递质的代谢发生紊乱。本研究采用Bic纹状体内注射以阻断GABA对纹状体DA神经末梢以及对纹状体SP神经元的抑制作用,以及在纹状体注射Bic之前,黑质内注射SP拮抗阻断SP对黑质DA神经元的兴奋作用。结果表明,在非缺血条件下80nmol GABA拮抗剂Bic纹状体内注射并不改变黑质的SP水平,亦不改变纹状体的DA、HVA水平,但DA的代谢产物DOPAC却明显增高。若再给予Bic纹状体内注射后10分钟,结扎MCA造成实验动物的局灶性脑缺血,则结果发现,注入Bic后黑质的SP含量明显增加,纹状体的DA、DOPAC、HVA的变化规律与非缺血的结果基本相似。但DOPAC变化更为明显(P<0.01),从而说明纹状体局部应用Bic有促进局部DA氧化脱胺过程的作用,并由此推论在缺血状态下,GABA拮抗剂可通过其使黑质SP释放的增加,而使促进DA氧化脱胺过程的作用更为明显。结合我室在相同的条件下所发现的缺血后纹状体DA含量下降的同时,DOPAC明显增高,表明氧化脱胺过程加剧的现象,推断缺血时局部GABA升高,对缺血的纹状体是有利的〔8〕。若在Bic纹状体内注射前给予SP拮抗剂黑质内注射,则上述Bic所引起的DA、DOPAC、HVA的变化均被明显逆转,其逆转的程度甚至低于非缺血状态纹状体内注射Bic的水平以及对照组的水平。从而清楚地证明了纹状体内注射Bic使DA更新加快的作用,可完全被黑质内注射SP拮抗剂所逆转。由此可得出结论,GABA抑制DA代谢的作用机制之一就是通过抑制纹状体一黑质SP通路兴奋DA神经元的作用而实现的〔9〕。
, 百拇医药
表明GABA、SP调控纹状体DA及其代谢产物的作用机制在纹状体缺血状态下仍起作用。因此,GABA能药物及SP拮抗剂在脑缺血时可用以减轻过量释放的DA的细胞毒作用,它们是否能成为脑缺血的一种治疗药物尚有待于进一步验证。
参考文献
1 Globus MY,Busto R,Dietrich WD,et al.Effect of ischemia on the in vivo release of striatal dopamine,glulamate,and gamma aminobutyric acid studied by intracerebral microdialysis.J Neurochem,1988,51∶1455。
2 Dienel GA,Cruz NF,Rosenfeld SJ.Temporal profiles of proteins responsive to transient ischemia.J Neurochem,1985,44∶600
, 百拇医药
3 Reid MS,Herrera-Marschitz M,Hokfelt T,et al.Striatonigral GABA,dynorphin,substance P and neurokinin A modulation of nigrostriatal dopamine re-lease;evidence for direct regulatory mechanisms.Exp Brain Res,1990,82∶293
4 Tamura A,Graham DI,McCulloch J,et al.Focal cere-bral ischemia in the rat;I Description of technique and early neuropathological consequences following middle cerebral artery J Cereb Blood Folw Metab,1981,1∶53
5 Bederson JB,Pitts LH,Tsuji M,et al.Rat middle cerebral artery occlusion;evaluation of the model and develop-ment of a neurologic examination.Stroke,1986,17∶472
, http://www.100md.com
6 Kim C,Speisky MB,Kharouba SN.Rapid and sensitive method for measuring norepinephrine,dopamine,5-hydroxytryp-tamine and their major metabolites in rat brain by high-performance liquid chromatography.Differential effect of probenecid,haloperidol and yohimbine on the concentrations of biogenic amines and metabolites in various regions of rat brain.J Chromatog,1987,386∶25。
7 Rowell D,Leeman S,Tregear GW,et al.Radioimmunoassay for substance P.Nature〔New Biol〕,1973,241∶252。
, 百拇医药
8 Ikeda J,Nagashima G,Saito N,et al.Putative neuroexcitation in cerebral ischemia and brain injury.Stroke,1990,21〔11 Suppl〕∶III65。
9 Herrera-Marschitz M,Nylander I,Reid M,et al.Diffe-rent functional roles for substance P and dynorphine in the striatonigral pathways of the.In:Henzy JL.ed.Substance P and Neurokinins.New York:Springer-Verlag.1987,353∶355。
(收稿:1993-02-26 修回:1993-07-28), 百拇医药
单位:300052天津市神经病学研究所神经化学研究室
关键词:脑缺血;多巴胺;P物质;γ-氨基丁酸
中华医学杂志931113 摘要 于纹状体内注射荷包丹碱(Bic)及黑质内注射P物质(SP)拮抗剂后结扎大鼠右侧大脑中动脉(MCA)造成局灶性脑缺血模型,采用放射免疫分析及高效液相色谱电化学检测方法对纹状体多巴胺(DA)的代谢进行观察。结果:纹状体内注射Bic 80nmol,黑质的SP水平无明显变化,纹状体的DA和高香草酸(HVA)变化亦不明显,而3-4二羟苯乙酸(DOPAC)的水平升高。若在给予Bic后结扎MCA,则黑质SP的含量明显升高,纹状体的DOPAC升高更为显著,而DA、HVA变化仍不明显,黑质内注射5nmol的SP拮抗剂,能够逆转上述Bic对纹状体DA、DOPAC及HVA的作用。表明纹状体GABA对DA代谢的调控主要是以黑质的SP为介导;GABA及SP调控纹状体DA及其代谢产物的作用在大脑中动脉闭塞引起纹状体缺血的状态下仍起作用。
, 百拇医药
近年来的实验业已证明,脑缺血导致多巴胺(DA)、γ-氨基丁酸(GABA)及P物质(SP)的代谢异常〔1,2〕,各递质间的调节失控,引起或加重神经组织结构破坏和功能障碍,因此,研究阐明缺血递质间的调控变化极为必要。正常情况下,GABA、DA、SP相互调控形成纹状体-黑质-纹状体在功能上的调节回路〔3〕。但三者间的调控在大脑中动脉闭塞引起纹状体缺血时是否还起作用?如何起作用?目前还知之甚少,本研究对此做了初步探讨。
材料与方法
1.脑缺血动物模型:雄性SD成年大鼠,体重250~350g。按Tamura等〔4〕及Bederson等〔5〕方法,结扎大鼠右侧大脑中动脉(MCAO),但手术步骤略有改变,经病理切片证实此方法可以造成大鼠颞区皮层及纹状体外三分之二区域组织坏死,此为缺血的中心区域,脑梗死发生率达100%。
, 百拇医药
2.药物注射:纹状体内注射荷包牡丹碱(Bicuculline,Bic)及黑质内注射SP拮抗剂〔D-Arg1,D-Phe5,D-Trp7,9,Leu11〕-SP。将大鼠麻醉,固定于立体定位仪上,根据Pellegrino鼠脑立体定位图谱,以坐标为L=3.5mm,A-P=1.6mm、D-V=5.5mm行右侧纹状体前外侧注射Bic 80nmol,以坐标为L=2.5mm、A-P=-3.2MM、D-V=8.5MM行右侧黑质注射SP拮抗剂5nmol,经验证上述注射部位均准确无误。注入药物均以生理盐水配制,洲入量为1μl,注入时间不得短于1分钟。注药对照组注入同容量的生理盐水。
3.标本选取:将大鼠断头处死后,迅速剖出鼠脑置于冰皿上,取右侧半球,自嗅结节前缘始作冠状切片,其厚度依次为1.5及2.0mm,在2.0mm厚脑片上取外2/3纹状体为测定标本。黑质区的标本自中脑大脑脚首端始作冠状切片,其厚度为1.6mm,然后在脑片上剖出所需黑质区域为测定标本。
, http://www.100md.com
4.标本处理:将所取标本称重,按1∶20(w/v)加入0.17mol/L过氯酸(PCA),在冰浴下超声粉碎制成匀浆,取20μl留测蛋白,余在4℃下离心(12000r/min)20分钟,取上清液250μl移至另一管中,再离心(4℃,12000r/min)10分钟,取上清液备高效液相色谱测定用。从标本处理至样品测定完毕全过程均在6小时内完成。测定SP的标本与上述步骤基本相同,但以1mol/L乙酸代替0.17mol/L PCA,此外,离心前还需经过加热过程,将提取的上清液贮存于-20℃待 。
5.高效液相色谱测定条件:采用Kim法〔6〕。流动相为:32mmol/L柠檬酸,1.25mmol/L Na2HPO4,0.1lmmol/L辛烷基磺酸钠,0.5mmol/L Na2EDTA,14%甲醇(V/V)。C18反相层析柱,室温下测定,流速1.2ml/mm,氧化电压+0.8V,检测器灵敏度5nA(AuFs).
6.SP放射免疫测定:参照Powell等〔7〕的方法略有改进。
, 百拇医药
结 果
1.于非缺血的正常状态,纹状体内注射Bic后黑质SP含量变化不明显,纹状体DA、高香草酸(HVA)的含量亦无明显变化,而3-4二羟苯乙酸(DOPAC)却明显高于对照组(P<0.05);而于缺血状态下,黑质SP含量明显高于对照组,纹状体的DA代谢产物DOPAC亦明显高于对照组(P<0.01),而DA及HVA的变化则不明显(表1)。
表1 不同状态下Bic对黑质SP、纹状体DA、DOPAC、HVA(
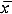 ±S)的作用 组别
±S)的作用 组别SP
DA
DOPAC
HVA
, 百拇医药
(pmol/mg蛋白)
(nmol/mg蛋白)
(nmol/mg蛋白)
(nmol/mg蛋白)
对照组
8.0±2.0
24.2±5.2
2.8±0.9
2.6±1.0
(6)
(5)
(5)
, http://www.100md.com
(5)
Bic组
8.9±1.4
25.5±3.2
5.6±2.2
3.8±1.0
(8)
(8)
(8)
(8)
Bic
11.5±3.1*
, http://www.100md.com 27.3±4.1
7.0±2.7**
3.6±1.2
MCAO组
(7)
(7)
(7)
(7)
注:括号内为动物数;与对照组比较*P<0.05**P<0.01
2.事先向黑质内注射SP拮抗剂5nmol,则发现,DA及其酸性代谢产物均明显降低,DOPAC恢复至盐水注射对照组水平,DA达盐水注射对照组水平以下(表2)。从而清楚地表明,SP拮抗剂不仅能完全逆转Bic促进DA更新的作用,而且通过其自身拮抗SP受体的作用抑制DA在纹状体的释放。
, http://www.100md.com
表2 SP拮抗剂黑质内注射逆转Bic对纹状体DA、DOPAC、HVA(nmol/mg蛋白,
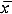 ±S)的作用 组别
±S)的作用 组别DA
DOPAC
HVA
Bic+MCAO
27.3±4.1
7.0±2.7
3.4±1.2
(7)
(70
, http://www.100md.com
(70
黑质SP拮抗剂+
17.2±1.9
2.8±0.9
2.2±0.4
Bic+MCAO
(5)
(5)
(5)
注:括号内为动物数;两组比较▲P<0.001
讨 论
脑缺血后递质的代谢异常,导致神经元的损伤及神经功能障碍,越来越受到研究者的重视。我室以前的实验已初步证明了脑缺血后DA、GABA及SP等神经递质的代谢发生紊乱。本研究采用Bic纹状体内注射以阻断GABA对纹状体DA神经末梢以及对纹状体SP神经元的抑制作用,以及在纹状体注射Bic之前,黑质内注射SP拮抗阻断SP对黑质DA神经元的兴奋作用。结果表明,在非缺血条件下80nmol GABA拮抗剂Bic纹状体内注射并不改变黑质的SP水平,亦不改变纹状体的DA、HVA水平,但DA的代谢产物DOPAC却明显增高。若再给予Bic纹状体内注射后10分钟,结扎MCA造成实验动物的局灶性脑缺血,则结果发现,注入Bic后黑质的SP含量明显增加,纹状体的DA、DOPAC、HVA的变化规律与非缺血的结果基本相似。但DOPAC变化更为明显(P<0.01),从而说明纹状体局部应用Bic有促进局部DA氧化脱胺过程的作用,并由此推论在缺血状态下,GABA拮抗剂可通过其使黑质SP释放的增加,而使促进DA氧化脱胺过程的作用更为明显。结合我室在相同的条件下所发现的缺血后纹状体DA含量下降的同时,DOPAC明显增高,表明氧化脱胺过程加剧的现象,推断缺血时局部GABA升高,对缺血的纹状体是有利的〔8〕。若在Bic纹状体内注射前给予SP拮抗剂黑质内注射,则上述Bic所引起的DA、DOPAC、HVA的变化均被明显逆转,其逆转的程度甚至低于非缺血状态纹状体内注射Bic的水平以及对照组的水平。从而清楚地证明了纹状体内注射Bic使DA更新加快的作用,可完全被黑质内注射SP拮抗剂所逆转。由此可得出结论,GABA抑制DA代谢的作用机制之一就是通过抑制纹状体一黑质SP通路兴奋DA神经元的作用而实现的〔9〕。
, 百拇医药
表明GABA、SP调控纹状体DA及其代谢产物的作用机制在纹状体缺血状态下仍起作用。因此,GABA能药物及SP拮抗剂在脑缺血时可用以减轻过量释放的DA的细胞毒作用,它们是否能成为脑缺血的一种治疗药物尚有待于进一步验证。
参考文献
1 Globus MY,Busto R,Dietrich WD,et al.Effect of ischemia on the in vivo release of striatal dopamine,glulamate,and gamma aminobutyric acid studied by intracerebral microdialysis.J Neurochem,1988,51∶1455。
2 Dienel GA,Cruz NF,Rosenfeld SJ.Temporal profiles of proteins responsive to transient ischemia.J Neurochem,1985,44∶600
, 百拇医药
3 Reid MS,Herrera-Marschitz M,Hokfelt T,et al.Striatonigral GABA,dynorphin,substance P and neurokinin A modulation of nigrostriatal dopamine re-lease;evidence for direct regulatory mechanisms.Exp Brain Res,1990,82∶293
4 Tamura A,Graham DI,McCulloch J,et al.Focal cere-bral ischemia in the rat;I Description of technique and early neuropathological consequences following middle cerebral artery J Cereb Blood Folw Metab,1981,1∶53
5 Bederson JB,Pitts LH,Tsuji M,et al.Rat middle cerebral artery occlusion;evaluation of the model and develop-ment of a neurologic examination.Stroke,1986,17∶472
, http://www.100md.com
6 Kim C,Speisky MB,Kharouba SN.Rapid and sensitive method for measuring norepinephrine,dopamine,5-hydroxytryp-tamine and their major metabolites in rat brain by high-performance liquid chromatography.Differential effect of probenecid,haloperidol and yohimbine on the concentrations of biogenic amines and metabolites in various regions of rat brain.J Chromatog,1987,386∶25。
7 Rowell D,Leeman S,Tregear GW,et al.Radioimmunoassay for substance P.Nature〔New Biol〕,1973,241∶252。
, 百拇医药
8 Ikeda J,Nagashima G,Saito N,et al.Putative neuroexcitation in cerebral ischemia and brain injury.Stroke,1990,21〔11 Suppl〕∶III65。
9 Herrera-Marschitz M,Nylander I,Reid M,et al.Diffe-rent functional roles for substance P and dynorphine in the striatonigral pathways of the.In:Henzy JL.ed.Substance P and Neurokinins.New York:Springer-Verlag.1987,353∶355。
(收稿:1993-02-26 修回:1993-07-28), 百拇医药