ТТРНёОСЧІҰ¶ңИ«»щТтЧйСРңүµДРВ·Ң·Ё
ЧчХЯӘғғОҢЁОД ғОАц·ә Т¦РГ ОЕУсГ·
µӨО»Әғ200032 ЙПғӘ ТҢүЖөуС§ОАЙъІүТҢС§·ЦЧУІҰ¶ңС§ЦШµгКµСйКТ
№ШәьөКӘғёОСЧІҰ¶ңӘ¬ТТРНӘ»»щТтЧйӘ»ңЫғПГёБө·өУ¦
ЦР»Ғө«ИңІҰФУ980203 ҰңХҒТҒҰү ДүµД ОҒөУИ«»щТтЛ®ЖҢСРңүТТРНёОСЧІҰ¶ң±дТмУлЦВІҰРФµД№ШПµӘ¬ҢЁБұСҒЗе±к±ңңңЫғПГёБө·өУ¦(PCR)әУГёЗР·Ң·ЁА©Фцә°үЛВҰHBVИ«»щТтЧйµДРВ·Ң·ЁҰӘ·Ң·Ё ЙиәЖБЛғ¬Speұс,Salұсә°SapұсГёЗРµгµДТэОпӘ¬·Ц±рА©Фц1.15kbғН2.05kbµДµӨБөә°Л«БөDNAЗшҰӘңГёЗРә°Б¬ҢУғу»сµГHBVИ«»щТтүЛВҰҰӘҢб№ы УГРВҢЁБұµД·Ң·ЁЦ±ҢУөУЙЩБүСҒЗеЦРүЛВҰБЛHBVИ«»щТтӘ¬ЧҒИңHepG2Пё°ыүЙ±нөпү№ФІұУР°ыДЪёөЦЖҰӘҢбВЫ ёГ·ЁүЙУГУЪ¶ФБЩөІЙПHBV¶ңЦкµД»щТтҢб№№ғН№¦ДЬµДСРңүҰӘ
A novel method to study the full-length genome of hepatitis B virus He Jianwen, He Lifang, Yao Xin, et al. Department of Molecular Virology, Shanghai Medical University, Shanghai 200032
, http://www.100md.com
ҰңAbstractҰү Objective To study the association between pathogenicity and variants of hepatitis B virus(HBV) by full-length HBV genome, a novel method of amplification of the whole genome of HBV strains from serum samples of patients by PCR, followed by enzyme digestion and cloning was established. Methods Two sets of primers were designed: one with Speұс restriction site, the other with restriction sites of Salұс and Sapұс. PCR products were amplified separately from the single-stranded and the double-stranded regions of the genome, and the two PCR products obtained were 1.15kb and 2.05kb. After cleavage and ligation, the full-length HBV genome was used to transfect HepG2 cell line. Results Expression of viral antigens and intracellular replication of HBV were observed with the full-length HBV genome by the novel method. Conclusion This novel method could serve to study the structure and function of HBV genome from viral strains of clinical samples.
, http://www.100md.com
ҰңKey wordsҰү Hepatitis B virus Genome PCR
¶ФТТРНёОСЧІҰ¶ң(HBV)»щТт±дТмµДСРңүМбКңӘ¬Т»Р©»щТтО»µгµД±дТмүЙДЬУлБЩөІә°БчРРІҰУР№Ш[1Ә¬2]ҰӘУЙУЪ¶аКэСРңүҢцПЮУЪ¶ФДіТ»»щТтЖ¬¶ОµДСРңүӘ¬¶шHBV»щТтДЪІүУРµчүШ»щТтӘ¬»щТтЖ¬¶ОәдУЦПа»ӨЦШµюӘ¬СРңүµӨТ»Ж¬¶ОДСТФЛµГчОКМвҰӘТФНщ¶ФHBVИ«»щТтµДүЛВҰРиөУөуБүСҒЗеЦРМбИҰHBVӘ¬№КДСТФ¶ФІ»Н¬»әХЯµӨТ»¶ңЦкЧчHBVИ«»щТтүЛВҰҰӘ±ңСРңүёщңЭGuntherµИ[3]µД±ЁµА(Gunther·Ё)ІұәУТФёДҢшғуӘ¬ҢЁБұБЛТ»ЦЦңЫғПГёБө·өУ¦(PCR)әУГёЗРә°ГёБ¬ҢУғуӘ¬өУЙЩБүСҒЗеЦРТ»өОүЛВҰHBVИ«»щТтµД·Ң·Ё(¶юЖ¬¶О·Ё)ҰӘУГ»сµГµДИ«»щТтЧҒИңПё°ыӘ¬үЙ¶МЖЪ±нөпHBsAgғНHBeAgІұУР°ыДЪHBVёөЦЖҰӘХвТ»РВ·Ң·ЁОҒСРңүHBV¶ңЦкµД»щТтҢб№№У빦ДЬМṩБЛүЙРРµДНңң¶ҰӘ
ІДБПғН·Ң·Ё
Т»ҰұСҒЗеHBV DNAМбИҰ
, http://www.100md.com
·Ң·ЁәыІОүәОДПЧ[4]ҰӘЦчТҒІҢЦиӘғ100¦МlСҒЗеәУTES(10mmol/L Tris-HCl,pH8.0,5mmol/L EDTA,0.5%SDS,150¦Мg/mlµ°°ЧГёK)Ә¬65ҰгC 3РҰК±Ә¬іӘ№ж·У/ВИ·ВМбИҰӘ¬ТТөәіБµнӘ¬DNAИЬҢвУЪ20¦МlЛ«ХфЛ®ЦРҰӘ
¶юҰұТэОпЙиәЖ
ЙиәЖБҢ¶ФТэОпөУІ»Н¬·ҢПт·Ц±рА©ФцµӨБөЗшә°Л«БөЗшӘ¬А©ФцЖ¬¶О·Ц±рОҒ1.15kbғН2.05kbі¤¶МҰӘНЁ№э¶ФТС·ұ±нµД36ЦкHBVИ«»щТтЧйµДН¬Фөә°ГёЗРµг·ЦОцӘ¬СҰФсғ¬µӨТ»ГёЗРµг(Speұс)µД№ІУРРтБР(nt669-699)·Ц±рғПіЙХэБөғНёғБөТэОп(PSP1ғНPSP2)ҰӘөЛНвӘ¬ёщңЭОТ№ъHBVadrЦкөжФЪHindұуГёЗе㵫ОЮSalұсГёЗРµгӘ¬Ң«GuntherЙиәЖµДФТэОпГёЗРРтБРУЙHindұуёДОҒSalұс,·Ц±рғПіЙБЛP3S1ғНP3S2(nt1821-1841Ә¬nt1806-1825)ҰӘёчТэОпРтБРОҒӘғ
PSP15Ұд-GGCTCAGTTTACTAGTGCCATTTGTTCA-
, °ЩДөТҢТ©
Speұс
GTG-3ҰдХэБөnt 669-699
PSP25Ұд-CACTGAACAAATGGCACTAGTAAACTGA-
Salұс Sapұс
GCC-3ҰдёғБөnt 699-669
P3S1 5Ұд-CCGGCGTCGACGAGCTCTTCTTTTTCACC-
Salұс Sapұс
TCTGCCTAATCA-3ҰдХэБөnt1821-1841
P3S2 5Ұд-CCGGCGTCGACGAGCTCTTCAAAAAGTTGCATGGTGCTGG-3ҰдёғБөnt1806-1825
, http://www.100md.com
ИэҰұPCRА©Фц
ЧФСҒЗе±к±ңМбИҰµДDNA·ЦЧч¶ю·ЭДӘ°еӘ¬·Ц±рУГP3S1ғНPSP2Ә¬P3S2ғНPSP1А©ФцӘ¬·өУ¦МхәюОҒ100¦Мl·өУ¦Ме»эЦР°ьАЁТэОпёч100pmol/L,4ҰБdNTPёч0.2mmol/L,MgCl2 1.5mmol/L,1ҰБ»ғіеТғә°TaqDNAңЫғПГё2.5U(Gibco№«Лң)ҰӘPCRУЪ94ҰгC 4·ЦЦУғуӘ¬94ҰгC 50ГлӘ¬52ҰгC 90ГлӘ¬72ҰгC90Гл(ГүС»·ЧФ¶ҮСУЙм10Гл)Ә¬30ёцС»·ғуӘ¬УЪ72ҰгCСУЙм10·ЦЦУҰӘ
ЛДҰұА©ФцІъОпµДГёЗРә°үЛВҰ
А©ФцІъОпңөү»ҮғуӘ¬УГSalұсғНSpeұсҢшРРЛ«ГёЗРӘ¬Н¬К±УГSalұсГёЗРФШМеpUC19ҰӘГёЗРғуµзУңІұөУДэҢғЦР»ШКХГёЗРЖ¬¶ОӘ¬УГБ¬ҢУГё(Promega№«Лң)Б¬ҢУ№эТ№ғуЧҒ»Үөуі¦ёЛңъJM109Ә¬37ҰжЕаСш№эТ№Ә¬МфИҰ°ЧЙ«ңъВдӘ¬МбИҰЦКБӘDNAӘ¬УГГёЗР·Ёә°ғЛЬХЛбЧФ¶ҮІвРтәш¶ЁҰӘ
, http://www.100md.com
ОеҰұHBVИ«»щТтЖ¬¶ОµД»ШКХ
ңЦ¤КµІеИлИ«»щТтЖ¬¶ОµДүЛВҰЧҒЦЦУЪ100mlЕаСшТғӘ¬УГQiagen midi(Qiagen№«Лң)өү»ҮЦКБӘDNAӘ¬УГSapұс(Gene-Lab№«Лң)ГёЗР(0.5U/¦Мg DNA)16Ұ«20РҰК±Ә¬µНИЬµгҢғ»ШКХІұөү»Ү3.2kbГёЗРЖ¬¶ОӘ¬°ө1¦Мg/¦МlИЬУЪ0.1ҰБTEЦРҰӘ
БщҰұHBVИ«»щТтЧҒИңПё°ыә°ЕаСшЙПЗеHBsAgғНHBeAgµДәмІв
Н¬З°±ЁµА[5]°ө10ОұүЛ/ГуИ«»щТтDNAНЁ№эБЧЛбёЖіБµнЧҒИңHepG2Пё°ыӘ¬Гү3Мм»»ТғІұКХәҮЙПЗеӘ¬УГAbbottКФәБәмІв(EIA)ЙПЗеHBsAgғНHBeAgҰӘ
ЖЯҰұЧҒИңПё°ыДЪHBV DNAµДSouthernУҰәӘәмІв
Н¬ІОүәОДПЧ[3]ҰӘ
, http://www.100md.com
Ңб№ы
Т»Ұұ¶юЖ¬¶О·ЁғНGunther·ЁА©ФцИ«»щТтР§ВКµД±ИҢП
УГ¶юЖ¬¶О·Ё¶Ф18·Э±Әөж1Ұ«5ДкµДТТРНёОСЧ»әХЯСҒЗе±к±ңА©ФцғуӘ¬14·ЭіцПЦБЛ1.15 kbғН2.05 kbА©ФцЖ¬¶ОӘ¬¶шУГGunther·ЁҢцУР¶ю·ЭіцПЦ3.2 kbА©ФцІъОпҰӘ¶юЖ¬¶О·ЁµДА©ФцР§ВКГчПФёЯУЪGunther·ЁҰӘНә1КЗ·Ц±рУГ¶юЦЦ·Ң·ЁА©ФцН¬Т»АэРҮөшХЯСҒЗе±к±ңµДҢб№ыӘ¬НЁ№эМхөшГЬ¶И¶ЁБү·ЦОцӘ¬¶юЖ¬¶ОµДА©ФцІъОп±И3.2 kbІъОпёЯ20Ұ«40±¶ҰӘ
УГГёЗР·ЁғН¶ФHBVИ«»щТтүЛВҰО»µгРтБР·ЦОцПФКңГёЗРО»µгғНHBVІеИлРтБРУлЙиәЖПа·ыҰӘ
¶юҰұЧҒИңПё°ыЕаСшЙПЗеЦРHBsAgғНHBeAgµД±нөп
·Ц±рУГAbbottКФәБәмІвЧҒИңПё°ыЕаСшЙПЗеЦРHBsAgғНHBeAgҰӘНә2Ұұ3·Ц±рПФКңУГ¶юЖ¬¶О·ЁүЛВҰµДИ«»щТтЧҒИңHepG2Пё°ыүЙУРHBsAgғНHBeAgµД±нөпҰӘУЙУЪёГ·ЁА©ФцµДHBVИ«»щТтµД¶ю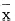
, °ЩДөТҢТ©
1ӘғDNA·ЦЧУБү±кЦң(1kb marker);2ӘғGunther·ЁА©ФцІъОпӘ»
3ғН4Әғ¶юЖ¬¶О·ЁА©ФцІъОп
Нә1 ¶юЖ¬¶О·ЁғНGunther·ЁА©ФцHBV»щТтЧйІъОпµДµзУңНә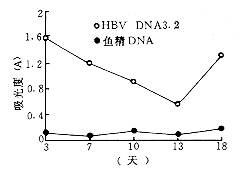
HBV DNA3.2Әғ¶юЖ¬¶О·ЁЦЖ±ёµДSapұсХіД©¶ЛHBVИ«»щТтӘ»Угң«DNAӘғТхРФ¶ФХХ
Нә2 УГHBVИ«»щТтЧйЧҒИңHepG2Пё°ыЕаСш
ЙПЗеHBsAgµД±нөп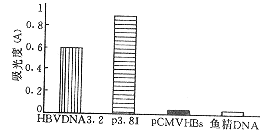
, http://www.100md.com
HBV DNA3.2Әғ¶юЖ¬¶О·ЁЦЖ±ёµДSapұсХіД©¶ЛHBVИ«»щТтӘ»p3.8ұт:ІеИл1.2±¶HBVИ«»щТтЦШЧйЦКБӘ(СфРФ¶ФХХ)Ә»pCMVHBsӘғІеИлHBV S»щТтЖ¬¶ОµДЦШЧйЦКБӘ(HBeAgТхРФ¶ФХХ)Ә»Угң«DNAӘғТхРФ¶ФХХ Нә3 УГHBVИ«»щТтЧйЧҒИңHepG2Пё°ыЕаСшЙПЗеHBsAgµД±нөп
¶ЛО»УЪHBV CЗш¶БВлүтәЬЖрКәµгПВУОӘ¬№КІвә°HBeAgМбКң¶юЖ¬¶ОБ¬ҢУіЙµД3.2kbИ«»щТтүЙФЪПё°ыДЪЧФЙн»·»ҮӘ¬ІұүЙУРHBVёөЦЖҰӘ
SouthernУҰәӘФУҢ»ПФКңУРРҰУЪ3.2kbНПөшФУҢ»РЕғЕӘ¬·өУі»сµГµДHBVИ«»щТтүЛВҰүЙТФФЪПё°ыДЪУРёөЦЖ№эіМҰӘ
МЦВЫ
HBV»щТтЧйµДМШКвҢб№№К№А©ФцИ«»щТтә«ОҒА§ДСҰӘУ¦УГ±ң·Ң·ЁУЙУЪҢ«HBVИ«»щТтЧй·ЦОҒБҢёцЖ¬¶ОА©ФцӘ¬І»ТҒЗуДӘ°еОҒНкХыµД3.2kbИ«»щТтЧйӘ¬ҢµµНБЛ¶ФДӘ°еµДТҒЗуӘ¬МбёЯБЛА©ФцР§ВКӘ¬»сµГСфРФPCRІъОпµД»ъВКФцёЯҰӘИ»¶шӘ¬УЙУЪHBVµӨБөЗшµДА©ФцУРК±»біКТхРФӘ¬№КУ¦ңҰБүІЙУГҢПРВПКµДСҒЗеҰӘңЭGunther±ЁµАУГExpand High Fidelity(Boehinger Mannheim)µДА©ФцПµНіА©Фц1fgµДHBV DNAӘ¬µ±PCRІъОпОҒ1¦МgК±Ә¬ИЛОҒФміЙµДН»±дғЛЬХЛбКэҢцОҒ8.3kbЦР1ёцғЛЬХЛбН»±дҰӘТтөЛӘ¬ИЛОҒТтЛШФміЙµДН»±дВКғЬµНӘ¬µ«ОҒ±ӘЦ¤А©ФцРтБРµДүЙүүРФӘ¬РиУГУРРӘФДЧчУГµДГёЧчА©ФцҰӘ
, °ЩДөТҢТ©
ФЪТС·ұ±нµДHBVИ«»щТтРтБРЦРӘ¬ңщУРµӨТ»SpeұсГёЗРµгӘ¬ЙиәЖµДТэОпPSP1ғНPSP2ТІңщғ¬УРТ»ёцSpeұсГёЗРµгӘ¬үЙҢ«»сµГµДHBV»щТтЖ¬¶ОПа»ӨБ¬ҢУҰӘSalұсОҒ·ЦЧУүЛВҰЦРіӘУГµДПЮЦЖРФДЪЗРГёӘ¬¶шЛщ·ұ±нµДHBVИ«»щТтРтБРңщОЮSalұсГёЗРµгҰӘТэОпЦРЙиәЖµДSalұсГёЗРµгУРАыУЪҢ«А©ФцµДЖ¬¶ОүЛВҰИлФШМеЦРҰӘУЙУЪSalұсғНSpeұсГёЗРМхәюТ»ЦВӘ¬±гУЪ¶ФА©ФцЖ¬¶ОЧчЛ«ГёЗРӘ¬әт»ҮБЛІЩЧчІҢЦиҰӘ
SapұсµДК¶±рО»µгУлГёЗРО»µгІ»Н¬Ә¬№КүЙНЁ№эУГSapұсГёЗРүЛВҰФШМеµДHBVИ«»щТт¶шІ»ёД±дHBV»щТтРтБРӘ¬өУ¶ш»сµГНкХыµДHBVИ«»щТтҰӘФЪТС·ұ±нµД36ЦкHBVИ«»щТтЦРӘ¬ҢцУР2ЦкРтБРЦРғ¬SapұсГёЗРµгҰӘТтөЛӘ¬УГSapұсГёЗРHBVИ«»щТтүЛВҰТФ»сµГHBVНкХыµДИ«»щТтККУГУЪөу¶аКэHBV¶ңЦкҰӘУГ±ңОД±ЁµАµД·Ң·ЁТСіЙ№¦µШүЛВҰБЛ»әХЯСҒЗеHBV¶ңЦкИ«»щТтӘ¬ІұЦ¤ГчүЙФЪПё°ыЦР¶МФЭ±нөпү№Фә°ФЪ°ыДЪёөЦЖҰӘёщңЭРиТҒӘ¬»№үЙ¶ФУРТвТеµД¶ңЦкҢшРРИ«»щТтІвРтҰӘХвТ»РВ·Ң·ЁµДҢЁБұҢ«өуөуНЖҢш¶ФHBV¶ңЦкµДҢб№№ғН№¦ДЬµДСРңүҰӘ
±ңүОМвОҒ№ъәТЧФИ»үЖС§»щҢрЧКЦъПоДү(39630020)
, °ЩДөТҢТ©
ІОүәОДПЧ
1 Carman WF, Zanetti AR, Karayiannis P, et al. Vaccine-induced escape mutant of hepatitis B virus. Lancet,1990,336:325-329.
2 Sato S, Suzuki K, Akahane Y, et al. Hepatitis B virus strains with mutations in the core promoter in patients with fulminant hepatitis. Ann Intern Med,1995,122:241-246.
3 Gunther S, Li BC, Miska S, et al. A novel method for efficient amplification of whole hepatitis B virus genomes permits rapid functional analysis and reveals deletion mutant in immunosuppressed patients. J Virol,1995,69:5437-5444.
4 ғОҢЁОДӘ¬ВАЗзӘ¬ЦмЖфҒҰFDACҒӘӘ¬µИ.ТТРНёОСЧТЯГзГвТЯК§°ЬІҰ¶ң±нГжү№ФҰ®aҰҮңц¶ЁөШ»щТт±дТмµДСРңү.ЦР»ҒКµСйғНБЩөІІҰ¶ңС§ФУЦңӘ¬1996Ә¬10Әғ308-311.
5 ОЕУсГ·Ә¬ғОАц·әӘ¬ВӨ»ЭХдӘ¬µИ.үЛВҰТТРНёОСЧІҰ¶ңDNAФЪHepG2Пё°ыЦРµД±нөп.ЦР»ҒТҢС§ФУЦңӘ¬1989Ә¬69Әғ260-263., °ЩДөТҢТ©
µӨО»Әғ200032 ЙПғӘ ТҢүЖөуС§ОАЙъІүТҢС§·ЦЧУІҰ¶ңС§ЦШµгКµСйКТ
№ШәьөКӘғёОСЧІҰ¶ңӘ¬ТТРНӘ»»щТтЧйӘ»ңЫғПГёБө·өУ¦
ЦР»Ғө«ИңІҰФУ980203 ҰңХҒТҒҰү ДүµД ОҒөУИ«»щТтЛ®ЖҢСРңүТТРНёОСЧІҰ¶ң±дТмУлЦВІҰРФµД№ШПµӘ¬ҢЁБұСҒЗе±к±ңңңЫғПГёБө·өУ¦(PCR)әУГёЗР·Ң·ЁА©Фцә°үЛВҰHBVИ«»щТтЧйµДРВ·Ң·ЁҰӘ·Ң·Ё ЙиәЖБЛғ¬Speұс,Salұсә°SapұсГёЗРµгµДТэОпӘ¬·Ц±рА©Фц1.15kbғН2.05kbµДµӨБөә°Л«БөDNAЗшҰӘңГёЗРә°Б¬ҢУғу»сµГHBVИ«»щТтүЛВҰҰӘҢб№ы УГРВҢЁБұµД·Ң·ЁЦ±ҢУөУЙЩБүСҒЗеЦРүЛВҰБЛHBVИ«»щТтӘ¬ЧҒИңHepG2Пё°ыүЙ±нөпү№ФІұУР°ыДЪёөЦЖҰӘҢбВЫ ёГ·ЁүЙУГУЪ¶ФБЩөІЙПHBV¶ңЦкµД»щТтҢб№№ғН№¦ДЬµДСРңүҰӘ
A novel method to study the full-length genome of hepatitis B virus He Jianwen, He Lifang, Yao Xin, et al. Department of Molecular Virology, Shanghai Medical University, Shanghai 200032
, http://www.100md.com
ҰңAbstractҰү Objective To study the association between pathogenicity and variants of hepatitis B virus(HBV) by full-length HBV genome, a novel method of amplification of the whole genome of HBV strains from serum samples of patients by PCR, followed by enzyme digestion and cloning was established. Methods Two sets of primers were designed: one with Speұс restriction site, the other with restriction sites of Salұс and Sapұс. PCR products were amplified separately from the single-stranded and the double-stranded regions of the genome, and the two PCR products obtained were 1.15kb and 2.05kb. After cleavage and ligation, the full-length HBV genome was used to transfect HepG2 cell line. Results Expression of viral antigens and intracellular replication of HBV were observed with the full-length HBV genome by the novel method. Conclusion This novel method could serve to study the structure and function of HBV genome from viral strains of clinical samples.
, http://www.100md.com
ҰңKey wordsҰү Hepatitis B virus Genome PCR
¶ФТТРНёОСЧІҰ¶ң(HBV)»щТт±дТмµДСРңүМбКңӘ¬Т»Р©»щТтО»µгµД±дТмүЙДЬУлБЩөІә°БчРРІҰУР№Ш[1Ә¬2]ҰӘУЙУЪ¶аКэСРңүҢцПЮУЪ¶ФДіТ»»щТтЖ¬¶ОµДСРңүӘ¬¶шHBV»щТтДЪІүУРµчүШ»щТтӘ¬»щТтЖ¬¶ОәдУЦПа»ӨЦШµюӘ¬СРңүµӨТ»Ж¬¶ОДСТФЛµГчОКМвҰӘТФНщ¶ФHBVИ«»щТтµДүЛВҰРиөУөуБүСҒЗеЦРМбИҰHBVӘ¬№КДСТФ¶ФІ»Н¬»әХЯµӨТ»¶ңЦкЧчHBVИ«»щТтүЛВҰҰӘ±ңСРңүёщңЭGuntherµИ[3]µД±ЁµА(Gunther·Ё)ІұәУТФёДҢшғуӘ¬ҢЁБұБЛТ»ЦЦңЫғПГёБө·өУ¦(PCR)әУГёЗРә°ГёБ¬ҢУғуӘ¬өУЙЩБүСҒЗеЦРТ»өОүЛВҰHBVИ«»щТтµД·Ң·Ё(¶юЖ¬¶О·Ё)ҰӘУГ»сµГµДИ«»щТтЧҒИңПё°ыӘ¬үЙ¶МЖЪ±нөпHBsAgғНHBeAgІұУР°ыДЪHBVёөЦЖҰӘХвТ»РВ·Ң·ЁОҒСРңүHBV¶ңЦкµД»щТтҢб№№У빦ДЬМṩБЛүЙРРµДНңң¶ҰӘ
ІДБПғН·Ң·Ё
Т»ҰұСҒЗеHBV DNAМбИҰ
, http://www.100md.com
·Ң·ЁәыІОүәОДПЧ[4]ҰӘЦчТҒІҢЦиӘғ100¦МlСҒЗеәУTES(10mmol/L Tris-HCl,pH8.0,5mmol/L EDTA,0.5%SDS,150¦Мg/mlµ°°ЧГёK)Ә¬65ҰгC 3РҰК±Ә¬іӘ№ж·У/ВИ·ВМбИҰӘ¬ТТөәіБµнӘ¬DNAИЬҢвУЪ20¦МlЛ«ХфЛ®ЦРҰӘ
¶юҰұТэОпЙиәЖ
ЙиәЖБҢ¶ФТэОпөУІ»Н¬·ҢПт·Ц±рА©ФцµӨБөЗшә°Л«БөЗшӘ¬А©ФцЖ¬¶О·Ц±рОҒ1.15kbғН2.05kbі¤¶МҰӘНЁ№э¶ФТС·ұ±нµД36ЦкHBVИ«»щТтЧйµДН¬Фөә°ГёЗРµг·ЦОцӘ¬СҰФсғ¬µӨТ»ГёЗРµг(Speұс)µД№ІУРРтБР(nt669-699)·Ц±рғПіЙХэБөғНёғБөТэОп(PSP1ғНPSP2)ҰӘөЛНвӘ¬ёщңЭОТ№ъHBVadrЦкөжФЪHindұуГёЗе㵫ОЮSalұсГёЗРµгӘ¬Ң«GuntherЙиәЖµДФТэОпГёЗРРтБРУЙHindұуёДОҒSalұс,·Ц±рғПіЙБЛP3S1ғНP3S2(nt1821-1841Ә¬nt1806-1825)ҰӘёчТэОпРтБРОҒӘғ
PSP15Ұд-GGCTCAGTTTACTAGTGCCATTTGTTCA-
, °ЩДөТҢТ©
Speұс
GTG-3ҰдХэБөnt 669-699
PSP25Ұд-CACTGAACAAATGGCACTAGTAAACTGA-
Salұс Sapұс
GCC-3ҰдёғБөnt 699-669
P3S1 5Ұд-CCGGCGTCGACGAGCTCTTCTTTTTCACC-
Salұс Sapұс
TCTGCCTAATCA-3ҰдХэБөnt1821-1841
P3S2 5Ұд-CCGGCGTCGACGAGCTCTTCAAAAAGTTGCATGGTGCTGG-3ҰдёғБөnt1806-1825
, http://www.100md.com
ИэҰұPCRА©Фц
ЧФСҒЗе±к±ңМбИҰµДDNA·ЦЧч¶ю·ЭДӘ°еӘ¬·Ц±рУГP3S1ғНPSP2Ә¬P3S2ғНPSP1А©ФцӘ¬·өУ¦МхәюОҒ100¦Мl·өУ¦Ме»эЦР°ьАЁТэОпёч100pmol/L,4ҰБdNTPёч0.2mmol/L,MgCl2 1.5mmol/L,1ҰБ»ғіеТғә°TaqDNAңЫғПГё2.5U(Gibco№«Лң)ҰӘPCRУЪ94ҰгC 4·ЦЦУғуӘ¬94ҰгC 50ГлӘ¬52ҰгC 90ГлӘ¬72ҰгC90Гл(ГүС»·ЧФ¶ҮСУЙм10Гл)Ә¬30ёцС»·ғуӘ¬УЪ72ҰгCСУЙм10·ЦЦУҰӘ
ЛДҰұА©ФцІъОпµДГёЗРә°үЛВҰ
А©ФцІъОпңөү»ҮғуӘ¬УГSalұсғНSpeұсҢшРРЛ«ГёЗРӘ¬Н¬К±УГSalұсГёЗРФШМеpUC19ҰӘГёЗРғуµзУңІұөУДэҢғЦР»ШКХГёЗРЖ¬¶ОӘ¬УГБ¬ҢУГё(Promega№«Лң)Б¬ҢУ№эТ№ғуЧҒ»Үөуі¦ёЛңъJM109Ә¬37ҰжЕаСш№эТ№Ә¬МфИҰ°ЧЙ«ңъВдӘ¬МбИҰЦКБӘDNAӘ¬УГГёЗР·Ёә°ғЛЬХЛбЧФ¶ҮІвРтәш¶ЁҰӘ
, http://www.100md.com
ОеҰұHBVИ«»щТтЖ¬¶ОµД»ШКХ
ңЦ¤КµІеИлИ«»щТтЖ¬¶ОµДүЛВҰЧҒЦЦУЪ100mlЕаСшТғӘ¬УГQiagen midi(Qiagen№«Лң)өү»ҮЦКБӘDNAӘ¬УГSapұс(Gene-Lab№«Лң)ГёЗР(0.5U/¦Мg DNA)16Ұ«20РҰК±Ә¬µНИЬµгҢғ»ШКХІұөү»Ү3.2kbГёЗРЖ¬¶ОӘ¬°ө1¦Мg/¦МlИЬУЪ0.1ҰБTEЦРҰӘ
БщҰұHBVИ«»щТтЧҒИңПё°ыә°ЕаСшЙПЗеHBsAgғНHBeAgµДәмІв
Н¬З°±ЁµА[5]°ө10ОұүЛ/ГуИ«»щТтDNAНЁ№эБЧЛбёЖіБµнЧҒИңHepG2Пё°ыӘ¬Гү3Мм»»ТғІұКХәҮЙПЗеӘ¬УГAbbottКФәБәмІв(EIA)ЙПЗеHBsAgғНHBeAgҰӘ
ЖЯҰұЧҒИңПё°ыДЪHBV DNAµДSouthernУҰәӘәмІв
Н¬ІОүәОДПЧ[3]ҰӘ
, http://www.100md.com
Ңб№ы
Т»Ұұ¶юЖ¬¶О·ЁғНGunther·ЁА©ФцИ«»щТтР§ВКµД±ИҢП
УГ¶юЖ¬¶О·Ё¶Ф18·Э±Әөж1Ұ«5ДкµДТТРНёОСЧ»әХЯСҒЗе±к±ңА©ФцғуӘ¬14·ЭіцПЦБЛ1.15 kbғН2.05 kbА©ФцЖ¬¶ОӘ¬¶шУГGunther·ЁҢцУР¶ю·ЭіцПЦ3.2 kbА©ФцІъОпҰӘ¶юЖ¬¶О·ЁµДА©ФцР§ВКГчПФёЯУЪGunther·ЁҰӘНә1КЗ·Ц±рУГ¶юЦЦ·Ң·ЁА©ФцН¬Т»АэРҮөшХЯСҒЗе±к±ңµДҢб№ыӘ¬НЁ№эМхөшГЬ¶И¶ЁБү·ЦОцӘ¬¶юЖ¬¶ОµДА©ФцІъОп±И3.2 kbІъОпёЯ20Ұ«40±¶ҰӘ
УГГёЗР·ЁғН¶ФHBVИ«»щТтүЛВҰО»µгРтБР·ЦОцПФКңГёЗРО»µгғНHBVІеИлРтБРУлЙиәЖПа·ыҰӘ
¶юҰұЧҒИңПё°ыЕаСшЙПЗеЦРHBsAgғНHBeAgµД±нөп
·Ц±рУГAbbottКФәБәмІвЧҒИңПё°ыЕаСшЙПЗеЦРHBsAgғНHBeAgҰӘНә2Ұұ3·Ц±рПФКңУГ¶юЖ¬¶О·ЁүЛВҰµДИ«»щТтЧҒИңHepG2Пё°ыүЙУРHBsAgғНHBeAgµД±нөпҰӘУЙУЪёГ·ЁА©ФцµДHBVИ«»щТтµД¶ю
, °ЩДөТҢТ©
1ӘғDNA·ЦЧУБү±кЦң(1kb marker);2ӘғGunther·ЁА©ФцІъОпӘ»
3ғН4Әғ¶юЖ¬¶О·ЁА©ФцІъОп
Нә1 ¶юЖ¬¶О·ЁғНGunther·ЁА©ФцHBV»щТтЧйІъОпµДµзУңНә

HBV DNA3.2Әғ¶юЖ¬¶О·ЁЦЖ±ёµДSapұсХіД©¶ЛHBVИ«»щТтӘ»Угң«DNAӘғТхРФ¶ФХХ
Нә2 УГHBVИ«»щТтЧйЧҒИңHepG2Пё°ыЕаСш
ЙПЗеHBsAgµД±нөп

, http://www.100md.com
HBV DNA3.2Әғ¶юЖ¬¶О·ЁЦЖ±ёµДSapұсХіД©¶ЛHBVИ«»щТтӘ»p3.8ұт:ІеИл1.2±¶HBVИ«»щТтЦШЧйЦКБӘ(СфРФ¶ФХХ)Ә»pCMVHBsӘғІеИлHBV S»щТтЖ¬¶ОµДЦШЧйЦКБӘ(HBeAgТхРФ¶ФХХ)Ә»Угң«DNAӘғТхРФ¶ФХХ Нә3 УГHBVИ«»щТтЧйЧҒИңHepG2Пё°ыЕаСшЙПЗеHBsAgµД±нөп
¶ЛО»УЪHBV CЗш¶БВлүтәЬЖрКәµгПВУОӘ¬№КІвә°HBeAgМбКң¶юЖ¬¶ОБ¬ҢУіЙµД3.2kbИ«»щТтүЙФЪПё°ыДЪЧФЙн»·»ҮӘ¬ІұүЙУРHBVёөЦЖҰӘ
SouthernУҰәӘФУҢ»ПФКңУРРҰУЪ3.2kbНПөшФУҢ»РЕғЕӘ¬·өУі»сµГµДHBVИ«»щТтүЛВҰүЙТФФЪПё°ыДЪУРёөЦЖ№эіМҰӘ
МЦВЫ
HBV»щТтЧйµДМШКвҢб№№К№А©ФцИ«»щТтә«ОҒА§ДСҰӘУ¦УГ±ң·Ң·ЁУЙУЪҢ«HBVИ«»щТтЧй·ЦОҒБҢёцЖ¬¶ОА©ФцӘ¬І»ТҒЗуДӘ°еОҒНкХыµД3.2kbИ«»щТтЧйӘ¬ҢµµНБЛ¶ФДӘ°еµДТҒЗуӘ¬МбёЯБЛА©ФцР§ВКӘ¬»сµГСфРФPCRІъОпµД»ъВКФцёЯҰӘИ»¶шӘ¬УЙУЪHBVµӨБөЗшµДА©ФцУРК±»біКТхРФӘ¬№КУ¦ңҰБүІЙУГҢПРВПКµДСҒЗеҰӘңЭGunther±ЁµАУГExpand High Fidelity(Boehinger Mannheim)µДА©ФцПµНіА©Фц1fgµДHBV DNAӘ¬µ±PCRІъОпОҒ1¦МgК±Ә¬ИЛОҒФміЙµДН»±дғЛЬХЛбКэҢцОҒ8.3kbЦР1ёцғЛЬХЛбН»±дҰӘТтөЛӘ¬ИЛОҒТтЛШФміЙµДН»±дВКғЬµНӘ¬µ«ОҒ±ӘЦ¤А©ФцРтБРµДүЙүүРФӘ¬РиУГУРРӘФДЧчУГµДГёЧчА©ФцҰӘ
, °ЩДөТҢТ©
ФЪТС·ұ±нµДHBVИ«»щТтРтБРЦРӘ¬ңщУРµӨТ»SpeұсГёЗРµгӘ¬ЙиәЖµДТэОпPSP1ғНPSP2ТІңщғ¬УРТ»ёцSpeұсГёЗРµгӘ¬үЙҢ«»сµГµДHBV»щТтЖ¬¶ОПа»ӨБ¬ҢУҰӘSalұсОҒ·ЦЧУүЛВҰЦРіӘУГµДПЮЦЖРФДЪЗРГёӘ¬¶шЛщ·ұ±нµДHBVИ«»щТтРтБРңщОЮSalұсГёЗРµгҰӘТэОпЦРЙиәЖµДSalұсГёЗРµгУРАыУЪҢ«А©ФцµДЖ¬¶ОүЛВҰИлФШМеЦРҰӘУЙУЪSalұсғНSpeұсГёЗРМхәюТ»ЦВӘ¬±гУЪ¶ФА©ФцЖ¬¶ОЧчЛ«ГёЗРӘ¬әт»ҮБЛІЩЧчІҢЦиҰӘ
SapұсµДК¶±рО»µгУлГёЗРО»µгІ»Н¬Ә¬№КүЙНЁ№эУГSapұсГёЗРүЛВҰФШМеµДHBVИ«»щТт¶шІ»ёД±дHBV»щТтРтБРӘ¬өУ¶ш»сµГНкХыµДHBVИ«»щТтҰӘФЪТС·ұ±нµД36ЦкHBVИ«»щТтЦРӘ¬ҢцУР2ЦкРтБРЦРғ¬SapұсГёЗРµгҰӘТтөЛӘ¬УГSapұсГёЗРHBVИ«»щТтүЛВҰТФ»сµГHBVНкХыµДИ«»щТтККУГУЪөу¶аКэHBV¶ңЦкҰӘУГ±ңОД±ЁµАµД·Ң·ЁТСіЙ№¦µШүЛВҰБЛ»әХЯСҒЗеHBV¶ңЦкИ«»щТтӘ¬ІұЦ¤ГчүЙФЪПё°ыЦР¶МФЭ±нөпү№Фә°ФЪ°ыДЪёөЦЖҰӘёщңЭРиТҒӘ¬»№үЙ¶ФУРТвТеµД¶ңЦкҢшРРИ«»щТтІвРтҰӘХвТ»РВ·Ң·ЁµДҢЁБұҢ«өуөуНЖҢш¶ФHBV¶ңЦкµДҢб№№ғН№¦ДЬµДСРңүҰӘ
±ңүОМвОҒ№ъәТЧФИ»үЖС§»щҢрЧКЦъПоДү(39630020)
, °ЩДөТҢТ©
ІОүәОДПЧ
1 Carman WF, Zanetti AR, Karayiannis P, et al. Vaccine-induced escape mutant of hepatitis B virus. Lancet,1990,336:325-329.
2 Sato S, Suzuki K, Akahane Y, et al. Hepatitis B virus strains with mutations in the core promoter in patients with fulminant hepatitis. Ann Intern Med,1995,122:241-246.
3 Gunther S, Li BC, Miska S, et al. A novel method for efficient amplification of whole hepatitis B virus genomes permits rapid functional analysis and reveals deletion mutant in immunosuppressed patients. J Virol,1995,69:5437-5444.
4 ғОҢЁОДӘ¬ВАЗзӘ¬ЦмЖфҒҰFDACҒӘӘ¬µИ.ТТРНёОСЧТЯГзГвТЯК§°ЬІҰ¶ң±нГжү№ФҰ®aҰҮңц¶ЁөШ»щТт±дТмµДСРңү.ЦР»ҒКµСйғНБЩөІІҰ¶ңС§ФУЦңӘ¬1996Ә¬10Әғ308-311.
5 ОЕУсГ·Ә¬ғОАц·әӘ¬ВӨ»ЭХдӘ¬µИ.үЛВҰТТРНёОСЧІҰ¶ңDNAФЪHepG2Пё°ыЦРµД±нөп.ЦР»ҒТҢС§ФУЦңӘ¬1989Ә¬69Әғ260-263., °ЩДөТҢТ©