胎儿骨基质对纯钛种植体-骨结合的作用研究△
作者:邹丽剑1 张涤生1 王 炜1 佘国义2
单位:
关键词:纯钛种植体;胎儿脱钙骨基质;骨诱导
中国修复重建外科杂志980317 摘 要 为探索胎儿脱钙骨基质(FDBM)对纯钛与骨结合的影响,采用荧光显微镜、偏光显微镜、定量组织学测量,以及扫描电镜-能谱分析等研究手段,对复合FDBM及未复合FDBM的钛-骨界面进行了骨密度、骨整合率、新骨生长率,以及界面上Ca、P含量等的对比实验研究。结果表明,FDBM植入钛-骨界面无抗原性,明显促进和加速了界面新骨形成,使钛-骨结合时间提前约2个月。认为,胎儿骨可能比成人骨内的诱导成骨因子作用大或含量高。FDBM作为无抗原性、制备简便、价格便宜、便于保存及骨诱导作用明显的骨诱导剂之一,具有深入研究的价值。
THE ROLE OF FETUS DECALCIFIED BONE MATRIX (FDBM) IN INDUCING PURE TITANIUM-BONG IMPLANT INTERGRATION/Zou Lijian, Zhang Dishen, Wang Wei et al. The 9th Affiliated People's Hospital, Shanghai Second Medical University, Shanghai, P. R. China 200011
, http://www.100md.com
Abstract Because of its high biological compatibility, titanium has been a good biomaterial. The implanted artificial bone made from titanium can contact with the vital and mature osseous tissue directly within 3~6 months, the so-called osteointergration. In order to promote the process of osteointergration, FDBM of rabbit was prepared and was combined with pure titanium so as to speed up osteointergration. The study focused on bone density, bone intergration rate, new bone growth rate around the pure titanium, and the Ca2+ and PO43- density of titanium-bone interface. A control group of pure titanium inplant without FDBM was set up. The results showed FDBM had no antigenicity. It could induce and speed up the new bone formation at titanium-bone interface. The titanium-bone intergration time was within 2 months. It was suggested that there were more bone morphogenesis protein (BMP) or other bone induction and bone formation factors in brephobone than that in child and adult bone. As a kind of bone induction material, FDBM was easy prepared, cheap in price, easy to storage, no antigenicity and obvious bone-inductive function.
, 百拇医药
Key words Pure titanium implant Fetus decalcified bone matrix Bone induction
许多方面的临床应用已证实,钛是一种生物相容性很好的医用生物材料,用钛制作的人工骨或种植体,能与生活的骨组织直接接触(光镜水平),Branemark将此造语为Osseointegration(骨整合、骨融合或骨结合)。目前,多数学者认为钛不能与骨组织发生化学性结合,也无促进骨形成作用[1]。钛植入骨组织后,界面新骨成熟需3个月~6个月。为了缩短骨整合时间,加速钛在应用中与骨组织的结合过程,曾有用微电流刺激,脱钙骨基质(decalcified bone matrix, DBM),骨基质明胶(bone matrix cetalin, BMC),骨形成蛋白(bone morphogenetic protein, BMP),以及高压氧等的报道[2,3]。其中以骨诱导剂对促进钛-骨结合的研究倍受关注。我们采用胎儿脱钙骨基质(foetus decalcified bone matrix, FDBM)作为骨诱导剂,研究其对钛-骨组织结合的影响。
, http://www.100md.com
1 材料与方法
1.1 材料准备
1.1.1 植入纯钛种植体的制备 采用国产TA0(99.80%),12 mm×3 mm,圆柱形,光滑面,经酸、碱和超声波清洗,再双蒸水冲洗后,自然干燥,装入小瓶,高压蒸气消毒备用。
1.1.2 FDBM的制备 在无菌条件下,取胎龄25天~27天同种胎兔的全部骨骼,去除附着的软组织及骨髓,在磁力器搅拌下,经双蒸水(2小时),纯乙醇(1小时),乙醚(30分钟)依次清洗后,置于37℃恒温箱过夜。处理后的骨组织经研磨、过筛,保留200目~450目大小的颗粒,放入0.5 mol/L的盐酸中脱钙(3小时),再经双蒸水(2小时)、纯乙醇(1小时)、乙醚(30分钟)依次清洗,于37℃恒温箱中过夜。处理完毕的FDBM粉放入无菌小瓶,置于环氧乙烷消毒机内低温消毒36小时,细菌培养结果为阴性,3天后备用。拧紧瓶盖,在室温干燥条件下可长期保存。
, 百拇医药
1.2 种植手术
采用新西兰健康大白兔9只,体重2 kg~2.5 kg。2.5%戊巴比妥钠(1.5ml/kg)经兔耳静脉麻醉后,按常规手术方法在胫骨前内侧中1/3段,以及肱骨中段作1 cm长切口,切开皮肤及骨膜,用直径3 mm骨钻慢速钻孔达骨髓腔。在兔右侧胫骨和肱骨内各植入1个复合FDBM的纯钛种植体,左侧胫骨和肱骨内单纯植入纯钛种植体作为对照。分层缝合创口。观察动物术后创口愈合情况,术后15,30,90及180天分四批处死动物。处死前15天肌肉注射四环素(50 mg/kg)作新骨标记。在30天时对未处死的每个动物在相同拍摄条件下拍X线片,以供分析。
1.3 光镜组织标本的制备
用空气栓塞法处死动物,迅速取胫骨段,参照X线片确定种植体部位。用骨锯将种植体植入区两端多余的胫骨去除,将所取植有种植体的骨块置于2%戊二醛和多聚甲醛的混合液内,在4℃冰箱内固定1周。再将标本置于丙酮液内1周以上进行系列脱脂、脱水。甲基丙烯酸甲酯和过氧化二苯甲酰包埋,在35℃恒温箱内凝聚1周。用Leitz 1600内圆锯式切片机沿种植体中心轴将标本一剖为二,取其中半块标本作带种植体的不脱钙骨块缓切片(100 μm),Sirius染色后光镜观察和定量组织学分析。
, http://www.100md.com
1.4 扫描电镜-能谱分析试样的制备和观测方法
选择30天和180天种植体复合FDBM和未复合FDBM,已经过包埋的同一动物左右胫骨标本,用切片机将两端修整后沿种植体长轴剖开,制成骨组织-界面-种植体的纵断光滑观察面。丙酮清洁观察面,自然干燥后用扫描电镜(JEOL JXA-840)在种植体与皮质骨结合的界面上随机选择10个点,再用能谱仪(LINK-860)在同一条件下对钛种植体-骨界面进行Ca、P、Ti等元素测试。
2 结果
2.1 创口观察
术后仅表现为局部轻度水肿,3天后消失,Ⅰ期愈合。左右创口反应相同。
2.2 骨密度测定
实验侧8只动物术后30天术区作X线片检查。根据组织灰度不同,用VIDAS图像分析仪对X线片作种植体周围骨组织的密度测定(表1)。经配对t检验,P<0.05,复合FDBM组优于对照组,有显著性差异。
, 百拇医药
2.3 组织学观察和定量组织学分析
2.3.1 普通光镜与荧光显微镜观察 实验侧种植后15天,界面新骨形成活跃。30天时界面已见大量新生骨组织,其在种植体两侧形成厚薄不均的骨壳,骨壳内部分骨组织已趋成熟,可见哈佛氏管。90天时骨壳厚度有所增加,种植体周围均为板层骨。180天时种植体周围板层骨内哈佛氏管丰富,板层骨壳内、外及部分界面仍有新骨活跃(图1a~d)。
表1 种植体与复合FDBM种植体界面区骨密度测定 动物编号
种植体
复合FDBM种植体
1
65.72
68.98
, http://www.100md.com
2
69.87
82.61
3
79.18
110.98
4
58.83
97.54
5
81.14
78.48
6
, http://www.100md.com
70.20
68.87
7
100.06
106.81
8
71.97
87.84
图1 复合FDBM种植体植入骨组织(荧光 ×10)
a 15天 b 30天 c 90天(偏光) d 180天
对照侧种植后15天,界面有少量新骨组织。30天时界面为较薄的骨壳,主要为编织骨,未见哈佛氏管。90天时界面上骨细胞排列开始有序,趋向于成熟的板层骨,可见到哈佛氏管(图2a~c)。180天时与实验侧所见基本相同。
, 百拇医药
2.3.2 定量组织学分析 新骨生长率(bone ingrowth fraction, BIF)测定:每张切片在光镜×10倍条件下,取种植体穿皮质骨、松质骨和位于髓腔内的种植体下端三个部位的两侧界面,共6个视野。对每个所取视野照相,通过VIDAS系统使图像扩大转现在屏幕上。每个视野的观察总面积固定为距界面同一宽度(约150 μm)的范围内,通过电脑自动识别在这一范围内已标记荧光的新骨组织,并用相应的程序测量新骨面积和观察总面积。将6个视野的新骨面积与观察总面积分别相加,按下式计算BIF,结果见表2。经统计学处理,P<0.05,复合FDBM侧优于对照侧,有显著性差异。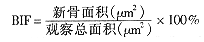
表2 种植体与复合FDBM种植体BIF测定值(%) 动物编号
种植体
复合FDBM种植体
, http://www.100md.com
1
33.12
49.98
2
53.72
61.26
3
44.20
41.36
4
38.05
39.12
5
, 百拇医药
36.35
35.87
6
47.58
52.23
7
35.25
42.23
8
10.89
21.62
9
25.61
, 百拇医药
32.12
2.4 扫描电镜-能谱分析
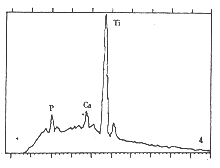
同一动物左右胫骨(复合FDBM侧和未复合FDBM侧)种植体植入标本在30天时钛-骨界面的Ca、P含量有明显差异(图3,4)。还可见到复合FDBM侧标本30天时钛-骨界面的Ca、P含量与未复合FDBM侧标本180天时的钛-骨界面的Ca、P水平相接近(图3,5)。
图2 种植体植入骨组织(光镜 ×4)
a 15天 b 30天 c 90天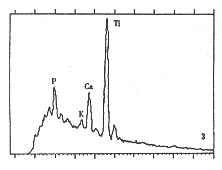

, 百拇医药
图3 TA0FDBM-骨组织界面(30天)Ca、P、Ti元素峰(扫描电镜-能谱分析) 图4 未复合FDBM侧30天时界面的Ca、P、Ti峰(SEM-EDA分析) 图5 TA0-骨组织界面(180天)Ca、P、Ti元素峰(扫描电镜-能谱分析)
3 讨论
骨基质具有骨诱导能力的假设最早由Levander、Urist及Mclean等提出。1965年Urist将同种DBM植入大鼠腹壁肌内,成功地诱导出骨组织,证明了上述假设的成立[4]。Urist认为,骨组织内含有一种化学物质,能诱导未分化的间充质细胞向骨系细胞方向分化,并将这种物质命名为骨形态发生蛋白或BMP。此后20年,Urist等一直致力于从DBM中提纯BMP的研究。1972年他们在DBM的基础上增加了多步脱蛋白处理,提取一种比DBM更具诱导活性的BMC[5]。又经过多次实验,终于在1982年,从牛BMC中提取出具有诱导活性纯度较高的牛骨形成蛋白[6]。目前已从牛、猪、羊等动物及人的骨基质中纯化出BMP,并已广泛应用于促进骨折愈合、骨不连、骨缺损及脊柱融合等植骨治疗中。近年来,不断有将其与钛、羟基磷灰石等种植体或其它生物材料复合应用,以促进骨再生的研究报道。有关FDBM的研究报道却很少。
, 百拇医药
我们采用FDBM作为骨诱导剂的目的是:①大量的动物实验及临床应用已证明,异体胎儿骨在诱导骨再生,促进骨修复方面与新鲜自体骨相近。②BMP在动物体内的确切存在部位尚不清楚。目前除骨组织外,从一些骨肉瘤组织,牙齿硬组织及某些上皮组织细胞内也可分离出BMP或类BMP物质[7]。Urist的实验证明,在骨组织中的BMP含量仅为0.01%,正常成人血清中BMP含量约为10 μg/ml,而生长中儿童的血清BMP含量比成人高,一般在20 μg/ml~70 μg/ml之间[8]。关于FDBM内的BMP含量尚未见报道,故可通过该实验了解FDBM的诱导活性。③骨基质中除含有BMP外,还含有细胞外基质因子、膜内成骨因子、骨骼生长因子等多种诱导、成骨因子[9],虽然已从骨基质中提纯出最有诱导能力的BMP,但并不能否定其它诱导因子的作用,因此骨基质尚有未挖掘出的应用价值。④有些学者认为某些BMP有抗原性,能够引起免疫反应,一些临床应用报道也证实了这一点[10],而胎儿骨具有更低的免疫原性,可以避免产生免疫反应。⑤BMC、BMP的制作方法复杂,处理时间长,不宜被常规骨库采用。⑥目前对BMP用于种植体界面的报道已较多。而将FDBM用于钛-骨界面的报道非常少,国内尚未见报道。
, 百拇医药
从我们的实验结果中可以看到,复合FDBM侧比未复合FDBM侧界面的骨密度、BIF及Ca、P沉积有明显提高。组织学观察,复合FDBM侧界面的成骨时间、骨成熟程度及成骨量与对照侧比较有明显差异。实验侧15天时界面新骨再生已十分活跃,30天时已为基本成熟的板层骨,并可见哈佛氏管。而对照侧30天时未见哈佛氏管,成骨量及骨成熟程度均不如实验侧。对照侧90天时的界面状态相当于实验侧30天时的界面反应。从时间上看,实验侧比对照侧界面愈合过程提前约2个月。扫描电镜-能谱分析结果也证实实验侧比同期对照侧界面的Ca、P沉积多,实验侧30天时的Ca、P峰值已接近对照侧180天时的Ca、P峰值。
从我们的实验结果看,FDBM的骨诱导活性很强。因此,我们推测胎儿骨内的BMP和其它骨诱导或成骨因子可能比儿童及成人骨内的含量高。我们应用复合FDBM侧未引起任何免疫反应,所采用的FDBM制备方法,不需要特殊设备和装置,综合吸收了国内外学者的经验,简易可靠,又可长期保存。作为无抗原性,又具较佳的骨诱导活性,制备简便,对促进钛-骨界面结合有明显作用的骨诱导剂之一,有必要进一步开拓其实验和临床应用的深度、广度。
, http://www.100md.com
4 参考文献
1 汪大林,徐君伍.钛在口腔医学中的应用研究.国外医学 口腔医学分册,1993;20(1):43
2 Sailer HF, Kolb E. Aplication of purified bone morphogenetic protein (BMP) in cranio-maxillo-facial surgery, BMP incompromised surgical reconstructions using titanium implants. J Craniomaxillofac Surg, 1994;22(1):2
3 Larsen PE, Stronczek MJ, Beck FM et al. Osseointegration of implants in radiated bone with and without adjunctive hyperbaric oxygen. J Oral Maxillofac Surg, 1993;51(3):280
, http://www.100md.com
4 Albrektsson T. Bone tissue response. In: Branemark PI, Zatb GA, Albrektsson T. Tissue-Intergrated Prostheses. Chicago: Quintessnce publishing Co, 1985:131~132
5 Urist MR, Zwata M, Ceceotti PWL. Bone morphogenesis in implants of insoluble bone gelatin. Proc Natlacad Sci USA, 1973;70(12):3511
6 Urist MR. A bovine low molecular weight bone morphogenetic protein (BMP) fraction. Clin Orthop, 1982;162:219
, 百拇医药
7 Kawai T. Bovine tooth-derived bone morphogenetic protein. J Dent Res, 1989;68(6):1069
8 陈志信,祝彼得,吴祖尧.骨形态发生蛋白与肌组织内骨化.中华骨科杂志,1993;1391):71
9 片桐岳信,须田立雄.骨诱道因子.细胞互学,1990;9:889
10 Sato K, Urist MR. Induced regeneration of calvaria by bone morphogenetic protein (BMP) in dogs. Clin Orthop, 1985;197:301
△ 上海市医学领先重点学科课题
1 上海第二医科大学附属第九人民医院整复外科(上海,200011)
2 放射科
(收稿:1996-07-03), 百拇医药
单位:
关键词:纯钛种植体;胎儿脱钙骨基质;骨诱导
中国修复重建外科杂志980317 摘 要 为探索胎儿脱钙骨基质(FDBM)对纯钛与骨结合的影响,采用荧光显微镜、偏光显微镜、定量组织学测量,以及扫描电镜-能谱分析等研究手段,对复合FDBM及未复合FDBM的钛-骨界面进行了骨密度、骨整合率、新骨生长率,以及界面上Ca、P含量等的对比实验研究。结果表明,FDBM植入钛-骨界面无抗原性,明显促进和加速了界面新骨形成,使钛-骨结合时间提前约2个月。认为,胎儿骨可能比成人骨内的诱导成骨因子作用大或含量高。FDBM作为无抗原性、制备简便、价格便宜、便于保存及骨诱导作用明显的骨诱导剂之一,具有深入研究的价值。
THE ROLE OF FETUS DECALCIFIED BONE MATRIX (FDBM) IN INDUCING PURE TITANIUM-BONG IMPLANT INTERGRATION/Zou Lijian, Zhang Dishen, Wang Wei et al. The 9th Affiliated People's Hospital, Shanghai Second Medical University, Shanghai, P. R. China 200011
, http://www.100md.com
Abstract Because of its high biological compatibility, titanium has been a good biomaterial. The implanted artificial bone made from titanium can contact with the vital and mature osseous tissue directly within 3~6 months, the so-called osteointergration. In order to promote the process of osteointergration, FDBM of rabbit was prepared and was combined with pure titanium so as to speed up osteointergration. The study focused on bone density, bone intergration rate, new bone growth rate around the pure titanium, and the Ca2+ and PO43- density of titanium-bone interface. A control group of pure titanium inplant without FDBM was set up. The results showed FDBM had no antigenicity. It could induce and speed up the new bone formation at titanium-bone interface. The titanium-bone intergration time was within 2 months. It was suggested that there were more bone morphogenesis protein (BMP) or other bone induction and bone formation factors in brephobone than that in child and adult bone. As a kind of bone induction material, FDBM was easy prepared, cheap in price, easy to storage, no antigenicity and obvious bone-inductive function.
, 百拇医药
Key words Pure titanium implant Fetus decalcified bone matrix Bone induction
许多方面的临床应用已证实,钛是一种生物相容性很好的医用生物材料,用钛制作的人工骨或种植体,能与生活的骨组织直接接触(光镜水平),Branemark将此造语为Osseointegration(骨整合、骨融合或骨结合)。目前,多数学者认为钛不能与骨组织发生化学性结合,也无促进骨形成作用[1]。钛植入骨组织后,界面新骨成熟需3个月~6个月。为了缩短骨整合时间,加速钛在应用中与骨组织的结合过程,曾有用微电流刺激,脱钙骨基质(decalcified bone matrix, DBM),骨基质明胶(bone matrix cetalin, BMC),骨形成蛋白(bone morphogenetic protein, BMP),以及高压氧等的报道[2,3]。其中以骨诱导剂对促进钛-骨结合的研究倍受关注。我们采用胎儿脱钙骨基质(foetus decalcified bone matrix, FDBM)作为骨诱导剂,研究其对钛-骨组织结合的影响。
, http://www.100md.com
1 材料与方法
1.1 材料准备
1.1.1 植入纯钛种植体的制备 采用国产TA0(99.80%),12 mm×3 mm,圆柱形,光滑面,经酸、碱和超声波清洗,再双蒸水冲洗后,自然干燥,装入小瓶,高压蒸气消毒备用。
1.1.2 FDBM的制备 在无菌条件下,取胎龄25天~27天同种胎兔的全部骨骼,去除附着的软组织及骨髓,在磁力器搅拌下,经双蒸水(2小时),纯乙醇(1小时),乙醚(30分钟)依次清洗后,置于37℃恒温箱过夜。处理后的骨组织经研磨、过筛,保留200目~450目大小的颗粒,放入0.5 mol/L的盐酸中脱钙(3小时),再经双蒸水(2小时)、纯乙醇(1小时)、乙醚(30分钟)依次清洗,于37℃恒温箱中过夜。处理完毕的FDBM粉放入无菌小瓶,置于环氧乙烷消毒机内低温消毒36小时,细菌培养结果为阴性,3天后备用。拧紧瓶盖,在室温干燥条件下可长期保存。
, 百拇医药
1.2 种植手术
采用新西兰健康大白兔9只,体重2 kg~2.5 kg。2.5%戊巴比妥钠(1.5ml/kg)经兔耳静脉麻醉后,按常规手术方法在胫骨前内侧中1/3段,以及肱骨中段作1 cm长切口,切开皮肤及骨膜,用直径3 mm骨钻慢速钻孔达骨髓腔。在兔右侧胫骨和肱骨内各植入1个复合FDBM的纯钛种植体,左侧胫骨和肱骨内单纯植入纯钛种植体作为对照。分层缝合创口。观察动物术后创口愈合情况,术后15,30,90及180天分四批处死动物。处死前15天肌肉注射四环素(50 mg/kg)作新骨标记。在30天时对未处死的每个动物在相同拍摄条件下拍X线片,以供分析。
1.3 光镜组织标本的制备
用空气栓塞法处死动物,迅速取胫骨段,参照X线片确定种植体部位。用骨锯将种植体植入区两端多余的胫骨去除,将所取植有种植体的骨块置于2%戊二醛和多聚甲醛的混合液内,在4℃冰箱内固定1周。再将标本置于丙酮液内1周以上进行系列脱脂、脱水。甲基丙烯酸甲酯和过氧化二苯甲酰包埋,在35℃恒温箱内凝聚1周。用Leitz 1600内圆锯式切片机沿种植体中心轴将标本一剖为二,取其中半块标本作带种植体的不脱钙骨块缓切片(100 μm),Sirius染色后光镜观察和定量组织学分析。
, http://www.100md.com
1.4 扫描电镜-能谱分析试样的制备和观测方法
选择30天和180天种植体复合FDBM和未复合FDBM,已经过包埋的同一动物左右胫骨标本,用切片机将两端修整后沿种植体长轴剖开,制成骨组织-界面-种植体的纵断光滑观察面。丙酮清洁观察面,自然干燥后用扫描电镜(JEOL JXA-840)在种植体与皮质骨结合的界面上随机选择10个点,再用能谱仪(LINK-860)在同一条件下对钛种植体-骨界面进行Ca、P、Ti等元素测试。
2 结果
2.1 创口观察
术后仅表现为局部轻度水肿,3天后消失,Ⅰ期愈合。左右创口反应相同。
2.2 骨密度测定
实验侧8只动物术后30天术区作X线片检查。根据组织灰度不同,用VIDAS图像分析仪对X线片作种植体周围骨组织的密度测定(表1)。经配对t检验,P<0.05,复合FDBM组优于对照组,有显著性差异。
, 百拇医药
2.3 组织学观察和定量组织学分析
2.3.1 普通光镜与荧光显微镜观察 实验侧种植后15天,界面新骨形成活跃。30天时界面已见大量新生骨组织,其在种植体两侧形成厚薄不均的骨壳,骨壳内部分骨组织已趋成熟,可见哈佛氏管。90天时骨壳厚度有所增加,种植体周围均为板层骨。180天时种植体周围板层骨内哈佛氏管丰富,板层骨壳内、外及部分界面仍有新骨活跃(图1a~d)。
表1 种植体与复合FDBM种植体界面区骨密度测定 动物编号
种植体
复合FDBM种植体
1
65.72
68.98
, http://www.100md.com
2
69.87
82.61
3
79.18
110.98
4
58.83
97.54
5
81.14
78.48
6
, http://www.100md.com
70.20
68.87
7
100.06
106.81
8
71.97
87.84

图1 复合FDBM种植体植入骨组织(荧光 ×10)
a 15天 b 30天 c 90天(偏光) d 180天
对照侧种植后15天,界面有少量新骨组织。30天时界面为较薄的骨壳,主要为编织骨,未见哈佛氏管。90天时界面上骨细胞排列开始有序,趋向于成熟的板层骨,可见到哈佛氏管(图2a~c)。180天时与实验侧所见基本相同。
, 百拇医药
2.3.2 定量组织学分析 新骨生长率(bone ingrowth fraction, BIF)测定:每张切片在光镜×10倍条件下,取种植体穿皮质骨、松质骨和位于髓腔内的种植体下端三个部位的两侧界面,共6个视野。对每个所取视野照相,通过VIDAS系统使图像扩大转现在屏幕上。每个视野的观察总面积固定为距界面同一宽度(约150 μm)的范围内,通过电脑自动识别在这一范围内已标记荧光的新骨组织,并用相应的程序测量新骨面积和观察总面积。将6个视野的新骨面积与观察总面积分别相加,按下式计算BIF,结果见表2。经统计学处理,P<0.05,复合FDBM侧优于对照侧,有显著性差异。
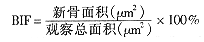
表2 种植体与复合FDBM种植体BIF测定值(%) 动物编号
种植体
复合FDBM种植体
, http://www.100md.com
1
33.12
49.98
2
53.72
61.26
3
44.20
41.36
4
38.05
39.12
5
, 百拇医药
36.35
35.87
6
47.58
52.23
7
35.25
42.23
8
10.89
21.62
9
25.61
, 百拇医药
32.12
2.4 扫描电镜-能谱分析
同一动物左右胫骨(复合FDBM侧和未复合FDBM侧)种植体植入标本在30天时钛-骨界面的Ca、P含量有明显差异(图3,4)。还可见到复合FDBM侧标本30天时钛-骨界面的Ca、P含量与未复合FDBM侧标本180天时的钛-骨界面的Ca、P水平相接近(图3,5)。

图2 种植体植入骨组织(光镜 ×4)
a 15天 b 30天 c 90天



, 百拇医药
图3 TA0FDBM-骨组织界面(30天)Ca、P、Ti元素峰(扫描电镜-能谱分析) 图4 未复合FDBM侧30天时界面的Ca、P、Ti峰(SEM-EDA分析) 图5 TA0-骨组织界面(180天)Ca、P、Ti元素峰(扫描电镜-能谱分析)
3 讨论
骨基质具有骨诱导能力的假设最早由Levander、Urist及Mclean等提出。1965年Urist将同种DBM植入大鼠腹壁肌内,成功地诱导出骨组织,证明了上述假设的成立[4]。Urist认为,骨组织内含有一种化学物质,能诱导未分化的间充质细胞向骨系细胞方向分化,并将这种物质命名为骨形态发生蛋白或BMP。此后20年,Urist等一直致力于从DBM中提纯BMP的研究。1972年他们在DBM的基础上增加了多步脱蛋白处理,提取一种比DBM更具诱导活性的BMC[5]。又经过多次实验,终于在1982年,从牛BMC中提取出具有诱导活性纯度较高的牛骨形成蛋白[6]。目前已从牛、猪、羊等动物及人的骨基质中纯化出BMP,并已广泛应用于促进骨折愈合、骨不连、骨缺损及脊柱融合等植骨治疗中。近年来,不断有将其与钛、羟基磷灰石等种植体或其它生物材料复合应用,以促进骨再生的研究报道。有关FDBM的研究报道却很少。
, 百拇医药
我们采用FDBM作为骨诱导剂的目的是:①大量的动物实验及临床应用已证明,异体胎儿骨在诱导骨再生,促进骨修复方面与新鲜自体骨相近。②BMP在动物体内的确切存在部位尚不清楚。目前除骨组织外,从一些骨肉瘤组织,牙齿硬组织及某些上皮组织细胞内也可分离出BMP或类BMP物质[7]。Urist的实验证明,在骨组织中的BMP含量仅为0.01%,正常成人血清中BMP含量约为10 μg/ml,而生长中儿童的血清BMP含量比成人高,一般在20 μg/ml~70 μg/ml之间[8]。关于FDBM内的BMP含量尚未见报道,故可通过该实验了解FDBM的诱导活性。③骨基质中除含有BMP外,还含有细胞外基质因子、膜内成骨因子、骨骼生长因子等多种诱导、成骨因子[9],虽然已从骨基质中提纯出最有诱导能力的BMP,但并不能否定其它诱导因子的作用,因此骨基质尚有未挖掘出的应用价值。④有些学者认为某些BMP有抗原性,能够引起免疫反应,一些临床应用报道也证实了这一点[10],而胎儿骨具有更低的免疫原性,可以避免产生免疫反应。⑤BMC、BMP的制作方法复杂,处理时间长,不宜被常规骨库采用。⑥目前对BMP用于种植体界面的报道已较多。而将FDBM用于钛-骨界面的报道非常少,国内尚未见报道。
, 百拇医药
从我们的实验结果中可以看到,复合FDBM侧比未复合FDBM侧界面的骨密度、BIF及Ca、P沉积有明显提高。组织学观察,复合FDBM侧界面的成骨时间、骨成熟程度及成骨量与对照侧比较有明显差异。实验侧15天时界面新骨再生已十分活跃,30天时已为基本成熟的板层骨,并可见哈佛氏管。而对照侧30天时未见哈佛氏管,成骨量及骨成熟程度均不如实验侧。对照侧90天时的界面状态相当于实验侧30天时的界面反应。从时间上看,实验侧比对照侧界面愈合过程提前约2个月。扫描电镜-能谱分析结果也证实实验侧比同期对照侧界面的Ca、P沉积多,实验侧30天时的Ca、P峰值已接近对照侧180天时的Ca、P峰值。
从我们的实验结果看,FDBM的骨诱导活性很强。因此,我们推测胎儿骨内的BMP和其它骨诱导或成骨因子可能比儿童及成人骨内的含量高。我们应用复合FDBM侧未引起任何免疫反应,所采用的FDBM制备方法,不需要特殊设备和装置,综合吸收了国内外学者的经验,简易可靠,又可长期保存。作为无抗原性,又具较佳的骨诱导活性,制备简便,对促进钛-骨界面结合有明显作用的骨诱导剂之一,有必要进一步开拓其实验和临床应用的深度、广度。
, http://www.100md.com
4 参考文献
1 汪大林,徐君伍.钛在口腔医学中的应用研究.国外医学 口腔医学分册,1993;20(1):43
2 Sailer HF, Kolb E. Aplication of purified bone morphogenetic protein (BMP) in cranio-maxillo-facial surgery, BMP incompromised surgical reconstructions using titanium implants. J Craniomaxillofac Surg, 1994;22(1):2
3 Larsen PE, Stronczek MJ, Beck FM et al. Osseointegration of implants in radiated bone with and without adjunctive hyperbaric oxygen. J Oral Maxillofac Surg, 1993;51(3):280
, http://www.100md.com
4 Albrektsson T. Bone tissue response. In: Branemark PI, Zatb GA, Albrektsson T. Tissue-Intergrated Prostheses. Chicago: Quintessnce publishing Co, 1985:131~132
5 Urist MR, Zwata M, Ceceotti PWL. Bone morphogenesis in implants of insoluble bone gelatin. Proc Natlacad Sci USA, 1973;70(12):3511
6 Urist MR. A bovine low molecular weight bone morphogenetic protein (BMP) fraction. Clin Orthop, 1982;162:219
, 百拇医药
7 Kawai T. Bovine tooth-derived bone morphogenetic protein. J Dent Res, 1989;68(6):1069
8 陈志信,祝彼得,吴祖尧.骨形态发生蛋白与肌组织内骨化.中华骨科杂志,1993;1391):71
9 片桐岳信,须田立雄.骨诱道因子.细胞互学,1990;9:889
10 Sato K, Urist MR. Induced regeneration of calvaria by bone morphogenetic protein (BMP) in dogs. Clin Orthop, 1985;197:301
△ 上海市医学领先重点学科课题
1 上海第二医科大学附属第九人民医院整复外科(上海,200011)
2 放射科
(收稿:1996-07-03), 百拇医药