脊神经节微血管内皮细胞阴离子微区的分布特点、生物学特性及损伤的影响
作者:周跃 刘正津 梅芳瑞 廖维宏 肖桃元
单位:周跃、梅芳瑞 400037 重庆,第三军医大学附属新桥医院骨科;刘正津 第三军医大学解剖教研室;肖桃元 电镜室;廖维宏 第三军医大学附属大坪医院、野战外科研究所
关键词:脊神经节;损伤;血管内皮细胞;阴离子微区;阳离子体金
中华创伤杂志980506 【摘要】 目的 探讨脊神经节(DRG)血-神经屏障微血管内皮细胞阴离子微区(AMD)的分布特点、生物学特性以及与损伤后血管通透性增加的关系。方法 健康家兔42只,分为手术对照组、机械性压迫组、炎性损伤组。采用阳离子胶体金(CCG)探针和系列酶消化包埋后标记法观测。结果 (1)DRG血管内皮细胞上存在着阴离子分布的极化区;(2)涎酸葡萄糖轭合物为DRG血管内皮细胞阴离子微区分子的主要成分。结论 DRG血管内皮细胞对血浆中蛋白仍具有阴离子通透性屏障作用,DRG微血管内皮细胞阴离子屏障的损伤将导致微血管通透性的显著增加。
, http://www.100md.com
Structural and Molecular Characteristics of and Effects of Different Injuries on Anionic Microdomains on Endoneurial Capillaries in Dorsal Root Ganglia ZHOU Yue, LIU Zheng-jin, MEI Fang-rui, et al. Dept. of Orthopedics, Second Affiliated Hospital, Third Military Medical University, Chongqing 400037
【Abstract】 Aim To explore the structural and molecular characteristics of anionic microdomains on the endoneurial capillaries, and the relation with the increased vascular permeability following dorsal root ganglia (DRG) injury. Methods Forty-two rabbits were randomly divided into the control group, the mechanical compression group and the inflammatory injury group. Cationic colloidal gold (CCG) probe and various enzymes digestion on CCG labelling were taken for the study. Results (1) There were anionic microdomains and distinct charge polarization in the endotheliocytes of DRG between luminal and albuminal fronts. (2) The sialoglycoconjugates were the major components of the negatively charged microdomains in DGR. Conclusion The endoneurial capillaries in DRG may become a barrier, especially be able to limit the plasma protein extravasation. Inflammatory injury can reduce largely the anionic charges on the luminal plasmalemma, destroy the distribution of anionic microdomains and enhance the vascular permeability significantly.
, 百拇医药
【Key words】 Dorsal root ganglia Injury Endotheliocyte Anionic microdomain Cationic colloidal gold
笔者采用阳离子胶体金(CCG)探针和系列酶消化包埋后标记等方法,探讨脊神经节(DRG)血-神经屏障微血管内皮细胞阴离子微区(AMD)的分布特点、生物学特性以及与损伤后血管通透性增加的关系。
材料与方法
一、动物及分组:健康家兔42只,雌雄不拘。体重2.2~3.1kg。随机分为3组:A组(手术对照组,兔数=7);B组(急性机械性压迫组,兔数=7);C组(炎性损伤组,兔数=28)。
二、模型复制:3%戊巴比妥钠(0.5~1.0ml/kg)耳静脉麻醉,常规消毒铺无菌巾,腰骶部后正中切口,咬除L5~7棘突和椎板,手术显微镜下仔细显露双侧DRG5和DRG6。左侧作为损伤侧,右侧作为非损伤侧。B组采用2枚微型手术血管夹(夹宽2mm,张开距3mm,压力45g),分别压迫左侧DRG5和DRG6。C组采用4-0铬制肠线,剪成0.5cm长,取4~6条,沿左侧DRG5和DRG6周围纵轴排列放置,并用无菌手术骨蜡固定,1~2层明胶海绵覆盖在硬脊膜表面,缝合伤口,送动物室饲养。A组 手术显露和术后处理同B组和C组一样,A组作为手术对照组,而B组和C组右侧的DRG5和DRG6作为自身对照组。
, 百拇医药
三、CCG探针的制备及电镜观察
1.CCG的制备:参照Skutelsky等[1]方法。首先用0.1mol/L K2CO3将胶体金(CG,8~12nm, Sigma公司)调至pH7.0,通过絮凝沉淀法[2]确定多聚-L-赖氨酸(PL,MW>300 000,Sigma公司)用来稳定不同浓度CG的量,将CG与溶解在双蒸水中的PL迅速混合成粗制的PL-G复合物,4℃超速离心10 000~20 000g/45min;吸去上清液,将0.01mol/L PBS(pH7.2)加入沉淀的PLG中,4℃保存。
2.标本采集及镜检:冰冻组织切片放入0.1mol/L氯化铵中作用3小时后,再放入已制备完毕的CCG(采用0.1mol/L PBS,pH2.0,内含0.1%BSA稀释成1∶40)中室温孵育3~6小时,然后用0.01mol/L PBS(pH7.2)漂洗3次,2%OsO4固定3小时,常规电镜包埋,透射电镜观察。电镜下CCG呈高电子密度颗粒。结果分析采用图像分析仪,计算不同部位每平方微米的CCG颗粒数(CCG number/μm2)。
, 百拇医药
四、阴离子微区分子的生物学特性:按照Lawrenson等[3]酶消化和包埋后标记法进行。组织标本经固定、脱水及树脂包埋,制成超薄镍网切片,将切片放置在湿盒中,每张切片分别滴加1滴酶消化液(酶消化组)或缓冲液(非消化组),37℃孵育1~2小时。其中胰蛋白酶2mg/ml PBS, pH7.3。番木瓜蛋白酶2mg/ml 醋酸缓冲液, pH6.1。肝素酶,160U/ml PBS, pH7.3。神经氨酸酶10U/ml醋酸缓冲液, pH5.0。经酶消化1小时后,滴加PBS(0.01mol/L, pH7.4)漂洗,然后在每张切片上滴加 CCG,室温下孵育1~2小时。最后用0.01mol/L,pH7.4PBS漂洗,醋酸双氧铀和枸橼酸铅双层染色,电镜观察CCG呈高电子密度颗粒。
五、统计学处理
实验结果的数据统计均在486/DX266型微机上采用Microsoft Excel 5.0的统计程序,行样本单因素和多因素方差分析,显著性t检验,结果以均数±标准差(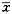 ±s)表示。
±s)表示。
, http://www.100md.com
结 果
一、DRG内CCG的分布特点及损伤的影响
DRG内微血管内皮细胞腔膜面的细胞质膜上,散在分布着数目不等的CCG高电子密度颗粒,非腔膜面也有CCG分布,但腔膜面的CCG颗粒明显较非腔膜面多。此外,内皮细胞突起也有比较多的CCG分布,吞饮小泡和小泡隔膜的表面则仅有极少量CCG颗粒分布(图1)。DRG急性压迫损伤后,其CCG分布与未损伤侧无明显差异,而炎性损伤后2周组,其内皮细胞腔膜面的CCG高电子密度颗粒却明显减少(P<0.05)(图2)。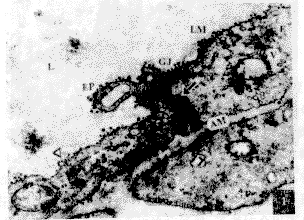
图1 正常DRG微血管内皮细胞(E)腔膜面(LM)和非腔膜面(AM)上均分布有CCG电子密度颗粒(△),腔膜面的CCG颗粒明显较非腔膜面多 TEM ×30 000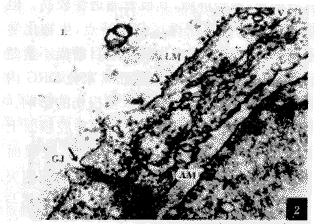
, http://www.100md.com
图2 DRG炎性损伤后2周,血管内皮细胞(E)腔膜面(LM)上的CCG高电子密度颗粒明显减少 TEM ×30 000
二、DRG内阴离子微区的分子特性
见附表。胰蛋白酶具有裂解赖氨酸和精氨酸的羧基键作用,经酶消化后的CCG颗粒与非消化组之间无显著性差异(P>0.05);番木瓜蛋白酶具有能裂解各种肽键的作用,该酶消化后的CCG颗粒数显著降低(P<0.05)(图3);肝素酶具有水解肝素和肝素硫酸酯的作用,消化组的CCG颗粒数与非消化组比较无显著性差异(P>0.05);神经氨酸酶具有水解N-酰神经氨酸葡萄糖酐作用,该酶消化组的CCG颗粒数较非消化组极显著降低(P<0.01)(图4)。
附表 酶消化对CCG标记物的影响(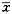 ±s,number/μm2) 组别
±s,number/μm2) 组别
, 百拇医药
消化酶
胰蛋白酶
番木瓜酶
肝素酶
神经氨酸酶
非消化组
12.3±3.6
15.5±4.9
13.1±3.3
14.4±5.2
消化组
13.8±4.1
8.2±2.8
, http://www.100md.com
12.8±4.7
4.8±1.6
P值
>0.05
<0.05
>0.05
<0.01
图3 番木瓜蛋白酶消化后的CCG颗粒数显著降低TEM ×30 000
图4 神经氨酸酶消化后的CCG颗粒数量显著降低 TEM ×30 000
, 百拇医药
讨 论
血-神经屏障的结构基础是血管内皮细胞。近年研究发现在中枢神经系统[4~6]和外周神经系统[7,8]血管内皮细胞表面有一层绒状外衣,称多糖外衣,这是一层规则排列的聚合物膜,带负电荷即AMD,对血浆中大部分带阴离子的蛋白具有静电通透屏障作用。微血管对循环状态下各种分子的通透性,不但受分子大小的影响,而且受分子电荷的影响,该屏障的破坏将导致血管通透性的增高和组织水肿。
DRG内血管内皮细胞形态结构和功能与中枢神经和外周神经系统不尽相同。虽然研究已证明,DRG缺乏有效的血-神经屏障,其血管通透性较高。但血管内皮细胞表面的阴离子微区分布特点,生物化学特性以及不同损伤方式对其产生的影响目前尚不清楚。对此,笔者采用CCG为探针,观察正常家兔DRG内微血管内皮细胞的阴离子分布特点以及损伤的影响。研究观察到DRG血管内皮细胞腔膜面和非腔膜面上都均匀分布着数量不等的高电子CCG颗粒,腔膜面上的CCG数量较非腔膜面高,尤以腔膜面上的细胞突起最显著,表明DRG血管内皮细胞的形态结构虽然与外周神经和中枢神经系统的血管内皮细胞有差异,缺乏有效的血-神经屏障(BNB)结构,但却分布有与外周神经系统相似的阴离子微区,对血浆中的阴离子蛋白具有通透屏障作用。采用蛋白水解酶和糖酵解酶消化组织标本,以探讨DRG血管内皮细胞阴离子微区分子的生物学特性,结果表明涎酸葡萄糖轭合物为其主要化学成分。
, http://www.100md.com
血管内皮细胞的阴离子屏障具有重要的临床意义,体内产生或体外来源的阳离子物质通过与内皮细胞阴离子屏障的作用,引起血管壁通透性增高和组织水肿。创伤和感染时,炎症细胞被激活并在全身重要器官内聚集,释放大量阳离子蛋白,白细胞、血小板及某些细菌还可释放肝素酶,分解内皮细胞及基底膜中的硫酸乙酰肝素,减少细胞表面的负电荷,促进阳离子蛋白的病理作用。负电荷减少或被中和,有助于炎症细胞与内皮细胞的粘附,使白细胞等释放的毒性物质直接作用于局部的内皮细胞,产生更大的损伤效应。血管内皮细胞腔膜面存在的阴离子微区,对血浆中大部分阴离子蛋白构成通透屏障作用。在体外培养的血管内皮细胞单层通透性研究中,Peterson等[9]发现中性粒细胞阳离子蛋白、弹性蛋白酶、鱼精蛋白酶等能显著增加白蛋白的跨内皮转运,同时可看见内皮细胞间隙增宽,加热不能消除这些阳离子蛋白的活性,而肝素可阻断其效应。外周神经压榨伤后将导致损伤远端神经内膜血管通透性的显著增高。Bush等[8]采用鼠的坐骨神经压榨伤模型,用阳离子探针研究神经轴突断裂后,对血-神经屏障内皮细胞表面阴离子分布状态的影响。实验发现伤后第4天,部分损伤神经血管内皮细胞出现暂时阴离子窗孔样结构。作者指出神经变性和再生期间,血-神经屏障通透性增加与内膜血管阴离子窗孔样结构的形成相关,同时也与内皮细胞部分多糖蛋白质复合物的不均匀分布和降低相关。本实验观察到,DRG急性压迫损伤的早期,内皮细胞阴离子微区的分布与未损伤侧无明显差异,但炎性损伤组伤后2周,血管内皮细胞腔膜面细胞质膜上的CCG高电子密度颗粒却明显减少,结果说明炎性损伤可通过降低血管内皮细胞腔膜面上的阴离子电荷,破坏其阴离子屏障来增加微血管的通透性,从而导致和加重组织水肿,并由此而造成神经功能的异常改变和障碍。对于炎性损伤是怎样降低和破坏血管内皮细胞表面阴离子屏障的确切机制,目前尚存在不同的见解,笔者考虑可能与炎性细胞和炎性组织所释放的大量炎性细胞介素的损伤和破坏效应相关,对此值得深入探讨。
, 百拇医药
参考文献
[1]Skutelsky E, Roth J. Cationic colloidal gold-new probe for the detection of anionic cell surface sites by electron microscopy. J Histoche Cytochem, 1986, 34∶693-696.
[2]Roth J, Binder M. Colloidal gold, ferritin and peroxidase as markers for electron microscopic double labeling lectin techniques. J Histochem Cytochem, 1978, 26∶163-165.
[3]Lawrenson JG, Reid AR, Allt G. Molecular characterization of anionic sites on the luminal front of endoneurial capillaries in sciatic nerve. J Neruocyto, 1994, 23∶37-42.
, 百拇医药
[4]Shimon HM, Wadhwani KC, Larson D, et al. Regional blood-brain barrier transport of cationized bovine serum albumin in awake rats. Am J Physiol, 1991, 261∶R476-481.
[5]Vorbrodt AW, Trowbridge RS. Ultrastructural study of transcellular transport of native and cationized albumin in cultured sheep brain microvascular endothelium. J Neurocyto, 1991, 20∶998-1006.
[6]Vorbrodt AW, Dobrogowska DH, Lossinsky AS. Ultrastructural study on the interaction of insulin-albumin-gold comples with mouse brain microvascular endothelial cells. J Neurocyto, 1994, 23∶201-208.
, 百拇医药
[7]Bush MS, Allt G. Blood-nerve barrier: Distribution of anionic sites on the endothelial plasma membrane and basal lamina. Brain Res, 1990, 535∶181-187.
[8]Bush MS, Reld AR, Allt G. Blood-nerve barrier: Ultrastructural and endothelial surface charge alterations following nerve crush. Neuropathology Applied Neurobiology, 1993, 19∶31-43.
[9]Peterson MW, Bush MS. Cationic neutrophil proteins increase transendothelial albumin movement. J Appl Physiol, 1987, 62∶1521.
(收稿:1997-08-08 修回:1998-04-08), 百拇医药
单位:周跃、梅芳瑞 400037 重庆,第三军医大学附属新桥医院骨科;刘正津 第三军医大学解剖教研室;肖桃元 电镜室;廖维宏 第三军医大学附属大坪医院、野战外科研究所
关键词:脊神经节;损伤;血管内皮细胞;阴离子微区;阳离子体金
中华创伤杂志980506 【摘要】 目的 探讨脊神经节(DRG)血-神经屏障微血管内皮细胞阴离子微区(AMD)的分布特点、生物学特性以及与损伤后血管通透性增加的关系。方法 健康家兔42只,分为手术对照组、机械性压迫组、炎性损伤组。采用阳离子胶体金(CCG)探针和系列酶消化包埋后标记法观测。结果 (1)DRG血管内皮细胞上存在着阴离子分布的极化区;(2)涎酸葡萄糖轭合物为DRG血管内皮细胞阴离子微区分子的主要成分。结论 DRG血管内皮细胞对血浆中蛋白仍具有阴离子通透性屏障作用,DRG微血管内皮细胞阴离子屏障的损伤将导致微血管通透性的显著增加。
, http://www.100md.com
Structural and Molecular Characteristics of and Effects of Different Injuries on Anionic Microdomains on Endoneurial Capillaries in Dorsal Root Ganglia ZHOU Yue, LIU Zheng-jin, MEI Fang-rui, et al. Dept. of Orthopedics, Second Affiliated Hospital, Third Military Medical University, Chongqing 400037
【Abstract】 Aim To explore the structural and molecular characteristics of anionic microdomains on the endoneurial capillaries, and the relation with the increased vascular permeability following dorsal root ganglia (DRG) injury. Methods Forty-two rabbits were randomly divided into the control group, the mechanical compression group and the inflammatory injury group. Cationic colloidal gold (CCG) probe and various enzymes digestion on CCG labelling were taken for the study. Results (1) There were anionic microdomains and distinct charge polarization in the endotheliocytes of DRG between luminal and albuminal fronts. (2) The sialoglycoconjugates were the major components of the negatively charged microdomains in DGR. Conclusion The endoneurial capillaries in DRG may become a barrier, especially be able to limit the plasma protein extravasation. Inflammatory injury can reduce largely the anionic charges on the luminal plasmalemma, destroy the distribution of anionic microdomains and enhance the vascular permeability significantly.
, 百拇医药
【Key words】 Dorsal root ganglia Injury Endotheliocyte Anionic microdomain Cationic colloidal gold
笔者采用阳离子胶体金(CCG)探针和系列酶消化包埋后标记等方法,探讨脊神经节(DRG)血-神经屏障微血管内皮细胞阴离子微区(AMD)的分布特点、生物学特性以及与损伤后血管通透性增加的关系。
材料与方法
一、动物及分组:健康家兔42只,雌雄不拘。体重2.2~3.1kg。随机分为3组:A组(手术对照组,兔数=7);B组(急性机械性压迫组,兔数=7);C组(炎性损伤组,兔数=28)。
二、模型复制:3%戊巴比妥钠(0.5~1.0ml/kg)耳静脉麻醉,常规消毒铺无菌巾,腰骶部后正中切口,咬除L5~7棘突和椎板,手术显微镜下仔细显露双侧DRG5和DRG6。左侧作为损伤侧,右侧作为非损伤侧。B组采用2枚微型手术血管夹(夹宽2mm,张开距3mm,压力45g),分别压迫左侧DRG5和DRG6。C组采用4-0铬制肠线,剪成0.5cm长,取4~6条,沿左侧DRG5和DRG6周围纵轴排列放置,并用无菌手术骨蜡固定,1~2层明胶海绵覆盖在硬脊膜表面,缝合伤口,送动物室饲养。A组 手术显露和术后处理同B组和C组一样,A组作为手术对照组,而B组和C组右侧的DRG5和DRG6作为自身对照组。
, 百拇医药
三、CCG探针的制备及电镜观察
1.CCG的制备:参照Skutelsky等[1]方法。首先用0.1mol/L K2CO3将胶体金(CG,8~12nm, Sigma公司)调至pH7.0,通过絮凝沉淀法[2]确定多聚-L-赖氨酸(PL,MW>300 000,Sigma公司)用来稳定不同浓度CG的量,将CG与溶解在双蒸水中的PL迅速混合成粗制的PL-G复合物,4℃超速离心10 000~20 000g/45min;吸去上清液,将0.01mol/L PBS(pH7.2)加入沉淀的PLG中,4℃保存。
2.标本采集及镜检:冰冻组织切片放入0.1mol/L氯化铵中作用3小时后,再放入已制备完毕的CCG(采用0.1mol/L PBS,pH2.0,内含0.1%BSA稀释成1∶40)中室温孵育3~6小时,然后用0.01mol/L PBS(pH7.2)漂洗3次,2%OsO4固定3小时,常规电镜包埋,透射电镜观察。电镜下CCG呈高电子密度颗粒。结果分析采用图像分析仪,计算不同部位每平方微米的CCG颗粒数(CCG number/μm2)。
, 百拇医药
四、阴离子微区分子的生物学特性:按照Lawrenson等[3]酶消化和包埋后标记法进行。组织标本经固定、脱水及树脂包埋,制成超薄镍网切片,将切片放置在湿盒中,每张切片分别滴加1滴酶消化液(酶消化组)或缓冲液(非消化组),37℃孵育1~2小时。其中胰蛋白酶2mg/ml PBS, pH7.3。番木瓜蛋白酶2mg/ml 醋酸缓冲液, pH6.1。肝素酶,160U/ml PBS, pH7.3。神经氨酸酶10U/ml醋酸缓冲液, pH5.0。经酶消化1小时后,滴加PBS(0.01mol/L, pH7.4)漂洗,然后在每张切片上滴加 CCG,室温下孵育1~2小时。最后用0.01mol/L,pH7.4PBS漂洗,醋酸双氧铀和枸橼酸铅双层染色,电镜观察CCG呈高电子密度颗粒。
五、统计学处理
实验结果的数据统计均在486/DX266型微机上采用Microsoft Excel 5.0的统计程序,行样本单因素和多因素方差分析,显著性t检验,结果以均数±标准差(
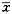 ±s)表示。
±s)表示。, http://www.100md.com
结 果
一、DRG内CCG的分布特点及损伤的影响
DRG内微血管内皮细胞腔膜面的细胞质膜上,散在分布着数目不等的CCG高电子密度颗粒,非腔膜面也有CCG分布,但腔膜面的CCG颗粒明显较非腔膜面多。此外,内皮细胞突起也有比较多的CCG分布,吞饮小泡和小泡隔膜的表面则仅有极少量CCG颗粒分布(图1)。DRG急性压迫损伤后,其CCG分布与未损伤侧无明显差异,而炎性损伤后2周组,其内皮细胞腔膜面的CCG高电子密度颗粒却明显减少(P<0.05)(图2)。

图1 正常DRG微血管内皮细胞(E)腔膜面(LM)和非腔膜面(AM)上均分布有CCG电子密度颗粒(△),腔膜面的CCG颗粒明显较非腔膜面多 TEM ×30 000

, http://www.100md.com
图2 DRG炎性损伤后2周,血管内皮细胞(E)腔膜面(LM)上的CCG高电子密度颗粒明显减少 TEM ×30 000
二、DRG内阴离子微区的分子特性
见附表。胰蛋白酶具有裂解赖氨酸和精氨酸的羧基键作用,经酶消化后的CCG颗粒与非消化组之间无显著性差异(P>0.05);番木瓜蛋白酶具有能裂解各种肽键的作用,该酶消化后的CCG颗粒数显著降低(P<0.05)(图3);肝素酶具有水解肝素和肝素硫酸酯的作用,消化组的CCG颗粒数与非消化组比较无显著性差异(P>0.05);神经氨酸酶具有水解N-酰神经氨酸葡萄糖酐作用,该酶消化组的CCG颗粒数较非消化组极显著降低(P<0.01)(图4)。
附表 酶消化对CCG标记物的影响(
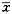 ±s,number/μm2) 组别
±s,number/μm2) 组别, 百拇医药
消化酶
胰蛋白酶
番木瓜酶
肝素酶
神经氨酸酶
非消化组
12.3±3.6
15.5±4.9
13.1±3.3
14.4±5.2
消化组
13.8±4.1
8.2±2.8
, http://www.100md.com
12.8±4.7
4.8±1.6
P值
>0.05
<0.05
>0.05
<0.01

图3 番木瓜蛋白酶消化后的CCG颗粒数显著降低TEM ×30 000

图4 神经氨酸酶消化后的CCG颗粒数量显著降低 TEM ×30 000
, 百拇医药
讨 论
血-神经屏障的结构基础是血管内皮细胞。近年研究发现在中枢神经系统[4~6]和外周神经系统[7,8]血管内皮细胞表面有一层绒状外衣,称多糖外衣,这是一层规则排列的聚合物膜,带负电荷即AMD,对血浆中大部分带阴离子的蛋白具有静电通透屏障作用。微血管对循环状态下各种分子的通透性,不但受分子大小的影响,而且受分子电荷的影响,该屏障的破坏将导致血管通透性的增高和组织水肿。
DRG内血管内皮细胞形态结构和功能与中枢神经和外周神经系统不尽相同。虽然研究已证明,DRG缺乏有效的血-神经屏障,其血管通透性较高。但血管内皮细胞表面的阴离子微区分布特点,生物化学特性以及不同损伤方式对其产生的影响目前尚不清楚。对此,笔者采用CCG为探针,观察正常家兔DRG内微血管内皮细胞的阴离子分布特点以及损伤的影响。研究观察到DRG血管内皮细胞腔膜面和非腔膜面上都均匀分布着数量不等的高电子CCG颗粒,腔膜面上的CCG数量较非腔膜面高,尤以腔膜面上的细胞突起最显著,表明DRG血管内皮细胞的形态结构虽然与外周神经和中枢神经系统的血管内皮细胞有差异,缺乏有效的血-神经屏障(BNB)结构,但却分布有与外周神经系统相似的阴离子微区,对血浆中的阴离子蛋白具有通透屏障作用。采用蛋白水解酶和糖酵解酶消化组织标本,以探讨DRG血管内皮细胞阴离子微区分子的生物学特性,结果表明涎酸葡萄糖轭合物为其主要化学成分。
, http://www.100md.com
血管内皮细胞的阴离子屏障具有重要的临床意义,体内产生或体外来源的阳离子物质通过与内皮细胞阴离子屏障的作用,引起血管壁通透性增高和组织水肿。创伤和感染时,炎症细胞被激活并在全身重要器官内聚集,释放大量阳离子蛋白,白细胞、血小板及某些细菌还可释放肝素酶,分解内皮细胞及基底膜中的硫酸乙酰肝素,减少细胞表面的负电荷,促进阳离子蛋白的病理作用。负电荷减少或被中和,有助于炎症细胞与内皮细胞的粘附,使白细胞等释放的毒性物质直接作用于局部的内皮细胞,产生更大的损伤效应。血管内皮细胞腔膜面存在的阴离子微区,对血浆中大部分阴离子蛋白构成通透屏障作用。在体外培养的血管内皮细胞单层通透性研究中,Peterson等[9]发现中性粒细胞阳离子蛋白、弹性蛋白酶、鱼精蛋白酶等能显著增加白蛋白的跨内皮转运,同时可看见内皮细胞间隙增宽,加热不能消除这些阳离子蛋白的活性,而肝素可阻断其效应。外周神经压榨伤后将导致损伤远端神经内膜血管通透性的显著增高。Bush等[8]采用鼠的坐骨神经压榨伤模型,用阳离子探针研究神经轴突断裂后,对血-神经屏障内皮细胞表面阴离子分布状态的影响。实验发现伤后第4天,部分损伤神经血管内皮细胞出现暂时阴离子窗孔样结构。作者指出神经变性和再生期间,血-神经屏障通透性增加与内膜血管阴离子窗孔样结构的形成相关,同时也与内皮细胞部分多糖蛋白质复合物的不均匀分布和降低相关。本实验观察到,DRG急性压迫损伤的早期,内皮细胞阴离子微区的分布与未损伤侧无明显差异,但炎性损伤组伤后2周,血管内皮细胞腔膜面细胞质膜上的CCG高电子密度颗粒却明显减少,结果说明炎性损伤可通过降低血管内皮细胞腔膜面上的阴离子电荷,破坏其阴离子屏障来增加微血管的通透性,从而导致和加重组织水肿,并由此而造成神经功能的异常改变和障碍。对于炎性损伤是怎样降低和破坏血管内皮细胞表面阴离子屏障的确切机制,目前尚存在不同的见解,笔者考虑可能与炎性细胞和炎性组织所释放的大量炎性细胞介素的损伤和破坏效应相关,对此值得深入探讨。
, 百拇医药
参考文献
[1]Skutelsky E, Roth J. Cationic colloidal gold-new probe for the detection of anionic cell surface sites by electron microscopy. J Histoche Cytochem, 1986, 34∶693-696.
[2]Roth J, Binder M. Colloidal gold, ferritin and peroxidase as markers for electron microscopic double labeling lectin techniques. J Histochem Cytochem, 1978, 26∶163-165.
[3]Lawrenson JG, Reid AR, Allt G. Molecular characterization of anionic sites on the luminal front of endoneurial capillaries in sciatic nerve. J Neruocyto, 1994, 23∶37-42.
, 百拇医药
[4]Shimon HM, Wadhwani KC, Larson D, et al. Regional blood-brain barrier transport of cationized bovine serum albumin in awake rats. Am J Physiol, 1991, 261∶R476-481.
[5]Vorbrodt AW, Trowbridge RS. Ultrastructural study of transcellular transport of native and cationized albumin in cultured sheep brain microvascular endothelium. J Neurocyto, 1991, 20∶998-1006.
[6]Vorbrodt AW, Dobrogowska DH, Lossinsky AS. Ultrastructural study on the interaction of insulin-albumin-gold comples with mouse brain microvascular endothelial cells. J Neurocyto, 1994, 23∶201-208.
, 百拇医药
[7]Bush MS, Allt G. Blood-nerve barrier: Distribution of anionic sites on the endothelial plasma membrane and basal lamina. Brain Res, 1990, 535∶181-187.
[8]Bush MS, Reld AR, Allt G. Blood-nerve barrier: Ultrastructural and endothelial surface charge alterations following nerve crush. Neuropathology Applied Neurobiology, 1993, 19∶31-43.
[9]Peterson MW, Bush MS. Cationic neutrophil proteins increase transendothelial albumin movement. J Appl Physiol, 1987, 62∶1521.
(收稿:1997-08-08 修回:1998-04-08), 百拇医药