»Ī—ű»Ī—™īů ůń‘ŌłįŻĶÚÕŲĶń—–ĺŅ
◊ų’Ŗ£ļĹĮņÁ Őņ‘∆’š Ľ∆ŌĢ√ų ”Š”ĹĽ™ ≥¬∆Ĺ • ļķŌÚ—Ű …Ř–°ň… “◊őńŃķ
Ķ•őĽ£ļ210009 ńŌĺ©ŐķĶņ“Ĺ—ß‘ļłĹ Ű“Ĺ‘ļ∂ýŅ∆(ĹĮņÁ°ĘŐņ‘∆’š°Ę”Š”ĹĽ™°Ę…Ř–°ň…°Ę“◊őńŃķ)£ĽńŌĺ©ŐķĶņ“Ĺ—ß‘ļŅ∆—ß—–ĺŅňý∑÷◊”…ķőÔ—ß—–ĺŅ “(Ľ∆ŌĢ√ų°ĘļķŌÚ—Ű)£¨≤°ņŪ—ßĹŐ—– “(≥¬∆Ĺ •)
ĻōľŁī £ļń‘»Ī—ű£Ľń‘»Ī—™£ĽÕ— …◊ų”√£Ľīů ů
÷–Ľ™“Ĺ—ß‘”÷ĺ980802 °ĺ’™“™°Ņ ńŅĶń ŐĹŐ÷ń‘ŌłįŻĶÚÕŲ‘ŕ»Ī—ű»Ī—™ń‘≤°(HIE)∑Ę≤°ĽķņŪ÷–Ķń◊ų”√°£∑Ĺ∑® ”√HE»ĺ…ę°ĘĶÁĺĶ°Ę‘≠őĽń©∂ňĪÍľ«(Tunel) ÷∂ő£¨∑÷Īū∂‘»Ī—ű3–° Īļů»Ī—™1°Ę4°Ę18°Ę24°Ę40ľį72–° ĪļÕ7Őž◊ťīů ůĶńń‘◊ť÷Į÷–ĶÚÕŲŌłįŻĶń–őŐ¨°Ę≥ŲŌ÷ Īľšľį√‹∂»ĹÝ––ĻŘ≤žļÕĪ»ĹŌ°£ĹŠĻŻ Ļ‚°ĘĶÁĺĶŌ¬Ō‘ ĺ Ķ—ť≤ŗń‘∆§÷ °Ęļ£¬Ūľį«ūń‘…Ůĺ≠‘™÷Śňű°Ę»ĺ…ę÷ ńżľĮ≤Ę≥ŲŌ÷ĶÚÕŲ–°ŐŚ£ĽTunel∑Ĺ∑®÷§ Ķ”–Ń—Ĺ‚DNAīś‘ŕ£Ľ»Ī—ű»Ī—™ļů18–° Ī∆§÷ ĶÚÕŲ◊Ó√ųŌ‘°£ĹŠ¬Ř ‘ŕHIEīů ů£¨ń‘ŌłįŻĶÚÕŲ≥ŲŌ÷≤ĽĶę‘Á”ŕĽĶňņ£¨∂Ý«“”ŽĽĶňņīś‘ŕ◊Ň”’ĶľľŃŃŅŌŗĻō–‘°£
, įŔńī“Ĺ“©
Brain cell apoptosis after cerebral hypoxia-ischemia in neonatal rat Jiang Li, Tang Yunzhen, Huang Xiaoming, et al. Department of Pediatrics, Nanjing Railway Medical college, Nanjing 210009
°ĺAbstract°Ņ Objective To investigate action of apoptosis in mechanisms of neonatal hypoxia-ischemia(HIE). Methods Using HE staining, electronmicroscope, and terminal deoxynuleotidyl transferase-mediated dUTP nick end labeling (TUNEL) technique, we observed the histological features, time course and density of apoptotic cells and compared the ipsilateral hemisphere after permanent ischemia 1, 4, 18, 24, 40, 72h, 7 days after 3h hypoxia with that of sham-group. Results Neurons in the cortex, hippocampus, thalamus exhibited cells shrink, chromatin condensation, apoptosis bodys under microscope, as demonstrated by in situ labeling of DNA breaks. The peak for apoptosis was shown at 18h in the cortex. Conclusion In the HIE, apoptosis appears earlier than necrosis, and both of the different cell death forms may exist induced dose relativity.
, įŔńī“Ĺ“©
°ĺKey words°Ņ Cerebral anoxia Cerebral ischemia Apoptosis Rats
(Natl Med J China, 1998, 78£ļ567-569)
īęÕ≥ĻŘĶ„»Ōő™£¨–¬…ķ∂ý»Ī—ű»Ī—™ń‘≤°(HIE) «”…”ŕľĪ–‘ń‘ňģ÷◊°ĘĽĶňņňý÷¬°£Īĺ—–ĺŅ÷ľ‘ŕĹ®ŃĘHIEĶń∂ĮőÔń£–Õ£¨ĻŘ≤žń‘ňū…ň÷–ń‘ŌłįŻňņÕŲĶńŃŪ“Ľ÷÷–ő Ĺ°™°™ŌłįŻĶÚÕŲ£¨ő™ŐĹŐ÷HIEĶń∑Ę≤°ĽķņŪŐŠĻ©“ņĺ›°£
≤ńŃŌļÕ∑Ĺ∑®
“Ľ°Ę≤ńŃŌ
ń£–Õ÷∆Īł£ļ–¬…ķ7ŐžĶńSDīů ů72÷Ľ£¨ňśĽķ∑÷ő™9◊ť£¨∆š÷–2◊ť∑÷Īūő™∂‘’’◊ťļÕľŔ ÷ ű◊ť(ĹŲ”őņŽ≥ŲĺĪ∂Į¬Ų£¨≤Ľ◊ŲĹŠ‘ķ)£¨∆š”ŗ7◊ťįī RiceĶ»[1]∑Ĺ∑®––◊ůĺĪ∂Į¬ŲĹŠ‘ķ űļů÷√”ŕ8%—ű∆Ý÷–3–° Īļů£¨∑÷Īū”ŕĹŠ‘ķļů1°Ę4°Ę18°Ę24°Ę40ļÕ72–° Īľį7Őž(∂‘’’ļÕľŔ ÷ ű◊ťÕ¨”ŕ18–° Ī)£¨ĺ≠–ń‘ŗ≤ŚĻ‹£¨…ķņŪ—őňģ≥ŚŌī£¨ļůĻŗ»Ž4 %∂ŗĺŘľ◊»©£¨ĻŗĪŌľī»°◊ůń‘£¨Õ‚ĻŐ∂®°£
, įŔńī“Ĺ“©
∂Ģ°Ę∑Ĺ∑®
1.Ļ‚ĺĶľž≤ť£ļ»°«ūń‘÷–1/3∆Ĺ√ś––Ļŕ◊ī«–∆¨£¨∆¨ļŮ5 ¶Őm£¨ ĮņĮįŁ¬Ů£¨HE»ĺ…ę£¨Ļ‚ĺĶľž≤ť°£
2.≥¨őĘĹŠĻĻĻŘ≤ž£ļ‘ŕĻ‚ĺĶľž≤ťĶń»°≤ń≤ŅőĽ£¨»°∆§÷ °Ęļ£¬Ū°Ę«ūń‘◊ť÷Į£¨≥£ĻśĻŐ∂®°ĘįŁ¬Ů°Ę«–∆¨°Ę»ĺ…ę£¨Õł ”ĶÁĺĶŌ¬ĻŘ≤ž°Ę…„∆¨°£
3.‘≠őĽń©∂ňÕ——űļň‹’ňŠ◊™“∆√ł(TdT)ĪÍľ«∑®(Tunel)[2]£ļ«–∆¨◊ŲHE»ĺ…ęĻ‚ĺĶĻŘ≤žļů£¨ŃŕĹŁī¶Ķń ĮņĮ«–∆¨∂®ő™ĪÍľ«į–◊ť÷Į£¨≤Ę»°∂‘’’◊ťŌŗ∂‘”¶◊ť÷Į◊ųő™“ű–‘∂‘’’°£≤…”√Ķ¬ĻķBoenriger MannheimgsĻęňĺ ‘ľŃ,ĺŖŐŚŃų≥Ő£ļ◊ť÷Į«–∆¨≥£ĻśÕ—ņĮļů£¨Ķőľ”20 ¶Őg/mlĶįį◊√łK£¨ňę’Űňģ∆ĮŌī°£Ĺę—ý∆¨ĹĢ»ŽTdTĽļ≥Ś“ļ(30 mmol/L TrizmaĽýī°“ļ£¨pH 7.2£¨140 mmol/LŐľňŠ«‚ń∆∂Ģľ◊ŽŌňŠ—ő£¨1 mmol/L COCl2) °£‘Ŕ∑ű”ż”ŕTunel∑ī”¶“ļ(50 ¶Ől TdTĽļ≥Ś“ļ8.3U£¨TdT 1 nmolĶōłŖ–ŃĽýŐŚ11-dUTP)°£”√0.01 mol/LŃ◊ňŠ—őĽļ≥Ś“ļ(PBS)∆ĮŌīļů£¨Ķőľ”ľÓ–‘Ń◊ňŠ√ł£¨‘Ŕ”√PBS∆ĮŌī°£Ĺę—ý∆¨÷√”ŕľÓ–‘Ń◊ňŠ√łŌ‘…ęĶ◊őÔ(NBT/BCIP)“ļ÷–Ī‹Ļ‚Ō‘…ę£¨ļůňę’Űňģ÷’÷Ļ∑ī”¶°£ļňĻŐļžłī»ĺ£¨∑‚ĻŐ£¨Ō‘őĘĺĶĻŘ≤ž’’Ōŗ°£Õ¨ Ī◊ŲTunel∑®»ĺ…ę∂‘’’ ‘—ť£¨ Tunel∑ī”¶“ļ÷–≤Ľľ”TdT√ł°£
, įŔńī“Ĺ“©
Õľ1 Ķ—ť◊ťīů ůń‘∆§÷ (HIEļů18–° Ī)£¨Ņ…ľŻļňń§÷‹őß–ő≥…Őō’ų–‘Ľ∑◊ī÷¬√‹»ĺ…ę÷ (™“)£¨‘ŕŌłįŻÕ‚ĶńĶÚÕŲ–°ŐŚ(°Ł) Tunel °Ń400 Õľ2 ∂‘’’◊ťīů ůń‘∆§÷ £¨őīľŻ√ųŌ‘Ķń—Ű–‘ŌłįŻ Tunel °Ń200 Õľ3 Ķ—ť◊ťīů ůń‘ļ£¬Ū(HIEļů24–° Ī)£¨Ņ…ľŻ…Ůĺ≠‘™īů≤Ņ∑÷ļň»ĺ…ę—Ű–‘£¨ļňĻŐňű Tunel °Ń200
4.ĻŘ≤ž÷łĪÍ£ļ”√≤‚őĘÕÝľ∆ ż—Ű–‘ŌłįŻ ż£¨40°ŃńŅĺĶ£¨6łŲ ”“į£¨∂‘∆Ĺĺý1.0 mm2ńŕĶÚÕŲŌłįŻ ż£¨ĹÝ––ŇķľšĪ»ĹŌ£¨Sas-6.04»ŪľĢĹÝ––ī¶ņŪ°£
ĹŠ ĻŻ
“Ľ°ĘĻ‚ĺĶŌ¬ĻŘ≤ž
»Ī—ű»Ī—™1–° Ī Ķ—ť≤ŗ…Ůĺ≠ŌłįŻ“‘«Š∂»ňģ÷◊ő™÷ų°£18–° Ī∆§÷ °Ęļ£¬ŪĽō°Ę«ūń‘◊ť÷Į÷–ŌłįŻ≥ŲŌ÷ĶÚÕŲĶš–ÕĶń3÷÷Īš–‘–őŐ¨[3]£ļŌłįŻ÷Śňű£ĽŌłįŻļňĻŐňű£¨÷‹őß”–Ņ’Ň›–ő≥…£ĽŅ…ľŻļňňť∆¨£¨Ķ•łŲ‘≤–őĶÚÕŲ–°ŐŚ°£24–° Īļů…Ůĺ≠ŌłįŻňū…ňĹ•“‘ļň»‹Ĺ‚°Ęń§∆∆Ń—ľįĽĶňņő™÷ų°£72–° Īń‘◊ť÷Į÷–Ņ…ľŻĹÁŌř«Ś≥ĢĶńĽĶňņ‘Ó£¨įťňś…Ůĺ≠ŌłįŻňņÕŲ£¨≤Ņ∑÷◊ť÷Į‘Ų…ķĽÓ‘ĺ°£
, įŔńī“Ĺ“©
»Ī—ű»Ī—™ļů1–° Ī‘ŕ∆§÷ ≤ŅőĽľī≥ŲŌ÷ĶÚÕŲŌłįŻ£¨ő™11.1°ņ1.8łŲ/mm2£¨4–° Ī◊Ó√ųŌ‘ő™21.8°ņ1.7łŲ/mm2£ĽĶÚÕŲĶńłŖ∑Ś Īľš‘ľő™18–° Ī£¨ĶÚÕŲŌłįŻ żő™44°ņ4łŲ/mm2£Ľ24–° ĪŌ¬ĹĶĶĹ38°ņ3łŲ/mm2£¨40–° ĪŌ¬ĹĶĶĹ13.5°ņ1.2łŲ/mm2£¨7Őž“—«ų”ŕ’ż≥££¨ő™1.5°ņ0.8łŲ/mm2°£∂‘’’◊ťő™0.8°ņ0.4łŲ/mm2°£ŃĹŃĹĪ»ĹŌ£ļ≥ż1–° Ī”Ž40–° Ī◊ťP>0.05Õ‚£¨”ŗłų◊ť÷ģľšĺýP<0.001°£
∂Ģ°ĘĶÁĺĶŌ¬ĻŘ≤ž
4°ę24–° Ī◊ť Ķ—ť≤ŗ…Ůĺ≠ŌłįŻ‘ŕĶÁĺĶŌ¬Ō‘Ō÷ĶÚÕŲŐō’ų£¨“‘18–° Īő™÷Ý£ļļňń§÷Śňű°ĘŇ›◊īÕĽ∆ū£¨»ĺ…ę÷ ÷¬√‹£¨įŻĹ¨Ņ’Ň›√ųŌ‘£¨ńŕ÷ ÕÝ÷◊’Õ°£24–° Īļů…Ůĺ≠ŌłįŻ–őըŕ“‘ĽĶňņő™÷ų°£
»ż°Ę‘≠őĽTdT»ĪŅŕń©∂ňĪÍľ«
, įŔńī“Ĺ“©
łų◊ť Ķ—ť≤ŗĺýŅ…“‘ĻŘ≤žĶĹĶÚÕŲŌłįŻ°™°™DNA∆¨∂őń©∂ňĪÍľ«Ķń—Ű–‘ŌłįŻ(Õľ1°ę3)£¨1–° Ī∆§÷ ≤ŅőĽ—Ű–‘ŌłįŻő™14.6°ņ2.3łŲ/mm2£¨4–° Īő™34°ņ4łŲ/mm2£¨18–° Ī—Ű–‘ŌłįŻ≥ …Ó◊Ō…ę£¨«“∑∂őßĻ„ő™61°ņ6łŲ/mm2£¨24–° Īő™51°ņ6łŲ/mm2°£∂‘’’◊ť—Ű–‘–ŇļŇ≤Ľ√ųŌ‘£¨ő™0.8°ņ0.4łŲ/mm2°£ŃĹŃĹĪ»ĹŌ£¨łų◊ť÷ģľšĺýP<0.01°£Tunel∑®”ŽHE»ĺ…ę‘ŕHIEīů ůń‘ŌłįŻĶÚÕŲ Īľš°ĘŃų≥Ő…Ō∑ĹŌÚ“Ľ÷¬(Õľ4)°£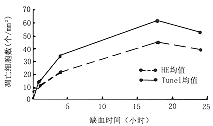
Õľ4 ŃĹ÷÷∑Ĺ∑®‘ŕŌŗÕ¨ ĪľšĶ„Ķńń‘∆§÷ ĶÚÕŲŌłįŻ żĪ»ĹŌ
Ő÷ ¬Ř
Ļż»•»Ōő™ń‘»Ī—™ļů…Ůĺ≠ŌłįŻňņÕŲ–ő Ĺ «ĽĶňņ°£◊‘1993ńÍņī”–Ī®Ķņ£¨≥… ž∂ĮőÔń‘»Ī—™ļů∑Ę…ķŌłįŻĶÚÕŲ£¨»Ī—™–‘ń‘ňū…ňń‘ŌłįŻňņÕŲīś‘ŕĽĶňņļÕĶÚÕŲŃĹ÷÷–ő Ĺ[4£¨5]°£Īĺ Ķ—ťňý”√ĶńTunel∑Ĺ∑®ĹŌ“Ľį„∑Ĺ∑®√Űł–£¨“Úő™∆šľž≤‚≥ŲĶńĶÚÕŲŌłįŻ‘Á”ŕ–őŐ¨—ßĶÚÕŲłńĪšļÕĶÚÕŲ–°ŐŚ–ő≥…°£
, įŔńī“Ĺ“©
ő“√«Õ®Ļż∂‘»Ī—ű»Ī—™ń‘ňū…ň–¬…ķīů ůń£–ÕĶńĻŘ≤ž£¨÷§ ĶŃň‘ŕHIE÷–īś‘ŕĶÚÕŲŌ÷Ōů°£≤Ę∑ĘŌ÷»Ī—ű3–° Īļů»Ī—™1–° ĪľīŅ…”–ŌłįŻļňń§∆ūŇ›°Ę»ĺ…ę÷ ńżľĮŌ÷Ōů°£ňś◊Ň»Ī—™ Īľš—”≥§£¨ĶÚÕŲŌłįŻ÷ūĹ•‘Ų∂ŗ£¨≥ŲŌ÷ŌłįŻĻŐňű°ĘĶÚÕŲ–°ŐŚĶ»ĶÚÕŲ÷–ÕŪ∆ŕ–őŐ¨Őō’ų£¨18–° ĪīÔłŖ∑Ś£¨24–° Īļůń‘ŌłįŻ–őŐ¨÷ū“‘ĽĶňņő™÷ų£¨40°ę72–° ĪĽĶňņ—Ō÷ō£¨72–° Ī°ę7ŐžĽĶňņĽ÷łī∆ŕ£¨ĶÚÕŲĪŪŌ÷÷ūĹ•ľű«ŠļÕŌŻ ß°£ŐŠ ĺ£¨‘ŕHIEń‘ňū…ň÷–…Ůĺ≠ŌłįŻňņÕŲ≤Ľ «ľÚĶ•ĶńĽĶňņ£¨∂Ýīś‘ŕłī‘”ĶńĶÚÕŲĻż≥Ő£Ľ Īľš«ķŌŖŌ‘ ĺ≥ŲĶÚÕŲ≥ŲŌ÷‘ŕ»Ī—ű»Ī—™ń‘ňū…ňĶń24–° Īńŕ£¨‘Á”ŕń‘ŌłįŻ√ųŌ‘ĽĶňņ÷ģ«į°£ĪŪ√ų£¨‘ŕHIE Īīś‘ŕĶÚÕŲļÕĽĶňņŃĹ÷÷≤ĽÕ¨ĶńŌłįŻňņÕŲĶń∑Ĺ Ĺ£¨īś‘ŕ◊Ň”’ĶľľŃŃŅŌŗĻō–‘°£
≤őŅľőńŌ◊
1 Hill IE, Macmanus JP, Rasquinha L, et al. DNA fragmentation indicative of apoptosis following unilateral cerebral hypoxia ischemia in the neonatal rat. Brain Res, 1995, 676£ļ398-403.
, įŔńī“Ĺ“©
2 Wijsman JH, Jonker RR, Keijzer R, et al. A new method to detect apoptosis in paraff insections: in situ end labeling of fragmented DNA.J Histochem Cytochem, 1993, 41£ļ7-12.
3 Charriaut Marlangue C, Margaill L, Represa A, et al. Apoptosis and necrosis after reversible focal ischemia. J Cereb Blood Flow Metab, 1996, 16£ļ186-194.
4 MacManus JP, Hill IE, Huang ZG, et al. DNA damage consistent with apoptosis in transient focal ischemic neocortex. Neuro report, 1994, 5£ļ493-496.
5 Sei Y, Von Lubitz KJ, Basile AS, et al. Internucleosomal DNA fragmentation in gerbil hippocampus following forebrain ischemia. Neurosci Lett, 1994, 171£ļ179-182.
( ’łŚ£ļ1997-11-10 –řĽō£ļ1998-02-23), http://www.100md.com
Ķ•őĽ£ļ210009 ńŌĺ©ŐķĶņ“Ĺ—ß‘ļłĹ Ű“Ĺ‘ļ∂ýŅ∆(ĹĮņÁ°ĘŐņ‘∆’š°Ę”Š”ĹĽ™°Ę…Ř–°ň…°Ę“◊őńŃķ)£ĽńŌĺ©ŐķĶņ“Ĺ—ß‘ļŅ∆—ß—–ĺŅňý∑÷◊”…ķőÔ—ß—–ĺŅ “(Ľ∆ŌĢ√ų°ĘļķŌÚ—Ű)£¨≤°ņŪ—ßĹŐ—– “(≥¬∆Ĺ •)
ĻōľŁī £ļń‘»Ī—ű£Ľń‘»Ī—™£ĽÕ— …◊ų”√£Ľīů ů
÷–Ľ™“Ĺ—ß‘”÷ĺ980802 °ĺ’™“™°Ņ ńŅĶń ŐĹŐ÷ń‘ŌłįŻĶÚÕŲ‘ŕ»Ī—ű»Ī—™ń‘≤°(HIE)∑Ę≤°ĽķņŪ÷–Ķń◊ų”√°£∑Ĺ∑® ”√HE»ĺ…ę°ĘĶÁĺĶ°Ę‘≠őĽń©∂ňĪÍľ«(Tunel) ÷∂ő£¨∑÷Īū∂‘»Ī—ű3–° Īļů»Ī—™1°Ę4°Ę18°Ę24°Ę40ľį72–° ĪļÕ7Őž◊ťīů ůĶńń‘◊ť÷Į÷–ĶÚÕŲŌłįŻĶń–őŐ¨°Ę≥ŲŌ÷ Īľšľį√‹∂»ĹÝ––ĻŘ≤žļÕĪ»ĹŌ°£ĹŠĻŻ Ļ‚°ĘĶÁĺĶŌ¬Ō‘ ĺ Ķ—ť≤ŗń‘∆§÷ °Ęļ£¬Ūľį«ūń‘…Ůĺ≠‘™÷Śňű°Ę»ĺ…ę÷ ńżľĮ≤Ę≥ŲŌ÷ĶÚÕŲ–°ŐŚ£ĽTunel∑Ĺ∑®÷§ Ķ”–Ń—Ĺ‚DNAīś‘ŕ£Ľ»Ī—ű»Ī—™ļů18–° Ī∆§÷ ĶÚÕŲ◊Ó√ųŌ‘°£ĹŠ¬Ř ‘ŕHIEīů ů£¨ń‘ŌłįŻĶÚÕŲ≥ŲŌ÷≤ĽĶę‘Á”ŕĽĶňņ£¨∂Ý«“”ŽĽĶňņīś‘ŕ◊Ň”’ĶľľŃŃŅŌŗĻō–‘°£
, įŔńī“Ĺ“©
Brain cell apoptosis after cerebral hypoxia-ischemia in neonatal rat Jiang Li, Tang Yunzhen, Huang Xiaoming, et al. Department of Pediatrics, Nanjing Railway Medical college, Nanjing 210009
°ĺAbstract°Ņ Objective To investigate action of apoptosis in mechanisms of neonatal hypoxia-ischemia(HIE). Methods Using HE staining, electronmicroscope, and terminal deoxynuleotidyl transferase-mediated dUTP nick end labeling (TUNEL) technique, we observed the histological features, time course and density of apoptotic cells and compared the ipsilateral hemisphere after permanent ischemia 1, 4, 18, 24, 40, 72h, 7 days after 3h hypoxia with that of sham-group. Results Neurons in the cortex, hippocampus, thalamus exhibited cells shrink, chromatin condensation, apoptosis bodys under microscope, as demonstrated by in situ labeling of DNA breaks. The peak for apoptosis was shown at 18h in the cortex. Conclusion In the HIE, apoptosis appears earlier than necrosis, and both of the different cell death forms may exist induced dose relativity.
, įŔńī“Ĺ“©
°ĺKey words°Ņ Cerebral anoxia Cerebral ischemia Apoptosis Rats
(Natl Med J China, 1998, 78£ļ567-569)
īęÕ≥ĻŘĶ„»Ōő™£¨–¬…ķ∂ý»Ī—ű»Ī—™ń‘≤°(HIE) «”…”ŕľĪ–‘ń‘ňģ÷◊°ĘĽĶňņňý÷¬°£Īĺ—–ĺŅ÷ľ‘ŕĹ®ŃĘHIEĶń∂ĮőÔń£–Õ£¨ĻŘ≤žń‘ňū…ň÷–ń‘ŌłįŻňņÕŲĶńŃŪ“Ľ÷÷–ő Ĺ°™°™ŌłįŻĶÚÕŲ£¨ő™ŐĹŐ÷HIEĶń∑Ę≤°ĽķņŪŐŠĻ©“ņĺ›°£
≤ńŃŌļÕ∑Ĺ∑®
“Ľ°Ę≤ńŃŌ
ń£–Õ÷∆Īł£ļ–¬…ķ7ŐžĶńSDīů ů72÷Ľ£¨ňśĽķ∑÷ő™9◊ť£¨∆š÷–2◊ť∑÷Īūő™∂‘’’◊ťļÕľŔ ÷ ű◊ť(ĹŲ”őņŽ≥ŲĺĪ∂Į¬Ų£¨≤Ľ◊ŲĹŠ‘ķ)£¨∆š”ŗ7◊ťįī RiceĶ»[1]∑Ĺ∑®––◊ůĺĪ∂Į¬ŲĹŠ‘ķ űļů÷√”ŕ8%—ű∆Ý÷–3–° Īļů£¨∑÷Īū”ŕĹŠ‘ķļů1°Ę4°Ę18°Ę24°Ę40ļÕ72–° Īľį7Őž(∂‘’’ļÕľŔ ÷ ű◊ťÕ¨”ŕ18–° Ī)£¨ĺ≠–ń‘ŗ≤ŚĻ‹£¨…ķņŪ—őňģ≥ŚŌī£¨ļůĻŗ»Ž4 %∂ŗĺŘľ◊»©£¨ĻŗĪŌľī»°◊ůń‘£¨Õ‚ĻŐ∂®°£
, įŔńī“Ĺ“©
∂Ģ°Ę∑Ĺ∑®
1.Ļ‚ĺĶľž≤ť£ļ»°«ūń‘÷–1/3∆Ĺ√ś––Ļŕ◊ī«–∆¨£¨∆¨ļŮ5 ¶Őm£¨ ĮņĮįŁ¬Ů£¨HE»ĺ…ę£¨Ļ‚ĺĶľž≤ť°£
2.≥¨őĘĹŠĻĻĻŘ≤ž£ļ‘ŕĻ‚ĺĶľž≤ťĶń»°≤ń≤ŅőĽ£¨»°∆§÷ °Ęļ£¬Ū°Ę«ūń‘◊ť÷Į£¨≥£ĻśĻŐ∂®°ĘįŁ¬Ů°Ę«–∆¨°Ę»ĺ…ę£¨Õł ”ĶÁĺĶŌ¬ĻŘ≤ž°Ę…„∆¨°£
3.‘≠őĽń©∂ňÕ——űļň‹’ňŠ◊™“∆√ł(TdT)ĪÍľ«∑®(Tunel)[2]£ļ«–∆¨◊ŲHE»ĺ…ęĻ‚ĺĶĻŘ≤žļů£¨ŃŕĹŁī¶Ķń ĮņĮ«–∆¨∂®ő™ĪÍľ«į–◊ť÷Į£¨≤Ę»°∂‘’’◊ťŌŗ∂‘”¶◊ť÷Į◊ųő™“ű–‘∂‘’’°£≤…”√Ķ¬ĻķBoenriger MannheimgsĻęňĺ ‘ľŃ,ĺŖŐŚŃų≥Ő£ļ◊ť÷Į«–∆¨≥£ĻśÕ—ņĮļů£¨Ķőľ”20 ¶Őg/mlĶįį◊√łK£¨ňę’Űňģ∆ĮŌī°£Ĺę—ý∆¨ĹĢ»ŽTdTĽļ≥Ś“ļ(30 mmol/L TrizmaĽýī°“ļ£¨pH 7.2£¨140 mmol/LŐľňŠ«‚ń∆∂Ģľ◊ŽŌňŠ—ő£¨1 mmol/L COCl2) °£‘Ŕ∑ű”ż”ŕTunel∑ī”¶“ļ(50 ¶Ől TdTĽļ≥Ś“ļ8.3U£¨TdT 1 nmolĶōłŖ–ŃĽýŐŚ11-dUTP)°£”√0.01 mol/LŃ◊ňŠ—őĽļ≥Ś“ļ(PBS)∆ĮŌīļů£¨Ķőľ”ľÓ–‘Ń◊ňŠ√ł£¨‘Ŕ”√PBS∆ĮŌī°£Ĺę—ý∆¨÷√”ŕľÓ–‘Ń◊ňŠ√łŌ‘…ęĶ◊őÔ(NBT/BCIP)“ļ÷–Ī‹Ļ‚Ō‘…ę£¨ļůňę’Űňģ÷’÷Ļ∑ī”¶°£ļňĻŐļžłī»ĺ£¨∑‚ĻŐ£¨Ō‘őĘĺĶĻŘ≤ž’’Ōŗ°£Õ¨ Ī◊ŲTunel∑®»ĺ…ę∂‘’’ ‘—ť£¨ Tunel∑ī”¶“ļ÷–≤Ľľ”TdT√ł°£

, įŔńī“Ĺ“©
Õľ1 Ķ—ť◊ťīů ůń‘∆§÷ (HIEļů18–° Ī)£¨Ņ…ľŻļňń§÷‹őß–ő≥…Őō’ų–‘Ľ∑◊ī÷¬√‹»ĺ…ę÷ (™“)£¨‘ŕŌłįŻÕ‚ĶńĶÚÕŲ–°ŐŚ(°Ł) Tunel °Ń400 Õľ2 ∂‘’’◊ťīů ůń‘∆§÷ £¨őīľŻ√ųŌ‘Ķń—Ű–‘ŌłįŻ Tunel °Ń200 Õľ3 Ķ—ť◊ťīů ůń‘ļ£¬Ū(HIEļů24–° Ī)£¨Ņ…ľŻ…Ůĺ≠‘™īů≤Ņ∑÷ļň»ĺ…ę—Ű–‘£¨ļňĻŐňű Tunel °Ń200
4.ĻŘ≤ž÷łĪÍ£ļ”√≤‚őĘÕÝľ∆ ż—Ű–‘ŌłįŻ ż£¨40°ŃńŅĺĶ£¨6łŲ ”“į£¨∂‘∆Ĺĺý1.0 mm2ńŕĶÚÕŲŌłįŻ ż£¨ĹÝ––ŇķľšĪ»ĹŌ£¨Sas-6.04»ŪľĢĹÝ––ī¶ņŪ°£
ĹŠ ĻŻ
“Ľ°ĘĻ‚ĺĶŌ¬ĻŘ≤ž
»Ī—ű»Ī—™1–° Ī Ķ—ť≤ŗ…Ůĺ≠ŌłįŻ“‘«Š∂»ňģ÷◊ő™÷ų°£18–° Ī∆§÷ °Ęļ£¬ŪĽō°Ę«ūń‘◊ť÷Į÷–ŌłįŻ≥ŲŌ÷ĶÚÕŲĶš–ÕĶń3÷÷Īš–‘–őŐ¨[3]£ļŌłįŻ÷Śňű£ĽŌłįŻļňĻŐňű£¨÷‹őß”–Ņ’Ň›–ő≥…£ĽŅ…ľŻļňňť∆¨£¨Ķ•łŲ‘≤–őĶÚÕŲ–°ŐŚ°£24–° Īļů…Ůĺ≠ŌłįŻňū…ňĹ•“‘ļň»‹Ĺ‚°Ęń§∆∆Ń—ľįĽĶňņő™÷ų°£72–° Īń‘◊ť÷Į÷–Ņ…ľŻĹÁŌř«Ś≥ĢĶńĽĶňņ‘Ó£¨įťňś…Ůĺ≠ŌłįŻňņÕŲ£¨≤Ņ∑÷◊ť÷Į‘Ų…ķĽÓ‘ĺ°£
, įŔńī“Ĺ“©
»Ī—ű»Ī—™ļů1–° Ī‘ŕ∆§÷ ≤ŅőĽľī≥ŲŌ÷ĶÚÕŲŌłįŻ£¨ő™11.1°ņ1.8łŲ/mm2£¨4–° Ī◊Ó√ųŌ‘ő™21.8°ņ1.7łŲ/mm2£ĽĶÚÕŲĶńłŖ∑Ś Īľš‘ľő™18–° Ī£¨ĶÚÕŲŌłįŻ żő™44°ņ4łŲ/mm2£Ľ24–° ĪŌ¬ĹĶĶĹ38°ņ3łŲ/mm2£¨40–° ĪŌ¬ĹĶĶĹ13.5°ņ1.2łŲ/mm2£¨7Őž“—«ų”ŕ’ż≥££¨ő™1.5°ņ0.8łŲ/mm2°£∂‘’’◊ťő™0.8°ņ0.4łŲ/mm2°£ŃĹŃĹĪ»ĹŌ£ļ≥ż1–° Ī”Ž40–° Ī◊ťP>0.05Õ‚£¨”ŗłų◊ť÷ģľšĺýP<0.001°£
∂Ģ°ĘĶÁĺĶŌ¬ĻŘ≤ž
4°ę24–° Ī◊ť Ķ—ť≤ŗ…Ůĺ≠ŌłįŻ‘ŕĶÁĺĶŌ¬Ō‘Ō÷ĶÚÕŲŐō’ų£¨“‘18–° Īő™÷Ý£ļļňń§÷Śňű°ĘŇ›◊īÕĽ∆ū£¨»ĺ…ę÷ ÷¬√‹£¨įŻĹ¨Ņ’Ň›√ųŌ‘£¨ńŕ÷ ÕÝ÷◊’Õ°£24–° Īļů…Ůĺ≠ŌłįŻ–őըŕ“‘ĽĶňņő™÷ų°£
»ż°Ę‘≠őĽTdT»ĪŅŕń©∂ňĪÍľ«
, įŔńī“Ĺ“©
łų◊ť Ķ—ť≤ŗĺýŅ…“‘ĻŘ≤žĶĹĶÚÕŲŌłįŻ°™°™DNA∆¨∂őń©∂ňĪÍľ«Ķń—Ű–‘ŌłįŻ(Õľ1°ę3)£¨1–° Ī∆§÷ ≤ŅőĽ—Ű–‘ŌłįŻő™14.6°ņ2.3łŲ/mm2£¨4–° Īő™34°ņ4łŲ/mm2£¨18–° Ī—Ű–‘ŌłįŻ≥ …Ó◊Ō…ę£¨«“∑∂őßĻ„ő™61°ņ6łŲ/mm2£¨24–° Īő™51°ņ6łŲ/mm2°£∂‘’’◊ť—Ű–‘–ŇļŇ≤Ľ√ųŌ‘£¨ő™0.8°ņ0.4łŲ/mm2°£ŃĹŃĹĪ»ĹŌ£¨łų◊ť÷ģľšĺýP<0.01°£Tunel∑®”ŽHE»ĺ…ę‘ŕHIEīů ůń‘ŌłįŻĶÚÕŲ Īľš°ĘŃų≥Ő…Ō∑ĹŌÚ“Ľ÷¬(Õľ4)°£

Õľ4 ŃĹ÷÷∑Ĺ∑®‘ŕŌŗÕ¨ ĪľšĶ„Ķńń‘∆§÷ ĶÚÕŲŌłįŻ żĪ»ĹŌ
Ő÷ ¬Ř
Ļż»•»Ōő™ń‘»Ī—™ļů…Ůĺ≠ŌłįŻňņÕŲ–ő Ĺ «ĽĶňņ°£◊‘1993ńÍņī”–Ī®Ķņ£¨≥… ž∂ĮőÔń‘»Ī—™ļů∑Ę…ķŌłįŻĶÚÕŲ£¨»Ī—™–‘ń‘ňū…ňń‘ŌłįŻňņÕŲīś‘ŕĽĶňņļÕĶÚÕŲŃĹ÷÷–ő Ĺ[4£¨5]°£Īĺ Ķ—ťňý”√ĶńTunel∑Ĺ∑®ĹŌ“Ľį„∑Ĺ∑®√Űł–£¨“Úő™∆šľž≤‚≥ŲĶńĶÚÕŲŌłįŻ‘Á”ŕ–őŐ¨—ßĶÚÕŲłńĪšļÕĶÚÕŲ–°ŐŚ–ő≥…°£
, įŔńī“Ĺ“©
ő“√«Õ®Ļż∂‘»Ī—ű»Ī—™ń‘ňū…ň–¬…ķīů ůń£–ÕĶńĻŘ≤ž£¨÷§ ĶŃň‘ŕHIE÷–īś‘ŕĶÚÕŲŌ÷Ōů°£≤Ę∑ĘŌ÷»Ī—ű3–° Īļů»Ī—™1–° ĪľīŅ…”–ŌłįŻļňń§∆ūŇ›°Ę»ĺ…ę÷ ńżľĮŌ÷Ōů°£ňś◊Ň»Ī—™ Īľš—”≥§£¨ĶÚÕŲŌłįŻ÷ūĹ•‘Ų∂ŗ£¨≥ŲŌ÷ŌłįŻĻŐňű°ĘĶÚÕŲ–°ŐŚĶ»ĶÚÕŲ÷–ÕŪ∆ŕ–őŐ¨Őō’ų£¨18–° ĪīÔłŖ∑Ś£¨24–° Īļůń‘ŌłįŻ–őŐ¨÷ū“‘ĽĶňņő™÷ų£¨40°ę72–° ĪĽĶňņ—Ō÷ō£¨72–° Ī°ę7ŐžĽĶňņĽ÷łī∆ŕ£¨ĶÚÕŲĪŪŌ÷÷ūĹ•ľű«ŠļÕŌŻ ß°£ŐŠ ĺ£¨‘ŕHIEń‘ňū…ň÷–…Ůĺ≠ŌłįŻňņÕŲ≤Ľ «ľÚĶ•ĶńĽĶňņ£¨∂Ýīś‘ŕłī‘”ĶńĶÚÕŲĻż≥Ő£Ľ Īľš«ķŌŖŌ‘ ĺ≥ŲĶÚÕŲ≥ŲŌ÷‘ŕ»Ī—ű»Ī—™ń‘ňū…ňĶń24–° Īńŕ£¨‘Á”ŕń‘ŌłįŻ√ųŌ‘ĽĶňņ÷ģ«į°£ĪŪ√ų£¨‘ŕHIE Īīś‘ŕĶÚÕŲļÕĽĶňņŃĹ÷÷≤ĽÕ¨ĶńŌłįŻňņÕŲĶń∑Ĺ Ĺ£¨īś‘ŕ◊Ň”’ĶľľŃŃŅŌŗĻō–‘°£
≤őŅľőńŌ◊
1 Hill IE, Macmanus JP, Rasquinha L, et al. DNA fragmentation indicative of apoptosis following unilateral cerebral hypoxia ischemia in the neonatal rat. Brain Res, 1995, 676£ļ398-403.
, įŔńī“Ĺ“©
2 Wijsman JH, Jonker RR, Keijzer R, et al. A new method to detect apoptosis in paraff insections: in situ end labeling of fragmented DNA.J Histochem Cytochem, 1993, 41£ļ7-12.
3 Charriaut Marlangue C, Margaill L, Represa A, et al. Apoptosis and necrosis after reversible focal ischemia. J Cereb Blood Flow Metab, 1996, 16£ļ186-194.
4 MacManus JP, Hill IE, Huang ZG, et al. DNA damage consistent with apoptosis in transient focal ischemic neocortex. Neuro report, 1994, 5£ļ493-496.
5 Sei Y, Von Lubitz KJ, Basile AS, et al. Internucleosomal DNA fragmentation in gerbil hippocampus following forebrain ischemia. Neurosci Lett, 1994, 171£ļ179-182.
( ’łŚ£ļ1997-11-10 –řĽō£ļ1998-02-23), http://www.100md.com