急性非甲-戊型肝炎患者血清庚型肝炎病毒核酸的检测
作者:李卓 王佑春 郝娃 牛京勤 武志明
单位:100054 北京市卫生局肝炎研究所(李卓、郝娃、牛京勤、武志明);中国药品生物制品检定所(王佑春)
关键词:
中华医学杂志980823 我们采用酶联免疫吸附方法(ELISA)检测了非甲-戊型肝炎患者的血清抗庚型肝炎病毒抗体(抗HGV),以逆转录套式聚合酶链反应(RT-PCR)检测抗HGV阳性血清HGV RNA。
一、对象与方法
1.病例及血清标本来源:25例急性非甲-戊型肝炎患者均为1996年5月至1997年5月北京佑安医院住院患者。临床诊断符合1995年全国传染病与寄生虫病学术会议制定的诊断标准。患者入院后采集血清置于-20 ℃冰箱保存。
, 百拇医药
2.引物设计:根据HGV序列(Gen Bank accession number U44402)在5′非编码区设计2对套式PCR引物,外引物正向序列为:AAG TCC TGG TAT GGG TGAT,反向序列为:TTCC GGG TGA GGG CGGG TGGCA;内引物正向序列为:TGG TAG GTC GTA AAT CCC GGT,反向序列为:ATG CAT GGG GCC ACC CAG CTCC。内引物扩增产物为300 bp核苷酸。
3.核酸提取:cDNA合成和扩增参照文献[1]的方法。扩增产物经2%琼脂糖凝胶电泳检测。
4.HGV基因序列测定:PCR产物直接测定序列,将提取的DNA直接克隆到TA Cloning Kit中的PCR Ⅱ质粒中,用USB测序试剂盒测定序列,全部操作按说明书进行。
5.抗HGV检测:抗HGV检测试剂由北京维康瑞公司馈赠。
, 百拇医药
二、结果
1.抗HGV水平检测:25例患者中,8例血清抗HGV阳性。
2.RT-PCR检测:对8例抗HGV阳性患者血清进行了HGV RNA检测,3例阳性,其扩增结果见附图。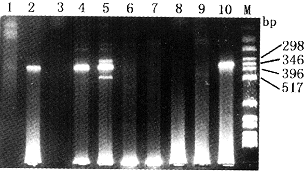
1.4~10患者血清标本;2.阳性对照;3.阴性对照;M.DNA分子量标准
附图 RT-PCR扩增产物图谱
3.HGV 5′非编码区基因序列分析:所测定的HGV 5′非编码区核苷酸序列与美国株HGV U 44402和HGV U 45966的比较,主要的变异在400~430 bp位置,其变异是以密码子的第3位核苷酸的替换为主,其氨基酸编码未发生变化。核苷酸水平的同源性分别为95%和97.8%。
, http://www.100md.com
三、讨论
近年来,在用敏感的方法排除了甲、乙、丙、丁、戊型肝炎病毒感染之后,仍有10%~15%的非甲-戊型的肝炎患者,因而提示可能有其他导致人类肝炎的病毒因子存在。1995年Simons与Linnen[2,3]分别从肝炎患者的血清中克隆出GBV-C和HGV病毒基因,证明HGV/GBV-C为正链RNA病毒。Mukaide等[4]搜集了16个国家146份血清进行HGV 5′非编码区序列测定,进行种系分析,认为可以分为3个亚型:(1) GBV-C可见于非洲、北美、亚洲及欧洲;(2) 新组主要见于亚洲及欧洲;(3) HGV主要见于欧洲、亚洲及洲,并认为HGV的演化较GBV-C为迟。对于HGN/GBV-C的诊断目前主要采用5′端非编码区的RT-PCR测定、HGV5′端是较为保守的非编码区,核苷酸的插入或缺失突变,可能引起多聚蛋白读码框架的转换。
在急性非甲-戊型肝炎患者中约8.7% HGV RNA阳性[4],本组结果显示了与美国株HGV的同源性高达95%,表明了在急性肝炎患者之中确有HGV感染存在,它是非甲-戊型肝炎的病源体之一。5例抗HGV阳性而PCR阴性的病例,可能是由于其他病毒性因素排除不够或病毒本身的变异以及感染人群取血时间的差异等因素所造成,也可能由于选择不同的多肽抗原进行酶联免疫吸附试验测定血清抗体只能作为一种感染指标,而不代表病毒复制,所以,对病毒复制的血清学诊断有待进一步研究。
, 百拇医药
参考文献
1 周育生,王海涛,唐时幸,等.中国人庚型肝炎病毒部分基因克隆和序列测定.军事医学科学院院刊,1996,20:160-162.
2 Simons JN, Leary TP, Dawson GJ, et al. Isolation of novel virus like sequences associated with human hepatitis. Nature Med, 1995, 1:564-565.
3 Linnen J, Wages J, Zhang-keck ZX, et al. Molecular cloning and disease association of hepatitis G virus: a transfusion transmissible agent. Science, 1996, 271:505-508.
4 Mukaide M, Mijokami M, Oritk E, et al. There are three subtypes of GB virus C hepatitis G virus (HGV): geographic distribution and HGV RNA levels. Hepatology, 1996, 24(4pt2) 287A:643.
(收稿:1997-09-30 修回:1998-04-15), 百拇医药
单位:100054 北京市卫生局肝炎研究所(李卓、郝娃、牛京勤、武志明);中国药品生物制品检定所(王佑春)
关键词:
中华医学杂志980823 我们采用酶联免疫吸附方法(ELISA)检测了非甲-戊型肝炎患者的血清抗庚型肝炎病毒抗体(抗HGV),以逆转录套式聚合酶链反应(RT-PCR)检测抗HGV阳性血清HGV RNA。
一、对象与方法
1.病例及血清标本来源:25例急性非甲-戊型肝炎患者均为1996年5月至1997年5月北京佑安医院住院患者。临床诊断符合1995年全国传染病与寄生虫病学术会议制定的诊断标准。患者入院后采集血清置于-20 ℃冰箱保存。
, 百拇医药
2.引物设计:根据HGV序列(Gen Bank accession number U44402)在5′非编码区设计2对套式PCR引物,外引物正向序列为:AAG TCC TGG TAT GGG TGAT,反向序列为:TTCC GGG TGA GGG CGGG TGGCA;内引物正向序列为:TGG TAG GTC GTA AAT CCC GGT,反向序列为:ATG CAT GGG GCC ACC CAG CTCC。内引物扩增产物为300 bp核苷酸。
3.核酸提取:cDNA合成和扩增参照文献[1]的方法。扩增产物经2%琼脂糖凝胶电泳检测。
4.HGV基因序列测定:PCR产物直接测定序列,将提取的DNA直接克隆到TA Cloning Kit中的PCR Ⅱ质粒中,用USB测序试剂盒测定序列,全部操作按说明书进行。
5.抗HGV检测:抗HGV检测试剂由北京维康瑞公司馈赠。
, 百拇医药
二、结果
1.抗HGV水平检测:25例患者中,8例血清抗HGV阳性。
2.RT-PCR检测:对8例抗HGV阳性患者血清进行了HGV RNA检测,3例阳性,其扩增结果见附图。

1.4~10患者血清标本;2.阳性对照;3.阴性对照;M.DNA分子量标准
附图 RT-PCR扩增产物图谱
3.HGV 5′非编码区基因序列分析:所测定的HGV 5′非编码区核苷酸序列与美国株HGV U 44402和HGV U 45966的比较,主要的变异在400~430 bp位置,其变异是以密码子的第3位核苷酸的替换为主,其氨基酸编码未发生变化。核苷酸水平的同源性分别为95%和97.8%。
, http://www.100md.com
三、讨论
近年来,在用敏感的方法排除了甲、乙、丙、丁、戊型肝炎病毒感染之后,仍有10%~15%的非甲-戊型的肝炎患者,因而提示可能有其他导致人类肝炎的病毒因子存在。1995年Simons与Linnen[2,3]分别从肝炎患者的血清中克隆出GBV-C和HGV病毒基因,证明HGV/GBV-C为正链RNA病毒。Mukaide等[4]搜集了16个国家146份血清进行HGV 5′非编码区序列测定,进行种系分析,认为可以分为3个亚型:(1) GBV-C可见于非洲、北美、亚洲及欧洲;(2) 新组主要见于亚洲及欧洲;(3) HGV主要见于欧洲、亚洲及洲,并认为HGV的演化较GBV-C为迟。对于HGN/GBV-C的诊断目前主要采用5′端非编码区的RT-PCR测定、HGV5′端是较为保守的非编码区,核苷酸的插入或缺失突变,可能引起多聚蛋白读码框架的转换。
在急性非甲-戊型肝炎患者中约8.7% HGV RNA阳性[4],本组结果显示了与美国株HGV的同源性高达95%,表明了在急性肝炎患者之中确有HGV感染存在,它是非甲-戊型肝炎的病源体之一。5例抗HGV阳性而PCR阴性的病例,可能是由于其他病毒性因素排除不够或病毒本身的变异以及感染人群取血时间的差异等因素所造成,也可能由于选择不同的多肽抗原进行酶联免疫吸附试验测定血清抗体只能作为一种感染指标,而不代表病毒复制,所以,对病毒复制的血清学诊断有待进一步研究。
, 百拇医药
参考文献
1 周育生,王海涛,唐时幸,等.中国人庚型肝炎病毒部分基因克隆和序列测定.军事医学科学院院刊,1996,20:160-162.
2 Simons JN, Leary TP, Dawson GJ, et al. Isolation of novel virus like sequences associated with human hepatitis. Nature Med, 1995, 1:564-565.
3 Linnen J, Wages J, Zhang-keck ZX, et al. Molecular cloning and disease association of hepatitis G virus: a transfusion transmissible agent. Science, 1996, 271:505-508.
4 Mukaide M, Mijokami M, Oritk E, et al. There are three subtypes of GB virus C hepatitis G virus (HGV): geographic distribution and HGV RNA levels. Hepatology, 1996, 24(4pt2) 287A:643.
(收稿:1997-09-30 修回:1998-04-15), 百拇医药