人巨细胞病毒促进HPV16永生化的宫颈皮细胞癌变研究
作者:刘朝奇 李 昆 司静懿 刘世德 宋国兴
单位:刘朝奇:湖北三峡学院医学院微生物学教研室(宜昌 443003);李 昆 司静懿 刘世德 宋国兴:中国医学科学院协和医科大学基础医学研究所
关键词:宫颈肿瘤;人乳头瘤病毒;人巨细胞病毒;肿瘤发生;上皮细胞
家用医学进修杂志990107
摘 要 目的:探讨宫颈癌的发生发展与人乳头瘤病毒(HPV)和人巨细胞病毒(HCMV)协同感染的关系。方法:本实验应用我室建立的HPV16永生化的人宫颈上皮细胞系,转染HCMV 即早基因(IE)。结果:HCMV整合在细胞染色体中,协同HPV16促进宫颈上皮细胞的恶性转化,在裸鼠中形成肿瘤。结论:HCMV IE基因可协同HPV16恶性转化宫颈上皮细胞,并对其协同机制进行了细胞和分子生物学的探讨。
, 百拇医药
Cellular and Molecular Biological Research on the Oncogenesis
of Cervical Epithelial Cells Coinduced
by Human Papillomavirus and Human Cytomegalovirus
Liu Chaoqi Li Kun Si Jinyi, et al
Department of Microbiology, Hubei Three Gorges University Medical College,Yichang 443003
Abstract Objective:The carcinogenesis of the human uterine cervical carcinoma is closely associated with human papillomavirus (HPV). The purpose of this article is to identify whether another sexually transmitted factor, human cytomegalovirus (HCMV) plays as a co-factor role in the carcinogenesis.Methods:Human cervical epithelial cells immortalized by HPV16 were transferred with the IE gene of HCMV. The condition and efficiency of IE gene were examined. Results:It was showed that the cervical epithelial cells could be completely transformed by HPV16 and IE gene of HCMV. The tumor was formed by injecting the transformed cells in nude mice.Conclusion:The co-operation of HPV and HCMV was observed in oncogenesis of human cervical carcinoma and moreover the cellular and molecular biological mechanism was discussed.
, 百拇医药
Key Words cervix neoplasm;HPV;HCMV;oncogenesis;epithelial cells
宫颈癌是女性生殖系统最常见的恶性肿瘤,在世界范围内其发病率仅次于乳腺癌据第二位,且引起较高的死亡率[1],是危害我国妇女的主要恶性肿瘤之一。因此宫颈癌的病因及其发病机制的研究一直受到国内外学者的高度重视,特别是近十几年来宫颈癌的病因及癌变机理的研究获得突破性的进展,人乳头瘤病毒(human papillomavirus,HPV)作为宫颈癌的主要致癌因素已得到大多数学者的公认[2]。笔者从流行病学、细胞及分子生物学亦作了大量证实[3]。体外细胞转化研究发现HPV仅能诱导人正常上皮细胞的永生化而不能使之充分恶性转化。因而HPV并非宫颈癌发生发展的唯一因素[4]。近几年来HPV与其它性传播因子,如HCMV在宫颈癌发生发展中作用的关系引起部分学者关注[5]。本课题应用本室建立的HPV16永生化的宫颈鳞状上皮细胞为模型,研究HCMV的即早基因(immediate early gene,IE)在癌变发生发展中的相互作用。
, http://www.100md.com
1 材料和方法
1.1 质粒DNA的制备和纯化
质粒pSV2 IE2和pHaMDR DNA(美国Fred Hutchinson Cancer Research Center 的Galloway教授惠赠)按常规方法(碱裂解法)。酶切鉴定后,取适量质粒DNA于Eppendorf管中,75%乙醇灭菌一定时间后,于无菌条件下干燥,溶于适量无菌去离子水中,测吸光度值定量。
1.2 细胞H8
细胞是取材于中国妇女宫颈鳞柱状上皮交界处之鳞状上皮,原代细胞培养,经HPV16 E6E7基因转化,形成永生化细胞。在本室已传代300代以上。
1.3 细胞磷酸钙介导的DNA转染及转染后克隆的筛选[6]
, 百拇医药
将H8细胞复苏后,于37℃,5%CO2饱和湿度下用无血清培养基培养。转染前24小时将细胞以1~2×105/cm2的密度接种于60mm培养皿,培养24小时,并于转染前4小时更换细胞培养液,使每一培养皿内的培养液为5ml。用一无菌透明玻璃管,加入220ul(20ug/ml)含pSV2 IE2和pHaMDR筛选标记质粒的溶液共转染,加入250ul 2XHBS(280mM NaCl,10mM KCl,1.5mM Na2HPO4,12mM葡萄糖,50mM HEPES,pH7.05),然后缓慢加入31ul 2Mol/L CaCl2,轻混30秒,置于室温孵育20~30分钟,将此磷酸钙-DNA悬液移入60mm培养皿中混匀,37℃,5%CO2培养箱中继续培养6小时,甘油休克2分钟后,加入培养液继续培养。48小时后,按1∶5传代,加入秋水仙素进行筛选,待长成克隆后,挑取克隆于24孔板继续培养。
, 百拇医药
1.4 细胞生长速度测定
将2×104/ml细胞接种于培养皿中,培养3天后,进行细胞计数,测定细胞的饱和密度。
1.5 软琼脂集落形成观察[7]
制备0.6%底层琼脂,消化处于对数生长期细胞,制成5×103/ml。将0.7%的琼脂和2×RPMI1640完全培养液以1∶1的比例混合,从中取3ml与0.2ml上述克隆的细胞悬液混合,将其铺于培养皿中的底层琼脂之上,37℃,5%CO2温箱中培养。二周后观察并计数细胞集落(含20个细胞以上者为一集落)然后按下列公式计算克隆形成率(colonyforming efficiency,CPE):CPE=形成细胞数/接种细胞数×100
1.6 裸鼠接种成瘤实验
, http://www.100md.com
将处于对数生长期的细胞经生理盐水清洗后,胰酶消化,计数,制备1~2×107细胞/ml细胞悬液,然后将0.25ml此细胞悬液接种于裸鼠背部,观察射部位有无肿瘤形成及其大小、形状。
1.7 Southen杂交[8]
取生长的肿瘤组织和培养的细胞,常规法提取基因组DNA,溶于适量TrisEDTA(pH8.0)中,测吸光度值进行定量后,贮存于4℃备用。基因组DNA EcoRI酶切后,DNA从琼脂糖凝胶转移到硝酸纤维素膜,随机引物法标记探针,68℃水浴杂交24小时,洗膜,放射自显影。
1.8 光学显微镜标本制备及观察
裸鼠被处死后立即取小块肿瘤组织放入Bouin's固定液中于4℃固定,常规HE染色后,观察、照相。
, 百拇医药 2 结果
2.1 质粒pSV2 IE2及pHaMDR的鉴定
pSV2 IE2经EcoRI酶切,琼脂糖凝胶电泳,可见2.9Kb的IE2基因和4.84Kb pSV2两条带(图1,本文附图均见封4,略),pHaMDR经BamHI或HindⅢ酶切琼脂糖电泳分别呈现两条或四条带(图2,略)。上述质粒限制内切酶鉴定结果与质粒图谱提供内容相符。
图1 pSV2IE2的酶切鉴定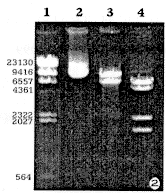
图2 pHaMDR的酶切鉴定
2.2 HCMV即早基因(IE2)恶性转化
, 百拇医药
HPV-16亚基因永生化的人宫颈上皮细胞。将含HCMV即早基因(pSV2 IE2)与表达多耐药基因的pHaMDR的质粒共转染入HPV-16亚基因永生化的H8细胞后,经秋水仙素筛选,约两周后正常H8细胞及单纯转染空载的细胞全部死亡,而转染pSV2IE2/pHaMDR及pHaMDR的细胞仍有散在细胞存活,经两周左右继续培养可见阳性克隆扩大培养后形成转化后细胞株,pSV2 IE2转染细胞命名为HE2。
2.3 细胞生长特性观察
H8和HE2细胞在相同条件下培养生长,发现细胞饱和密度H8细胞为2.1×106±5.8×105/cm2,而HE2细胞为6.5×106±6.3×105/cm2。在双层软琼脂培养中,HE2细胞在两周后可见集落形成,其集落形成率为28.8%,H8细胞的约0.9%。将细胞接种入裸鼠体内。结果发现HE2细胞系在接种二周后出现肿块并迅速增大(图3,略),而单纯转染pHaMDR的H8细胞在8周后仍未见肿物出现。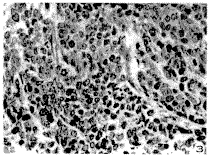
, http://www.100md.com
图3 HE2细胞接种于裸鼠形成肿瘤的组织学特征
2.4 病理检查结果
光镜下可见肿瘤组织表现为低分化鳞状上皮细胞癌的形态特点:组织结构异型性明显,细胞呈巢状或片状排列,细胞大小不一。可见灶状坏死,细胞核梭形或卵圆形,核浆比例增大,病理性核分裂相多见,核膜厚,染色质粗大,可见浸犯周围的肌肉组织(图4,略)。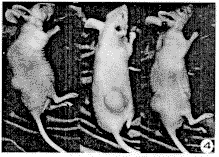
图4 HE2细胞接种后肿瘤形成的裸鼠
2.5 H8和HE2细胞及肿瘤组织内HCMVIE2亚基因片段的检测
用2.9Kb的HCMVIE2基因片段对H8和HE2细胞及HE2诱发裸鼠肿瘤组织进行Southern杂交,结果显示HE2细胞及其诱发肿瘤组织DNA出现同样杂交带,H8细胞未见阳性杂交带,表明HCMVIE2 DNA整合在转化细胞及其诱发的肿瘤组织中(图5,略)。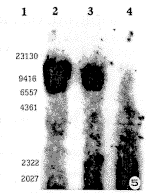
, 百拇医药
图5 H8,HE2细胞及其诱发的肿瘤级织的杂交分析
3 讨论
宫颈癌的发生发展是一个相当复杂的生物学过程,它往往经历多因素、多步骤、长时间的作用,与感染、激素、多孕多产、吸烟、性行为及免疫状态密切相关[9]。其中病毒病因的研究一直受到国内外学者的高度重视。许多研究表明HPV和宫颈癌关系密切,HPV是宫颈癌的致癌主要因素,但不是唯一致癌因素,单独HPV-16尚不足以引起人正常鳞状上皮细胞充分恶变,仅达到细胞转化的“永生化”(immortalization),即相当于临床的“癌前”阶段,当有协同因子共同作用时就会导致宫颈癌的发生(4)。HPV的可能协同因子――HCMV,是一种广泛感染人群的双股DNA肿瘤病毒,也是性传播因子,与多种人类肿瘤的发生可能相关。其作用机制有转化片段(mtr)Ⅰ,Ⅱ,Ⅲ及IE基因[10]。IE基因可上调细胞转录因子NFkB,能与P53和RB结合,从而使细胞增殖,细胞不能终止在G1/S期,导致细胞恶性转化[11]。本实验室已经用HPV16亚基因片断转染人原代正常宫颈上皮细胞,经300多代生长,形成永生化细胞株,但不能在裸鼠中形成肿瘤。进一步转入突变型P53或TPA,可使细胞完全恶性转化[12]。为了探讨宫颈癌发生中HCMV的协同作用,本实验室应用PCR方法检测了宫颈癌和对照组妇女宫颈标本中HPV和HCMV的存在状况,它们的阳性率分别为63.2%和84.2%,其中HPV16/18阳性中同时HCMV阳性的为87.5%(21/24)。提示HCMV和HPV可能协同诱导宫颈癌的发生[13]。因此本实验应用HPV16转染人原代宫颈上皮细胞形成的永生化细胞,转入HCMVIE2基因。实验结果显示IE2基因转染H8细胞后,使软琼脂克隆形成率增加,在裸鼠体内导致肿瘤的发生,光镜观察证明为鳞癌,从而首次在国内外应用细胞培养和动物实验直接证实了HCMVIE2是HPV导致宫颈癌发生的协同因子之一。因此本实验充分表明HPV和HCMV在宫颈癌发生发展中起着重要的作用。
, http://www.100md.com
参考文献
1 Euardo LF Franco. Epidemiology of anogenital warts and cancer. Obstetrics and Gynecology Clinics of North America 1996;23(3):597
2 Zur Hausen H. Molecular pathogenesis of cancer of the cervix and its causation by specific human papillomavirus types. Curr Top Microbiol Immunol 1994;186:131
3 Si JY, Lee K, Zhang W et al. A research for the relationship between human papillomavirus and human uterine cervical carcinoma: II Molecular genetic and ultrsstructural study on the transforming activity of recombinant retrovirus containing human papillomavirus type 16 subgenomic sequences. J Cancer Res Clin Oncol 1991;117:460
, 百拇医药
4 Donnan SPB, Wong FWS, Ho SC, et al. Reproductive and sexual risk factors and human papillomavirus infection in cervical cancer among Hong Kong Chinese. Int J Epidemiol 1989;18:32
5 Koffa M, Koumantaksi E, Ergazaki M,et al. Association of herpesvirus infection with the development of genital cancer. Int J Cancer 1995;63:58
6 Sambrook J, Fritsch EF, Maniatis T. Molecular cloning . A laboratory manual.2nd ed. Cold Spring Harbor Laboratory Press. New York 1989:786~792
, http://www.100md.com
7 鄂征,徐新来,李吉友,等。 组织培养和分子细胞学技术。第二版,北京:人民卫生出版社 1993:156~158
8 Sambrook J, Fritsch EF, Maniatis T. Molecular cloning. A laboratory manual.2nd ed. Cold Spring Harbor Laboratory Press. New York 1989:474~491
9 刘朝奇,孙瑜。宫颈癌的病因研究进展。国外医学*肿瘤学分册 1988;2:81
10 刘朝奇,李昆,司静懿。人巨细胞病毒转化作用的研究进展。国外医学*微生物学分册 1997;20(5):4
11 Yurochko AD, Kowalik TF, Huong SM, et al. Human cytomegalovirus upregulates NF-κB activity by transactivating the NF-κB p105/p50 and p65 promoters. J Virol 1995;69(9):5391
, 百拇医药
12 Si JY, Lee K, Yang LB, et al. The cellular and molecular biological research for the carcinogenic effect of HPV genes on cervical cancer: II The transformation of cells in vitro with viral oncogenes.In: "14th International papillomavirus Conference Final Program and Abstracts".Eds: Alexander Meisels, Thomas R. Broker, Harald zur Hausen. Universite Laval, Quebec City, Canada 1995:124
13 赵蔚明,司静懿,李昆,等。子宫颈癌p53基因突变及HPV和HCMV感染的研究。中华妇产科学杂志 1995;30(11):654
(1998-12-15 收稿), http://www.100md.com
单位:刘朝奇:湖北三峡学院医学院微生物学教研室(宜昌 443003);李 昆 司静懿 刘世德 宋国兴:中国医学科学院协和医科大学基础医学研究所
关键词:宫颈肿瘤;人乳头瘤病毒;人巨细胞病毒;肿瘤发生;上皮细胞
家用医学进修杂志990107
摘 要 目的:探讨宫颈癌的发生发展与人乳头瘤病毒(HPV)和人巨细胞病毒(HCMV)协同感染的关系。方法:本实验应用我室建立的HPV16永生化的人宫颈上皮细胞系,转染HCMV 即早基因(IE)。结果:HCMV整合在细胞染色体中,协同HPV16促进宫颈上皮细胞的恶性转化,在裸鼠中形成肿瘤。结论:HCMV IE基因可协同HPV16恶性转化宫颈上皮细胞,并对其协同机制进行了细胞和分子生物学的探讨。
, 百拇医药
Cellular and Molecular Biological Research on the Oncogenesis
of Cervical Epithelial Cells Coinduced
by Human Papillomavirus and Human Cytomegalovirus
Liu Chaoqi Li Kun Si Jinyi, et al
Department of Microbiology, Hubei Three Gorges University Medical College,Yichang 443003
Abstract Objective:The carcinogenesis of the human uterine cervical carcinoma is closely associated with human papillomavirus (HPV). The purpose of this article is to identify whether another sexually transmitted factor, human cytomegalovirus (HCMV) plays as a co-factor role in the carcinogenesis.Methods:Human cervical epithelial cells immortalized by HPV16 were transferred with the IE gene of HCMV. The condition and efficiency of IE gene were examined. Results:It was showed that the cervical epithelial cells could be completely transformed by HPV16 and IE gene of HCMV. The tumor was formed by injecting the transformed cells in nude mice.Conclusion:The co-operation of HPV and HCMV was observed in oncogenesis of human cervical carcinoma and moreover the cellular and molecular biological mechanism was discussed.
, 百拇医药
Key Words cervix neoplasm;HPV;HCMV;oncogenesis;epithelial cells
宫颈癌是女性生殖系统最常见的恶性肿瘤,在世界范围内其发病率仅次于乳腺癌据第二位,且引起较高的死亡率[1],是危害我国妇女的主要恶性肿瘤之一。因此宫颈癌的病因及其发病机制的研究一直受到国内外学者的高度重视,特别是近十几年来宫颈癌的病因及癌变机理的研究获得突破性的进展,人乳头瘤病毒(human papillomavirus,HPV)作为宫颈癌的主要致癌因素已得到大多数学者的公认[2]。笔者从流行病学、细胞及分子生物学亦作了大量证实[3]。体外细胞转化研究发现HPV仅能诱导人正常上皮细胞的永生化而不能使之充分恶性转化。因而HPV并非宫颈癌发生发展的唯一因素[4]。近几年来HPV与其它性传播因子,如HCMV在宫颈癌发生发展中作用的关系引起部分学者关注[5]。本课题应用本室建立的HPV16永生化的宫颈鳞状上皮细胞为模型,研究HCMV的即早基因(immediate early gene,IE)在癌变发生发展中的相互作用。
, http://www.100md.com
1 材料和方法
1.1 质粒DNA的制备和纯化
质粒pSV2 IE2和pHaMDR DNA(美国Fred Hutchinson Cancer Research Center 的Galloway教授惠赠)按常规方法(碱裂解法)。酶切鉴定后,取适量质粒DNA于Eppendorf管中,75%乙醇灭菌一定时间后,于无菌条件下干燥,溶于适量无菌去离子水中,测吸光度值定量。
1.2 细胞H8
细胞是取材于中国妇女宫颈鳞柱状上皮交界处之鳞状上皮,原代细胞培养,经HPV16 E6E7基因转化,形成永生化细胞。在本室已传代300代以上。
1.3 细胞磷酸钙介导的DNA转染及转染后克隆的筛选[6]
, 百拇医药
将H8细胞复苏后,于37℃,5%CO2饱和湿度下用无血清培养基培养。转染前24小时将细胞以1~2×105/cm2的密度接种于60mm培养皿,培养24小时,并于转染前4小时更换细胞培养液,使每一培养皿内的培养液为5ml。用一无菌透明玻璃管,加入220ul(20ug/ml)含pSV2 IE2和pHaMDR筛选标记质粒的溶液共转染,加入250ul 2XHBS(280mM NaCl,10mM KCl,1.5mM Na2HPO4,12mM葡萄糖,50mM HEPES,pH7.05),然后缓慢加入31ul 2Mol/L CaCl2,轻混30秒,置于室温孵育20~30分钟,将此磷酸钙-DNA悬液移入60mm培养皿中混匀,37℃,5%CO2培养箱中继续培养6小时,甘油休克2分钟后,加入培养液继续培养。48小时后,按1∶5传代,加入秋水仙素进行筛选,待长成克隆后,挑取克隆于24孔板继续培养。
, 百拇医药
1.4 细胞生长速度测定
将2×104/ml细胞接种于培养皿中,培养3天后,进行细胞计数,测定细胞的饱和密度。
1.5 软琼脂集落形成观察[7]
制备0.6%底层琼脂,消化处于对数生长期细胞,制成5×103/ml。将0.7%的琼脂和2×RPMI1640完全培养液以1∶1的比例混合,从中取3ml与0.2ml上述克隆的细胞悬液混合,将其铺于培养皿中的底层琼脂之上,37℃,5%CO2温箱中培养。二周后观察并计数细胞集落(含20个细胞以上者为一集落)然后按下列公式计算克隆形成率(colonyforming efficiency,CPE):CPE=形成细胞数/接种细胞数×100
1.6 裸鼠接种成瘤实验
, http://www.100md.com
将处于对数生长期的细胞经生理盐水清洗后,胰酶消化,计数,制备1~2×107细胞/ml细胞悬液,然后将0.25ml此细胞悬液接种于裸鼠背部,观察射部位有无肿瘤形成及其大小、形状。
1.7 Southen杂交[8]
取生长的肿瘤组织和培养的细胞,常规法提取基因组DNA,溶于适量TrisEDTA(pH8.0)中,测吸光度值进行定量后,贮存于4℃备用。基因组DNA EcoRI酶切后,DNA从琼脂糖凝胶转移到硝酸纤维素膜,随机引物法标记探针,68℃水浴杂交24小时,洗膜,放射自显影。
1.8 光学显微镜标本制备及观察
裸鼠被处死后立即取小块肿瘤组织放入Bouin's固定液中于4℃固定,常规HE染色后,观察、照相。
, 百拇医药 2 结果
2.1 质粒pSV2 IE2及pHaMDR的鉴定
pSV2 IE2经EcoRI酶切,琼脂糖凝胶电泳,可见2.9Kb的IE2基因和4.84Kb pSV2两条带(图1,本文附图均见封4,略),pHaMDR经BamHI或HindⅢ酶切琼脂糖电泳分别呈现两条或四条带(图2,略)。上述质粒限制内切酶鉴定结果与质粒图谱提供内容相符。

图1 pSV2IE2的酶切鉴定

图2 pHaMDR的酶切鉴定
2.2 HCMV即早基因(IE2)恶性转化
, 百拇医药
HPV-16亚基因永生化的人宫颈上皮细胞。将含HCMV即早基因(pSV2 IE2)与表达多耐药基因的pHaMDR的质粒共转染入HPV-16亚基因永生化的H8细胞后,经秋水仙素筛选,约两周后正常H8细胞及单纯转染空载的细胞全部死亡,而转染pSV2IE2/pHaMDR及pHaMDR的细胞仍有散在细胞存活,经两周左右继续培养可见阳性克隆扩大培养后形成转化后细胞株,pSV2 IE2转染细胞命名为HE2。
2.3 细胞生长特性观察
H8和HE2细胞在相同条件下培养生长,发现细胞饱和密度H8细胞为2.1×106±5.8×105/cm2,而HE2细胞为6.5×106±6.3×105/cm2。在双层软琼脂培养中,HE2细胞在两周后可见集落形成,其集落形成率为28.8%,H8细胞的约0.9%。将细胞接种入裸鼠体内。结果发现HE2细胞系在接种二周后出现肿块并迅速增大(图3,略),而单纯转染pHaMDR的H8细胞在8周后仍未见肿物出现。

, http://www.100md.com
图3 HE2细胞接种于裸鼠形成肿瘤的组织学特征
2.4 病理检查结果
光镜下可见肿瘤组织表现为低分化鳞状上皮细胞癌的形态特点:组织结构异型性明显,细胞呈巢状或片状排列,细胞大小不一。可见灶状坏死,细胞核梭形或卵圆形,核浆比例增大,病理性核分裂相多见,核膜厚,染色质粗大,可见浸犯周围的肌肉组织(图4,略)。

图4 HE2细胞接种后肿瘤形成的裸鼠
2.5 H8和HE2细胞及肿瘤组织内HCMVIE2亚基因片段的检测
用2.9Kb的HCMVIE2基因片段对H8和HE2细胞及HE2诱发裸鼠肿瘤组织进行Southern杂交,结果显示HE2细胞及其诱发肿瘤组织DNA出现同样杂交带,H8细胞未见阳性杂交带,表明HCMVIE2 DNA整合在转化细胞及其诱发的肿瘤组织中(图5,略)。

, 百拇医药
图5 H8,HE2细胞及其诱发的肿瘤级织的杂交分析
3 讨论
宫颈癌的发生发展是一个相当复杂的生物学过程,它往往经历多因素、多步骤、长时间的作用,与感染、激素、多孕多产、吸烟、性行为及免疫状态密切相关[9]。其中病毒病因的研究一直受到国内外学者的高度重视。许多研究表明HPV和宫颈癌关系密切,HPV是宫颈癌的致癌主要因素,但不是唯一致癌因素,单独HPV-16尚不足以引起人正常鳞状上皮细胞充分恶变,仅达到细胞转化的“永生化”(immortalization),即相当于临床的“癌前”阶段,当有协同因子共同作用时就会导致宫颈癌的发生(4)。HPV的可能协同因子――HCMV,是一种广泛感染人群的双股DNA肿瘤病毒,也是性传播因子,与多种人类肿瘤的发生可能相关。其作用机制有转化片段(mtr)Ⅰ,Ⅱ,Ⅲ及IE基因[10]。IE基因可上调细胞转录因子NFkB,能与P53和RB结合,从而使细胞增殖,细胞不能终止在G1/S期,导致细胞恶性转化[11]。本实验室已经用HPV16亚基因片断转染人原代正常宫颈上皮细胞,经300多代生长,形成永生化细胞株,但不能在裸鼠中形成肿瘤。进一步转入突变型P53或TPA,可使细胞完全恶性转化[12]。为了探讨宫颈癌发生中HCMV的协同作用,本实验室应用PCR方法检测了宫颈癌和对照组妇女宫颈标本中HPV和HCMV的存在状况,它们的阳性率分别为63.2%和84.2%,其中HPV16/18阳性中同时HCMV阳性的为87.5%(21/24)。提示HCMV和HPV可能协同诱导宫颈癌的发生[13]。因此本实验应用HPV16转染人原代宫颈上皮细胞形成的永生化细胞,转入HCMVIE2基因。实验结果显示IE2基因转染H8细胞后,使软琼脂克隆形成率增加,在裸鼠体内导致肿瘤的发生,光镜观察证明为鳞癌,从而首次在国内外应用细胞培养和动物实验直接证实了HCMVIE2是HPV导致宫颈癌发生的协同因子之一。因此本实验充分表明HPV和HCMV在宫颈癌发生发展中起着重要的作用。
, http://www.100md.com
参考文献
1 Euardo LF Franco. Epidemiology of anogenital warts and cancer. Obstetrics and Gynecology Clinics of North America 1996;23(3):597
2 Zur Hausen H. Molecular pathogenesis of cancer of the cervix and its causation by specific human papillomavirus types. Curr Top Microbiol Immunol 1994;186:131
3 Si JY, Lee K, Zhang W et al. A research for the relationship between human papillomavirus and human uterine cervical carcinoma: II Molecular genetic and ultrsstructural study on the transforming activity of recombinant retrovirus containing human papillomavirus type 16 subgenomic sequences. J Cancer Res Clin Oncol 1991;117:460
, 百拇医药
4 Donnan SPB, Wong FWS, Ho SC, et al. Reproductive and sexual risk factors and human papillomavirus infection in cervical cancer among Hong Kong Chinese. Int J Epidemiol 1989;18:32
5 Koffa M, Koumantaksi E, Ergazaki M,et al. Association of herpesvirus infection with the development of genital cancer. Int J Cancer 1995;63:58
6 Sambrook J, Fritsch EF, Maniatis T. Molecular cloning . A laboratory manual.2nd ed. Cold Spring Harbor Laboratory Press. New York 1989:786~792
, http://www.100md.com
7 鄂征,徐新来,李吉友,等。 组织培养和分子细胞学技术。第二版,北京:人民卫生出版社 1993:156~158
8 Sambrook J, Fritsch EF, Maniatis T. Molecular cloning. A laboratory manual.2nd ed. Cold Spring Harbor Laboratory Press. New York 1989:474~491
9 刘朝奇,孙瑜。宫颈癌的病因研究进展。国外医学*肿瘤学分册 1988;2:81
10 刘朝奇,李昆,司静懿。人巨细胞病毒转化作用的研究进展。国外医学*微生物学分册 1997;20(5):4
11 Yurochko AD, Kowalik TF, Huong SM, et al. Human cytomegalovirus upregulates NF-κB activity by transactivating the NF-κB p105/p50 and p65 promoters. J Virol 1995;69(9):5391
, 百拇医药
12 Si JY, Lee K, Yang LB, et al. The cellular and molecular biological research for the carcinogenic effect of HPV genes on cervical cancer: II The transformation of cells in vitro with viral oncogenes.In: "14th International papillomavirus Conference Final Program and Abstracts".Eds: Alexander Meisels, Thomas R. Broker, Harald zur Hausen. Universite Laval, Quebec City, Canada 1995:124
13 赵蔚明,司静懿,李昆,等。子宫颈癌p53基因突变及HPV和HCMV感染的研究。中华妇产科学杂志 1995;30(11):654
(1998-12-15 收稿), http://www.100md.com