血清CEA、NSE、CYFRA21-1联合检测对肺癌诊断价值的探讨
作者:夏冬根 侯永健
单位:上海市第四人民医院(200081)
关键词:肺肿瘤;癌胚抗原;磷酸丙酮酸水合酶;角蛋白;肿瘤标记,生物学
实用医学杂志990211摘 要 目的:探索血清肿瘤标志物癌胚抗原(CEA)、神经元特异性烯醇化酶(NSE)、CYFRA21-1联合检测在肺癌诊断中的临床价值。方法:采用放射免疫法测定92例肺癌、238例良性肺病(BLD)和33例健康人血清中CEA、NSE、CYFRA21-1的水平。结果:肺癌组CEA、NSE、CYFRA21-1的测定值分别为29.7±27.6 μg/L、21.1±29.4 μg/L、13.2±14.6 μg/L,均显著高于BLD和健康对照组(P<0.01)。三项肿瘤标志物联合诊断肺癌的敏感性、特异性、准确性,阳性预测值和阴性预测值分别为94.6%、92.2%、92.8%、80.6%和98.0%,除特异性稍低外,其余均显著高于单项检测和二项联检。三项联检还可使早期肺癌的诊断率提高到60.0%。结论:CEA、NSE、CYFRA21-1是诊断肺癌有价值的肿瘤标志物,三者联检将有助于肺癌,尤其是早期肺癌的诊断。
, http://www.100md.com
随着肺癌发病率愈来愈高,肿瘤专家正在积极寻找肺癌早期诊断的新方法。癌胚抗原(CEA)是最早用于肺癌诊断的肿瘤标志物之一,其诊断价值早已被肯定。近年来,新的肿瘤标志物CYFRA21-1和神经元特异性烯醇化酶(NSE)被认为是迄今为止所发现的用于诊断鳞癌和小细胞肺癌(SCLC)较灵敏的肿瘤标志物之一[1,2],但其单项检测仍有一定的局限性。为此,我们从1996年起采用CEA、NSE、CYFRA21-1联合诊断肺癌,取得了较好的效果,现报告如下。
1 对象和方法
1.1 一般资料 (1)肺癌组:92例,男62例,女30例,年龄44~87岁,平均56.3岁。全部病人均经病理确诊,并按国际抗癌联盟1986年修订的TNM标准进行分期。其中非小细胞肺癌(NSCLC)76例(鳞癌39例,腺癌37例),小细胞肺癌(SCLC)11例,未分型癌5例;(2)良性肺病(BLD)组:238例,男155例,女83例,年龄25~88岁,平均53.6岁。根据临床表现、实验室检查和X线胸片等确诊。其中肺炎78例,慢性支气管炎131例,支气管哮喘9例,结核性胸膜炎8例,自发性气胸2例,支气管扩张症10例;(3)健康对照组:33例,为本院健康体检者。其中男21例,女12例,年龄42~72岁,平均52.4岁。
, http://www.100md.com
1.2 方法 肿瘤标志物测定:静脉采血后(弃去溶血标本)分离血清,-20℃保存。CEA采用中国原子能科学研究院放射免疫双抗体试剂盒;NSE采用中国医学科学院肿瘤研究所佳科生物技术公司IRMA试剂盒;CYFRA21-1采用美国Centocor公司IRMA试剂盒。
1.3 统计学处理 各组肿瘤标志物测定数值的显著性检验用方差分析,阳性率比较用χ2检验。
2 结果
2.1 肺癌组、BLD及健康对照组的血清肿瘤标志物水平,见表1。根据33例健康对照组测定结果,我们以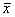 ±2s为正常范围,则各项肿瘤标志物正常值分别为CEA<15 μg/L,NSE<20 μg/L,CYFRA21-1<3.3 μg/L。33例健康人,无1例高于正常值。238例BLD中,假阳性23例,其中CEA 12例,NSE 4例,CYFRA21-1 7例。
±2s为正常范围,则各项肿瘤标志物正常值分别为CEA<15 μg/L,NSE<20 μg/L,CYFRA21-1<3.3 μg/L。33例健康人,无1例高于正常值。238例BLD中,假阳性23例,其中CEA 12例,NSE 4例,CYFRA21-1 7例。
, http://www.100md.com
表1 各组受试者血清三项肿瘤标志物水平(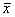 ±s,μg/L) 分组
±s,μg/L) 分组
例数
CEA
NSE
CYFRA21-1
肺癌组
92
29.7±27.6*
21.1±29.4*
13.2±14.6*
, 百拇医药
BLD
238
10.2±2.2△
12.5±6.4△
1.6±1.2△
对照组
33
11.1±1.9
11.3±4.4
1.5±0.9
与BLD及对照组比较* P<0.01;与对照组比较△ P>0.05
, 百拇医药
2.2 不同类型肺癌三项肿瘤标志物水平及阳性率比较,见表2。NSCLC患者血清CEA、CYFRA21-1水平及阳性率均显著高于SCLC(P<0.01),其中腺癌患者的CEA水平最高,阳性率高达62.2%,并显著高于鳞癌(P<0.05),鳞癌患者血清CYFRA21-1水平最高,阳性率高达64.1%,且明显高于腺癌(P<0.05),SCLC患者血清NSE水平和阳性率均明显高于NSCLC(P<0.01),阳性率高达72.7%。结果表明,CEA对腺癌、NSE对SCLC、CYFRA21-1对鳞癌的诊断价值最高。
表2 不同细胞类型肺癌患者三项标志物水平及阳性率比较 组织学类型
例数
CEA
NSE
CYFRA21-1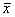 ±s(μg/L)
±s(μg/L)
, 百拇医药
阳性率(%)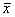 ±s(μg/L)
±s(μg/L)
阳性率(%)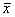 ±s(μg/L)
±s(μg/L)
阳性率(%)
非小细胞癌
76
31.4±27.4*
43.2*
13.1±11.0*
27.6*
, 百拇医药
13.9±14.9*
63.2*
鳞癌
39
21.3±20.5*
41.0*
14.8±11.2*
28.2*
17.6±16.4*
64.1*
, 百拇医药
腺癌
37
42.4±29.4*
62.2*△
11.7±11.4*
13.5*△
11.7±14.3*
40.5*△
小细胞癌
11
11.7±4.8
, 百拇医药
27.3
39.6±16.0
72.7
4.2±3.4
27.3
与SCLC比较*P<0.01,与鳞癌比较△P<0.05
2.3 不同病期肺癌三项肿瘤标志物水平及阳性率比较,见表3。Ⅲ、Ⅳ期肺癌血清CEA、NSE、CYFRA21-1水平和阳性率均明显高于Ⅰ、Ⅱ期肺癌(P<0.01),三项肿瘤标志物水平和阳性率随病情发展呈逐步增高趋势。Ⅰ、Ⅱ期SCLC患者CEA和CYFRA21-1均在正常范围内,表明CEA和CYFRA21-1对SCLC无早期诊断价值。结果还表明,CEA、NSE、CYFRA21-1三项联检将Ⅰ、Ⅱ期早期肺癌的阳性率从单项检测的20.0%~33.3%提高到60.0%。
, http://www.100md.com
表3 不同病期肺癌的三项标志物水平及阳性率比较 分期
类型
例数
CEA
NSE
CYFRA21-1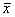 ±s(μg/L)
±s(μg/L)
阳性率(%)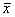 ±s(μg/L)
±s(μg/L)
阳性率(%)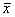 ±s(μg/L)
±s(μg/L)
, 百拇医药
阳性率(%)
Ⅰ、Ⅱ
肺癌
15
14.1±6.3*
26.7*
10.2±11.1*
20.0*
3.2±1.6*
33.3*
NSCLC
, http://www.100md.com
12
16.6±8.7
33.3
9.2±10.4
16.7
3.4±1.5
41.7
SCLC
3
8.8±0.6
0
23.6±7.6
33.3
, 百拇医药
1.0±0.6
0
Ⅲ
肺癌
41
26.1±22.6
58.7
20.9±28.2
42.6
13.8±14.6
65.8
NSCLC
36
, 百拇医药
28.8±25.9
61.1
14.0±10.2
30.6
14.0±12.2
69.4
SCLC
5
10.4±4.0
20.0
43.9±34.8
80.0
, 百拇医药 4.1±4.0
20.0
Ⅳ
肺癌
31
32.4±18.7
61.3
25.3±36.0
45.2
15.3±16.2
71.0
NSCLC
28
, http://www.100md.com
34.1±19.8
64.3
16.4±11.8
32.1
16.8±11.7
75.0
SCLC
3
12.8±7.5
33.3
59.5±52.8
100.0
, 百拇医药 5.0±4.7
33.3
与Ⅲ、Ⅳ期肺癌比较*P<0.01
2.4 不同类型肺癌三项标志物联检阳性率比较,见图1。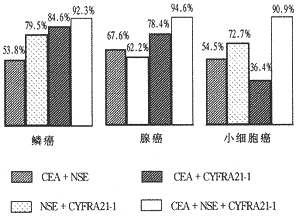
图1不同类型肺癌三项标志物联检阳性率比较
对任何一种类型肺癌,三项肿瘤标志物联检阳性率最高,二项联检则NSCLC以CYFRA21-1、CEA阳性率较高,SCLC以NSE、CYFRA21-1较高。
2.5 三项肿瘤标志物联检对肺癌诊断价值的评估,见表4。三项肿瘤标志物联检其敏感性从单项和二项联检的34.8%~70.7%提高到94.6%,极为有效地提高了肺癌的诊断率。此外,三项联检的准确性、阳性预测值和阴性预测值也明显高于单项和二项联检,但其特异性仅从单项检测的93.3%~95.5%稍下降为92.2%。结果表明,CEA、NSE、CYFRA21-1三项肿瘤标志物联合检测是目前诊断肺癌最有价值的组合方法。
, 百拇医药
表4 血清CEA、NSE、CYFRA21-1和三者联合检测对肺癌诊断价值的分析(%)
敏感
性
特异
性
准确
性
阳性预
测值
阴性预
测值
CEA
53.3
, http://www.100md.com
93.3
82.2
73.1
85.3
NSE
34.8
95.5
77.5
72.7
81.0
CYFRA21-1
62.0
94.0
, 百拇医药
84.4
78.1
87.8
CEA+NSE
58.7
93.3
83.6
75.0
86.8
CEA+CYFRA21-1
70.7
93.3
86.6
, http://www.100md.com
78.3
90.3
NSE+CYFRA21-1
68.5
94.0
86.1
79.7
89.6
CEA+NSE+CYFRA21-1
94.6
92.2
92.8
, 百拇医药 80.6
98.0
3 讨论
CEA、NSE、CYFRA21-1均为非器官特异性肿瘤标志物,其单项检测对肺癌均有一定的诊断价值,但由于上述肿瘤标志物对各种类型肺癌的敏感性差异较大,就总体而言,其敏感性均受限制,本文结果分别为53.3%、34.8%和62.0%。由于CEA原本主要存在于消化系及泌尿生殖系等富含腺体细胞的组织中;NSE则是由两个γ亚单位组成的糖酵解酶,原本存在于正常神经细胞和神经内分泌细胞中;CYFRA21-1是一分子量为3998.8道尔顿,细胞角质蛋白19的片断(CK19),原本存在于几乎所有的上皮细胞内[3],故三者分别对肺腺癌、SCLC及鳞癌相对敏感[1,2],本文表2所示与之一致,各自阳性率均为几类型肺癌中最高者,分别为62.2%、72.7%、64.1%。而腺癌、SCLC和鳞癌三种类型占肺癌总体的大部分。因此,本文选择CEA、NSE及CYFRA21-1三项指标来研究肿瘤标志物联检的肺癌诊断价值是合理的。
, http://www.100md.com
从本文以CEA、NSE、CYFRA21-1三项肿瘤标志物不同组合联检的肺癌诊断结果中不难看出,较各单项检测的敏感性、准确性以及阳性、阴性预测值均有明显提高。尤以NSE、CYFRA21-1联检对SCLC、CEA、CYFRA21-1联检对NSCLC阳性诊断率的提高更为显著。这与有关报道也较为一致[4,5],可能与CYFRA21-1对肺癌诊断的特异性相对较高有关。而CEA、NSE、CYFRA21-1三项联检,其敏感性、准确性以及预测价值均明显优于二项联检。
本文结果还显示,就肺癌早期诊断而言,NSE对SCLC、CYFRA21-1对NSCLC的Ⅰ、Ⅱ期诊断价值较大。CEA、NSE、CYFRA21-1三项联检可将早期肺癌诊断率提高到60.0%。CEA、CYFRA21-1对SCLC的早期诊断似意义不大。
综上分析,我们认为,在肺癌诊断中,CEA、NSE和CYFRA21-1是有用的肿瘤标志物,三者联检是目前最有价值的组合方法,它将有助于肺癌,尤其是早期肺癌的诊断。
, 百拇医药
4 参考文献
1 Ebert W,Hoppe M,Muley T,et al. Monitoring of therapy in inoperable lung cancer patients by measurement of CYFRA21-1, TPA-TP CEA,and NSE. Anticancer Res,1997,17(4B):2875~2878.
2 Najemnik C, Mohn Staudner A,Vetter H,et al. Evaluation of CYFRA21-1 as a marker for lung cancer. Wien Klin Wochenschr,1996,108(15):467~472.
3 Pujol JL,Grenier J,Daures JP,et al. Serum fragment of cytokeratin subunit 19 measured by CYFRA21-1 immunoradiometric assay as a marker of lung cancer. Cancer Res,1993,53(1):61~66.
4 王广贤,等. CYFRA21-1,CEA在肺癌检测中的价值. 放射免疫学杂志,1998,11(4):202~203.
5 Stieber P,Dienemann H,Hasholzner U,et al. Comparison of cytokeratin fragment 19 (CYFRA21-1),tissue polypeptide antigen (TPA) and tissue polypeptide specific antigen(TPS) as tumour markers in lung cancer. Eur J Clin Chem Clin Biochem,1993,31(10):689~694., 百拇医药
单位:上海市第四人民医院(200081)
关键词:肺肿瘤;癌胚抗原;磷酸丙酮酸水合酶;角蛋白;肿瘤标记,生物学
实用医学杂志990211摘 要 目的:探索血清肿瘤标志物癌胚抗原(CEA)、神经元特异性烯醇化酶(NSE)、CYFRA21-1联合检测在肺癌诊断中的临床价值。方法:采用放射免疫法测定92例肺癌、238例良性肺病(BLD)和33例健康人血清中CEA、NSE、CYFRA21-1的水平。结果:肺癌组CEA、NSE、CYFRA21-1的测定值分别为29.7±27.6 μg/L、21.1±29.4 μg/L、13.2±14.6 μg/L,均显著高于BLD和健康对照组(P<0.01)。三项肿瘤标志物联合诊断肺癌的敏感性、特异性、准确性,阳性预测值和阴性预测值分别为94.6%、92.2%、92.8%、80.6%和98.0%,除特异性稍低外,其余均显著高于单项检测和二项联检。三项联检还可使早期肺癌的诊断率提高到60.0%。结论:CEA、NSE、CYFRA21-1是诊断肺癌有价值的肿瘤标志物,三者联检将有助于肺癌,尤其是早期肺癌的诊断。
, http://www.100md.com
随着肺癌发病率愈来愈高,肿瘤专家正在积极寻找肺癌早期诊断的新方法。癌胚抗原(CEA)是最早用于肺癌诊断的肿瘤标志物之一,其诊断价值早已被肯定。近年来,新的肿瘤标志物CYFRA21-1和神经元特异性烯醇化酶(NSE)被认为是迄今为止所发现的用于诊断鳞癌和小细胞肺癌(SCLC)较灵敏的肿瘤标志物之一[1,2],但其单项检测仍有一定的局限性。为此,我们从1996年起采用CEA、NSE、CYFRA21-1联合诊断肺癌,取得了较好的效果,现报告如下。
1 对象和方法
1.1 一般资料 (1)肺癌组:92例,男62例,女30例,年龄44~87岁,平均56.3岁。全部病人均经病理确诊,并按国际抗癌联盟1986年修订的TNM标准进行分期。其中非小细胞肺癌(NSCLC)76例(鳞癌39例,腺癌37例),小细胞肺癌(SCLC)11例,未分型癌5例;(2)良性肺病(BLD)组:238例,男155例,女83例,年龄25~88岁,平均53.6岁。根据临床表现、实验室检查和X线胸片等确诊。其中肺炎78例,慢性支气管炎131例,支气管哮喘9例,结核性胸膜炎8例,自发性气胸2例,支气管扩张症10例;(3)健康对照组:33例,为本院健康体检者。其中男21例,女12例,年龄42~72岁,平均52.4岁。
, http://www.100md.com
1.2 方法 肿瘤标志物测定:静脉采血后(弃去溶血标本)分离血清,-20℃保存。CEA采用中国原子能科学研究院放射免疫双抗体试剂盒;NSE采用中国医学科学院肿瘤研究所佳科生物技术公司IRMA试剂盒;CYFRA21-1采用美国Centocor公司IRMA试剂盒。
1.3 统计学处理 各组肿瘤标志物测定数值的显著性检验用方差分析,阳性率比较用χ2检验。
2 结果
2.1 肺癌组、BLD及健康对照组的血清肿瘤标志物水平,见表1。根据33例健康对照组测定结果,我们以
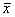 ±2s为正常范围,则各项肿瘤标志物正常值分别为CEA<15 μg/L,NSE<20 μg/L,CYFRA21-1<3.3 μg/L。33例健康人,无1例高于正常值。238例BLD中,假阳性23例,其中CEA 12例,NSE 4例,CYFRA21-1 7例。
±2s为正常范围,则各项肿瘤标志物正常值分别为CEA<15 μg/L,NSE<20 μg/L,CYFRA21-1<3.3 μg/L。33例健康人,无1例高于正常值。238例BLD中,假阳性23例,其中CEA 12例,NSE 4例,CYFRA21-1 7例。, http://www.100md.com
表1 各组受试者血清三项肿瘤标志物水平(
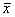 ±s,μg/L) 分组
±s,μg/L) 分组例数
CEA
NSE
CYFRA21-1
肺癌组
92
29.7±27.6*
21.1±29.4*
13.2±14.6*
, 百拇医药
BLD
238
10.2±2.2△
12.5±6.4△
1.6±1.2△
对照组
33
11.1±1.9
11.3±4.4
1.5±0.9
与BLD及对照组比较* P<0.01;与对照组比较△ P>0.05
, 百拇医药
2.2 不同类型肺癌三项肿瘤标志物水平及阳性率比较,见表2。NSCLC患者血清CEA、CYFRA21-1水平及阳性率均显著高于SCLC(P<0.01),其中腺癌患者的CEA水平最高,阳性率高达62.2%,并显著高于鳞癌(P<0.05),鳞癌患者血清CYFRA21-1水平最高,阳性率高达64.1%,且明显高于腺癌(P<0.05),SCLC患者血清NSE水平和阳性率均明显高于NSCLC(P<0.01),阳性率高达72.7%。结果表明,CEA对腺癌、NSE对SCLC、CYFRA21-1对鳞癌的诊断价值最高。
表2 不同细胞类型肺癌患者三项标志物水平及阳性率比较 组织学类型
例数
CEA
NSE
CYFRA21-1
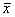 ±s(μg/L)
±s(μg/L), 百拇医药
阳性率(%)
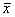 ±s(μg/L)
±s(μg/L)阳性率(%)
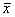 ±s(μg/L)
±s(μg/L)阳性率(%)
非小细胞癌
76
31.4±27.4*
43.2*
13.1±11.0*
27.6*
, 百拇医药
13.9±14.9*
63.2*
鳞癌
39
21.3±20.5*
41.0*
14.8±11.2*
28.2*
17.6±16.4*
64.1*
, 百拇医药
腺癌
37
42.4±29.4*
62.2*△
11.7±11.4*
13.5*△
11.7±14.3*
40.5*△
小细胞癌
11
11.7±4.8
, 百拇医药
27.3
39.6±16.0
72.7
4.2±3.4
27.3
与SCLC比较*P<0.01,与鳞癌比较△P<0.05
2.3 不同病期肺癌三项肿瘤标志物水平及阳性率比较,见表3。Ⅲ、Ⅳ期肺癌血清CEA、NSE、CYFRA21-1水平和阳性率均明显高于Ⅰ、Ⅱ期肺癌(P<0.01),三项肿瘤标志物水平和阳性率随病情发展呈逐步增高趋势。Ⅰ、Ⅱ期SCLC患者CEA和CYFRA21-1均在正常范围内,表明CEA和CYFRA21-1对SCLC无早期诊断价值。结果还表明,CEA、NSE、CYFRA21-1三项联检将Ⅰ、Ⅱ期早期肺癌的阳性率从单项检测的20.0%~33.3%提高到60.0%。
, http://www.100md.com
表3 不同病期肺癌的三项标志物水平及阳性率比较 分期
类型
例数
CEA
NSE
CYFRA21-1
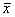 ±s(μg/L)
±s(μg/L)阳性率(%)
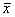 ±s(μg/L)
±s(μg/L)阳性率(%)
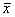 ±s(μg/L)
±s(μg/L), 百拇医药
阳性率(%)
Ⅰ、Ⅱ
肺癌
15
14.1±6.3*
26.7*
10.2±11.1*
20.0*
3.2±1.6*
33.3*
NSCLC
, http://www.100md.com
12
16.6±8.7
33.3
9.2±10.4
16.7
3.4±1.5
41.7
SCLC
3
8.8±0.6
0
23.6±7.6
33.3
, 百拇医药
1.0±0.6
0
Ⅲ
肺癌
41
26.1±22.6
58.7
20.9±28.2
42.6
13.8±14.6
65.8
NSCLC
36
, 百拇医药
28.8±25.9
61.1
14.0±10.2
30.6
14.0±12.2
69.4
SCLC
5
10.4±4.0
20.0
43.9±34.8
80.0
, 百拇医药 4.1±4.0
20.0
Ⅳ
肺癌
31
32.4±18.7
61.3
25.3±36.0
45.2
15.3±16.2
71.0
NSCLC
28
, http://www.100md.com
34.1±19.8
64.3
16.4±11.8
32.1
16.8±11.7
75.0
SCLC
3
12.8±7.5
33.3
59.5±52.8
100.0
, 百拇医药 5.0±4.7
33.3
与Ⅲ、Ⅳ期肺癌比较*P<0.01
2.4 不同类型肺癌三项标志物联检阳性率比较,见图1。

图1不同类型肺癌三项标志物联检阳性率比较
对任何一种类型肺癌,三项肿瘤标志物联检阳性率最高,二项联检则NSCLC以CYFRA21-1、CEA阳性率较高,SCLC以NSE、CYFRA21-1较高。
2.5 三项肿瘤标志物联检对肺癌诊断价值的评估,见表4。三项肿瘤标志物联检其敏感性从单项和二项联检的34.8%~70.7%提高到94.6%,极为有效地提高了肺癌的诊断率。此外,三项联检的准确性、阳性预测值和阴性预测值也明显高于单项和二项联检,但其特异性仅从单项检测的93.3%~95.5%稍下降为92.2%。结果表明,CEA、NSE、CYFRA21-1三项肿瘤标志物联合检测是目前诊断肺癌最有价值的组合方法。
, 百拇医药
表4 血清CEA、NSE、CYFRA21-1和三者联合检测对肺癌诊断价值的分析(%)
敏感
性
特异
性
准确
性
阳性预
测值
阴性预
测值
CEA
53.3
, http://www.100md.com
93.3
82.2
73.1
85.3
NSE
34.8
95.5
77.5
72.7
81.0
CYFRA21-1
62.0
94.0
, 百拇医药
84.4
78.1
87.8
CEA+NSE
58.7
93.3
83.6
75.0
86.8
CEA+CYFRA21-1
70.7
93.3
86.6
, http://www.100md.com
78.3
90.3
NSE+CYFRA21-1
68.5
94.0
86.1
79.7
89.6
CEA+NSE+CYFRA21-1
94.6
92.2
92.8
, 百拇医药 80.6
98.0
3 讨论
CEA、NSE、CYFRA21-1均为非器官特异性肿瘤标志物,其单项检测对肺癌均有一定的诊断价值,但由于上述肿瘤标志物对各种类型肺癌的敏感性差异较大,就总体而言,其敏感性均受限制,本文结果分别为53.3%、34.8%和62.0%。由于CEA原本主要存在于消化系及泌尿生殖系等富含腺体细胞的组织中;NSE则是由两个γ亚单位组成的糖酵解酶,原本存在于正常神经细胞和神经内分泌细胞中;CYFRA21-1是一分子量为3998.8道尔顿,细胞角质蛋白19的片断(CK19),原本存在于几乎所有的上皮细胞内[3],故三者分别对肺腺癌、SCLC及鳞癌相对敏感[1,2],本文表2所示与之一致,各自阳性率均为几类型肺癌中最高者,分别为62.2%、72.7%、64.1%。而腺癌、SCLC和鳞癌三种类型占肺癌总体的大部分。因此,本文选择CEA、NSE及CYFRA21-1三项指标来研究肿瘤标志物联检的肺癌诊断价值是合理的。
, http://www.100md.com
从本文以CEA、NSE、CYFRA21-1三项肿瘤标志物不同组合联检的肺癌诊断结果中不难看出,较各单项检测的敏感性、准确性以及阳性、阴性预测值均有明显提高。尤以NSE、CYFRA21-1联检对SCLC、CEA、CYFRA21-1联检对NSCLC阳性诊断率的提高更为显著。这与有关报道也较为一致[4,5],可能与CYFRA21-1对肺癌诊断的特异性相对较高有关。而CEA、NSE、CYFRA21-1三项联检,其敏感性、准确性以及预测价值均明显优于二项联检。
本文结果还显示,就肺癌早期诊断而言,NSE对SCLC、CYFRA21-1对NSCLC的Ⅰ、Ⅱ期诊断价值较大。CEA、NSE、CYFRA21-1三项联检可将早期肺癌诊断率提高到60.0%。CEA、CYFRA21-1对SCLC的早期诊断似意义不大。
综上分析,我们认为,在肺癌诊断中,CEA、NSE和CYFRA21-1是有用的肿瘤标志物,三者联检是目前最有价值的组合方法,它将有助于肺癌,尤其是早期肺癌的诊断。
, 百拇医药
4 参考文献
1 Ebert W,Hoppe M,Muley T,et al. Monitoring of therapy in inoperable lung cancer patients by measurement of CYFRA21-1, TPA-TP CEA,and NSE. Anticancer Res,1997,17(4B):2875~2878.
2 Najemnik C, Mohn Staudner A,Vetter H,et al. Evaluation of CYFRA21-1 as a marker for lung cancer. Wien Klin Wochenschr,1996,108(15):467~472.
3 Pujol JL,Grenier J,Daures JP,et al. Serum fragment of cytokeratin subunit 19 measured by CYFRA21-1 immunoradiometric assay as a marker of lung cancer. Cancer Res,1993,53(1):61~66.
4 王广贤,等. CYFRA21-1,CEA在肺癌检测中的价值. 放射免疫学杂志,1998,11(4):202~203.
5 Stieber P,Dienemann H,Hasholzner U,et al. Comparison of cytokeratin fragment 19 (CYFRA21-1),tissue polypeptide antigen (TPA) and tissue polypeptide specific antigen(TPS) as tumour markers in lung cancer. Eur J Clin Chem Clin Biochem,1993,31(10):689~694., 百拇医药