血小板源伤口愈合因子促糖尿病大鼠难愈伤口愈合的机理探讨
作者:张 艳 朱旭东 陈荣德
单位:第三军医大学大坪医院野战外科研究所一室
关键词:糖尿病;血小板源伤口愈合因子;伤口愈合
重庆医学990203
摘 要 本实验以糖尿病大鼠海绵死腔伤为难愈伤口模型结合离体细胞培养,研究血小板源伤口愈合因子(PDWHF)改善难愈伤口愈合的作用并探讨其可能机理。结果表明:局部应用PDWHF后,伤口组织总DNA、羟脯氨酸含量增高;组织学表现为肉芽组织中成纤维细胞显著增生,胶原纤维沉积增加。离体实验发现PDWHF可促进成纤维细胞的分化和增殖。提示:PDWHF可通过促进伤口肉芽组织中的细胞合成代谢及增殖,增加胶原的合成与沉积进而改善糖尿病伤口的愈合。
Study On The Mechanisms Of PDWHF On Impaired Wound
, http://www.100md.com
Healing In Rats With Diabetic Disease
Department One of Research Institute of Surgery & Daping Hospital
The 3 rd Military Medical University,Chongqing,400042
Zhong Yan,Zhu Xudong,Chen Rongde
Abstract:The experiment was designed to study the effects and mechanisms of PDWHF on the healing process of impaired wounds in diabetic rats,through the subcutaneous sponge implanted diabetic rats model and in vitro cell cultures.The results showed that local application with PDWHF could remarkably increase the content of DNA and hydroxyproline.Histological observations showed that there were obvious fibroblasts hyperplasia and increased collagen fibers deposition in the grannulation tissues.In vitro experiments demonstrated that PDWHF could promote the differentiation and proliferation of fibroblasts.It is suggested that PDWHF could improve the healing process of impaired diabetic wounds through the enhancement of synthetic metabolism and the proliferation of grannulation tissue cells,and the promotion of collagen synthesis and deposition.
, 百拇医药
Key words:Diabetes Platelet-derived wound healing factors Wound healing
糖尿病伤口愈合迟缓是临床上常见的难题,其有关机理尚未阐明,但至少与伤口组织细胞和伤口微环境生长因子的种类及含量失衡相关。探讨外源性生长因子改善糖尿病伤口愈合的可能性及作用机理一直是近年来伤口愈合研究领域中的重点内容之一[1-3]。血小板源伤口愈合因子(Platelet derived wound healing factors,PDWHF)是血小板在体外经凝血酶刺激脱颗粒时所释放的多种生长因子混合物,主要由血小板衍生长因子(PDGF)、表皮生长因子(EGF)、转 化生长因子-α/β(TFG-α/β)、胰岛素样生长因子-Ⅰ(IGF-Ⅰ)组成。本研究以糖尿病大鼠皮下“死腔伤”为伤口模型结合体外细胞培养实验,就PDWHF的促愈作用及相关机理进行了初步研究。
材料与方法
, 百拇医药
一、动物模型及分组:雄性SD大鼠44只,体重200~250g,分为三组。正常组(n=12),大鼠致伤在无菌条件下进行,大鼠麻醉、脱毛后,沿脊柱方向做两条深达筋膜长约4cm的平行切口,伤口距脊椎垂直距离约为1cm,钝性剥离伤口两端的皮肤,造成皮下袋囊,放入两块已消毒好的聚乙烯醇海绵(直径1cm,厚度0.2cm,重量8.6±0.22mg),缝合伤口。按J.Niinikoski法[4]术后当日及以后连续6日海绵注入20ul牛血清白蛋白液(5mg/ml)。糖尿病致伤对照组(n=16),腹腔注射新鲜配制四氧嘧啶(1.5mg/10g体重),测得血糖值大于180mg/dl一、二日后,即可致伤[5]。手术方式与正常组相同,于术后当日及以后连续6日海绵内注入20ul牛血清白蛋白液(5mg/ml)。糖尿病致伤治疗组(n=16),手术后当日及以后连续6日向海绵内注入20ul PDWHF液(5mg/ml)。PDWHF液参照Knighton方法[6]制备。
二、“死腔伤口”肉芽组织生长参数的测定:各组动物分别在伤后5、7、10、14日活杀,取出海绵,二联苯胺法测定其中总DNA、氯胺-T法测定羟脯氨酸量[7]。
, http://www.100md.com
三、离体实验:按本室建立的方法[8]培养伤口成纤维细胞,生长融合的细胞经0.25%胰蛋白酶消化30秒,倾去消化液,加入1640液洗涤2次,用1640/1%FCS培养液将细胞调成浓度为1×104/ml的细胞悬液,点接细胞悬液100ul到96孔培养板中,37℃、5%CO2条件卵下卵育12hr,吸去培养液,按加入的卵育液不同,将培养细胞分为三组:空白对照组:1640加0.5%FCS(简称BM);阳性对照组:1640加10%FCS;PDWHF处理组:BM/1%PDWHF、BM/3%PDWHF、BM/5%PDWHF、BM/7% PDWHF、BM/10%PDWHF、BM/12%PDWHF。待测样本与细胞共孵育48小时后,MTT法测定细胞的增殖情况。
结 果
一、糖尿病组、PDWHF治疗组伤口组织形态学观察:伤后10日PDWHF治疗组较糖尿病对照组伤口肉芽组织有明显的成纤维细胞增生、聚集,细胞呈长梭状较非治疗组成熟(图1,2)。
, http://www.100md.com
二、PDWHF促糖尿病大鼠肉芽组织生长:正常组、糖尿病组、PDWHF治疗组海绵中总DNA、羟脯氨酸含量及各组间比较结果(见表1、2)。
三、PDWHF对鼠伤口成纤维细胞增殖的影响:测定结果表明,在1%~7%的浓度范围内,PDWHF可显著促进伤口成纤维细胞的生长,明显高于0.5%FCS组(P<0.01);当PDWHF的浓度为10%时,其促生长作用已不再明显,与0.5%FCS组无显著差异(P>0.05),远远低于10%FCS组(P<0.01)。当PDWHF的浓度为12%时,其对伤口成纤维细胞的生长呈现出明显抑制作用(见图3)。
表1 各组动物伤后不同天数伤口海绵中DNA含量(微克/克湿海绵)
5日
7日
10日
, 百拇医药
14日
正常组
280±32
447±56
505±38
479±35
糖尿病对照组
63±12
123±14
215±24
386±36
糖尿病治疗组
177±24*##
, http://www.100md.com
328±32*##
464±28##
494±32#
.P<0.05,..P<0.01与正常组比较;#P<0.05,##P<0.01与糖尿病对照组比较;表2 各组动物伤后不同天数伤口海绵中羟脯氨酸含量(微克/克湿海绵)
5日
7日
10日
14日
正常组
301±31
817±93
, 百拇医药
2375±371
4243±306
糖尿病对照组
108±14
382±36
1020±121
1951±248
糖尿病治疗组
194±24**##
596±47**#
1626±295*#
3974±365##
, http://www.100md.com
.P<0.05,..P<0.01与正常组比较;#P<0.05,##P<0.01与糖尿病对照组比较;
图1,伤后10日糖尿病对照组伤口组织切片
(苏木素染色×40)
图2,伤后10日糖尿病治疗组伤口组织切片
(苏木素染色×40)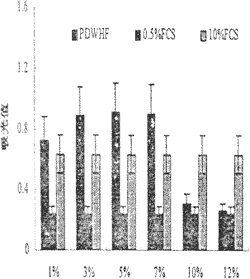
图3 不同浓度的PDWHF对鼠成纤维细胞增殖作用的影响
讨 论
, 百拇医药
糖尿病患者伤口愈合障碍的机理至今尚未阐明,但伤口局部微环境中各类生长因子的代谢平衡失调是导致糖尿病患者伤口愈合不良的重要原因之一。以往研究发现,伤口局部施用不同种类的外源性生长因子(如aFGF、bFGF、TGF-α、TGF-β、EGF/胰岛素)干预正常伤口愈合过程或愈合不良伤口均可增强伤口的抗张力强度,加速伤口的愈合,尤其是当数种生长因子伍用时效果更明显[1-3]。PDWHF是多种生长因子的混合物,含有PDGF、TGF-β、EGF、IGF-Ⅰ、PDEGF、PGF-4等,其对伤口愈合过程的影响作用及机理研究较少。本研究结果表明,在大鼠糖尿病“死腔伤口”模型中局部应用PDWHF后,伤口局部组织中DNA和羟脯氨酸含量较糖尿病对照组显著增加,伤口14日可恢复接近正常水平[9]。组织学可观察到伤口肉芽组织成纤维细胞明显增生,胶元沉积增加。离体实验发现浓度为1~7%时,PDWHF可刺激低浓度血清培养条件下成纤维细胞的增生。当PDWHF浓度为10%时,其促细胞增生作用已不再明显,PDWHF浓度达12%,其对成纤维细胞的综合作用表现为抑制效应。提示,PDWHF可通过促进伤口肉芽组织中的细胞增殖,增加胶原的合成与沉积,增强细胞的合成代谢进而促进伤口的愈合。PDWHF促进成纤维细胞的增殖可能与直接刺激细胞TGFβ mRNA及Ⅰ型胶原mRNA的表达,进而使细胞合成胶原基质等有关[10]。本研究结果还提示,PDWHF的促愈机制中,生长因子的相互促进与相互制约可能同时存在。而生长因子的相互制约在防止伤口愈合过度如疤痕疙瘩的形成中可能起着十分重要的作用。由于活体伤口微环境极为复杂,PDWHF对“死腔伤口”模型以及离体成纤维培养细胞的影响只能从某一个方面反映出在体时其生物学作用的规律[11]。因此,研究生长因子间的相互关系在伤口愈合机理中的作用,对指导临床应用生长因子有着重要的理论意义。
, http://www.100md.com
参考文献
1 Albertson S,Hummel RP,Breeden M,et al.PDGF and FGF reverse the healing impairment in protein-malmourished diabetic mice.Surg,1993,114:368-373
2 Brown RL,Breeden MP,and Greenhalgh DG.PDGF and TGF alpha act synergistically to improve wound healing in the genetically diabetic mouse.J Surg Res,1994,56:562-567
3 Mwllin TN,Cashen DE,Ronan JJ,et al.Acidic fibroblast growth factor accelerates dermal wound healing in diabetic mice.J Invest Dermal,1995,104:850-855
, http://www.100md.com
4 Niinikoski J,Renvall S,Laato M,et al.Effect of a Hexosylceramide fraction of the hemodialysate Socoseryl on experimental granulation tissue.Eur Surg Res,1986,18:58-64
5 Covington DS,Xue H,Pizzni R,et al.Streptoxocin and alloxan are comparable agents in the diabetic model impaired Wound healing.Diabetes Res,1993,23:47-53
6 Knighton DR,Ciresi K,Fiegel VD,et al.Stimulation of repair in chronic,nonhealing,cutaneous ulcer using platelet-derived wound healing formula.Surg Gyn & Obst,1990,170:56-61
, 百拇医药
7 郑少雄,蔡文仪,邱明才等.血、尿羟脯氨酸测定的方法改进.中华医学检验杂志.1983,6(3):157
8 朱旭东,张艳,陈荣德.伤口修复细胞的简易培养方法.中国修复重建外科杂志,1994,8(3):157
9 Miller EJ and Grat S.Collagen structure and function.In Wound healing biochemical and clinical aspects,Cohen IK,Diegelmann RF,and Lindlad WJ,editors.W.B.Saunders Company,1992,pp130
10 Clark R AF,Nielsen LD,Welch MP,et al.Collageen matrices attenuate the collagen synthetic response of cultured fibroblasts to TGF-β.J Cell Sci,1995,108:1251
11 Grant MB,Khaw PT,Schultz GS et al.Effect of epidermal growth factor beta on corneal cell chemotaxis.Invest Ophthalmol Vis Sci,1992,33(12):3292, http://www.100md.com
单位:第三军医大学大坪医院野战外科研究所一室
关键词:糖尿病;血小板源伤口愈合因子;伤口愈合
重庆医学990203
摘 要 本实验以糖尿病大鼠海绵死腔伤为难愈伤口模型结合离体细胞培养,研究血小板源伤口愈合因子(PDWHF)改善难愈伤口愈合的作用并探讨其可能机理。结果表明:局部应用PDWHF后,伤口组织总DNA、羟脯氨酸含量增高;组织学表现为肉芽组织中成纤维细胞显著增生,胶原纤维沉积增加。离体实验发现PDWHF可促进成纤维细胞的分化和增殖。提示:PDWHF可通过促进伤口肉芽组织中的细胞合成代谢及增殖,增加胶原的合成与沉积进而改善糖尿病伤口的愈合。
Study On The Mechanisms Of PDWHF On Impaired Wound
, http://www.100md.com
Healing In Rats With Diabetic Disease
Department One of Research Institute of Surgery & Daping Hospital
The 3 rd Military Medical University,Chongqing,400042
Zhong Yan,Zhu Xudong,Chen Rongde
Abstract:The experiment was designed to study the effects and mechanisms of PDWHF on the healing process of impaired wounds in diabetic rats,through the subcutaneous sponge implanted diabetic rats model and in vitro cell cultures.The results showed that local application with PDWHF could remarkably increase the content of DNA and hydroxyproline.Histological observations showed that there were obvious fibroblasts hyperplasia and increased collagen fibers deposition in the grannulation tissues.In vitro experiments demonstrated that PDWHF could promote the differentiation and proliferation of fibroblasts.It is suggested that PDWHF could improve the healing process of impaired diabetic wounds through the enhancement of synthetic metabolism and the proliferation of grannulation tissue cells,and the promotion of collagen synthesis and deposition.
, 百拇医药
Key words:Diabetes Platelet-derived wound healing factors Wound healing
糖尿病伤口愈合迟缓是临床上常见的难题,其有关机理尚未阐明,但至少与伤口组织细胞和伤口微环境生长因子的种类及含量失衡相关。探讨外源性生长因子改善糖尿病伤口愈合的可能性及作用机理一直是近年来伤口愈合研究领域中的重点内容之一[1-3]。血小板源伤口愈合因子(Platelet derived wound healing factors,PDWHF)是血小板在体外经凝血酶刺激脱颗粒时所释放的多种生长因子混合物,主要由血小板衍生长因子(PDGF)、表皮生长因子(EGF)、转 化生长因子-α/β(TFG-α/β)、胰岛素样生长因子-Ⅰ(IGF-Ⅰ)组成。本研究以糖尿病大鼠皮下“死腔伤”为伤口模型结合体外细胞培养实验,就PDWHF的促愈作用及相关机理进行了初步研究。
材料与方法
, 百拇医药
一、动物模型及分组:雄性SD大鼠44只,体重200~250g,分为三组。正常组(n=12),大鼠致伤在无菌条件下进行,大鼠麻醉、脱毛后,沿脊柱方向做两条深达筋膜长约4cm的平行切口,伤口距脊椎垂直距离约为1cm,钝性剥离伤口两端的皮肤,造成皮下袋囊,放入两块已消毒好的聚乙烯醇海绵(直径1cm,厚度0.2cm,重量8.6±0.22mg),缝合伤口。按J.Niinikoski法[4]术后当日及以后连续6日海绵注入20ul牛血清白蛋白液(5mg/ml)。糖尿病致伤对照组(n=16),腹腔注射新鲜配制四氧嘧啶(1.5mg/10g体重),测得血糖值大于180mg/dl一、二日后,即可致伤[5]。手术方式与正常组相同,于术后当日及以后连续6日海绵内注入20ul牛血清白蛋白液(5mg/ml)。糖尿病致伤治疗组(n=16),手术后当日及以后连续6日向海绵内注入20ul PDWHF液(5mg/ml)。PDWHF液参照Knighton方法[6]制备。
二、“死腔伤口”肉芽组织生长参数的测定:各组动物分别在伤后5、7、10、14日活杀,取出海绵,二联苯胺法测定其中总DNA、氯胺-T法测定羟脯氨酸量[7]。
, http://www.100md.com
三、离体实验:按本室建立的方法[8]培养伤口成纤维细胞,生长融合的细胞经0.25%胰蛋白酶消化30秒,倾去消化液,加入1640液洗涤2次,用1640/1%FCS培养液将细胞调成浓度为1×104/ml的细胞悬液,点接细胞悬液100ul到96孔培养板中,37℃、5%CO2条件卵下卵育12hr,吸去培养液,按加入的卵育液不同,将培养细胞分为三组:空白对照组:1640加0.5%FCS(简称BM);阳性对照组:1640加10%FCS;PDWHF处理组:BM/1%PDWHF、BM/3%PDWHF、BM/5%PDWHF、BM/7% PDWHF、BM/10%PDWHF、BM/12%PDWHF。待测样本与细胞共孵育48小时后,MTT法测定细胞的增殖情况。
结 果
一、糖尿病组、PDWHF治疗组伤口组织形态学观察:伤后10日PDWHF治疗组较糖尿病对照组伤口肉芽组织有明显的成纤维细胞增生、聚集,细胞呈长梭状较非治疗组成熟(图1,2)。
, http://www.100md.com
二、PDWHF促糖尿病大鼠肉芽组织生长:正常组、糖尿病组、PDWHF治疗组海绵中总DNA、羟脯氨酸含量及各组间比较结果(见表1、2)。
三、PDWHF对鼠伤口成纤维细胞增殖的影响:测定结果表明,在1%~7%的浓度范围内,PDWHF可显著促进伤口成纤维细胞的生长,明显高于0.5%FCS组(P<0.01);当PDWHF的浓度为10%时,其促生长作用已不再明显,与0.5%FCS组无显著差异(P>0.05),远远低于10%FCS组(P<0.01)。当PDWHF的浓度为12%时,其对伤口成纤维细胞的生长呈现出明显抑制作用(见图3)。
表1 各组动物伤后不同天数伤口海绵中DNA含量(微克/克湿海绵)
5日
7日
10日
, 百拇医药
14日
正常组
280±32
447±56
505±38
479±35
糖尿病对照组
63±12
123±14
215±24
386±36
糖尿病治疗组
177±24*##
, http://www.100md.com
328±32*##
464±28##
494±32#
.P<0.05,..P<0.01与正常组比较;#P<0.05,##P<0.01与糖尿病对照组比较;表2 各组动物伤后不同天数伤口海绵中羟脯氨酸含量(微克/克湿海绵)
5日
7日
10日
14日
正常组
301±31
817±93
, 百拇医药
2375±371
4243±306
糖尿病对照组
108±14
382±36
1020±121
1951±248
糖尿病治疗组
194±24**##
596±47**#
1626±295*#
3974±365##
, http://www.100md.com
.P<0.05,..P<0.01与正常组比较;#P<0.05,##P<0.01与糖尿病对照组比较;

图1,伤后10日糖尿病对照组伤口组织切片
(苏木素染色×40)

图2,伤后10日糖尿病治疗组伤口组织切片
(苏木素染色×40)

图3 不同浓度的PDWHF对鼠成纤维细胞增殖作用的影响
讨 论
, 百拇医药
糖尿病患者伤口愈合障碍的机理至今尚未阐明,但伤口局部微环境中各类生长因子的代谢平衡失调是导致糖尿病患者伤口愈合不良的重要原因之一。以往研究发现,伤口局部施用不同种类的外源性生长因子(如aFGF、bFGF、TGF-α、TGF-β、EGF/胰岛素)干预正常伤口愈合过程或愈合不良伤口均可增强伤口的抗张力强度,加速伤口的愈合,尤其是当数种生长因子伍用时效果更明显[1-3]。PDWHF是多种生长因子的混合物,含有PDGF、TGF-β、EGF、IGF-Ⅰ、PDEGF、PGF-4等,其对伤口愈合过程的影响作用及机理研究较少。本研究结果表明,在大鼠糖尿病“死腔伤口”模型中局部应用PDWHF后,伤口局部组织中DNA和羟脯氨酸含量较糖尿病对照组显著增加,伤口14日可恢复接近正常水平[9]。组织学可观察到伤口肉芽组织成纤维细胞明显增生,胶元沉积增加。离体实验发现浓度为1~7%时,PDWHF可刺激低浓度血清培养条件下成纤维细胞的增生。当PDWHF浓度为10%时,其促细胞增生作用已不再明显,PDWHF浓度达12%,其对成纤维细胞的综合作用表现为抑制效应。提示,PDWHF可通过促进伤口肉芽组织中的细胞增殖,增加胶原的合成与沉积,增强细胞的合成代谢进而促进伤口的愈合。PDWHF促进成纤维细胞的增殖可能与直接刺激细胞TGFβ mRNA及Ⅰ型胶原mRNA的表达,进而使细胞合成胶原基质等有关[10]。本研究结果还提示,PDWHF的促愈机制中,生长因子的相互促进与相互制约可能同时存在。而生长因子的相互制约在防止伤口愈合过度如疤痕疙瘩的形成中可能起着十分重要的作用。由于活体伤口微环境极为复杂,PDWHF对“死腔伤口”模型以及离体成纤维培养细胞的影响只能从某一个方面反映出在体时其生物学作用的规律[11]。因此,研究生长因子间的相互关系在伤口愈合机理中的作用,对指导临床应用生长因子有着重要的理论意义。
, http://www.100md.com
参考文献
1 Albertson S,Hummel RP,Breeden M,et al.PDGF and FGF reverse the healing impairment in protein-malmourished diabetic mice.Surg,1993,114:368-373
2 Brown RL,Breeden MP,and Greenhalgh DG.PDGF and TGF alpha act synergistically to improve wound healing in the genetically diabetic mouse.J Surg Res,1994,56:562-567
3 Mwllin TN,Cashen DE,Ronan JJ,et al.Acidic fibroblast growth factor accelerates dermal wound healing in diabetic mice.J Invest Dermal,1995,104:850-855
, http://www.100md.com
4 Niinikoski J,Renvall S,Laato M,et al.Effect of a Hexosylceramide fraction of the hemodialysate Socoseryl on experimental granulation tissue.Eur Surg Res,1986,18:58-64
5 Covington DS,Xue H,Pizzni R,et al.Streptoxocin and alloxan are comparable agents in the diabetic model impaired Wound healing.Diabetes Res,1993,23:47-53
6 Knighton DR,Ciresi K,Fiegel VD,et al.Stimulation of repair in chronic,nonhealing,cutaneous ulcer using platelet-derived wound healing formula.Surg Gyn & Obst,1990,170:56-61
, 百拇医药
7 郑少雄,蔡文仪,邱明才等.血、尿羟脯氨酸测定的方法改进.中华医学检验杂志.1983,6(3):157
8 朱旭东,张艳,陈荣德.伤口修复细胞的简易培养方法.中国修复重建外科杂志,1994,8(3):157
9 Miller EJ and Grat S.Collagen structure and function.In Wound healing biochemical and clinical aspects,Cohen IK,Diegelmann RF,and Lindlad WJ,editors.W.B.Saunders Company,1992,pp130
10 Clark R AF,Nielsen LD,Welch MP,et al.Collageen matrices attenuate the collagen synthetic response of cultured fibroblasts to TGF-β.J Cell Sci,1995,108:1251
11 Grant MB,Khaw PT,Schultz GS et al.Effect of epidermal growth factor beta on corneal cell chemotaxis.Invest Ophthalmol Vis Sci,1992,33(12):3292, http://www.100md.com