肺癌性胸液GST-π含量测定及临床意义
作者:谢家印 肖世全 邹强 张培炽
单位:
谢家印 肖世全 张培炽 第三军医大学大坪医院肿瘤科(重庆,400042);邹强 第三军医大学免疫学教研室(重庆,400038)
关键词:肺肿瘤;胸膜积液;恶性;谷胱甘肽S-转移酶/诊断应用
New Page 1
【摘要】目的:探讨肺癌性胸液GST-π含量与临床诊断和疗效关系。方法:采用BA-ELISA方法检测了279例肺癌患者(118例合并胸腔积液)血清和胸液GST-π含量。结果:118例肺癌患者(除15例小细胞肺癌患者外)血清及胸液GST-π含量明显高于健康人及胸肺良性病患者(P<0.01),且胸液GST-π含量明显高于其血清水平(P<0.01),肺癌患者胸液GST-π阳性率为65.2%,高于其血清水平(45.76%)。31例化疗有效的肺癌患者胸液GST-π水平明显低于72例化疗无效患者(29.97μg/L±7.78μg/L与34.01μg/L±9.98μg/L,P<0.05)。结论:胸液GST-π测定不但可作为非小细胞肺癌的诊断标志物,而且对预测联合化疗疗效有一定指导作用。
, http://www.100md.com
中图号:R734.2;R730.43 文献标识码:A 文章编号:1000-467X(1999)02-0203-02
Determination of pleural fluid GST-π in patients with
lung cancer and their clinical significance
XIE Jia-yin, XIAO Shi-quan, ZHOU Qang, et al.
Department of Tumor, DaPin Hospital, Third Military Medical University, Chongqing 400042,China
【Abstract】 Objective: To assess the relation between the pleural fluid GST-π and the clinical diagnosis or therapeutic respone in patients with lung cancer. Methods: GST-π level in serum and pleural fluid of 279 patients with lung cancer (including 118 patients complicating with pleural effusion) was measured by asandwich enzyme-linked immunosorbent assay. Results: Serum or pleural fluid GST-π level in 118 Patients with lung cancer (except 15 patients with small cell lung carcinoma) was higher than those of 30 healthy control subjects and 26 patients with benign pleuropulmonary disease (P<0.01),and then the positive rate of pleural fluid GST-π (65.2%) in the lung cancer patients was higher than their serum GST-π (45.76%), their GST-π ratio of pleural fluid to serum was more than 1.46 in approximately 60.17% of patients. Pleural fluid GST-π Level of 31 patients with non-small cell lung cancer responsing to chemotherapy was lower than those of 72 nonresponders (29.97μg/L± 7.78μg/L versus 34.01μg/L± 9.98μg/L,P< 0.05)。Conclusion: The pleural fluid GST-π level may be a useful marker in the diagnosis of lung cancer, and then it may be a parameter for predicting therapeutic response to combination chemotherapy regimens.
, 百拇医药
Key words: Lung neoplasma; Pleural effusion; Malignancy;Glutathione S-transferase-π /Diagnostic application
谷胱甘肽S-转移酶(Glutathione S-Transferase-π)在人体内分布广泛,主要在肾脏、胎盘及胎肝内含量较高,参与体内多种生物转化功能,如解毒和合成多种生理功能的蛋白质。近年来研究发现GST-π在肿瘤组织中明显高于正常组织,认为它与肿瘤细胞发生、发展密切相关[1]。本文检测了肺癌患者胸液GST-π含量,旨在对肺癌诊断和治疗提供参考依据。
1 材料与方法
1.1 对象
健康对照组:健康献血员标本30例。
, 百拇医药
胸肺良性病组:共26例,男性18例,女性8例,年龄31~68岁,平均为50.28岁,其中肺炎后胸膜炎7例,结核性胸膜炎13例,肺梗塞2例,膈下炎症(急性胰腺炎)2例,系统性红斑狼疮2例,根据胸膜活检及胸部摄片确定诊断。
肺癌组:共279例,男性188例,女性91例,年龄24~80岁,平均58.26岁,其中小细胞肺癌48例,鳞癌115例,腺癌105例,大细胞癌11例,279例中有胸腔积液118例(小细胞肺癌15例).全部病例均经胸膜活检,支纤镜及经皮肺活检等病理检查确诊,所有肺癌患者均接受2个疗程以上化疗,疗效评价参照统一标准[2]。
1.2 标本收集
留空腹新鲜全血4ml和常规胸穿抽液(胸水加抗凝剂)后,立即离心,取上清液加PMSF蛋白抑制剂,然后加少许5%NaN3防腐,置-80℃冰箱保存待测。纯化GST-π及兔抗人GST-π(军事医学科学院李春海教授惠赠),生物素化抗GST-π(自制),小牛血清,亲和素标记的辣根过氧化物酶(A-HRP,购自军事医学科学院),其余试剂均为国产分析纯。酶联仪为Bio-Red(美国),40孔聚苯乙烯酶联板为天津产。
, 百拇医药
1.3 BA-ELISA法测定GST-π
先用方阵滴定选择合适的抗GST-π抗体、B-IgG、A-HRP工作浓度,用BA-ELISA法测定GST-π标准曲线,然后测定待测血清、胸液标本。
1.4 统计
结果采用回归分析及方差分析,t检验进行统计学处理,浓度(μg/L)以均数±标准差(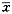 ±s)表示。
±s)表示。
2 结果
肺癌组血清GST-π含量显著高于健康人组(P<0.01),其阳性率分别为45.76%(54/118)、3.33%(1/30);肺癌组胸液GST-π含量显著高于胸肺良性病组(P<0.01),其阳性率分别为65.2%(77/118)、3.85%(1/26)。肺癌组胸液/血清GST-π比值也显著高于胸肺良性病组(P<0.01),其阳性率分别为60.17%(71/118)、3.85%(1/26),肺癌患者组胸液GST-π含量显著高于其血清水平(P<0.01),而胸肺良性病组中胸液和血清GST-π含量无显著性差异(P>0.05)见表1。
, http://www.100md.com
表1 血清和胸液GST-π测定结果(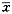 ±s)(μg/L)
±s)(μg/L)
对象
血清
胸液
胸液/血清
GST-π
n
GST-π
n
GST-π
, http://www.100md.com
健康对照组
30
9.28±2.10
胸肺良性组
26
10.91±3.90
26
11.25±2.46△
1.04±0.21
肺癌组
279
17.81±5.95▲
, 百拇医药
118
25.97±9.85▲*
1.54±0.84▲
△胸肺良性组胸液与血清比较P>0.05
▲肺癌组血清、胸液GST-π及胸液/血清GST-π比值与良性组比较P<0.01
*肺癌组胸液与血清比较P<0.01
103例各型非小细胞肺癌患者之间其胸液GST-π含量及胸液/血清GST-π比值均无显著性差异(P>0.05),但均显著高于小细胞肺癌组(P<0.01)见表2。
表2 各型肺癌胸液GST-π测定结果(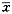 ±s)(μg/L)
±s)(μg/L)
, http://www.100md.com
分型
n
胸液
胸液/血清
GST-π
GST-π
小细胞肺癌
15
11.38±4.59
1.16±0.11
腺癌
48
31.72±8.30*
, http://www.100md.com
1.72±0.16*
鳞癌
50
30.55±5.28*
1.71±0.39*
大细胞癌
5
30.45±6.21*
1.66±0.10*
*与小细胞肺癌比较P<0.01
15例小细胞肺癌(13例化疗有效,2例化疗无效)其胸液GST-π含量均低于良性胸液或胸液/血清GST-π比值的上限值。31例非小细胞肺癌对化疗有效,72例无效,其胸液GST-π阳性率分别为48.39%(15/31)、70.83%(51/72)。有效组患者胸液/血清GST-π比值低于上限值1.46占64.52%(20/31),而无效组患者占26.39%(19/72)。两组比较,有效组患者胸液GST-π含量或胸液/血清GST-π比值均明显低于无效组患者(P<0.05)见表3。所有患者胸液GST-π含量及胸液/血清GST-π比值与化疗方案、胸液量及性质均无显著差异。
, 百拇医药
表3 胸液GST-π与非小细胞肺癌化疗疗效关系比较
疗效
n
GST-π(μg/L)
胸液/血清GST-π
有效组
31
29.97±7.78☆
1.58±0.31☆
无效组
72
34.01±9.98
, 百拇医药
1.76±0.38
★有效组与无效组比较P<0.05
3 讨论
研究表明GST-π在多种肿瘤组织中表达增加,可能与肿瘤细胞生长、代谢有关,也有将GST-π作为胃癌、肝癌等癌前期标记物[3]。正常肺组织细胞GST-π表达极少,而在肺癌旁病变组织及癌组织中GST-π的表达明显高于正常肺组织[4,5]。本文观察了279例肺癌患者血清GST-π含量变化,其结果与国外报道一致[6],认为血清GST-π含量测定可作为肺癌诊断的标记物。通过测定118例肺癌患者胸液中GST-π含量均值为25.97μg/L±9.85μg/L(阳性率为65.2%)明显高于其患者血清水平(阳性率为45.76%),其胸液/血清GST-π比值阳性率为60.17%。结果提示非小细胞肺癌胸液GST-π含量(或阳性率)高于其血清水平,其中胸液/血清GST-π比值测定更能准确反映肺癌患者胸液GST-π含量的实际水平,还可排除非肺源性因素的干扰。其中15例小细胞肺癌患者胸液GST-π含量与胸、肺良性者无显著性差异,此现象可能与小细胞肺癌组织细胞缺乏产生GST-π的能力有关。
, 百拇医药
有报道肺癌细胞表达GST-π水平与化疗耐药性也密切相关。周中军等[7]体外研究发现阿霉素耐药性肺癌细胞株(GLC/ADM)表达GST-π大约比GLC细胞高10倍,通过反义GST-πRNA介入其细胞对阿霉素耐药性降低。Cheng等[8]研究发现卵巢癌细胞高表达GST-π与对铂类药物易产生耐药性相关。本实验结果表明小细胞肺癌胸液GST-π含量测定对其诊断及化疗疗效观察意义不大,而在非小细胞肺癌对化疗有效患者,其胸液GST-π水平(29.97μg/L±7.78μg/L)均明显低于无效患者(34.01μg/L±9.98μg/L)。因此通过测定非小细胞肺癌患者胸液GST-π对预测化疗疗效有一定指导意义。
参考文献
1 Howie AF, Forrester LM, Glancey MJ, et al. Glutathione S transferase and glutathione peroxidase expression in normal and tumor human tissues〔J〕. Carcinogenesis, 1990, 11:451.
, http://www.100md.com
2 查人俊主编.现代肺癌诊断与治疗〔J〕.北京:人民军医出版社,1993:291.
3 Sato K. Glutathion transferase as marker of preneoplasia and neoplasia〔J〕. Adv Cancer Res, 1989, 52:205.
4 聂坤荣,李春海,诸亚君,等.肺癌谷胱甘肽硫转移酶表达的免疫组化研究〔J〕.中华结核和呼吸杂志,1993,16(3):141.
5 di Ilio C, Del Boccio G, Aceto A, et al. Elevation of glutathione transferase activity in human lung tumor〔J〕.Carcinogenesis, 1988,9:335.
6 toyoaki Hida MD, Masaki Kuwabara BS, Yutaka Ariyoski MD, et al. Serum Glutathion S-transferase-π level as a tumor marker for non-small cell lung cancer〔J〕. Cancer March 1, 1994,73:1377.
, 百拇医药
7 周中军,金顺钱,罗贤懋,等.谷胱甘肽-硫转移酶在肺癌细胞耐药中的作用〔J〕.生物化学杂志,1996,12(2):196.
8 Xiusi Cheng MD, Junzo Kigawa MD, Yukihisa Minagawa MD, et al. Glutathion S transferase π expression and glutathione concentration in ovarian Carcinoma before and after chemotherapy〔J〕.Cancer February 1, 1997,79(3):521.
收稿日期:1998-02-19;修回日期:1999-01-07, 百拇医药
单位:
谢家印 肖世全 张培炽 第三军医大学大坪医院肿瘤科(重庆,400042);邹强 第三军医大学免疫学教研室(重庆,400038)
关键词:肺肿瘤;胸膜积液;恶性;谷胱甘肽S-转移酶/诊断应用
New Page 1
【摘要】目的:探讨肺癌性胸液GST-π含量与临床诊断和疗效关系。方法:采用BA-ELISA方法检测了279例肺癌患者(118例合并胸腔积液)血清和胸液GST-π含量。结果:118例肺癌患者(除15例小细胞肺癌患者外)血清及胸液GST-π含量明显高于健康人及胸肺良性病患者(P<0.01),且胸液GST-π含量明显高于其血清水平(P<0.01),肺癌患者胸液GST-π阳性率为65.2%,高于其血清水平(45.76%)。31例化疗有效的肺癌患者胸液GST-π水平明显低于72例化疗无效患者(29.97μg/L±7.78μg/L与34.01μg/L±9.98μg/L,P<0.05)。结论:胸液GST-π测定不但可作为非小细胞肺癌的诊断标志物,而且对预测联合化疗疗效有一定指导作用。
, http://www.100md.com
中图号:R734.2;R730.43 文献标识码:A 文章编号:1000-467X(1999)02-0203-02
Determination of pleural fluid GST-π in patients with
lung cancer and their clinical significance
XIE Jia-yin, XIAO Shi-quan, ZHOU Qang, et al.
Department of Tumor, DaPin Hospital, Third Military Medical University, Chongqing 400042,China
【Abstract】 Objective: To assess the relation between the pleural fluid GST-π and the clinical diagnosis or therapeutic respone in patients with lung cancer. Methods: GST-π level in serum and pleural fluid of 279 patients with lung cancer (including 118 patients complicating with pleural effusion) was measured by asandwich enzyme-linked immunosorbent assay. Results: Serum or pleural fluid GST-π level in 118 Patients with lung cancer (except 15 patients with small cell lung carcinoma) was higher than those of 30 healthy control subjects and 26 patients with benign pleuropulmonary disease (P<0.01),and then the positive rate of pleural fluid GST-π (65.2%) in the lung cancer patients was higher than their serum GST-π (45.76%), their GST-π ratio of pleural fluid to serum was more than 1.46 in approximately 60.17% of patients. Pleural fluid GST-π Level of 31 patients with non-small cell lung cancer responsing to chemotherapy was lower than those of 72 nonresponders (29.97μg/L± 7.78μg/L versus 34.01μg/L± 9.98μg/L,P< 0.05)。Conclusion: The pleural fluid GST-π level may be a useful marker in the diagnosis of lung cancer, and then it may be a parameter for predicting therapeutic response to combination chemotherapy regimens.
, 百拇医药
Key words: Lung neoplasma; Pleural effusion; Malignancy;Glutathione S-transferase-π /Diagnostic application
谷胱甘肽S-转移酶(Glutathione S-Transferase-π)在人体内分布广泛,主要在肾脏、胎盘及胎肝内含量较高,参与体内多种生物转化功能,如解毒和合成多种生理功能的蛋白质。近年来研究发现GST-π在肿瘤组织中明显高于正常组织,认为它与肿瘤细胞发生、发展密切相关[1]。本文检测了肺癌患者胸液GST-π含量,旨在对肺癌诊断和治疗提供参考依据。
1 材料与方法
1.1 对象
健康对照组:健康献血员标本30例。
, 百拇医药
胸肺良性病组:共26例,男性18例,女性8例,年龄31~68岁,平均为50.28岁,其中肺炎后胸膜炎7例,结核性胸膜炎13例,肺梗塞2例,膈下炎症(急性胰腺炎)2例,系统性红斑狼疮2例,根据胸膜活检及胸部摄片确定诊断。
肺癌组:共279例,男性188例,女性91例,年龄24~80岁,平均58.26岁,其中小细胞肺癌48例,鳞癌115例,腺癌105例,大细胞癌11例,279例中有胸腔积液118例(小细胞肺癌15例).全部病例均经胸膜活检,支纤镜及经皮肺活检等病理检查确诊,所有肺癌患者均接受2个疗程以上化疗,疗效评价参照统一标准[2]。
1.2 标本收集
留空腹新鲜全血4ml和常规胸穿抽液(胸水加抗凝剂)后,立即离心,取上清液加PMSF蛋白抑制剂,然后加少许5%NaN3防腐,置-80℃冰箱保存待测。纯化GST-π及兔抗人GST-π(军事医学科学院李春海教授惠赠),生物素化抗GST-π(自制),小牛血清,亲和素标记的辣根过氧化物酶(A-HRP,购自军事医学科学院),其余试剂均为国产分析纯。酶联仪为Bio-Red(美国),40孔聚苯乙烯酶联板为天津产。
, 百拇医药
1.3 BA-ELISA法测定GST-π
先用方阵滴定选择合适的抗GST-π抗体、B-IgG、A-HRP工作浓度,用BA-ELISA法测定GST-π标准曲线,然后测定待测血清、胸液标本。
1.4 统计
结果采用回归分析及方差分析,t检验进行统计学处理,浓度(μg/L)以均数±标准差(
2 结果
肺癌组血清GST-π含量显著高于健康人组(P<0.01),其阳性率分别为45.76%(54/118)、3.33%(1/30);肺癌组胸液GST-π含量显著高于胸肺良性病组(P<0.01),其阳性率分别为65.2%(77/118)、3.85%(1/26)。肺癌组胸液/血清GST-π比值也显著高于胸肺良性病组(P<0.01),其阳性率分别为60.17%(71/118)、3.85%(1/26),肺癌患者组胸液GST-π含量显著高于其血清水平(P<0.01),而胸肺良性病组中胸液和血清GST-π含量无显著性差异(P>0.05)见表1。
, http://www.100md.com
表1 血清和胸液GST-π测定结果(
对象
血清
胸液
胸液/血清
GST-π
n
GST-π
n
GST-π
, http://www.100md.com
健康对照组
30
9.28±2.10
胸肺良性组
26
10.91±3.90
26
11.25±2.46△
1.04±0.21
肺癌组
279
17.81±5.95▲
, 百拇医药
118
25.97±9.85▲*
1.54±0.84▲
△胸肺良性组胸液与血清比较P>0.05
▲肺癌组血清、胸液GST-π及胸液/血清GST-π比值与良性组比较P<0.01
*肺癌组胸液与血清比较P<0.01
103例各型非小细胞肺癌患者之间其胸液GST-π含量及胸液/血清GST-π比值均无显著性差异(P>0.05),但均显著高于小细胞肺癌组(P<0.01)见表2。
表2 各型肺癌胸液GST-π测定结果(
, http://www.100md.com
分型
n
胸液
胸液/血清
GST-π
GST-π
小细胞肺癌
15
11.38±4.59
1.16±0.11
腺癌
48
31.72±8.30*
, http://www.100md.com
1.72±0.16*
鳞癌
50
30.55±5.28*
1.71±0.39*
大细胞癌
5
30.45±6.21*
1.66±0.10*
*与小细胞肺癌比较P<0.01
15例小细胞肺癌(13例化疗有效,2例化疗无效)其胸液GST-π含量均低于良性胸液或胸液/血清GST-π比值的上限值。31例非小细胞肺癌对化疗有效,72例无效,其胸液GST-π阳性率分别为48.39%(15/31)、70.83%(51/72)。有效组患者胸液/血清GST-π比值低于上限值1.46占64.52%(20/31),而无效组患者占26.39%(19/72)。两组比较,有效组患者胸液GST-π含量或胸液/血清GST-π比值均明显低于无效组患者(P<0.05)见表3。所有患者胸液GST-π含量及胸液/血清GST-π比值与化疗方案、胸液量及性质均无显著差异。
, 百拇医药
表3 胸液GST-π与非小细胞肺癌化疗疗效关系比较
疗效
n
GST-π(μg/L)
胸液/血清GST-π
有效组
31
29.97±7.78☆
1.58±0.31☆
无效组
72
34.01±9.98
, 百拇医药
1.76±0.38
★有效组与无效组比较P<0.05
3 讨论
研究表明GST-π在多种肿瘤组织中表达增加,可能与肿瘤细胞生长、代谢有关,也有将GST-π作为胃癌、肝癌等癌前期标记物[3]。正常肺组织细胞GST-π表达极少,而在肺癌旁病变组织及癌组织中GST-π的表达明显高于正常肺组织[4,5]。本文观察了279例肺癌患者血清GST-π含量变化,其结果与国外报道一致[6],认为血清GST-π含量测定可作为肺癌诊断的标记物。通过测定118例肺癌患者胸液中GST-π含量均值为25.97μg/L±9.85μg/L(阳性率为65.2%)明显高于其患者血清水平(阳性率为45.76%),其胸液/血清GST-π比值阳性率为60.17%。结果提示非小细胞肺癌胸液GST-π含量(或阳性率)高于其血清水平,其中胸液/血清GST-π比值测定更能准确反映肺癌患者胸液GST-π含量的实际水平,还可排除非肺源性因素的干扰。其中15例小细胞肺癌患者胸液GST-π含量与胸、肺良性者无显著性差异,此现象可能与小细胞肺癌组织细胞缺乏产生GST-π的能力有关。
, 百拇医药
有报道肺癌细胞表达GST-π水平与化疗耐药性也密切相关。周中军等[7]体外研究发现阿霉素耐药性肺癌细胞株(GLC/ADM)表达GST-π大约比GLC细胞高10倍,通过反义GST-πRNA介入其细胞对阿霉素耐药性降低。Cheng等[8]研究发现卵巢癌细胞高表达GST-π与对铂类药物易产生耐药性相关。本实验结果表明小细胞肺癌胸液GST-π含量测定对其诊断及化疗疗效观察意义不大,而在非小细胞肺癌对化疗有效患者,其胸液GST-π水平(29.97μg/L±7.78μg/L)均明显低于无效患者(34.01μg/L±9.98μg/L)。因此通过测定非小细胞肺癌患者胸液GST-π对预测化疗疗效有一定指导意义。
参考文献
1 Howie AF, Forrester LM, Glancey MJ, et al. Glutathione S transferase and glutathione peroxidase expression in normal and tumor human tissues〔J〕. Carcinogenesis, 1990, 11:451.
, http://www.100md.com
2 查人俊主编.现代肺癌诊断与治疗〔J〕.北京:人民军医出版社,1993:291.
3 Sato K. Glutathion transferase as marker of preneoplasia and neoplasia〔J〕. Adv Cancer Res, 1989, 52:205.
4 聂坤荣,李春海,诸亚君,等.肺癌谷胱甘肽硫转移酶表达的免疫组化研究〔J〕.中华结核和呼吸杂志,1993,16(3):141.
5 di Ilio C, Del Boccio G, Aceto A, et al. Elevation of glutathione transferase activity in human lung tumor〔J〕.Carcinogenesis, 1988,9:335.
6 toyoaki Hida MD, Masaki Kuwabara BS, Yutaka Ariyoski MD, et al. Serum Glutathion S-transferase-π level as a tumor marker for non-small cell lung cancer〔J〕. Cancer March 1, 1994,73:1377.
, 百拇医药
7 周中军,金顺钱,罗贤懋,等.谷胱甘肽-硫转移酶在肺癌细胞耐药中的作用〔J〕.生物化学杂志,1996,12(2):196.
8 Xiusi Cheng MD, Junzo Kigawa MD, Yukihisa Minagawa MD, et al. Glutathion S transferase π expression and glutathione concentration in ovarian Carcinoma before and after chemotherapy〔J〕.Cancer February 1, 1997,79(3):521.
收稿日期:1998-02-19;修回日期:1999-01-07, 百拇医药