高碘对小鼠抗氧化能力的影响
作者:项建梅 陈祖培 邸红军 阎玉芹 陈贯一
单位:项建梅 陈祖培 阎玉芹 陈贯一 天津医科大学 内分泌研究所,天津 300070;邸红军 天津医科大学 基础医学院,天津 300070
关键词:高碘甲肿;抗氧化酶;脂质过氧化物
高碘对小鼠抗氧化能力的影响 摘要 目的 对高碘4、6、12个月时期的小鼠甲状腺形态学、甲状腺激素及抗氧化能力进行动态观察研究。方法 采用生化方法测定血、脑组织、甲状腺组织中SOD、CAT、GSH-Px、LPO及血清T3、T4。结果 高碘甲肿显示为弥漫胶质性甲状腺肿,在甲肿形成过程中血清T4一直处于较高水平。此外,抗氧化能力测定结果显示4个月时虽已出现甲肿且血中抗氧化酶活性降低,LPO升高,但脑和甲状腺组织的抗氧化能力呈代偿过程,6个月后SOD、GSH-Px活性均降低,同时LPO含升高。呈现失代偿。结论 提示自由基损伤作用加重了高碘对机体特别是甲状腺的直接损害。
, 百拇医药
中图分类号 Q613.44;Q954.62 [文献标识码]A [文章编号]1000-4955(1999)04-0245-04
Effects of iodine excess on antioxidizing ability of mice
XIANG Jian-mei,CHEN Zu-pei,DI Hong-jun,et al
(The institute of Endocrinology,Tianjin Medical University,Tianjin 300070,China)
Abstract Objective To study the morphology of thyroid,hormone level in serum and antioxidizing ability of the mice which fed with iodine excess food in three different peroid of four,six and twelve month.Methods Biochemical method was used to determine not only the SOD.CAT.GSH-Px.LPO level in blood brain tissue and thyroid tissue but also T3,T4 level in serum.Results Iodine excess goiter formed wide apread glutinous goiter,and T4 in serum was still in high level in the forming course.Moreover the activity of antioxidizing enzyme reduced and LPO rose four months later,but antioxidizing ability in brain and thyroid however showed within compensation.With LPO rising constantly,the activity of SOD and GSH-Px decreased considerably and the compensation was broken six months later.Conclusions The damage of body espicially the thyroid caused by iodine excess was aggravated by radical injury.
, 百拇医药
Key words LPO;Indine excess goiter;Antioxidizing enzyme
多年来大量流行病学调查及动物实验分析表明,摄入过量碘也可以引起甲状腺肿,即高碘甲肿。高碘同低碘一样对人体有极大危害,可导致许多碘过多疾病的发生。因此受到许多科研人员的重视,从各种不同途径进行了大量研究。本实验在给动物饲以高碘水后3个不同时期对其甲状腺形态学、甲状腺激素以及血、甲状腺及脑组织的谷胱甘肽过氧化物酶(GSH-Px)、超氧化物歧化酶(SOD)、过氧化氢酶(CAT)的活性及脂质过氧化物(LPO)的含量进行了观察和分析,现报告如下。
1 材料与方法
1.1 动物模型复制:采用纯系昆明小鼠,生后3周断乳,体重为18~22g,雌雄各半。随机分为两组,即高碘实验组(HI)和正常对照组(NI)(各90只)。两组均饲以标准鼠饲料(碘含量为150~180ng/g),实验组饮含碘化钾的去离子水,浓度为3000μg/L。对照组饮用自来水(碘含量为2~4μg/L)。以上两组分别在喂养4、6、12个月时各处死30只。
, 百拇医药
1.2 样品制备:动物断头取抗凝和不抗凝血以及脑、甲状腺组织。全血测GSH-Px(单位以U/ml表示)、CAT(单位以U/gHb表示)活性,分离血浆测LPO(单位以nM/ml表示)含量,用生理盐水洗红细胞3次,3000rpm 10min,得红细胞压积,加一倍冷去离子水制成溶血液,测SOD(单位以NU/gHb表示)活性。甲状腺称重后,制成组织切片。其余脑和甲状腺组织在冰浴下用pH7.4的PBS制备成20%脑匀浆液和10%甲状腺匀浆液,测定GSH-Px(U/mgPr)、SOD(NU/mgPr)、LPO(nM/mgPr)。不抗凝血分离血清测三碘甲腺原氨酸(T3,ng/ml)、四碘甲腺原氨酸(T4,ng/ml)、促甲状腺激素受体抗体(TRAb)。
1.3 组织形态学观察:光镜下观察甲状腺形态变化,对甲状腺组织的形态进行分析和研究。
1.4 激素及抗氧化能力测定:CAT、SOD、GSH-Px、LPO检测均采用南京建成生物工程研究所生产的试剂盒进行测定。血清T3、T4的测定均采用放射免疫分析法。TRAb测定采用天津医科大学生物制药厂生产的药盒,用酶联免疫吸附测定法测定。
, 百拇医药
2 实验结果
2.1 体重、甲状腺和脑重比较:实验结果显示各时期HI组甲状腺重量及甲状腺/体重比均明显高于NI组,两组脑重无明显变化(见表1)。
表1 体重、甲状腺与脑湿重(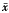 ±s)
±s)
组别
例数
体重(g)
甲状腺(mg)
脑(mg)
甲状腺/体重(mg/g)
, 百拇医药
NI4
HI4
34
41
40.1±3.5
37.7±4.1**
3.79±0.89
6.02±1.59**
422.3±36.4
425.4±30.0
0.094±0.027
0.162±0.050**
, 百拇医药
NI6
HI6
38
25
39.8±6.07
39.6±5.36
4.64±1.08
5.61±1.79**
407.9±27.8
410.5±26.2
0.123±0.031
0.144±0.039*
, 百拇医药
NI12
HI12
30
31
40.9±5.77
42.2±3.85
3.50±1.02
7.84±3.57*
412.9±25.4
426.8±17.9
0.086±0.020
0.184±0.079*
, 百拇医药
注:HI组与NI组相比,*P<0.05;**P<0.01
2.2 组织形态学观察:肉眼所见:NI组小鼠甲状腺大小正常,为淡红色,质软。三个不同时期HI组小鼠甲状腺体积均明显大于同期NI组,为淡肤色,随高碘时间延长,质地韧实感增强,12个月时韧如橡皮。光镜所见:NI组甲状腺滤泡多呈圆或椭圆形,中等大小,滤泡上皮细胞多为立方形,滤泡腔内充满胶质,滤泡间偶见新生小滤泡(见图1)。HI组甲状腺滤泡明显增大,上皮细胞多为扁平状,滤泡腔内充满丰富浓染胶质,滤泡间隙小血管未见明显充血,亦未见明显增生小滤泡(见图2)。
图1 正常组小鼠甲状腺组织H.E×100
, 百拇医药
图2 高碘组(1年时)小鼠甲状腺组织H.E×100
2.3 甲状腺激素测定:激素测定结果显示3个不同时期血清T3与NI组相比均无明显差异,而血清T4在整个高碘甲肿形成过程中,一直维持较高水平,均显著高于同期NI组,并且HI组T3/T4比值也明显低于NI组。HI组TRAb值在6个月时明显高于NI组,4和12个月时未见差异(见表2)。
表2 甲状腺激素的变化(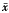 ±s)
±s)
组别
例数
, http://www.100md.com T3(ng/ml)
T4(ng/ml)
T3/T4
TRAb(S/M值)
NI4
HI4
8
8
1.041±0.17
0.948±0.15
77.65±11.03
, 百拇医药
94.07±11.36*
0.014±0.003
0.010±0.002*
0.68±0.03
0.66±0.03
NI6
HI6
10
9
1.109±0.37
1.394±0.29
, 百拇医药 29.00±9.38
57.67±9.56**
0.034±0.005
0.025±0.005*
0.44±0.07
0.60±0.04**
NI12
HI12
10
10
1.128±0.32
, 百拇医药
0.938±0.17
38.54±10.06
50.99±15.16*
0.030±0.007
0.020±0.005**
0.45±0.09
0.40±0.09
注:HI组与NI组相比,*P<0.05;**P<0.01
2.4 抗氧化能力测定
2.4.1 血液中抗氧化酶活性及LPO含量:HI组血液中的SOD活性从4个月时就比NI组显著降低,且LPO含量明显升高(P<0.01)。全血CAT活性仅6个月时降低,其余各期CAT活性与对照组无显著差异,GSH-Px活性4、6、12个月与对照组比较均无差异。(见表3)
, http://www.100md.com
表3 血液中抗氧化酶活性及LPO含量测定(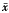 ±s)
±s)
组别
例数
CAT(U/gHb)
SOD(NU/gHb)
GSH-Px(U/ml)
LPO(nM/ml)
NI4
HI4
14
, 百拇医药
14
72.0±16.7
68.2±17.6
14807.4±1553.6
13139.6±1103.9**
5.75±0.62
5.67±0.41
8.20±1.9
13.63±4.4**
NI6
HI6
, 百拇医药
20
20
80.4±14.8
70.9±8.85*
14757.0±960.6
14095.6±729.8*
1.95±0.80
2.31±1.02
9.41±1.71
11.90±1.63*
NI12
, http://www.100md.com
HI12
16
16
94.86±17.9
96.20±20.4
15810.4±1711.0
14577.9±948.8*
17.28±3.63
18.50±2.25
20.09±5.91
25.06±6.48*
, 百拇医药
注:HI组与NI组相比,*P<0.05;**P<0.01
2.4.2 脑组织中抗氧化酶活性及LPO含量:结果显示HI组SOD活性4个月时即降低,而GSH-Px活性4个月时升高,这可能是代偿性机制所致,6个月时降低,LPO含量4个月时明显降低,而6个月、12个月时明显升高。(见表4)。
表4 脑中抗氧化酶活性及LPO含量测定(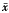 ±s)
±s)
组别
例数
SOD(NU/mgPr)
GSH-Px(U/mgPr)
, 百拇医药
LPO(nM/mgPr)
NI4
HI4
20
20
428.4±22.4
398.52±27.6**
7.52±0.92
9.47±0.67**
3.01±0.39
2.45±0.21**
, 百拇医药
NI6
HI6
16
16
283.6±20.4
254.1±27.3
3.87±0.81
3.08±0.63*
1.83±0.36
2.17±0.48*
NI12
HI12
, http://www.100md.com
16
16
243.0±28.6
220.7±23.5*
6.33±0.99
5.64±0.78*
2.48±0.31
2.84±0.30*
注:HI组与NI组相比,*P<0.05;**P<0.01
2.4.3 甲状腺抗氧化酶活性及LPO测定:结果显示4个月时HI组GSH-Px活性升高,6个月、12个月时降低;SOD活性12个月时才明显下降;而LPO含量4个月时降低,6个月、12个月时升高(见表5)。
, http://www.100md.com
表5 甲状腺中抗氧化酶活性及LPO含量测定(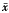 ±s)
±s)
组别
例数
SOD(NU/mgPr)
GSH-Px(U/mgPr)
LPO(nM/mgPr)
NI4
HI4
30
30
, http://www.100md.com
165.7±2.25
166.3±6.1
4.69±0.23
5.80±0.13**
1.15±0.07
1.01±0.1**
NI6
HI6
30
30
279.7±8.6
270.6±6.0
, 百拇医药
6.03±0.56
5.04±0.12**
1.07±0.18
1.29±0.02*
NI12
HI12
30
30
226.1±11.0
193.7±4.87*
7.00±2.23
, 百拇医药
4.15±0.58*
1.27±0.12
1.74±0.12*
注:HI组与NI组相比,*P<0.05;**P<0.01
3 讨论
对于高碘甲肿发病机理的认识说法很多,多数学者认为与碘阻断效应(又称Wolff-Chaikoff effect)密切相关,它是由于碘抑制了甲状腺内过氧化酶的活性,从而影响到甲状腺激素合成过程中原子碘的活化、酪氨酸的活化及其有机化过程[1]。而近年来的研究证明,高碘甲肿的发病机理是甲状腺胶质(T4、T3、二碘甲腺原氨酸、一碘甲腺原氨酸)在甲状腺滤泡腔中过度堆积的结果[2]。本实验形态学观察结果显示HI组甲状腺腺体色淡,质地韧如橡皮,滤泡明显增大,上皮细胞多为扁平状,滤泡腔内充满丰富胶质,滤泡间隙小血管未见明显充血,亦未见明显增生小滤泡。这与以往报导一致[3],可证实实验动物高碘甲肿主要是由于滤泡腔内胶质增多引起的大滤泡胶质性甲状腺肿,外观色淡是由于间隙小血管血流减少所至,而泡腔内胶质过多堆积导致了腺体的韧实感。关于甲状腺激素测定的结果,流行病学调查发现高碘病人血清T3、T4都在正常范围[1,4,5]。而实验性高碘动物模型血清T3、T4测定结果报导不尽相同,朱惠民等于1986和1988年分别报导结果为T3、T4各组间差异无显著性意义[4];在1989年报导T4高于对照组,T3降低,T3/T4比值低于对照组[2];而1995年报导为T4显著高于对照组,T3两组间差异无显著性意义[6]。本实验结果为HI组T4显著高于NI组,T3两组间差异无显著性意义,HI组T3/T4比值低于NI组。这一结果进一步证实了高碘甲肿并不是像低碘甲肿一样由于血清T4降低导致垂体分泌TSH过多刺激甲状腺肿大,而是在高碘状态下,甲状腺合成了较多的甲状腺激素,为了保持机体的正常代谢,通过机体的自动调节将大量激素储存在甲状腺滤泡内,致使形成胶质性甲肿。这与以往报导一致[6]。
, 百拇医药
近年来有关自由基损伤与疾病的关系的研究已涉及许多系统,其中对自由基损伤作用与地方性甲状腺肿和地方性克汀病的发病机理的研究已逐步展开,由于高碘同样可引起许多碘过多疾病,因而研究高碘状态下机体抗氧化能力的变化,对进一步了解高碘与甲肿及其它高碘疾病的关系有一定的意义。
本文测定了动物饲以高碘后4、6、12个月3个不同时期全血CAT、GSH-Px、红细胞SOD活性及血浆LPO含量;脑及甲状腺组织中SOD、GSH-Px活性及LPO含量。结果显示:高碘4个月时血中SOD活性下降、LPO含量升高。4个月以后各种抗氧酶活性持续下降,LPO持续升高,脑组织中4个月时SOD活性下降、GSH-Px活性代偿性升高、LPO含量降低;6个月后SOD、GSH-Px活性均降低,同时LPO含量升高。甲状腺中4个月时GSH-Px活性升高、其升高可能是代偿性机制所致。LPO含量下降;6个月时GSH-Px活性降低,LPO含量升高;12个月时SOD、GSH-Px活性降低,LPO含量升高。研究结果证实高碘4个月后,虽然已出现甲肿,并且血液中抗氧化过酶活性降低,LPO升高,呈现典型失代偿过程。但是脑组织和甲状腺中抗氧化酶活性有不同程度升高,还可以保护脑和甲状腺免受自由基损伤。而6个月后代偿能力逐渐下降而呈失代偿过程,无法抵抗自由基损伤,加重高碘对机体特别是对甲状腺的损害。由于自由基特别是LPO直接损伤含磷脂的细胞膜则诱发自家免疫过程,这也可进一步解释高碘性甲状腺肿的部分病人并发自家免疫性甲状腺疾病,但这一发病环节有待进一步证实。
, http://www.100md.com
基金来源:天津市自然科学基金资助项目(942409002)
作者简介:项建梅,女,1967年生,学士
参考文献
[1] 卢倜章,马 泰.高碘性甲状腺肿[J].新医学,1983,14(9):500.
[2] 朱惠民,王凤荣,尹桂山,等.高碘地方性甲状腺肿发病机理的实验研究[J].中国地方病学杂志,1989,8(4):220.
[3] 山东省医学科学院.高碘甲状腺肿实验动物模型的研究[A].第二届全国地方性甲状腺肿地方性克汀病学术会议资料汇编[C].中国地方病学杂志编辑部,1984.342.
[4] 朱惠民,胡宣扬,姚玉霞,等.实验性高碘甲状腺肿[J].中国地方病学杂志,1986,5(1):1.
[5] 马 泰,卢倜章,于志恒.碘缺乏病[M].北京:人民卫生出版社,1993.116.
[6] 朱惠民,秦 立,于志恒.甲状腺激素治疗高碘甲状腺肿的实验研究[A].全国第五届碘缺乏病学术会议论文专辑[C].中国地方病学杂志编辑部,1995.113.
收稿日期1997-10-17;修行日期1998-06-04, http://www.100md.com
单位:项建梅 陈祖培 阎玉芹 陈贯一 天津医科大学 内分泌研究所,天津 300070;邸红军 天津医科大学 基础医学院,天津 300070
关键词:高碘甲肿;抗氧化酶;脂质过氧化物
高碘对小鼠抗氧化能力的影响 摘要 目的 对高碘4、6、12个月时期的小鼠甲状腺形态学、甲状腺激素及抗氧化能力进行动态观察研究。方法 采用生化方法测定血、脑组织、甲状腺组织中SOD、CAT、GSH-Px、LPO及血清T3、T4。结果 高碘甲肿显示为弥漫胶质性甲状腺肿,在甲肿形成过程中血清T4一直处于较高水平。此外,抗氧化能力测定结果显示4个月时虽已出现甲肿且血中抗氧化酶活性降低,LPO升高,但脑和甲状腺组织的抗氧化能力呈代偿过程,6个月后SOD、GSH-Px活性均降低,同时LPO含升高。呈现失代偿。结论 提示自由基损伤作用加重了高碘对机体特别是甲状腺的直接损害。
, 百拇医药
中图分类号 Q613.44;Q954.62 [文献标识码]A [文章编号]1000-4955(1999)04-0245-04
Effects of iodine excess on antioxidizing ability of mice
XIANG Jian-mei,CHEN Zu-pei,DI Hong-jun,et al
(The institute of Endocrinology,Tianjin Medical University,Tianjin 300070,China)
Abstract Objective To study the morphology of thyroid,hormone level in serum and antioxidizing ability of the mice which fed with iodine excess food in three different peroid of four,six and twelve month.Methods Biochemical method was used to determine not only the SOD.CAT.GSH-Px.LPO level in blood brain tissue and thyroid tissue but also T3,T4 level in serum.Results Iodine excess goiter formed wide apread glutinous goiter,and T4 in serum was still in high level in the forming course.Moreover the activity of antioxidizing enzyme reduced and LPO rose four months later,but antioxidizing ability in brain and thyroid however showed within compensation.With LPO rising constantly,the activity of SOD and GSH-Px decreased considerably and the compensation was broken six months later.Conclusions The damage of body espicially the thyroid caused by iodine excess was aggravated by radical injury.
, 百拇医药
Key words LPO;Indine excess goiter;Antioxidizing enzyme
多年来大量流行病学调查及动物实验分析表明,摄入过量碘也可以引起甲状腺肿,即高碘甲肿。高碘同低碘一样对人体有极大危害,可导致许多碘过多疾病的发生。因此受到许多科研人员的重视,从各种不同途径进行了大量研究。本实验在给动物饲以高碘水后3个不同时期对其甲状腺形态学、甲状腺激素以及血、甲状腺及脑组织的谷胱甘肽过氧化物酶(GSH-Px)、超氧化物歧化酶(SOD)、过氧化氢酶(CAT)的活性及脂质过氧化物(LPO)的含量进行了观察和分析,现报告如下。
1 材料与方法
1.1 动物模型复制:采用纯系昆明小鼠,生后3周断乳,体重为18~22g,雌雄各半。随机分为两组,即高碘实验组(HI)和正常对照组(NI)(各90只)。两组均饲以标准鼠饲料(碘含量为150~180ng/g),实验组饮含碘化钾的去离子水,浓度为3000μg/L。对照组饮用自来水(碘含量为2~4μg/L)。以上两组分别在喂养4、6、12个月时各处死30只。
, 百拇医药
1.2 样品制备:动物断头取抗凝和不抗凝血以及脑、甲状腺组织。全血测GSH-Px(单位以U/ml表示)、CAT(单位以U/gHb表示)活性,分离血浆测LPO(单位以nM/ml表示)含量,用生理盐水洗红细胞3次,3000rpm 10min,得红细胞压积,加一倍冷去离子水制成溶血液,测SOD(单位以NU/gHb表示)活性。甲状腺称重后,制成组织切片。其余脑和甲状腺组织在冰浴下用pH7.4的PBS制备成20%脑匀浆液和10%甲状腺匀浆液,测定GSH-Px(U/mgPr)、SOD(NU/mgPr)、LPO(nM/mgPr)。不抗凝血分离血清测三碘甲腺原氨酸(T3,ng/ml)、四碘甲腺原氨酸(T4,ng/ml)、促甲状腺激素受体抗体(TRAb)。
1.3 组织形态学观察:光镜下观察甲状腺形态变化,对甲状腺组织的形态进行分析和研究。
1.4 激素及抗氧化能力测定:CAT、SOD、GSH-Px、LPO检测均采用南京建成生物工程研究所生产的试剂盒进行测定。血清T3、T4的测定均采用放射免疫分析法。TRAb测定采用天津医科大学生物制药厂生产的药盒,用酶联免疫吸附测定法测定。
, 百拇医药
2 实验结果
2.1 体重、甲状腺和脑重比较:实验结果显示各时期HI组甲状腺重量及甲状腺/体重比均明显高于NI组,两组脑重无明显变化(见表1)。
表1 体重、甲状腺与脑湿重(
组别
例数
体重(g)
甲状腺(mg)
脑(mg)
甲状腺/体重(mg/g)
, 百拇医药
NI4
HI4
34
41
40.1±3.5
37.7±4.1**
3.79±0.89
6.02±1.59**
422.3±36.4
425.4±30.0
0.094±0.027
0.162±0.050**
, 百拇医药
NI6
HI6
38
25
39.8±6.07
39.6±5.36
4.64±1.08
5.61±1.79**
407.9±27.8
410.5±26.2
0.123±0.031
0.144±0.039*
, 百拇医药
NI12
HI12
30
31
40.9±5.77
42.2±3.85
3.50±1.02
7.84±3.57*
412.9±25.4
426.8±17.9
0.086±0.020
0.184±0.079*
, 百拇医药
注:HI组与NI组相比,*P<0.05;**P<0.01
2.2 组织形态学观察:肉眼所见:NI组小鼠甲状腺大小正常,为淡红色,质软。三个不同时期HI组小鼠甲状腺体积均明显大于同期NI组,为淡肤色,随高碘时间延长,质地韧实感增强,12个月时韧如橡皮。光镜所见:NI组甲状腺滤泡多呈圆或椭圆形,中等大小,滤泡上皮细胞多为立方形,滤泡腔内充满胶质,滤泡间偶见新生小滤泡(见图1)。HI组甲状腺滤泡明显增大,上皮细胞多为扁平状,滤泡腔内充满丰富浓染胶质,滤泡间隙小血管未见明显充血,亦未见明显增生小滤泡(见图2)。

图1 正常组小鼠甲状腺组织H.E×100

, 百拇医药
图2 高碘组(1年时)小鼠甲状腺组织H.E×100
2.3 甲状腺激素测定:激素测定结果显示3个不同时期血清T3与NI组相比均无明显差异,而血清T4在整个高碘甲肿形成过程中,一直维持较高水平,均显著高于同期NI组,并且HI组T3/T4比值也明显低于NI组。HI组TRAb值在6个月时明显高于NI组,4和12个月时未见差异(见表2)。
表2 甲状腺激素的变化(
组别
例数
, http://www.100md.com T3(ng/ml)
T4(ng/ml)
T3/T4
TRAb(S/M值)
NI4
HI4
8
8
1.041±0.17
0.948±0.15
77.65±11.03
, 百拇医药
94.07±11.36*
0.014±0.003
0.010±0.002*
0.68±0.03
0.66±0.03
NI6
HI6
10
9
1.109±0.37
1.394±0.29
, 百拇医药 29.00±9.38
57.67±9.56**
0.034±0.005
0.025±0.005*
0.44±0.07
0.60±0.04**
NI12
HI12
10
10
1.128±0.32
, 百拇医药
0.938±0.17
38.54±10.06
50.99±15.16*
0.030±0.007
0.020±0.005**
0.45±0.09
0.40±0.09
注:HI组与NI组相比,*P<0.05;**P<0.01
2.4 抗氧化能力测定
2.4.1 血液中抗氧化酶活性及LPO含量:HI组血液中的SOD活性从4个月时就比NI组显著降低,且LPO含量明显升高(P<0.01)。全血CAT活性仅6个月时降低,其余各期CAT活性与对照组无显著差异,GSH-Px活性4、6、12个月与对照组比较均无差异。(见表3)
, http://www.100md.com
表3 血液中抗氧化酶活性及LPO含量测定(
组别
例数
CAT(U/gHb)
SOD(NU/gHb)
GSH-Px(U/ml)
LPO(nM/ml)
NI4
HI4
14
, 百拇医药
14
72.0±16.7
68.2±17.6
14807.4±1553.6
13139.6±1103.9**
5.75±0.62
5.67±0.41
8.20±1.9
13.63±4.4**
NI6
HI6
, 百拇医药
20
20
80.4±14.8
70.9±8.85*
14757.0±960.6
14095.6±729.8*
1.95±0.80
2.31±1.02
9.41±1.71
11.90±1.63*
NI12
, http://www.100md.com
HI12
16
16
94.86±17.9
96.20±20.4
15810.4±1711.0
14577.9±948.8*
17.28±3.63
18.50±2.25
20.09±5.91
25.06±6.48*
, 百拇医药
注:HI组与NI组相比,*P<0.05;**P<0.01
2.4.2 脑组织中抗氧化酶活性及LPO含量:结果显示HI组SOD活性4个月时即降低,而GSH-Px活性4个月时升高,这可能是代偿性机制所致,6个月时降低,LPO含量4个月时明显降低,而6个月、12个月时明显升高。(见表4)。
表4 脑中抗氧化酶活性及LPO含量测定(
组别
例数
SOD(NU/mgPr)
GSH-Px(U/mgPr)
, 百拇医药
LPO(nM/mgPr)
NI4
HI4
20
20
428.4±22.4
398.52±27.6**
7.52±0.92
9.47±0.67**
3.01±0.39
2.45±0.21**
, 百拇医药
NI6
HI6
16
16
283.6±20.4
254.1±27.3
3.87±0.81
3.08±0.63*
1.83±0.36
2.17±0.48*
NI12
HI12
, http://www.100md.com
16
16
243.0±28.6
220.7±23.5*
6.33±0.99
5.64±0.78*
2.48±0.31
2.84±0.30*
注:HI组与NI组相比,*P<0.05;**P<0.01
2.4.3 甲状腺抗氧化酶活性及LPO测定:结果显示4个月时HI组GSH-Px活性升高,6个月、12个月时降低;SOD活性12个月时才明显下降;而LPO含量4个月时降低,6个月、12个月时升高(见表5)。
, http://www.100md.com
表5 甲状腺中抗氧化酶活性及LPO含量测定(
组别
例数
SOD(NU/mgPr)
GSH-Px(U/mgPr)
LPO(nM/mgPr)
NI4
HI4
30
30
, http://www.100md.com
165.7±2.25
166.3±6.1
4.69±0.23
5.80±0.13**
1.15±0.07
1.01±0.1**
NI6
HI6
30
30
279.7±8.6
270.6±6.0
, 百拇医药
6.03±0.56
5.04±0.12**
1.07±0.18
1.29±0.02*
NI12
HI12
30
30
226.1±11.0
193.7±4.87*
7.00±2.23
, 百拇医药
4.15±0.58*
1.27±0.12
1.74±0.12*
注:HI组与NI组相比,*P<0.05;**P<0.01
3 讨论
对于高碘甲肿发病机理的认识说法很多,多数学者认为与碘阻断效应(又称Wolff-Chaikoff effect)密切相关,它是由于碘抑制了甲状腺内过氧化酶的活性,从而影响到甲状腺激素合成过程中原子碘的活化、酪氨酸的活化及其有机化过程[1]。而近年来的研究证明,高碘甲肿的发病机理是甲状腺胶质(T4、T3、二碘甲腺原氨酸、一碘甲腺原氨酸)在甲状腺滤泡腔中过度堆积的结果[2]。本实验形态学观察结果显示HI组甲状腺腺体色淡,质地韧如橡皮,滤泡明显增大,上皮细胞多为扁平状,滤泡腔内充满丰富胶质,滤泡间隙小血管未见明显充血,亦未见明显增生小滤泡。这与以往报导一致[3],可证实实验动物高碘甲肿主要是由于滤泡腔内胶质增多引起的大滤泡胶质性甲状腺肿,外观色淡是由于间隙小血管血流减少所至,而泡腔内胶质过多堆积导致了腺体的韧实感。关于甲状腺激素测定的结果,流行病学调查发现高碘病人血清T3、T4都在正常范围[1,4,5]。而实验性高碘动物模型血清T3、T4测定结果报导不尽相同,朱惠民等于1986和1988年分别报导结果为T3、T4各组间差异无显著性意义[4];在1989年报导T4高于对照组,T3降低,T3/T4比值低于对照组[2];而1995年报导为T4显著高于对照组,T3两组间差异无显著性意义[6]。本实验结果为HI组T4显著高于NI组,T3两组间差异无显著性意义,HI组T3/T4比值低于NI组。这一结果进一步证实了高碘甲肿并不是像低碘甲肿一样由于血清T4降低导致垂体分泌TSH过多刺激甲状腺肿大,而是在高碘状态下,甲状腺合成了较多的甲状腺激素,为了保持机体的正常代谢,通过机体的自动调节将大量激素储存在甲状腺滤泡内,致使形成胶质性甲肿。这与以往报导一致[6]。
, 百拇医药
近年来有关自由基损伤与疾病的关系的研究已涉及许多系统,其中对自由基损伤作用与地方性甲状腺肿和地方性克汀病的发病机理的研究已逐步展开,由于高碘同样可引起许多碘过多疾病,因而研究高碘状态下机体抗氧化能力的变化,对进一步了解高碘与甲肿及其它高碘疾病的关系有一定的意义。
本文测定了动物饲以高碘后4、6、12个月3个不同时期全血CAT、GSH-Px、红细胞SOD活性及血浆LPO含量;脑及甲状腺组织中SOD、GSH-Px活性及LPO含量。结果显示:高碘4个月时血中SOD活性下降、LPO含量升高。4个月以后各种抗氧酶活性持续下降,LPO持续升高,脑组织中4个月时SOD活性下降、GSH-Px活性代偿性升高、LPO含量降低;6个月后SOD、GSH-Px活性均降低,同时LPO含量升高。甲状腺中4个月时GSH-Px活性升高、其升高可能是代偿性机制所致。LPO含量下降;6个月时GSH-Px活性降低,LPO含量升高;12个月时SOD、GSH-Px活性降低,LPO含量升高。研究结果证实高碘4个月后,虽然已出现甲肿,并且血液中抗氧化过酶活性降低,LPO升高,呈现典型失代偿过程。但是脑组织和甲状腺中抗氧化酶活性有不同程度升高,还可以保护脑和甲状腺免受自由基损伤。而6个月后代偿能力逐渐下降而呈失代偿过程,无法抵抗自由基损伤,加重高碘对机体特别是对甲状腺的损害。由于自由基特别是LPO直接损伤含磷脂的细胞膜则诱发自家免疫过程,这也可进一步解释高碘性甲状腺肿的部分病人并发自家免疫性甲状腺疾病,但这一发病环节有待进一步证实。
, http://www.100md.com
基金来源:天津市自然科学基金资助项目(942409002)
作者简介:项建梅,女,1967年生,学士
参考文献
[1] 卢倜章,马 泰.高碘性甲状腺肿[J].新医学,1983,14(9):500.
[2] 朱惠民,王凤荣,尹桂山,等.高碘地方性甲状腺肿发病机理的实验研究[J].中国地方病学杂志,1989,8(4):220.
[3] 山东省医学科学院.高碘甲状腺肿实验动物模型的研究[A].第二届全国地方性甲状腺肿地方性克汀病学术会议资料汇编[C].中国地方病学杂志编辑部,1984.342.
[4] 朱惠民,胡宣扬,姚玉霞,等.实验性高碘甲状腺肿[J].中国地方病学杂志,1986,5(1):1.
[5] 马 泰,卢倜章,于志恒.碘缺乏病[M].北京:人民卫生出版社,1993.116.
[6] 朱惠民,秦 立,于志恒.甲状腺激素治疗高碘甲状腺肿的实验研究[A].全国第五届碘缺乏病学术会议论文专辑[C].中国地方病学杂志编辑部,1995.113.
收稿日期1997-10-17;修行日期1998-06-04, http://www.100md.com