4-取代四氢吡喃类5-脂氧化酶抑制剂的研究进展
作者:张为革 李洪涛 计志忠
单位:沈阳药科大学制药系,沈阳 110015
关键词:5-脂氧化酶抑制剂;4-取代四氢吡喃类化合物;构效关系
摘 要 对4摘 要 对4-取代四氢吡喃类5-脂氧化酶抑制剂的发现与发展过程及构效关系研究进展进行了综述.
人体内花生四烯酸(arachidonic acid,AA)5-脂氧化酶(5-lipoxygenase,5-LO)代谢途径的产物白三烯(leukotrienes,LTs)是重要的炎症介质〔1〕(inflammatory mediator).5-脂氧化酶抑制剂可用于治疗风湿性关节炎、哮喘等疾病〔3,4〕.5-LO抑制剂的研究工作始于70年代末,经过近20年的探索,现已发现了20余种不同结构类型的化合物具有抑制5-LO的活性,如吡唑啉衍生物〔5〕、花生四烯酸类似物〔6〕、胺基酚类化合物〔7〕、苯醌和萘醌衍生物〔8〕、色酮类化合物〔9〕和咖啡酸类化合物〔10〕等.80年代至90年代初期报道最多的三种5-LO抑制剂是具有氧化还原活性的自由基清除剂4-取代-2,6-二叔丁基酚类化合物及其类似物2-取代-5-羟基-4,6-二叔丁基嘧啶类化合物〔11〕、可与5-LO活性中心的Fe3+相络合的异羟肟酸类化合物〔12〕和羟基脲类化合物〔13〕以及通过拮抗5-LO活化蛋白(5-lipoxygenase activating protein,FLAP)来抑制5-LO活性的喹啉基(桥连)芳基类化合物〔14〕,而近年来报道最多的一类5-LO抑制剂是4-取代四氢吡喃衍生物.此类化合物具有抑酶作用强、选择性好、作用机理独特、化学结构新颖等特点,因而倍受药物化学家的关注.
, 百拇医药
在寻找无氧化还原性(non-redox)且直接作用于酶活性部位(activesite-directed)的5-LO抑制剂的过程中,Bird等人根据5-LO活性部位结构特征和催化作用原理,于1991年设计并合成了(羟烷基)咪唑类化合物〔15〕,假想机理如图1所示,具有碱性的咪唑N原子与分子中的羟基形成氢键,使羟基去质子化,去质子化的羟基与酶活性部位Fe3+络合;咪唑的另一个N原子通过氢键与酶中的碱性基团结合.为了探索类似物的抑酶活性,又设计了噻唑衍生物(2).化合物(1),(2)在抑制大鼠PMN 5-LO活性实验中,IC50分别为7.6 μmol/L和5.1 μmol/L,在大鼠全血实验中IC50超过30 μmol/L.为了验证假想机理正确与否,又合成了分子中不含有羟基(不能形成具有络合能力的去质子化羟基)的化合物(3),令人惊讶的是该化合物具有比(1),(2)更强的抑酶活性,在大鼠PMN实验和大鼠全血实验中,IC50分别为0.11 μmol/L和0.5 μmol/L.在大鼠血液活体外实验中,灌胃给药,抑制LTB4生成的ED50为10 mg/kg.伏安法实验证明,该化合物不具有氧化还原活性;紫外光谱测定实验证实,此化合物不与三氯化铁形成络合物.这即是说:化合物(3)是口服有效的、非氧化还原型、非络合型5-LO抑制剂.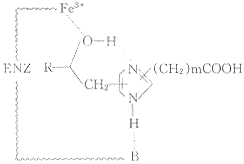
, http://www.100md.com
Fig.1 Hypothetical metchanism of hydroxyalkyl imidazoles
1992年Crawley等报道了以化合物(3)为先导化合物进行构效关系研究的结果〔16〕.以甲氧基替代2-噻唑基团得到了乙二醇二甲醚衍生物(4),化合物(4)以三种不同方式环合,分别得到化合物(5),(6),(7).在抑制离子载体A 23187刺激的人全血LTB4生成的实验中,化合物(3)~(7)的IC50分别为0.4,0.4,0.2,0.7,9.6 μmol/L.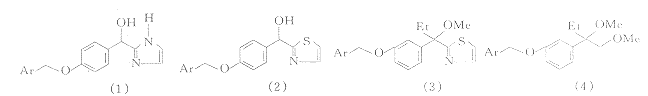
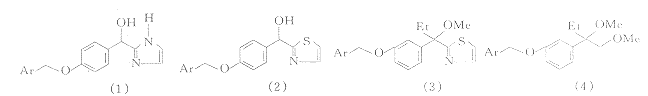
, http://www.100md.com
化合物(6)是甲氧基四氢呋喃衍生物,通过改变饱和杂环结构,得到化合物(8)~(11),在同上的体外实验中,四者的IC50分别为1.7,2.5,0.07,0.2 μmol/L.其中4-甲氧基四氢吡喃衍生物(10)活性最好.用亚甲基、羰基、硫原子等替代四氢吡喃中的氧原子所得化合物的抑酶活性均明显低于化合物(10).尽管化合物(10)体外活性甚高,但在体内实验中效果不够理想,且水溶性较差,饱和浓度只有0.08 μmol/L.为了降低整个分子的疏水性.Crawley等将2-萘基作了改动,合成了化合物(12)~(16),在抑制人全血LTs生成的实验中,这5个化合物的IC50依次为0.2,0.3,0.05,0.03,0.02 μmol/L.化合物(12),(13)的疏水性虽有所降低,但活性并未提高.(14)的疏水性变化很大,但活性变化很小.(15),(16)体外抑酶活性较高,在抑制大鼠炎症渗出物LTB4生成的模型中,灌胃给药,ED50分别为3.0,0.3 mg/kg.(16)明显优于(15),产生这一现象的原因是F原子的引入提高了化合物在体内的稳定性,使血药浓度升高,药物作用时间延长.临床实验结果显示,化合物(16)具有抑酶活性高,选择性好等优点,优于Zileuton和MK-886.每人单次剂量1 000 mg,未见明显的副作用.取出血液进行活体外A 23187刺激LTs生成实验口服剂量350 mg以上,24 h内LTs的生成完全被抑制.该化合物在人体内的半衰期约为12~16 h.
, http://www.100md.com
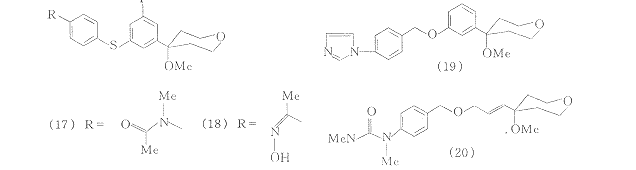
以化合物(16)为先导化合物的构效关系研究证实,以酰胺、肟等氢键给予者/接受者系统替代(16)中的二氢吡啶酮结构,所得化合物(17),(18)在多种药理实验模型中活性与(16)相差不大〔17〕.以其它芳环或双键替代(16)中的氟苯基团所得化合物(19),(20)仍具有良好的抑制5-LO的活性〔18,19〕.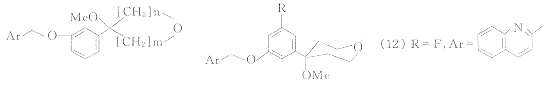
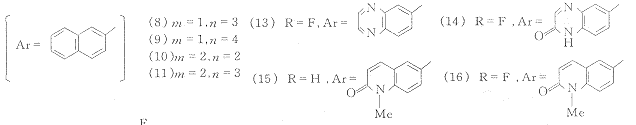
, http://www.100md.com
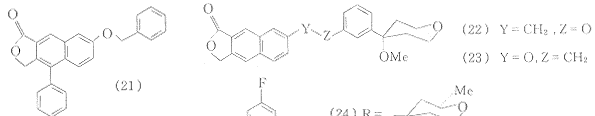
1994年Ducharme等将具有抑制5-LO活性的萘木酚内酯(21)的结构片段与4-甲氧基四氢吡喃基团杂合,得化合物(22),(23).在抑制人外周血液多形核白细胞LTB4合成实验中,两者的IC50分别为0.9 nmol/L和1.5 nmol/L.(22)的活性优于Zileuton等其他5-LO抑制剂〔20〕.
酶催化反应通常具有立体专一性,直接作用于酶活性部位的抑制剂如有手征性,其对映异构体间的抑酶活性应存在较大差异.1993年Crawley合成了含有两个手性碳的四氢吡喃衍生物,对映异构体(2R,4S)-(24)和(2S,3R)-(25)在抑制人全血5-LO活性实验中IC50分别为0.7,0.02 μmol/L,IC50之比达35∶1〔21〕.这一结果揭示了四氢吡喃类化合物的空间结构对抑酶活性的影响,并从一个侧面说明该类化合物可能是直接作用于5-LO活性部位的5-LO抑制剂.
, http://www.100md.com
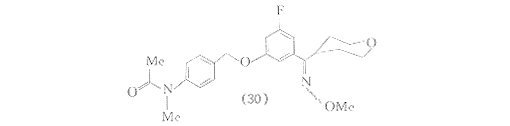
上述各种四氢吡喃类5-LO抑制剂所共有的结构特征是4位连有甲氧基,深入的研究工作证明,4位的甲氧基并不是该类化合物具有抑酶活性的必需基团.Bruneau等于1991年报道的化合物(26)是以甲硫基替代(10)中的甲氧基而得到的四氢吡喃衍生物,该化合物对抗原诱发的大鼠白三烯依赖型支气管狭窄具有明显的抑制作用,是体内有效的5-LO抑制剂〔25〕.以羟基替换4位甲氧基的(2S,4R)2-甲基四氢吡喃衍生物(27)是口服有效的5-LO抑制剂〔26〕.化合物(28)具有两个四氢吡喃基团,其中一个基团的4位连有羟基,经灌胃给药,该化合物可抑制酵母多糖诱发的小鼠气囊LTB4的产生〔27〕.4-位上无甲氧基等取代基的化合物(29),(30)是高活性的5-LO抑制剂〔28,29〕.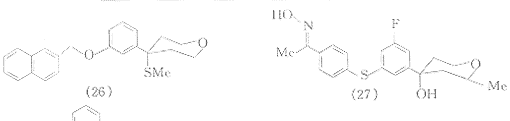
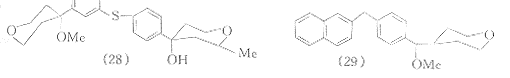
, 百拇医药
综上所述,4-取代四氢吡喃衍生物及其类似物与其他5-LO抑制剂不同,它既不是自由基清除剂,也不是金属离子络合剂,又不属于酶底物AA的类似物.关于此类化合物的作用机制目前尚无定论,通常认为此类化合物中包括氢键给予者/接受者体系,可与5-LO活性部位通过氢键结合,是可逆的5-LO抑制剂.在此类化合物的研究过程中,拼合原理的应用导致化合物(22),(23)的发现,因此推测利用拼合原理将4-取代四氢吡喃结构片段与其他类型的5-LO抑制剂结构片段相杂合,可望找到活性更高的5-LO抑制剂.另外,计算机辅助药物设计在药物化学研究中的作用日趋明显,可以预见,利用计算机辅助药物设计系统研究此类化合物,进一步优化结构,有可能得到高活性的化合物,同时也可以设计出结构新颖的4-取代四氢吡喃类似物,为5-LO抑制剂的研究开辟新的领域.虽然此类化合物的研究起步较晚,但发展速度快,有希望在近期开发出具有实际应用价值的新型5-LO抑制剂,为治疗哮喘、关节炎等疾病提供崭新的手段.
作者简介:张为革 通讯联系人
, 百拇医药
参考文献
1 Bray MA,ford-Hulchison AW,Smith MJH.Leukotriene B4:an inflammatory mediator in vivo.Prostaglandins,1981,22(2):213~222
2 Piper PJ.Pharmacology of leukotrienes.Br Med Bull,1983,39(2):255~259
3 Israel E,Dermarlcarian R,Rosenberg M,et al.The effect of 5-lipoxygenase inhibitors on asthma induced by air.N Engl J Med,1990,323(5):1740~1744
4 Weinblatt M,Kremer J,Helfgitt S,et al.A 5-lipoxygenase inhibitor in rheumatoid arthritis(RA).Arthritis Rheum,1990,33(1):S152
, 百拇医药
5 Higgs GA,Flower RJ,Vane JR.A new approach to anti-inflammatory drugs.Biochem Pharmacol,1979,28(12):1959~1961
6 Arai Y,Shimoji K,Konno M,et al.Synthesis and 5-lipoxygenase inhibitory activities of eicosanoid compounds.J Med Chem,1983,26(1):72~78
7 Ohluma H,Tomita K,Hoshino Y,et al.5-Hydroxyanthranilic acid derivatives as 5-lipoxygenase inhibitors.J Antibiot,1993,46(5):705~711
8 Ohluwa S,Terao S,Terashita Z,et al.Dual inhibitors of thromboxane A2 synthase and 5-lipoxygenase with scavenging activity of active oxygen species,synthesis of a novel series of (3-pyridylmethyl)benzoquionone derivatives.J Med Chem,1991,34(1):267~276
, 百拇医药
9 Horie T,Tominaga H,Kawamura Y,et al.Synthesis of 5,7,8-and 5,6,7-trioxygenated 3-alkyl-3′,4′-digydroxyflavones and their inhibitory activities against arachidonate 5-lipoxygenase.J Med Chem,1991,34(7):2169~2176
10 Nisgizawa M,Izuhara B,Kaneko K,et al.3-Caffeoyl-4-sinapoylquinic acid,a novel lipoxygenase inhibitor from gardeniae fructus.Chem Pharm Bull,1987,35(5):2133~2135
11 Hidaka T,Hosoe K,Ariki Y,et al.Pharmacological properties of a new anti-inflammatory compounds-(3,5-ditert-butyl-4-hydroxy-benzylidiene)-γ-butyrolactone〔KME-4〕 and its inhibitory effects on prostaglandin synthetase and 5-lipoxygenase.Jpn J Pharmacol,1984,36(1):77~85
, 百拇医药
12 Corey EI,Cashman JR,Kantner SR,et al.Rationally designed,potent competitive inhibitors of leukotriene biosynthesis.J Am Chem Soc,1984,106(5):1503~1504
13 Greco MN,Hageman WE,Powell ET,et al.Benzothiazole hydroxy ureas as inhibitors of 5-lipoxygenase:use of the hydroxyrurea miety as a replacement for hydroxamic acid.J Med Chem,1992,35(17):3180~3183
14 Wong A,Hwang SM,Kreft A,et al.Wy-49232 inhibits and reverses the calcium ionophere A 23187-induced 5-lipoxygenase translocation in rat basophilic leukemia cell.XI Washington International Spring Symposium,May 13-17,1991
, 百拇医药
15 Bird TGC,Bruneau P,Grawley GC,et al.(Methoxyalkyl)thiazoles:a new series of potent,selective and orally active 5-lipoxygenase inhibitors displaying enantioselectivity.J Med Chem,1991,34(7):2176~2186
16 Grawley GC,Dowell RI,Edwards PN.Methoxytetrahydropyrans,a new series of selective and orally potent 5-lipoxygenase inhibitors.J Med Chem,1992,35(14):2600~2609
17 Walker ERH.The design of therapeutically effective 5-lipoxygenase inhibitors.Eur Med Chem,1995,30(Suppl.):399~416
, http://www.100md.com
18 Sleven RW,Man T,Ando K.Preparation of imidazole lipoxygenase inhibitors.PCT Int Appl,WO 94 29299.1994-12-22
19 Dellaria JF,Basha A,Black LA,et al.〔(4-Allixypran-4-yl)substituted〕 ether,arylalkyl-,arylalkenyl-,and arylalkynyl urea inhibitors of 5-lipoxygenase.US 5440062.1995-11-16
20 Ducharme Y,Brideau C,Dube D,et al.Naphthalenic lignan lactones as selective,nonredox 5-lipoxygenase inhibitors,synthesis and biological activity of (methoxyalkyl)thiazole and methoxyrtetrahydropyran hydrids.J Med Chem,1994,37(4):512~518
, http://www.100md.com
21 Grawley GC,Briggs MT,Dowell RI,et al.4-Methoxy-2-methyltetrahydropyrans:chiral leukotriene biosynthesis inhibitors,related ICI D 2138 which display enantioselectivity.J Med Chem,1993,36(2):295~296
22 Bruneau PAR,Dowell RI,Waterson D.Preparation of axyltetrahydropyrans and related cyclic ethers as 5-lipoxygenase inhibitors.Eur Pat Appl,EP 462830.1991-10-20
23 Larger MS.〔(Tetrahydropyranyl)thienylthio〕acetophenone oxim and 〔(tetrahydropyranyl)-phenylthio〕acetophenone oxim as lipoxygenase inhibitors.PCT Int Appl,WO 94 17054.1994-08-04
, http://www.100md.com
24 Edwards PN.Preparation of pyranyl(thio)ethers as 5-lipoxygenase inhibitors.PCT Int Appl,WO 95 30669.1995-11-16
25 Dellaria JF,Cherneslry LT,Brooks DW.Preparation of 4-benzyltetrahydropyrons and analogs as lipoxygenase inhibitors.PCT Int Appl,WO 94 05281.1994-05-17
26 Dellaria JF,Basha A,Black LA,et al.Pyran-4-ylmethyl substituted arylalkylaryl-arylalkenylaryl-arylalkynyl-arylurea,inhibitors of 5-lipoxygenas.US 5484786.1995-01-16
, 百拇医药
27 Dellaria JF,Black LA,Brooks DW.Preparation of trans-heterocyclylcyclohexane 1,4-diethers as inhibitor of 5-lipoxygenase.PCT Int Appl,WO 94 05638.1994-03-17
28 Braneau PAR,Lambert-van Der Brempt C,Chrisline MP.Preparation of cycloalkane derivatives containing dihydroquinotone moiety.Can Pat Appl,CA 2094465.1993-10-14
29 Edwards PN,Larye MS.Preparation of 3-hydroxy-3-substituted alkyl pyrrolidines as 5-lipoxygenase inhibitiors.Eur Pat Appl,EP 586229.1994-03-09
收稿日期:1999-03-10, 百拇医药
单位:沈阳药科大学制药系,沈阳 110015
关键词:5-脂氧化酶抑制剂;4-取代四氢吡喃类化合物;构效关系
摘 要 对4摘 要 对4-取代四氢吡喃类5-脂氧化酶抑制剂的发现与发展过程及构效关系研究进展进行了综述.
人体内花生四烯酸(arachidonic acid,AA)5-脂氧化酶(5-lipoxygenase,5-LO)代谢途径的产物白三烯(leukotrienes,LTs)是重要的炎症介质〔1〕(inflammatory mediator).5-脂氧化酶抑制剂可用于治疗风湿性关节炎、哮喘等疾病〔3,4〕.5-LO抑制剂的研究工作始于70年代末,经过近20年的探索,现已发现了20余种不同结构类型的化合物具有抑制5-LO的活性,如吡唑啉衍生物〔5〕、花生四烯酸类似物〔6〕、胺基酚类化合物〔7〕、苯醌和萘醌衍生物〔8〕、色酮类化合物〔9〕和咖啡酸类化合物〔10〕等.80年代至90年代初期报道最多的三种5-LO抑制剂是具有氧化还原活性的自由基清除剂4-取代-2,6-二叔丁基酚类化合物及其类似物2-取代-5-羟基-4,6-二叔丁基嘧啶类化合物〔11〕、可与5-LO活性中心的Fe3+相络合的异羟肟酸类化合物〔12〕和羟基脲类化合物〔13〕以及通过拮抗5-LO活化蛋白(5-lipoxygenase activating protein,FLAP)来抑制5-LO活性的喹啉基(桥连)芳基类化合物〔14〕,而近年来报道最多的一类5-LO抑制剂是4-取代四氢吡喃衍生物.此类化合物具有抑酶作用强、选择性好、作用机理独特、化学结构新颖等特点,因而倍受药物化学家的关注.
, 百拇医药
在寻找无氧化还原性(non-redox)且直接作用于酶活性部位(activesite-directed)的5-LO抑制剂的过程中,Bird等人根据5-LO活性部位结构特征和催化作用原理,于1991年设计并合成了(羟烷基)咪唑类化合物〔15〕,假想机理如图1所示,具有碱性的咪唑N原子与分子中的羟基形成氢键,使羟基去质子化,去质子化的羟基与酶活性部位Fe3+络合;咪唑的另一个N原子通过氢键与酶中的碱性基团结合.为了探索类似物的抑酶活性,又设计了噻唑衍生物(2).化合物(1),(2)在抑制大鼠PMN 5-LO活性实验中,IC50分别为7.6 μmol/L和5.1 μmol/L,在大鼠全血实验中IC50超过30 μmol/L.为了验证假想机理正确与否,又合成了分子中不含有羟基(不能形成具有络合能力的去质子化羟基)的化合物(3),令人惊讶的是该化合物具有比(1),(2)更强的抑酶活性,在大鼠PMN实验和大鼠全血实验中,IC50分别为0.11 μmol/L和0.5 μmol/L.在大鼠血液活体外实验中,灌胃给药,抑制LTB4生成的ED50为10 mg/kg.伏安法实验证明,该化合物不具有氧化还原活性;紫外光谱测定实验证实,此化合物不与三氯化铁形成络合物.这即是说:化合物(3)是口服有效的、非氧化还原型、非络合型5-LO抑制剂.

, http://www.100md.com
Fig.1 Hypothetical metchanism of hydroxyalkyl imidazoles
1992年Crawley等报道了以化合物(3)为先导化合物进行构效关系研究的结果〔16〕.以甲氧基替代2-噻唑基团得到了乙二醇二甲醚衍生物(4),化合物(4)以三种不同方式环合,分别得到化合物(5),(6),(7).在抑制离子载体A 23187刺激的人全血LTB4生成的实验中,化合物(3)~(7)的IC50分别为0.4,0.4,0.2,0.7,9.6 μmol/L.
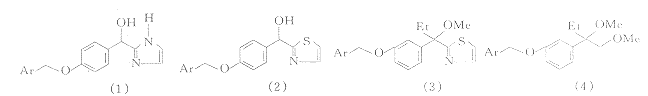
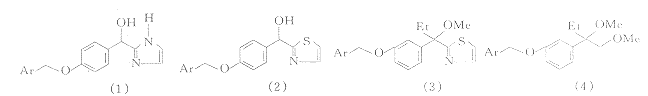
, http://www.100md.com
化合物(6)是甲氧基四氢呋喃衍生物,通过改变饱和杂环结构,得到化合物(8)~(11),在同上的体外实验中,四者的IC50分别为1.7,2.5,0.07,0.2 μmol/L.其中4-甲氧基四氢吡喃衍生物(10)活性最好.用亚甲基、羰基、硫原子等替代四氢吡喃中的氧原子所得化合物的抑酶活性均明显低于化合物(10).尽管化合物(10)体外活性甚高,但在体内实验中效果不够理想,且水溶性较差,饱和浓度只有0.08 μmol/L.为了降低整个分子的疏水性.Crawley等将2-萘基作了改动,合成了化合物(12)~(16),在抑制人全血LTs生成的实验中,这5个化合物的IC50依次为0.2,0.3,0.05,0.03,0.02 μmol/L.化合物(12),(13)的疏水性虽有所降低,但活性并未提高.(14)的疏水性变化很大,但活性变化很小.(15),(16)体外抑酶活性较高,在抑制大鼠炎症渗出物LTB4生成的模型中,灌胃给药,ED50分别为3.0,0.3 mg/kg.(16)明显优于(15),产生这一现象的原因是F原子的引入提高了化合物在体内的稳定性,使血药浓度升高,药物作用时间延长.临床实验结果显示,化合物(16)具有抑酶活性高,选择性好等优点,优于Zileuton和MK-886.每人单次剂量1 000 mg,未见明显的副作用.取出血液进行活体外A 23187刺激LTs生成实验口服剂量350 mg以上,24 h内LTs的生成完全被抑制.该化合物在人体内的半衰期约为12~16 h.
, http://www.100md.com
以化合物(16)为先导化合物的构效关系研究证实,以酰胺、肟等氢键给予者/接受者系统替代(16)中的二氢吡啶酮结构,所得化合物(17),(18)在多种药理实验模型中活性与(16)相差不大〔17〕.以其它芳环或双键替代(16)中的氟苯基团所得化合物(19),(20)仍具有良好的抑制5-LO的活性〔18,19〕.

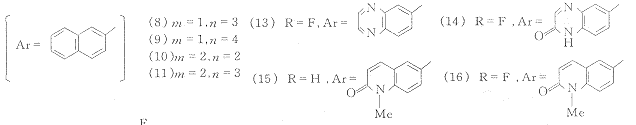


, http://www.100md.com
1994年Ducharme等将具有抑制5-LO活性的萘木酚内酯(21)的结构片段与4-甲氧基四氢吡喃基团杂合,得化合物(22),(23).在抑制人外周血液多形核白细胞LTB4合成实验中,两者的IC50分别为0.9 nmol/L和1.5 nmol/L.(22)的活性优于Zileuton等其他5-LO抑制剂〔20〕.
酶催化反应通常具有立体专一性,直接作用于酶活性部位的抑制剂如有手征性,其对映异构体间的抑酶活性应存在较大差异.1993年Crawley合成了含有两个手性碳的四氢吡喃衍生物,对映异构体(2R,4S)-(24)和(2S,3R)-(25)在抑制人全血5-LO活性实验中IC50分别为0.7,0.02 μmol/L,IC50之比达35∶1〔21〕.这一结果揭示了四氢吡喃类化合物的空间结构对抑酶活性的影响,并从一个侧面说明该类化合物可能是直接作用于5-LO活性部位的5-LO抑制剂.
, http://www.100md.com
上述各种四氢吡喃类5-LO抑制剂所共有的结构特征是4位连有甲氧基,深入的研究工作证明,4位的甲氧基并不是该类化合物具有抑酶活性的必需基团.Bruneau等于1991年报道的化合物(26)是以甲硫基替代(10)中的甲氧基而得到的四氢吡喃衍生物,该化合物对抗原诱发的大鼠白三烯依赖型支气管狭窄具有明显的抑制作用,是体内有效的5-LO抑制剂〔25〕.以羟基替换4位甲氧基的(2S,4R)2-甲基四氢吡喃衍生物(27)是口服有效的5-LO抑制剂〔26〕.化合物(28)具有两个四氢吡喃基团,其中一个基团的4位连有羟基,经灌胃给药,该化合物可抑制酵母多糖诱发的小鼠气囊LTB4的产生〔27〕.4-位上无甲氧基等取代基的化合物(29),(30)是高活性的5-LO抑制剂〔28,29〕.

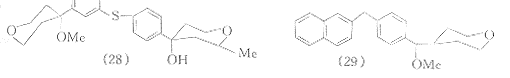

, 百拇医药
综上所述,4-取代四氢吡喃衍生物及其类似物与其他5-LO抑制剂不同,它既不是自由基清除剂,也不是金属离子络合剂,又不属于酶底物AA的类似物.关于此类化合物的作用机制目前尚无定论,通常认为此类化合物中包括氢键给予者/接受者体系,可与5-LO活性部位通过氢键结合,是可逆的5-LO抑制剂.在此类化合物的研究过程中,拼合原理的应用导致化合物(22),(23)的发现,因此推测利用拼合原理将4-取代四氢吡喃结构片段与其他类型的5-LO抑制剂结构片段相杂合,可望找到活性更高的5-LO抑制剂.另外,计算机辅助药物设计在药物化学研究中的作用日趋明显,可以预见,利用计算机辅助药物设计系统研究此类化合物,进一步优化结构,有可能得到高活性的化合物,同时也可以设计出结构新颖的4-取代四氢吡喃类似物,为5-LO抑制剂的研究开辟新的领域.虽然此类化合物的研究起步较晚,但发展速度快,有希望在近期开发出具有实际应用价值的新型5-LO抑制剂,为治疗哮喘、关节炎等疾病提供崭新的手段.
作者简介:张为革 通讯联系人
, 百拇医药
参考文献
1 Bray MA,ford-Hulchison AW,Smith MJH.Leukotriene B4:an inflammatory mediator in vivo.Prostaglandins,1981,22(2):213~222
2 Piper PJ.Pharmacology of leukotrienes.Br Med Bull,1983,39(2):255~259
3 Israel E,Dermarlcarian R,Rosenberg M,et al.The effect of 5-lipoxygenase inhibitors on asthma induced by air.N Engl J Med,1990,323(5):1740~1744
4 Weinblatt M,Kremer J,Helfgitt S,et al.A 5-lipoxygenase inhibitor in rheumatoid arthritis(RA).Arthritis Rheum,1990,33(1):S152
, 百拇医药
5 Higgs GA,Flower RJ,Vane JR.A new approach to anti-inflammatory drugs.Biochem Pharmacol,1979,28(12):1959~1961
6 Arai Y,Shimoji K,Konno M,et al.Synthesis and 5-lipoxygenase inhibitory activities of eicosanoid compounds.J Med Chem,1983,26(1):72~78
7 Ohluma H,Tomita K,Hoshino Y,et al.5-Hydroxyanthranilic acid derivatives as 5-lipoxygenase inhibitors.J Antibiot,1993,46(5):705~711
8 Ohluwa S,Terao S,Terashita Z,et al.Dual inhibitors of thromboxane A2 synthase and 5-lipoxygenase with scavenging activity of active oxygen species,synthesis of a novel series of (3-pyridylmethyl)benzoquionone derivatives.J Med Chem,1991,34(1):267~276
, 百拇医药
9 Horie T,Tominaga H,Kawamura Y,et al.Synthesis of 5,7,8-and 5,6,7-trioxygenated 3-alkyl-3′,4′-digydroxyflavones and their inhibitory activities against arachidonate 5-lipoxygenase.J Med Chem,1991,34(7):2169~2176
10 Nisgizawa M,Izuhara B,Kaneko K,et al.3-Caffeoyl-4-sinapoylquinic acid,a novel lipoxygenase inhibitor from gardeniae fructus.Chem Pharm Bull,1987,35(5):2133~2135
11 Hidaka T,Hosoe K,Ariki Y,et al.Pharmacological properties of a new anti-inflammatory compounds-(3,5-ditert-butyl-4-hydroxy-benzylidiene)-γ-butyrolactone〔KME-4〕 and its inhibitory effects on prostaglandin synthetase and 5-lipoxygenase.Jpn J Pharmacol,1984,36(1):77~85
, 百拇医药
12 Corey EI,Cashman JR,Kantner SR,et al.Rationally designed,potent competitive inhibitors of leukotriene biosynthesis.J Am Chem Soc,1984,106(5):1503~1504
13 Greco MN,Hageman WE,Powell ET,et al.Benzothiazole hydroxy ureas as inhibitors of 5-lipoxygenase:use of the hydroxyrurea miety as a replacement for hydroxamic acid.J Med Chem,1992,35(17):3180~3183
14 Wong A,Hwang SM,Kreft A,et al.Wy-49232 inhibits and reverses the calcium ionophere A 23187-induced 5-lipoxygenase translocation in rat basophilic leukemia cell.XI Washington International Spring Symposium,May 13-17,1991
, 百拇医药
15 Bird TGC,Bruneau P,Grawley GC,et al.(Methoxyalkyl)thiazoles:a new series of potent,selective and orally active 5-lipoxygenase inhibitors displaying enantioselectivity.J Med Chem,1991,34(7):2176~2186
16 Grawley GC,Dowell RI,Edwards PN.Methoxytetrahydropyrans,a new series of selective and orally potent 5-lipoxygenase inhibitors.J Med Chem,1992,35(14):2600~2609
17 Walker ERH.The design of therapeutically effective 5-lipoxygenase inhibitors.Eur Med Chem,1995,30(Suppl.):399~416
, http://www.100md.com
18 Sleven RW,Man T,Ando K.Preparation of imidazole lipoxygenase inhibitors.PCT Int Appl,WO 94 29299.1994-12-22
19 Dellaria JF,Basha A,Black LA,et al.〔(4-Allixypran-4-yl)substituted〕 ether,arylalkyl-,arylalkenyl-,and arylalkynyl urea inhibitors of 5-lipoxygenase.US 5440062.1995-11-16
20 Ducharme Y,Brideau C,Dube D,et al.Naphthalenic lignan lactones as selective,nonredox 5-lipoxygenase inhibitors,synthesis and biological activity of (methoxyalkyl)thiazole and methoxyrtetrahydropyran hydrids.J Med Chem,1994,37(4):512~518
, http://www.100md.com
21 Grawley GC,Briggs MT,Dowell RI,et al.4-Methoxy-2-methyltetrahydropyrans:chiral leukotriene biosynthesis inhibitors,related ICI D 2138 which display enantioselectivity.J Med Chem,1993,36(2):295~296
22 Bruneau PAR,Dowell RI,Waterson D.Preparation of axyltetrahydropyrans and related cyclic ethers as 5-lipoxygenase inhibitors.Eur Pat Appl,EP 462830.1991-10-20
23 Larger MS.〔(Tetrahydropyranyl)thienylthio〕acetophenone oxim and 〔(tetrahydropyranyl)-phenylthio〕acetophenone oxim as lipoxygenase inhibitors.PCT Int Appl,WO 94 17054.1994-08-04
, http://www.100md.com
24 Edwards PN.Preparation of pyranyl(thio)ethers as 5-lipoxygenase inhibitors.PCT Int Appl,WO 95 30669.1995-11-16
25 Dellaria JF,Cherneslry LT,Brooks DW.Preparation of 4-benzyltetrahydropyrons and analogs as lipoxygenase inhibitors.PCT Int Appl,WO 94 05281.1994-05-17
26 Dellaria JF,Basha A,Black LA,et al.Pyran-4-ylmethyl substituted arylalkylaryl-arylalkenylaryl-arylalkynyl-arylurea,inhibitors of 5-lipoxygenas.US 5484786.1995-01-16
, 百拇医药
27 Dellaria JF,Black LA,Brooks DW.Preparation of trans-heterocyclylcyclohexane 1,4-diethers as inhibitor of 5-lipoxygenase.PCT Int Appl,WO 94 05638.1994-03-17
28 Braneau PAR,Lambert-van Der Brempt C,Chrisline MP.Preparation of cycloalkane derivatives containing dihydroquinotone moiety.Can Pat Appl,CA 2094465.1993-10-14
29 Edwards PN,Larye MS.Preparation of 3-hydroxy-3-substituted alkyl pyrrolidines as 5-lipoxygenase inhibitiors.Eur Pat Appl,EP 586229.1994-03-09
收稿日期:1999-03-10, 百拇医药