���Գ���άϸ���������Ӷ�������ϸ����ֳ�ͷֻ�������
���ߣ��½��� ��ƽ ʷ���� ţ��Ӣ Ф���� ���ƾ�
��λ��710032 ���������ľ�ҽ��ѧ��ǻҽѧԺ(�½�������ƽ��ʷ���ϡ�ţ��Ӣ��Ф����)�������������������(���ƾ�)
�ؼ��ʣ�����ϸ�������Գ���άϸ���������ӣ�ϸ������
New Page 2
��ժҪ�� Ŀ�� ̽�ּ��Գ���άϸ����������(basic fibroblast growth factor, bFGF)������������ϸ����ֳ�ͷֻ���ЧӦ������ ���������η���3H-TdR���뷨��ͼ����������������bFGF(hbFGF)��ϸ��DNA����ԭ���ס���άճ�����ס���������ø�����γɵ��ϳɺ������ر����Ӱ�졣��� hbFGFŨ����1��10��g/Lʱ�����ٽ�ϸ������ֳ��Ũ��Ϊ1��100��g/Lʱ�������̼�������ϸ��DNA�ĺϳɡ�hbFGF�ڸ�Ũ����(10��1000 ��g/L)�����ͽ�ԭ����άճ�����ס�����������A����ͼ�������ø�ı�����ǿ�������ͽ�ԭ����������������ĺϳ��ܵ����ƣ���ͬŨ�ȵ�bFGF��ϸ�����γɵ��ı���������Ӱ�졣���� bFGF���ܴٽ�����������������ϸ�����������ϸ���ֻ���
, ��Ĵҽҩ
The effects of basic fibroblast growth factor on proliferation and differentiation of human dental pulp cells in vitro
HAO Jianjun, WANG Ping, SHI Junnan, et al. School of Stomatology, Fourth Military Medical University, Xi'an 710032
��Abstract�� Objective To evaluate the effects of human basic fibroblast growth factor (hbFGF) on proliferation and differentiation of human dental pulp cells in vitro.Methods The syntheses of DNA, collagen, fibronection (FN), alkaline phosphatase (ALP) and bone morphogenetic protein (BMP), and the expression of agglutinin were measured with imagine processing and analysis system. Results hbFGF at concentration of 1��10 ��g/L stimulated the cell proliferation measured by MTT colorimetric assay, and promoted incorporation of 3H-thymidine at 1��100��g/L. The expression of type �� collagen, FN, Con A receptor, and ALP significantly increased at hbFGF concentration of 10��1 000 ��g/L, but the expression of type �� collagen and WGA receptor markedly decreased at the same concentration. There was no significant difference in expression of BMP.Conclusion bFGF has the capability to promote the differentiation of dental pulp cells to odontoblasts in culture.
, http://www.100md.com
��Key words�� Dental pulp cell Basic fibroblast growth factor Cell culture
���Գ���άϸ����������(basic fibroblast growth factor, bFGF)�dz���άϸ���������Ӽ������Ҫ��Ա֮һ����ϸ����˿���Ѻͷֻ��к�ǿ�ĵ������ã�ͨ���Է��ں��Է��ڲ�����̥���������ٷ���[1��2]��Ŀǰ��֪bFGF������ϸ������˿�����дٽ�����[3]�����й�ϸ���ֻ��ĵ���ЧӦ�������١����Dz���������ϸ��������������ͨ�����hbFGF��ϸ��DNA����ԭ���ס���ά�����(fibronectin, FN)����������ø(alkaline phosphatase, ALP)�����γɵ���(bone morphogenetic protein, BMP)�ϳɼ���������������Ӱ�죬̽������ϸ����hbFGF�յ����������ֻ�������ѧЧӦ��
���Ϻͷ���
, http://www.100md.com
һ������
hbFGF���麣����˾��3H-���������������(3H-TdR)���й�ԭ�����о�����3-(4��5-��������-2)-2��5-�������ĵ�������(MTT)��������˾��ABC�Լ��У�����Vector��˾�����ޱ���������(DMEM)������Gibco��˾��̥ţѪ��(FCS)���������ţ������Ʒ�����ȵ���ø������Difcoʵ���ҡ�ͼ������ǣ�Quantament 570�ͣ�Ӣ��Leico��˾��ʵ���ÿ������1��
����ʵ�鷽��
1.ʵ����飺�ٶ����飺����ҺΪDMEM��1%FCS����ʵ���飺��hbFGFԭҺ�ú�1% FCS��DMEM����Һϡ����0.1 ��g/L��1 ��g/L��10 ��g/L��100 ��g/L��1 000 ��g/L 5��Ũ���ݶȡ�
��1 ʵ�����õĿ����ֲ�������� ����
, http://www.100md.com
��Դ
����Ũ��
FN����
������˾
1��400
���ͽ�ԭ�
�Ϻ�ҽ�ƴ�ѧ����ѧ������
1��100
���ͽ�ԭ����
���ľ�ҽ��ѧ����ѧ������
1��200
�����ػ�ConA
, http://www.100md.com
������˾
10 mg/L
�����ػ�WGA
������˾
10 mg/L
ALP����
���ľ�ҽ��ѧ����ѧ������
1��100
BMP�
���ľ�ҽ��ѧ��ǻ����ѧ������
1��200
2.MTT����ȡ��������������ϸ����5��[4]������ϸ��Ũ����2��107/L����ÿ��100��l������96�װ壬ÿ��4�ס���������Ϊ37 �桢5% CO2������ʪ�ȡ��ں�10% FCS��DMEMҺ������48 h���ɺ�1% FCS��DMEMҺ����24 h���ٻ���ʵ������ĸ�������Һ����72 h��ÿ����MTT 20 ��l����������4 h��������Һ�壬ÿ����150 ��l��������(DMSO)��5 min��ø���Dz���490 nm������ܶ�ֵ(Aֵ)��ȡƽ��ֵ��ͳ��ѧ������
, http://www.100md.com
3.3 H-TdR�������飺�����ʵ�鷽��ͬMTT������ֹ����ǰ6 h����3H-TdR��ʹ��Ũ��Ϊÿ��1.85��107Bq��6 h����ֹ��Ӧ�������淽������������˸Һ����Һ����˸�������ⶨÿ���걾��ÿ������������
4.ϸ��������IJⶨ��������ʵ��ͬMTT����ϸ����4%��ۼ�ȩҺ�̶�����ABC����ConA����Ⱦɫ��ͼ������Dz�������ϸ���������ÿ20��25��ϸ��Ϊ1����Ԫ��ÿ��ʵ�����4����Ԫ��
5.��������ͽ�ԭ��FN��ConA���塢����������(WGA)���塢ALP��BMP��Ⱦɫ�����Ͱ붨���ⶨ��ϸ��������ֹʱ����4%��ۼ�ȩҺ(pH7.3)�̶�48 h��ABC�����������黯Ⱦɫ��ͼ����������ͱ�ͬ�ο�����4�����
������ϸ�������С���ֹ�������������FN����������ͽ�ԭȾɫ�������ϸ��Ⱦɫ��������ʵ���顣��ʵ�����ϸ����չ���ã�ϸ����Ϊ���Σ�bFGF(1��10��100 ��g/L)���ϸ���ɼ������࣬FN����������ͽ�ԭ��ConA���塢WGA���塢ALP��BMP������Ⱦɫ��Ҫλ�ڰ�����bFGF���Ũ��0.1��1��10��100��100 ��g/L���ֱ���F0.1��F1��F10��F100��F1 000��ʾ���������2��ͼ1��3��
, ��Ĵҽҩ
һ��hbFGF��������ϸ����ֳ��DNA�ϳɺ�ϸ��ճ��������
�������(��2)��bFGF(1��10 ��g/L)�������̼��������������������άϸ����ֳ��bFGF(1��10��100 ��g/L)�����Դٽ�ϸ��DNA�ĺϳɡ���FGF(0.1��1 000 ��g/L)���������á�bFGF(0.1��10 ��g/L)��ϸ
ͼ1 hbFGF������������ϸ�����ͽ�ԭ��FN���������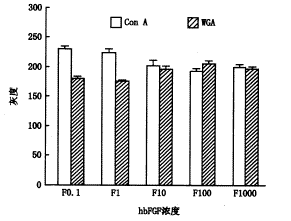
ͼ2 hbFGF������������ϸ��ConA��WGA���������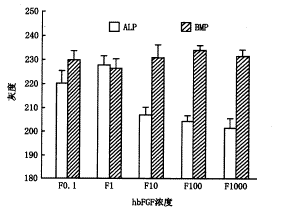
ͼ3 hbFGF������������ϸ��ALP��BMP���������
, ��Ĵҽҩ
��2 hbFGF��������ϸ����ֳ��DNA�ϳɡ�ϸ��ճ��������( ��s,n=4) ������Ŀ
��s,n=4) ������Ŀ
����
F0.1
F1
F10
F100
F1 000
MTT(Aֵ)
0.14��0.02
0.16��0.01
0.19��0.01��
, ��Ĵҽҩ
0.24��0.03��
0.17��0.04
0.14��0.04
3 H-TdR(������/min)
738��54
636��24
3 219��165��
5 076��165��
2 975��834��
555��71
, ��Ĵҽҩ
ϸ�������(��m2)
3 592��307
4 161��107��
5 197��380��
4 315��276��
3 444��311
3 282��193
ע����P<0.01����ʵ�����������Ƚ�
����չ���á�
����hbFGF��ϸ�����ʱ��������
, ��Ĵҽҩ
t����������(ͼ1)��F0.1��F1��F10��F100��F1 000����֮���ϸ����������ͽ�ԭ��FN���������������(P<0.01)����հ�ϸ���������ʲ���������
����hbFGF��ϸ��������������������
t����������(ͼ2)��F0.1��F1����������֮�������������(P<0.05)��
�ġ�hbFGF��ϸ��ALP��BMP���������
t����������(ͼ3)��F10��F100��F1000���ALP����������֮�������������(P<0.05)��BMP����֮�������������(P>0.05)������
���Dz���MTT��3H-TdR�������ַ����ⶨbFGF��������ϸ����ֳ��Ӱ�죬���߽������ȫ��ͬ�����뷨��ӳϸ����ֳ���ں���ı仯����MTT��ӳϸ�����Ѻ���ϸ�����ɷֵĸı䡣bFGF(0.1��10 ��g/L)��ϸ�����������˵��bFGF������ϸ����ճ��ЧӦ��
, ��Ĵҽҩ
I��III�ͽ�ԭ����������ϸ������Ҫ��ϸ������ʳɷݡ�����ϸ���ķֻ���������У������I��III�ͽ�ԭ�ı���Ҳ��֮�仯������ͷϸ�������������ϸ���ֻ������У�I�ͽ�ԭ�������࣬III�ͽ�ԭ�ɷּ���[5]��������ij�������ϸ������FN��I�ͽ�ԭ��������III�ͽ�ԭ����������ʾ��������Һ��bFGFŨ�ȵ����ߣ�������ϸ���ϳ�I��III�ͽ�ԭ�ı��������仯��ϸ�������������ϸ���ֻ������ƣ�bFGF�е�������ϸ���ֻ������á�
һ��ϸ������֯�ķֻ����쳣���������������������ı仯���������������ϸ������ConA��WGA���壬��������ϸ������ConA���壬������WGA����[6]�������ڸ�Ũ��bFGF(10��1 000 ��g/L)�����£�����������������ϸ���������������巢�������仯��������ͷϸ�����������ϸ���ֻ�ʱϸ����������������ı仯���ƣ�֤ʵbFGF�дٽ�����ϸ�����������ϸ���ֻ���������
ALP������ϸ���ֻ��ͳ���ı�־��֮һ��������������bFGFŨ����10��1 000 ��g/Lʱ��ALP�ϳ��������ӣ���ʾ������������ϸ���зֻ��ͳ�������ơ�BMP�����п��ܷ�ӳ����ϸ���ķֻ�״̬���γ�Ӳ��֯��������������bFGF������ϸ��BMP����������Ӱ�죬�������bFGF�ٽ�����ϸ���ֻ��Ϳ��������ޣ�����ϸ���ij��컹δ�ﵽһ���̶ȡ�
, http://www.100md.com
����������bFGFͨ������ϸ������ֳ״̬�����ʷ��ں�ϸ�����͵ı����������ϸ�����������ϸ���ֻ��Ĺ��̡�ϸ���ķֻ���һ�����ӵĹ��̣���Ҫ�����������ӡ���������Լ�ϸ�������������ۺ�����[7]������bFGF�����Dz���ϸ���ֻ�����Ҫ����֮һ�������յ����������ģ��йظ�������ϸ���ֻ���ϵ���о��д����
ע�ͣ�������Ȼ��ѧ������������(39700160)
�����
[1]�½�����ʷ����.����άϸ���������ӵ��о���չ.�����������ܲ�ѧ��־��1994��4��111-113.
[2] Thesleff I, Partanen AM, Vainio S. Epithelial-mesenchymal interactions in tooth morphogenesis: the roles of extracellular matrix, growth factors, and cell surface receptors. J Craniofac Genet Devl Biol, 1991, 11:229-237.
, http://www.100md.com
[3] Nakashima M. The effects of growth factors on DNA synthesis and alkaline phosphatase activity in bovine dental pulp cells. Archs Oral Biol, 1992, 37:231-236.
[4] ��ƽ��ʷ���ϣ��½���.ţѪ����άճ���������������������άϸ����ֳ��DNA�ϳɺ�ϸ����̬��Ӱ��.�����������ܲ�ѧ��־��1995��5��17-19.
[5] Bronkers ALJJ, Lyraruu DM, Woltgens JHM. Immunohistochemistry of extracellular matrix proteins during various stages of dentinogenesis. Connect Tissue Res, 1989, 22:65-70.
, http://www.100md.com
[6] Endo K. Lectin histochemical study on human dental pulp: special reference to odontoblasts and pulp cells. Meikai Daiguku Shigaku Zashi, 1989,18:360-381.
[7] Ruch JV, Lesot H, Bege-Kin C, Odontoblast differentiation. Int J Dev Biol, 1995, 39:51-68.
�ո壺1998-02-16
�أ�1998-12-20, ��Ĵҽҩ
��λ��710032 ���������ľ�ҽ��ѧ��ǻҽѧԺ(�½�������ƽ��ʷ���ϡ�ţ��Ӣ��Ф����)�������������������(���ƾ�)
�ؼ��ʣ�����ϸ�������Գ���άϸ���������ӣ�ϸ������
New Page 2
��ժҪ�� Ŀ�� ̽�ּ��Գ���άϸ����������(basic fibroblast growth factor, bFGF)������������ϸ����ֳ�ͷֻ���ЧӦ������ ���������η���3H-TdR���뷨��ͼ����������������bFGF(hbFGF)��ϸ��DNA����ԭ���ס���άճ�����ס���������ø�����γɵ��ϳɺ������ر����Ӱ�졣��� hbFGFŨ����1��10��g/Lʱ�����ٽ�ϸ������ֳ��Ũ��Ϊ1��100��g/Lʱ�������̼�������ϸ��DNA�ĺϳɡ�hbFGF�ڸ�Ũ����(10��1000 ��g/L)�����ͽ�ԭ����άճ�����ס�����������A����ͼ�������ø�ı�����ǿ�������ͽ�ԭ����������������ĺϳ��ܵ����ƣ���ͬŨ�ȵ�bFGF��ϸ�����γɵ��ı���������Ӱ�졣���� bFGF���ܴٽ�����������������ϸ�����������ϸ���ֻ���
, ��Ĵҽҩ
The effects of basic fibroblast growth factor on proliferation and differentiation of human dental pulp cells in vitro
HAO Jianjun, WANG Ping, SHI Junnan, et al. School of Stomatology, Fourth Military Medical University, Xi'an 710032
��Abstract�� Objective To evaluate the effects of human basic fibroblast growth factor (hbFGF) on proliferation and differentiation of human dental pulp cells in vitro.Methods The syntheses of DNA, collagen, fibronection (FN), alkaline phosphatase (ALP) and bone morphogenetic protein (BMP), and the expression of agglutinin were measured with imagine processing and analysis system. Results hbFGF at concentration of 1��10 ��g/L stimulated the cell proliferation measured by MTT colorimetric assay, and promoted incorporation of 3H-thymidine at 1��100��g/L. The expression of type �� collagen, FN, Con A receptor, and ALP significantly increased at hbFGF concentration of 10��1 000 ��g/L, but the expression of type �� collagen and WGA receptor markedly decreased at the same concentration. There was no significant difference in expression of BMP.Conclusion bFGF has the capability to promote the differentiation of dental pulp cells to odontoblasts in culture.
, http://www.100md.com
��Key words�� Dental pulp cell Basic fibroblast growth factor Cell culture
���Գ���άϸ����������(basic fibroblast growth factor, bFGF)�dz���άϸ���������Ӽ������Ҫ��Ա֮һ����ϸ����˿���Ѻͷֻ��к�ǿ�ĵ������ã�ͨ���Է��ں��Է��ڲ�����̥���������ٷ���[1��2]��Ŀǰ��֪bFGF������ϸ������˿�����дٽ�����[3]�����й�ϸ���ֻ��ĵ���ЧӦ�������١����Dz���������ϸ��������������ͨ�����hbFGF��ϸ��DNA����ԭ���ס���ά�����(fibronectin, FN)����������ø(alkaline phosphatase, ALP)�����γɵ���(bone morphogenetic protein, BMP)�ϳɼ���������������Ӱ�죬̽������ϸ����hbFGF�յ����������ֻ�������ѧЧӦ��
���Ϻͷ���
, http://www.100md.com
һ������
hbFGF���麣����˾��3H-���������������(3H-TdR)���й�ԭ�����о�����3-(4��5-��������-2)-2��5-�������ĵ�������(MTT)��������˾��ABC�Լ��У�����Vector��˾�����ޱ���������(DMEM)������Gibco��˾��̥ţѪ��(FCS)���������ţ������Ʒ�����ȵ���ø������Difcoʵ���ҡ�ͼ������ǣ�Quantament 570�ͣ�Ӣ��Leico��˾��ʵ���ÿ������1��
����ʵ�鷽��
1.ʵ����飺�ٶ����飺����ҺΪDMEM��1%FCS����ʵ���飺��hbFGFԭҺ�ú�1% FCS��DMEM����Һϡ����0.1 ��g/L��1 ��g/L��10 ��g/L��100 ��g/L��1 000 ��g/L 5��Ũ���ݶȡ�
��1 ʵ�����õĿ����ֲ�������� ����
, http://www.100md.com
��Դ
����Ũ��
FN����
������˾
1��400
���ͽ�ԭ�
�Ϻ�ҽ�ƴ�ѧ����ѧ������
1��100
���ͽ�ԭ����
���ľ�ҽ��ѧ����ѧ������
1��200
�����ػ�ConA
, http://www.100md.com
������˾
10 mg/L
�����ػ�WGA
������˾
10 mg/L
ALP����
���ľ�ҽ��ѧ����ѧ������
1��100
BMP�
���ľ�ҽ��ѧ��ǻ����ѧ������
1��200
2.MTT����ȡ��������������ϸ����5��[4]������ϸ��Ũ����2��107/L����ÿ��100��l������96�װ壬ÿ��4�ס���������Ϊ37 �桢5% CO2������ʪ�ȡ��ں�10% FCS��DMEMҺ������48 h���ɺ�1% FCS��DMEMҺ����24 h���ٻ���ʵ������ĸ�������Һ����72 h��ÿ����MTT 20 ��l����������4 h��������Һ�壬ÿ����150 ��l��������(DMSO)��5 min��ø���Dz���490 nm������ܶ�ֵ(Aֵ)��ȡƽ��ֵ��ͳ��ѧ������
, http://www.100md.com
3.3 H-TdR�������飺�����ʵ�鷽��ͬMTT������ֹ����ǰ6 h����3H-TdR��ʹ��Ũ��Ϊÿ��1.85��107Bq��6 h����ֹ��Ӧ�������淽������������˸Һ����Һ����˸�������ⶨÿ���걾��ÿ������������
4.ϸ��������IJⶨ��������ʵ��ͬMTT����ϸ����4%��ۼ�ȩҺ�̶�����ABC����ConA����Ⱦɫ��ͼ������Dz�������ϸ���������ÿ20��25��ϸ��Ϊ1����Ԫ��ÿ��ʵ�����4����Ԫ��
5.��������ͽ�ԭ��FN��ConA���塢����������(WGA)���塢ALP��BMP��Ⱦɫ�����Ͱ붨���ⶨ��ϸ��������ֹʱ����4%��ۼ�ȩҺ(pH7.3)�̶�48 h��ABC�����������黯Ⱦɫ��ͼ����������ͱ�ͬ�ο�����4�����
������ϸ�������С���ֹ�������������FN����������ͽ�ԭȾɫ�������ϸ��Ⱦɫ��������ʵ���顣��ʵ�����ϸ����չ���ã�ϸ����Ϊ���Σ�bFGF(1��10��100 ��g/L)���ϸ���ɼ������࣬FN����������ͽ�ԭ��ConA���塢WGA���塢ALP��BMP������Ⱦɫ��Ҫλ�ڰ�����bFGF���Ũ��0.1��1��10��100��100 ��g/L���ֱ���F0.1��F1��F10��F100��F1 000��ʾ���������2��ͼ1��3��
, ��Ĵҽҩ
һ��hbFGF��������ϸ����ֳ��DNA�ϳɺ�ϸ��ճ��������
�������(��2)��bFGF(1��10 ��g/L)�������̼��������������������άϸ����ֳ��bFGF(1��10��100 ��g/L)�����Դٽ�ϸ��DNA�ĺϳɡ���FGF(0.1��1 000 ��g/L)���������á�bFGF(0.1��10 ��g/L)��ϸ

ͼ1 hbFGF������������ϸ�����ͽ�ԭ��FN���������

ͼ2 hbFGF������������ϸ��ConA��WGA���������

ͼ3 hbFGF������������ϸ��ALP��BMP���������
, ��Ĵҽҩ
��2 hbFGF��������ϸ����ֳ��DNA�ϳɡ�ϸ��ճ��������(
 ��s,n=4) ������Ŀ
��s,n=4) ������Ŀ����
F0.1
F1
F10
F100
F1 000
MTT(Aֵ)
0.14��0.02
0.16��0.01
0.19��0.01��
, ��Ĵҽҩ
0.24��0.03��
0.17��0.04
0.14��0.04
3 H-TdR(������/min)
738��54
636��24
3 219��165��
5 076��165��
2 975��834��
555��71
, ��Ĵҽҩ
ϸ�������(��m2)
3 592��307
4 161��107��
5 197��380��
4 315��276��
3 444��311
3 282��193
ע����P<0.01����ʵ�����������Ƚ�
����չ���á�
����hbFGF��ϸ�����ʱ��������
, ��Ĵҽҩ
t����������(ͼ1)��F0.1��F1��F10��F100��F1 000����֮���ϸ����������ͽ�ԭ��FN���������������(P<0.01)����հ�ϸ���������ʲ���������
����hbFGF��ϸ��������������������
t����������(ͼ2)��F0.1��F1����������֮�������������(P<0.05)��
�ġ�hbFGF��ϸ��ALP��BMP���������
t����������(ͼ3)��F10��F100��F1000���ALP����������֮�������������(P<0.05)��BMP����֮�������������(P>0.05)������
���Dz���MTT��3H-TdR�������ַ����ⶨbFGF��������ϸ����ֳ��Ӱ�죬���߽������ȫ��ͬ�����뷨��ӳϸ����ֳ���ں���ı仯����MTT��ӳϸ�����Ѻ���ϸ�����ɷֵĸı䡣bFGF(0.1��10 ��g/L)��ϸ�����������˵��bFGF������ϸ����ճ��ЧӦ��
, ��Ĵҽҩ
I��III�ͽ�ԭ����������ϸ������Ҫ��ϸ������ʳɷݡ�����ϸ���ķֻ���������У������I��III�ͽ�ԭ�ı���Ҳ��֮�仯������ͷϸ�������������ϸ���ֻ������У�I�ͽ�ԭ�������࣬III�ͽ�ԭ�ɷּ���[5]��������ij�������ϸ������FN��I�ͽ�ԭ��������III�ͽ�ԭ����������ʾ��������Һ��bFGFŨ�ȵ����ߣ�������ϸ���ϳ�I��III�ͽ�ԭ�ı��������仯��ϸ�������������ϸ���ֻ������ƣ�bFGF�е�������ϸ���ֻ������á�
һ��ϸ������֯�ķֻ����쳣���������������������ı仯���������������ϸ������ConA��WGA���壬��������ϸ������ConA���壬������WGA����[6]�������ڸ�Ũ��bFGF(10��1 000 ��g/L)�����£�����������������ϸ���������������巢�������仯��������ͷϸ�����������ϸ���ֻ�ʱϸ����������������ı仯���ƣ�֤ʵbFGF�дٽ�����ϸ�����������ϸ���ֻ���������
ALP������ϸ���ֻ��ͳ���ı�־��֮һ��������������bFGFŨ����10��1 000 ��g/Lʱ��ALP�ϳ��������ӣ���ʾ������������ϸ���зֻ��ͳ�������ơ�BMP�����п��ܷ�ӳ����ϸ���ķֻ�״̬���γ�Ӳ��֯��������������bFGF������ϸ��BMP����������Ӱ�죬�������bFGF�ٽ�����ϸ���ֻ��Ϳ��������ޣ�����ϸ���ij��컹δ�ﵽһ���̶ȡ�
, http://www.100md.com
����������bFGFͨ������ϸ������ֳ״̬�����ʷ��ں�ϸ�����͵ı����������ϸ�����������ϸ���ֻ��Ĺ��̡�ϸ���ķֻ���һ�����ӵĹ��̣���Ҫ�����������ӡ���������Լ�ϸ�������������ۺ�����[7]������bFGF�����Dz���ϸ���ֻ�����Ҫ����֮һ�������յ����������ģ��йظ�������ϸ���ֻ���ϵ���о��д����
ע�ͣ�������Ȼ��ѧ������������(39700160)
�����
[1]�½�����ʷ����.����άϸ���������ӵ��о���չ.�����������ܲ�ѧ��־��1994��4��111-113.
[2] Thesleff I, Partanen AM, Vainio S. Epithelial-mesenchymal interactions in tooth morphogenesis: the roles of extracellular matrix, growth factors, and cell surface receptors. J Craniofac Genet Devl Biol, 1991, 11:229-237.
, http://www.100md.com
[3] Nakashima M. The effects of growth factors on DNA synthesis and alkaline phosphatase activity in bovine dental pulp cells. Archs Oral Biol, 1992, 37:231-236.
[4] ��ƽ��ʷ���ϣ��½���.ţѪ����άճ���������������������άϸ����ֳ��DNA�ϳɺ�ϸ����̬��Ӱ��.�����������ܲ�ѧ��־��1995��5��17-19.
[5] Bronkers ALJJ, Lyraruu DM, Woltgens JHM. Immunohistochemistry of extracellular matrix proteins during various stages of dentinogenesis. Connect Tissue Res, 1989, 22:65-70.
, http://www.100md.com
[6] Endo K. Lectin histochemical study on human dental pulp: special reference to odontoblasts and pulp cells. Meikai Daiguku Shigaku Zashi, 1989,18:360-381.
[7] Ruch JV, Lesot H, Bege-Kin C, Odontoblast differentiation. Int J Dev Biol, 1995, 39:51-68.
�ո壺1998-02-16
�أ�1998-12-20, ��Ĵҽҩ