高效液相色谱法测定人血浆中紫杉醇浓度
作者:董慧 赵春景 马文秀 代青 肖文华 胡绍毅
单位:董慧 赵春景 马文秀 代青 第三军医大学附属西南医院药剂科 重庆,400038;肖文华 胡绍毅 第三军医大学附属西南医院肿瘤科 重庆,400038
关键词:紫杉醇;高效液相色谱法;血药浓度
第三军医大学学报990522 Determination of Taxol in human plasma by HPLC
提 要 目的:建立人血浆中紫杉醇的高效液相色谱测定法。方法:血浆中紫杉醇用醋酸乙酯提取后在C18柱上以甲醇-水(65∶35,v/v)为流动相,检测波长227nm,以峰面积外标法定量。结果:该法萃取回收率为94.58%,方法回收率为99.19%;日内、日间RSD均小于4%(n=5),应用本法测定了两例癌症患者静脉输注紫杉醇的经时血药浓度符合二室开放模型。结论:本法操作简便,灵敏度高,专属性强。
, 百拇医药
中图法分类号 R446.1;R979.5
紫杉醇(Taxol)是一种具有抗肿瘤活性的天然产物,其化学结构新颖,作用机制独特,它在癌细胞分裂时能与细胞微管蛋白结合,促使细胞中微管稳定和聚合,使细胞有丝分裂受到阻断,从而抑制肿瘤生长,是近年来受到广泛重视的一类新型抗肿瘤药物[1,2]。为了研究紫杉醇在人体内的代谢过程,我们建立了简便灵敏的HPLC-UV检测法,能定量地分析血浆中紫杉醇的含量。
1 材料与方法
1.1 药品与试药 紫杉醇注射液(商品名:紫素,北京协和药厂,批号:960625);紫杉醇对照品(纯度>99%,由四川省凉山洲生物研究所提供);甲醇为色谱纯,醋酸乙酯为分析试剂;超纯水(由Millipore超纯水器制备)。
1.2 仪器与色谱条件 Waters 810液相色谱仪,包括510泵,484可变波长紫外检测器,Baseline 810计算机控制及处理系统;μ-Bondapak C18柱(3.9×150mm,10μm);流动相为甲醇-水(65∶35,v/v);流速为1ml/min;柱温为30℃±1℃;检测波长为227nm;灵敏度0.002AUFS。
, 百拇医药
1.3 对照品溶液的制备 贮备液:精密称取紫杉醇对照品适量,用甲醇配成浓度为
200mg/L和20mg/L的对照品贮备液,置4℃保存,两周内稳定。
工作液:临用时精密吸取贮备液,用甲醇稀释成浓度为0.2~30mg/L的工作液备用。
1.4 血浆样品处理 取1ml待测血浆,加醋酸乙酯4ml在旋涡混合器上混匀3min,1000×g离心15min,分离醋酸乙酯层,同法重复萃取一次,合并醋酸乙酯,于40℃恒温水浴中,用氮气流吹干,残留物以流动相200μl溶解,取20μl进样。
2 结果
2.1 方法学研究
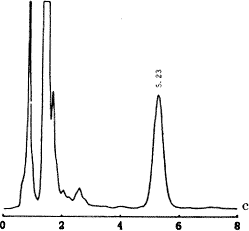
2.1.1 色谱行为 图1中a、b、c分别为空白血浆,空白血浆加紫杉醇及患者血浆样品的HPLC色谱图,血浆中内源性物质对紫杉醇测定无干扰。

, http://www.100md.com
图1 空白血浆(a),外加紫杉醇标准血浆样品(b)及患者血浆样品(c)的HPLC色谱图
2.1.2 血浆标准曲线 取0.9ml空白血浆7份,精确加入紫杉醇工作液各100μl,配成0.02、0.05、0.1、0.5、1.0、2.0、3.0mg/L的标准浓度,按1.4项方法处理、测定。以峰面积对浓度进行回归,回归方程为:C=167406.6965X-5695.9522,r=0.9998。最低有效检测浓度为0.01mg/L。
2.1.3 回收率实验 萃取回收率:于空白血浆中加入不同量的紫杉醇对照品工作液,配成浓度为0.05mg/L和3.0mg/L的溶液,经预处理后测定,并与相应量的未经处理的标准品对照测定,按峰面积比计算得平均萃取回收率为94.58%,RSD为1.15%。
方法回收率:于空白血浆中加入一定量的紫杉醇对照品工作液,分别配成高、中、低3个不同浓度的样品,经预处理后测定,所得数据按回归方程计算测得量,其平均回收率(n=9)为99.19%,RSD为3.56%。
, 百拇医药
2.1.4 精密度实验 取0.05、1.0、3.0mg/L 3种浓度的紫杉醇血样,分别于同一天及连续5d提取5份样品,依法测定,计算日内RSD分别为3.95%、1.78%和2.15%;日间RSD为3.24%、1.41%和2.38%。
2.2 临床应用 两名男性癌症患者(恶性淋巴瘤与肺癌各1例),4周内未接受任何化疗和放疗,均给予紫杉醇注射液240mg(分别相当于132mg/m2和134mg/m2)于5%葡萄糖注射液500ml中4h恒速静脉输注后即刻、5、15、30min及1、2、3、6、12、24h采血测定血药浓度,数据经3P87药代动力学程序处理分析,表明两例患者的血浆药物浓度经时变化符合二室开放模型。图2为两例患者平均血药浓度-时间曲线。主要药代动力学参数见表1。
图2 两例癌症患者静脉输注紫杉醇240mg后平均血药浓度-时间曲线
, 百拇医药
表1 两例患者静脉输注紫杉醇后主要药代动力学参数 病例
α
β
t1/2α
t1/2β
vd
AUC
Cls
(h-1)
(h-1)
(h)
, http://www.100md.com (h)
(L/m2)
(μmol.h)
[ml.min-1.(m2)-1]
1
4.692
0.088
0.148
7.867
100.66
, http://www.100md.com
17.440
147.58
2
2.467
0.081
0.281
8.581
102.27
18.956
138.05
3 讨论
考虑到癌症患者临床用药复杂,因而选择了可能同时应用的地塞米松、胃复安、恩丹西酮、苯海拉明、西米替丁、能量合剂、维生素B6等8种药物,在相同色谱条件下进样,均不干扰紫杉醇的测定。
, http://www.100md.com
紫杉醇的血药浓度受到静脉给药方案的影响,而且个体差异较大。从本组两例患者输注紫杉醇的初步检测结果可见,紫杉醇在输注过程中,血药浓度逐渐增加,输注一旦停止,血药浓度即开始下降,24h时的浓度(0.06μmol/L),仍在体外能引起微管变化,细胞毒性所需浓度(0.01~0.1μmol/L)的范围之内。体内血药浓度衰减过程为双相性;分布容积较大,表明药物与血浆蛋白及组织成分,尤其是微管蛋白等广泛结合。两例患者的药动学参数均与文献[3]报道采用相同剂量所得参数的范围接近。
作者简介:董慧,女,62岁,主任药师
参考文献
1 Manfredi J J,Horwitz S B.Taxol:An antimitotic agent with a new mechanism of action.Pharmacol Ther,1984,25(1):83
, http://www.100md.com
2 Liebmann J,Cook J A,Lipschuitz C,et al.The influence of cremophor EL on the cell cycle effects of paclitaxel.(Taxol) in human tumor cell lines.Cancer Chemother Pharmacol,1994,33(4):331
3 Longnecker S M,Donehower R C,Cates A E,et al.High-performance liquid chromatographic assay for taxol in human plasma and urine and pharmacokinetics in a phase I trial.Cancer Treat Rep,1987,71(1):53
(收稿:1998-03-18;修回:1998-06-08), 百拇医药
单位:董慧 赵春景 马文秀 代青 第三军医大学附属西南医院药剂科 重庆,400038;肖文华 胡绍毅 第三军医大学附属西南医院肿瘤科 重庆,400038
关键词:紫杉醇;高效液相色谱法;血药浓度
第三军医大学学报990522 Determination of Taxol in human plasma by HPLC
提 要 目的:建立人血浆中紫杉醇的高效液相色谱测定法。方法:血浆中紫杉醇用醋酸乙酯提取后在C18柱上以甲醇-水(65∶35,v/v)为流动相,检测波长227nm,以峰面积外标法定量。结果:该法萃取回收率为94.58%,方法回收率为99.19%;日内、日间RSD均小于4%(n=5),应用本法测定了两例癌症患者静脉输注紫杉醇的经时血药浓度符合二室开放模型。结论:本法操作简便,灵敏度高,专属性强。
, 百拇医药
中图法分类号 R446.1;R979.5
紫杉醇(Taxol)是一种具有抗肿瘤活性的天然产物,其化学结构新颖,作用机制独特,它在癌细胞分裂时能与细胞微管蛋白结合,促使细胞中微管稳定和聚合,使细胞有丝分裂受到阻断,从而抑制肿瘤生长,是近年来受到广泛重视的一类新型抗肿瘤药物[1,2]。为了研究紫杉醇在人体内的代谢过程,我们建立了简便灵敏的HPLC-UV检测法,能定量地分析血浆中紫杉醇的含量。
1 材料与方法
1.1 药品与试药 紫杉醇注射液(商品名:紫素,北京协和药厂,批号:960625);紫杉醇对照品(纯度>99%,由四川省凉山洲生物研究所提供);甲醇为色谱纯,醋酸乙酯为分析试剂;超纯水(由Millipore超纯水器制备)。
1.2 仪器与色谱条件 Waters 810液相色谱仪,包括510泵,484可变波长紫外检测器,Baseline 810计算机控制及处理系统;μ-Bondapak C18柱(3.9×150mm,10μm);流动相为甲醇-水(65∶35,v/v);流速为1ml/min;柱温为30℃±1℃;检测波长为227nm;灵敏度0.002AUFS。
, 百拇医药
1.3 对照品溶液的制备 贮备液:精密称取紫杉醇对照品适量,用甲醇配成浓度为
200mg/L和20mg/L的对照品贮备液,置4℃保存,两周内稳定。
工作液:临用时精密吸取贮备液,用甲醇稀释成浓度为0.2~30mg/L的工作液备用。
1.4 血浆样品处理 取1ml待测血浆,加醋酸乙酯4ml在旋涡混合器上混匀3min,1000×g离心15min,分离醋酸乙酯层,同法重复萃取一次,合并醋酸乙酯,于40℃恒温水浴中,用氮气流吹干,残留物以流动相200μl溶解,取20μl进样。
2 结果
2.1 方法学研究
2.1.1 色谱行为 图1中a、b、c分别为空白血浆,空白血浆加紫杉醇及患者血浆样品的HPLC色谱图,血浆中内源性物质对紫杉醇测定无干扰。



, http://www.100md.com
图1 空白血浆(a),外加紫杉醇标准血浆样品(b)及患者血浆样品(c)的HPLC色谱图
2.1.2 血浆标准曲线 取0.9ml空白血浆7份,精确加入紫杉醇工作液各100μl,配成0.02、0.05、0.1、0.5、1.0、2.0、3.0mg/L的标准浓度,按1.4项方法处理、测定。以峰面积对浓度进行回归,回归方程为:C=167406.6965X-5695.9522,r=0.9998。最低有效检测浓度为0.01mg/L。
2.1.3 回收率实验 萃取回收率:于空白血浆中加入不同量的紫杉醇对照品工作液,配成浓度为0.05mg/L和3.0mg/L的溶液,经预处理后测定,并与相应量的未经处理的标准品对照测定,按峰面积比计算得平均萃取回收率为94.58%,RSD为1.15%。
方法回收率:于空白血浆中加入一定量的紫杉醇对照品工作液,分别配成高、中、低3个不同浓度的样品,经预处理后测定,所得数据按回归方程计算测得量,其平均回收率(n=9)为99.19%,RSD为3.56%。
, 百拇医药
2.1.4 精密度实验 取0.05、1.0、3.0mg/L 3种浓度的紫杉醇血样,分别于同一天及连续5d提取5份样品,依法测定,计算日内RSD分别为3.95%、1.78%和2.15%;日间RSD为3.24%、1.41%和2.38%。
2.2 临床应用 两名男性癌症患者(恶性淋巴瘤与肺癌各1例),4周内未接受任何化疗和放疗,均给予紫杉醇注射液240mg(分别相当于132mg/m2和134mg/m2)于5%葡萄糖注射液500ml中4h恒速静脉输注后即刻、5、15、30min及1、2、3、6、12、24h采血测定血药浓度,数据经3P87药代动力学程序处理分析,表明两例患者的血浆药物浓度经时变化符合二室开放模型。图2为两例患者平均血药浓度-时间曲线。主要药代动力学参数见表1。

图2 两例癌症患者静脉输注紫杉醇240mg后平均血药浓度-时间曲线
, 百拇医药
表1 两例患者静脉输注紫杉醇后主要药代动力学参数 病例
α
β
t1/2α
t1/2β
vd
AUC
Cls
(h-1)
(h-1)
(h)
, http://www.100md.com (h)
(L/m2)
(μmol.h)
[ml.min-1.(m2)-1]
1
4.692
0.088
0.148
7.867
100.66
, http://www.100md.com
17.440
147.58
2
2.467
0.081
0.281
8.581
102.27
18.956
138.05
3 讨论
考虑到癌症患者临床用药复杂,因而选择了可能同时应用的地塞米松、胃复安、恩丹西酮、苯海拉明、西米替丁、能量合剂、维生素B6等8种药物,在相同色谱条件下进样,均不干扰紫杉醇的测定。
, http://www.100md.com
紫杉醇的血药浓度受到静脉给药方案的影响,而且个体差异较大。从本组两例患者输注紫杉醇的初步检测结果可见,紫杉醇在输注过程中,血药浓度逐渐增加,输注一旦停止,血药浓度即开始下降,24h时的浓度(0.06μmol/L),仍在体外能引起微管变化,细胞毒性所需浓度(0.01~0.1μmol/L)的范围之内。体内血药浓度衰减过程为双相性;分布容积较大,表明药物与血浆蛋白及组织成分,尤其是微管蛋白等广泛结合。两例患者的药动学参数均与文献[3]报道采用相同剂量所得参数的范围接近。
作者简介:董慧,女,62岁,主任药师
参考文献
1 Manfredi J J,Horwitz S B.Taxol:An antimitotic agent with a new mechanism of action.Pharmacol Ther,1984,25(1):83
, http://www.100md.com
2 Liebmann J,Cook J A,Lipschuitz C,et al.The influence of cremophor EL on the cell cycle effects of paclitaxel.(Taxol) in human tumor cell lines.Cancer Chemother Pharmacol,1994,33(4):331
3 Longnecker S M,Donehower R C,Cates A E,et al.High-performance liquid chromatographic assay for taxol in human plasma and urine and pharmacokinetics in a phase I trial.Cancer Treat Rep,1987,71(1):53
(收稿:1998-03-18;修回:1998-06-08), 百拇医药