高锰酸钾褪色法测定尿液草酸
作者:陈军浩 顾光煜 王以立
单位:南京大学医学院附属南京鼓楼医院检验科
关键词:草酸;草酸钙;高锰酸钾;比色法
临床检验杂志990503 摘要 过量的CaCl2和无水乙醇在尿液pH为5时,可与草酸形成草酸钙沉淀。用草酸钙平衡过的0.02 mol/L乙酸及去离子水洗涤沉淀,可以除去沉淀物中的干扰物质。在60°C酸性环境中,草酸还原高锰酸钾,使其在525 nm处吸光度下降。根据吸光度的变化可计算出尿液中草酸含量。本法平均回收率88.8%。批内、批间CV分别为10.4%、15.5%。本法无需特殊设备,适合一般常规实验室使用。
Potassium permanganate decolorization method for urinary oxalate estimation
, 百拇医药
CHEN Junhao,GU Guanyi,WANG Yili(Department of Laboratory,Affiliated Hospital of GuLou ,Medical College of Nanjing University,Nanjing,210008)
Abstract Oxalate is first coprecipitated at pH 5 as calcium oxalate with excess calcium ions and ethanol.Interference in the precipitate is removed with 0.02 mol/L acetic acid equilibrated calcium oxalate crystal,and then washing with deionized water.Absorbances of KMnO4 is decolorized in the presence of oxalate.It can measure the concentration of oxalate in urine from the change of absorbances.The mean percentage recovery is 88.8%.The coefficients of variation within-day and between-day are 10.4% and 15.5%。It can be set up as a rotine method of urinary oxalate assessment in clinical laboratory.
, 百拇医药
Key words oxalate; potassium permanganate; colorimetric method
草酸测定在肾内及肾外结石的形成及研究等方面有十分重要的意义。虽然草酸测定的方法很多,如比色法、色谱法、酶法、间接法等,但均因操作复杂、费时或需特殊设备而无法被一般常规实验室所接受。我们根据在酸性环境中,草酸与高锰酸钾发生化学反应使高锰酸钾溶液褪色。据此,建立了高锰酸钾褪色法测定尿液草酸的方法。取得满意的结果。现报告如下。
1 试剂与仪器
1.1 试剂
1.1.1 100 mmol/L高锰酸钾贮存液 称取高锰酸钾15.8 g,溶解于1 000 ml去离子水中,加盖,置4°C冰箱内避光,可保存三个月。
1.1.2 1.0 mmol/L高锰酸钾应用液 取高锰酸钾贮存液1 ml,加去离子水至100 ml,加盖置4°C冰箱至少可保存一周。
, 百拇医药
1.1.3 0.1 mol/L草酸标准贮存液 准确称取草酸(H2C2O4.2H2O)1.26 g,溶解于100 ml去离子水中。
1.1.4 1 μmol/ml草酸标准应用液 吸取草酸标准贮存液1.0 ml,加去离子水至100 ml。
1.1.5 500 mmol/L CaCl2溶液 称取无水CaCl2 5.5 g,溶于100 ml去离子水中。
1.1.6 0.02 mol/L乙酸-草酸钙平衡液 取500 mmol/L CaCl2溶液1 ml,与草酸贮存液5 ml混匀,室温过夜。用去离子水反复洗沉淀4次,将其加入到0.02 mol/L乙酸溶液中平衡2小时左右。过滤除去沉淀物,备用。
, 百拇医药
所用试剂均为分析纯。
1.2 仪器 日立U-2001型分光光度计。
2 方法
2.1 尿液草酸沉淀 取新鲜尿液5 ml,用精密pH试纸,以1 mol/L H2SO4或1 mol/L NaOH调pH至5.0。取该弱酸化的尿液0.5 ml,加500 mmol/L CaCl2 0.1 ml,再加入无水乙醇2 ml,充分混匀后,4°C冰箱静置3小时以上。取出3 000 r/min离心10 min,弃上清液。向沉淀物中加入0.02 mmol/L乙酸-草酸钙平衡液5 ml,充分混匀,以4 000 r/min离心10 min,弃上清液。再向试管中加入去离子水5 ml,充分混匀,4 000 r/min离心10 min,小心弃上清液。将试管倒置于滤纸上,沥干水分,待测。
, 百拇医药 2.2 尿液草酸测定 向上述含草酸钙沉淀的试管中加入1 mol/L H2SO4及去离子水各1.0 ml,溶解沉淀物,再加高锰酸钾应用液3.0 ml,混匀,置60°C水浴10 min后,3 000 r/min离心10 min,取上清液于525 nm比色。同时做空白及标准测定管。
2.3 尿液草酸浓度计算
3 实验与结果
3.1 吸收曲线 对空白管(高锰酸钾应用液)、测定比色液进行波长扫描,两者吸收曲线完全相同。图1为高锰酸钾应用液和测定比色液吸收曲线。在525 nm及545 nm处分别有一吸收峰,525 nm处吸光度略高于545 nm,故我们选择525 nm作为测定波长。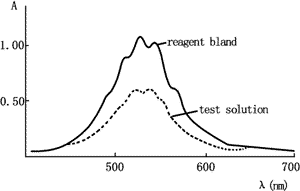
, http://www.100md.com
Figure 1 Absorption curve of potassium permanganate
图1 空白管和测定管光谱吸收曲线
3.2 标准曲线 取10支试管,分别加入草酸标准应用液0.05 ml、0.10 ml、0.15 ml、0.20 ml、0.25 ml、0.30 ml、0.35 ml、0.40 ml、0.45 ml及0.50 ml,再分别加入2 mol/L H2SO4各0.5 ml,用去离子水补至2.0 ml。各管换算为尿样品浓度分别为0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9及1.0 μmol/ml。加高锰酸钾应用液3.0 ml,接下按方法2.2操作。结果表明本法测定尿液草酸线性范围至少为0.1~1.0 (μmol/L)。相关系数r=0.9986,以Y表示吸光度差,X表示草酸浓度,直线回归方程Y=2.155X+0.038。
, 百拇医药
3.3 精密度和回收率 取2份健康体检者尿液样品,调pH为5.0,置4°C冰箱保存。一份用于批内精密度测定,结果为(n=10):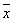 =0.216 μmol/ml;s=0.0225;CV=10.4%。另一份用于批间精密度测定,结果为(n=5):
=0.216 μmol/ml;s=0.0225;CV=10.4%。另一份用于批间精密度测定,结果为(n=5):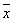 =0.155 μmol/ml;s=0.024;CV=15.5%。回收率测定:取4支试管分别加入尿液标本0.5 ml,再各加入0.25 ml草酸标准应用液,则每管草酸的加入量为0.25 μmol。实际平均回收量为0.222 μmol,计算得平均回收率88.8%。
=0.155 μmol/ml;s=0.024;CV=15.5%。回收率测定:取4支试管分别加入尿液标本0.5 ml,再各加入0.25 ml草酸标准应用液,则每管草酸的加入量为0.25 μmol。实际平均回收量为0.222 μmol,计算得平均回收率88.8%。
3.5 干扰试验 取一份尿液标本,用200 g/L葡萄糖溶液调尿糖分别为10 g/L(++++)、20 g/L。尿糖10 g/L时无干扰,20 g/L时较原尿液测定值高34.4%。向尿液中加入3 g/L抗坏血酸溶液,使浓度分别为150 mg/L、300 mg/L。尿液抗坏血酸为150 mg/L时无干扰,300 mg/L时较原尿液测定值高25.2%,有显著的正干扰。向尿液中加入不同量血液红细胞,尿液分析仪测定结果分别为PRO++、BLD++及PRO+++、BLD++++。各浓度蛋白质和红细胞对尿液草酸测定结果无明显影响。
, 百拇医药
4 讨论
尿结石在许多地区有较高的发病率。在所有尿结石患者中,以草酸钙和磷酸钙为结石主要成分的占70%以上[1]。据Januzvic[2]对由尿路排出或手术取得的结石分析结果表明草酸是尿结石的主要组成部分之一。以往人们十分重视钙在这些疾病中的作用,最近的研究表明草酸对尿结石形成的危险更大[1]。所以尿液草酸的测定有十分重要的意义。
用高锰酸钾褪色法测定尿液草酸,重要的是尽量完全获取草酸钙沉淀并除去非特异干扰物质。我们参考文献[3],在pH=5时,用过量的氯化钙和无水乙醇共同沉淀尿中草酸,该沉淀物中含大量磷酸盐及蛋白质等。可用0.02 mol/L乙酸-草酸钙平衡液洗涤沉淀,以除去大部分杂质,而草酸钙不丢失[3],再以去离子水洗涤,得到比较纯的草酸钙沉淀。我们用磺柳酸法未能在处理过的草酸钙中检出蛋白质。文献报告[3]用0.1 mol/L乙酸-草酸钙平衡液洗涤沉淀,而我们用0.02 mol/L乙酸-草酸钙平衡液,也能够获得满意效果,故改用0.02 mol/L乙酸-草酸钙平衡液,以减低洗涤液酸浓度,有利于沉淀物中蛋白质的消除。
, http://www.100md.com
反应液离心除去由Mn5+形成的棕色沉淀物后,上清比色液一小时内吸光度无变化。我们用草酸标准液测得本法最低检出量为0.1 μmol/ml,最高检出量为1.0 μmol/ml。在实际尿液草酸测定中,需沉淀、洗涤等步骤,不可避免引起草酸丢失[5],故实际测试中的最低检出量还需对尿草酸沉淀方式进行评价。本法较其它无需分离而直接测定草酸实验的回收率低,也是上述原因引起的。一般正常人24小时尿草酸排出量在0.29~0.52 mmol之间[5],约为0.19~0.35 μmol/ml,本法线性范围基本能够满足临床需要。
尿液草酸测定干扰因素较多,不同方法间结果差异较大[6],本法经洗涤后,可除去部分干扰物。文献报告[3]洗涤后沉淀物中钙的含量(mmol/L)与草酸含量相当,可用钙离子浓度间接反映草酸浓度,且与比色法、酶法有良好的相关性,证明沉淀物已比较纯。我们试验结果表明,一般病理浓度尿糖、VitC及血尿对本法无干扰,异常高浓度尿糖及VitC对本法仍然有正干扰。
, 百拇医药
参考文献
1 Conyers A J,Bals R,Rofe A M.The relation of clinical catastrophes,endogenous oxalate production,and urolithiasis.Clin Chem,1990,36:1717
2 Januzoric L J,Prtenjak G.Quantitative analysis of calcium oxalate and calcium oxalate-phosphate urinary stones.Clin Chem,1990,36:1164
3 Sribonlue P,Suwantrai S,Prasongwatana V.An indirect method for urinary oxalate estimation.Clin Chem Acta,1998,273:59
4 董维宪,主编.各种离子的化学分别检出法.北京师范大学出版社.236
5 孟泽,徐俊,曹红琴.比色法测定尿中草酸.临床检验杂志,1996,14(1):5
6 Zerwekh G E,Drake E,Gregory J,et al.Assay of urinary oxalate:six methodologies compared.Clin Chem,1983,29:1977
(1999-01-15收稿,1999-05-13修回), http://www.100md.com
单位:南京大学医学院附属南京鼓楼医院检验科
关键词:草酸;草酸钙;高锰酸钾;比色法
临床检验杂志990503 摘要 过量的CaCl2和无水乙醇在尿液pH为5时,可与草酸形成草酸钙沉淀。用草酸钙平衡过的0.02 mol/L乙酸及去离子水洗涤沉淀,可以除去沉淀物中的干扰物质。在60°C酸性环境中,草酸还原高锰酸钾,使其在525 nm处吸光度下降。根据吸光度的变化可计算出尿液中草酸含量。本法平均回收率88.8%。批内、批间CV分别为10.4%、15.5%。本法无需特殊设备,适合一般常规实验室使用。
Potassium permanganate decolorization method for urinary oxalate estimation
, 百拇医药
CHEN Junhao,GU Guanyi,WANG Yili(Department of Laboratory,Affiliated Hospital of GuLou ,Medical College of Nanjing University,Nanjing,210008)
Abstract Oxalate is first coprecipitated at pH 5 as calcium oxalate with excess calcium ions and ethanol.Interference in the precipitate is removed with 0.02 mol/L acetic acid equilibrated calcium oxalate crystal,and then washing with deionized water.Absorbances of KMnO4 is decolorized in the presence of oxalate.It can measure the concentration of oxalate in urine from the change of absorbances.The mean percentage recovery is 88.8%.The coefficients of variation within-day and between-day are 10.4% and 15.5%。It can be set up as a rotine method of urinary oxalate assessment in clinical laboratory.
, 百拇医药
Key words oxalate; potassium permanganate; colorimetric method
草酸测定在肾内及肾外结石的形成及研究等方面有十分重要的意义。虽然草酸测定的方法很多,如比色法、色谱法、酶法、间接法等,但均因操作复杂、费时或需特殊设备而无法被一般常规实验室所接受。我们根据在酸性环境中,草酸与高锰酸钾发生化学反应使高锰酸钾溶液褪色。据此,建立了高锰酸钾褪色法测定尿液草酸的方法。取得满意的结果。现报告如下。
1 试剂与仪器
1.1 试剂
1.1.1 100 mmol/L高锰酸钾贮存液 称取高锰酸钾15.8 g,溶解于1 000 ml去离子水中,加盖,置4°C冰箱内避光,可保存三个月。
1.1.2 1.0 mmol/L高锰酸钾应用液 取高锰酸钾贮存液1 ml,加去离子水至100 ml,加盖置4°C冰箱至少可保存一周。
, 百拇医药
1.1.3 0.1 mol/L草酸标准贮存液 准确称取草酸(H2C2O4.2H2O)1.26 g,溶解于100 ml去离子水中。
1.1.4 1 μmol/ml草酸标准应用液 吸取草酸标准贮存液1.0 ml,加去离子水至100 ml。
1.1.5 500 mmol/L CaCl2溶液 称取无水CaCl2 5.5 g,溶于100 ml去离子水中。
1.1.6 0.02 mol/L乙酸-草酸钙平衡液 取500 mmol/L CaCl2溶液1 ml,与草酸贮存液5 ml混匀,室温过夜。用去离子水反复洗沉淀4次,将其加入到0.02 mol/L乙酸溶液中平衡2小时左右。过滤除去沉淀物,备用。
, 百拇医药
所用试剂均为分析纯。
1.2 仪器 日立U-2001型分光光度计。
2 方法
2.1 尿液草酸沉淀 取新鲜尿液5 ml,用精密pH试纸,以1 mol/L H2SO4或1 mol/L NaOH调pH至5.0。取该弱酸化的尿液0.5 ml,加500 mmol/L CaCl2 0.1 ml,再加入无水乙醇2 ml,充分混匀后,4°C冰箱静置3小时以上。取出3 000 r/min离心10 min,弃上清液。向沉淀物中加入0.02 mmol/L乙酸-草酸钙平衡液5 ml,充分混匀,以4 000 r/min离心10 min,弃上清液。再向试管中加入去离子水5 ml,充分混匀,4 000 r/min离心10 min,小心弃上清液。将试管倒置于滤纸上,沥干水分,待测。
, 百拇医药 2.2 尿液草酸测定 向上述含草酸钙沉淀的试管中加入1 mol/L H2SO4及去离子水各1.0 ml,溶解沉淀物,再加高锰酸钾应用液3.0 ml,混匀,置60°C水浴10 min后,3 000 r/min离心10 min,取上清液于525 nm比色。同时做空白及标准测定管。
2.3 尿液草酸浓度计算

3 实验与结果
3.1 吸收曲线 对空白管(高锰酸钾应用液)、测定比色液进行波长扫描,两者吸收曲线完全相同。图1为高锰酸钾应用液和测定比色液吸收曲线。在525 nm及545 nm处分别有一吸收峰,525 nm处吸光度略高于545 nm,故我们选择525 nm作为测定波长。

, http://www.100md.com
Figure 1 Absorption curve of potassium permanganate
图1 空白管和测定管光谱吸收曲线
3.2 标准曲线 取10支试管,分别加入草酸标准应用液0.05 ml、0.10 ml、0.15 ml、0.20 ml、0.25 ml、0.30 ml、0.35 ml、0.40 ml、0.45 ml及0.50 ml,再分别加入2 mol/L H2SO4各0.5 ml,用去离子水补至2.0 ml。各管换算为尿样品浓度分别为0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9及1.0 μmol/ml。加高锰酸钾应用液3.0 ml,接下按方法2.2操作。结果表明本法测定尿液草酸线性范围至少为0.1~1.0 (μmol/L)。相关系数r=0.9986,以Y表示吸光度差,X表示草酸浓度,直线回归方程Y=2.155X+0.038。
, 百拇医药
3.3 精密度和回收率 取2份健康体检者尿液样品,调pH为5.0,置4°C冰箱保存。一份用于批内精密度测定,结果为(n=10):
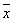 =0.216 μmol/ml;s=0.0225;CV=10.4%。另一份用于批间精密度测定,结果为(n=5):
=0.216 μmol/ml;s=0.0225;CV=10.4%。另一份用于批间精密度测定,结果为(n=5):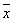 =0.155 μmol/ml;s=0.024;CV=15.5%。回收率测定:取4支试管分别加入尿液标本0.5 ml,再各加入0.25 ml草酸标准应用液,则每管草酸的加入量为0.25 μmol。实际平均回收量为0.222 μmol,计算得平均回收率88.8%。
=0.155 μmol/ml;s=0.024;CV=15.5%。回收率测定:取4支试管分别加入尿液标本0.5 ml,再各加入0.25 ml草酸标准应用液,则每管草酸的加入量为0.25 μmol。实际平均回收量为0.222 μmol,计算得平均回收率88.8%。3.5 干扰试验 取一份尿液标本,用200 g/L葡萄糖溶液调尿糖分别为10 g/L(++++)、20 g/L。尿糖10 g/L时无干扰,20 g/L时较原尿液测定值高34.4%。向尿液中加入3 g/L抗坏血酸溶液,使浓度分别为150 mg/L、300 mg/L。尿液抗坏血酸为150 mg/L时无干扰,300 mg/L时较原尿液测定值高25.2%,有显著的正干扰。向尿液中加入不同量血液红细胞,尿液分析仪测定结果分别为PRO++、BLD++及PRO+++、BLD++++。各浓度蛋白质和红细胞对尿液草酸测定结果无明显影响。
, 百拇医药
4 讨论
尿结石在许多地区有较高的发病率。在所有尿结石患者中,以草酸钙和磷酸钙为结石主要成分的占70%以上[1]。据Januzvic[2]对由尿路排出或手术取得的结石分析结果表明草酸是尿结石的主要组成部分之一。以往人们十分重视钙在这些疾病中的作用,最近的研究表明草酸对尿结石形成的危险更大[1]。所以尿液草酸的测定有十分重要的意义。
用高锰酸钾褪色法测定尿液草酸,重要的是尽量完全获取草酸钙沉淀并除去非特异干扰物质。我们参考文献[3],在pH=5时,用过量的氯化钙和无水乙醇共同沉淀尿中草酸,该沉淀物中含大量磷酸盐及蛋白质等。可用0.02 mol/L乙酸-草酸钙平衡液洗涤沉淀,以除去大部分杂质,而草酸钙不丢失[3],再以去离子水洗涤,得到比较纯的草酸钙沉淀。我们用磺柳酸法未能在处理过的草酸钙中检出蛋白质。文献报告[3]用0.1 mol/L乙酸-草酸钙平衡液洗涤沉淀,而我们用0.02 mol/L乙酸-草酸钙平衡液,也能够获得满意效果,故改用0.02 mol/L乙酸-草酸钙平衡液,以减低洗涤液酸浓度,有利于沉淀物中蛋白质的消除。
, http://www.100md.com
反应液离心除去由Mn5+形成的棕色沉淀物后,上清比色液一小时内吸光度无变化。我们用草酸标准液测得本法最低检出量为0.1 μmol/ml,最高检出量为1.0 μmol/ml。在实际尿液草酸测定中,需沉淀、洗涤等步骤,不可避免引起草酸丢失[5],故实际测试中的最低检出量还需对尿草酸沉淀方式进行评价。本法较其它无需分离而直接测定草酸实验的回收率低,也是上述原因引起的。一般正常人24小时尿草酸排出量在0.29~0.52 mmol之间[5],约为0.19~0.35 μmol/ml,本法线性范围基本能够满足临床需要。
尿液草酸测定干扰因素较多,不同方法间结果差异较大[6],本法经洗涤后,可除去部分干扰物。文献报告[3]洗涤后沉淀物中钙的含量(mmol/L)与草酸含量相当,可用钙离子浓度间接反映草酸浓度,且与比色法、酶法有良好的相关性,证明沉淀物已比较纯。我们试验结果表明,一般病理浓度尿糖、VitC及血尿对本法无干扰,异常高浓度尿糖及VitC对本法仍然有正干扰。
, 百拇医药
参考文献
1 Conyers A J,Bals R,Rofe A M.The relation of clinical catastrophes,endogenous oxalate production,and urolithiasis.Clin Chem,1990,36:1717
2 Januzoric L J,Prtenjak G.Quantitative analysis of calcium oxalate and calcium oxalate-phosphate urinary stones.Clin Chem,1990,36:1164
3 Sribonlue P,Suwantrai S,Prasongwatana V.An indirect method for urinary oxalate estimation.Clin Chem Acta,1998,273:59
4 董维宪,主编.各种离子的化学分别检出法.北京师范大学出版社.236
5 孟泽,徐俊,曹红琴.比色法测定尿中草酸.临床检验杂志,1996,14(1):5
6 Zerwekh G E,Drake E,Gregory J,et al.Assay of urinary oxalate:six methodologies compared.Clin Chem,1983,29:1977
(1999-01-15收稿,1999-05-13修回), http://www.100md.com