���������ֹ��ȷ��ⶨ����
���ߣ����ʤ ������ ������ ������ �˽�ϼ
��λ������ʡ�ط��������о��������� ���� 710003
�ؼ��ʣ������������������ֹ��ȷ�
�й��ط���ѧ��־990629 [ժҪ] Ŀ�� �����ʺ�������(Na2SeO3-KIO3)�������ij�����ķֹ��ȷ������� �о�Se4+�����������Ӧ�����չ������ԣ��������ʵĸ���������Բⶨ�������Լ���������Ӧʱ�䡢�ⶨ��Χ�Ƚ������Ż�ѡ��� ������ͼ����Ϊ0.02��g��Ħ������ϵ����365Ϊ1.8��104���Բ�ͬ�����������������IJⶨ�����ڱ���С��6.2%���������С��9.7%��ȷ�ȷ�ΧΪ97.9%��105.6%���÷������������ⶨ����������Բ���(P>0.2)������ �÷������м�㡢���á�������ȷ���ŵ㣬�ʺ�������(Na2SeO3-KIO3)�������ij��������
, ��Ĵҽҩ
[��ͼ�����] R115 [���ױ�ʶ��] A[���±��]1000-4955(1999)06-0480-04
Spectrophotometric determination of salt selenium with diaminonaphthalene
ZHU Can-sheng,MA Chang-an,LIU Hui-lan,et al.
(Shanxi Provincial Institute for Endemic Disease Control,Xi'an 710003,China)
[Abstract] Objective To establish a spectrophotometric method for measurement salt selenium for routine salt quality monitoring.Methods Studying the spectrophotometric features of the reaction between Se4+ and 2,3-diaminonaphthalene,and elemination of interfering substances;Optimizing measurement wavelength,reagent,reaction periods,and determination range.Results Detecting limit of this method is 0.02��g ��365 is 1.8��104;Intra CV is less than 6.2%;There is no signifi cant difference between this method and flurometric method fo salt selenium defermination (P>0.2)��inter CV is less than 9.7%;recovery ranges between 97.9%��105.6%.Conclusions This method for salt selenium is convenient,economic,sensitive,and accurate,suitable for salt selenium monitoring.
, ��Ĵҽҩ
[Key words] Diaminonaphthalene;Spectrophotometry;Salt Selenium
ʳ�μ�������Ⱥ��������㡢���еķ�����Ŀǰ���ڷ��ƿ�ɽ������ǽڲ��������������ߵ�λ��Ӧ��չ�����ij����⣬�Կ����������ĺ��������������������������Ӧ����Һ����ֵ�������������õ����Թ�ϵ���ɹ��Ľ���������(Na2SeO3-KIO3)�������ķֹ��ȷ���
1 ʵ��
1.1 ԭ�� ��pH1.5��2.0��Һ�У�2,3-��������ѡ���Ե���Se4+��Ӧ���ɻ�ɫ��4,5-���������ԣ���Ϊ��������ȡ����365nm����������Һ����ֵ����������ֱ�߹�ϵ��
1.2 ���� �����״�ʹ�õIJ�����������1+1�������5h���ϣ���������ˮ����ˮ��ϴ�ྻ�������ù��IJ�������������ˮ��ϴ����0.5%ϴ�·���Һ�н���2h���ϣ���������ˮ����ˮ��ϴ����
, ��Ĵҽҩ
200mlĥ�����ǣ�125ml��Һ©��(��������Ϳ��)��10ml�����Թܣ��ɵ�����ˮԡ����������723�ͷֹ��ȼ�(�Ϻ���������������)��
1.3 �Լ� �����Լ����ر�ָ���⣬��Ϊ��������
��������Һ����ȡ0.1000g���������������������У�����2ml�����ᡣ�ڷ�ˮԡ�ϼ�����ȥ����(Լ3��4h)����������8.4ml���ᣬ��������2min,Ȼ���ô�ˮ������100ml������Һ1.00ml��1.00mg������ȷ��ȡ���� ����������1.095g���ڴ�ˮ�У�ϡ��500ml(Se1.00mg/ml)��
������Һ������������Һ��0.1mol/L����ϡ�ͳ�1.00ml��1.000��g���������ڱ����ڱ��á�
1+4�����ȡ100ml���ᣬ����400ml��ˮ�С�
, ��Ĵҽҩ
0.02%�Ӻ���Һ����ȡ20mg�Ӻ죬����������ˮ�У���1�ΰ�ˮ��ʹ��ȫ�ܽ⣬�Ӵ�ˮϡ����100ml��
����Լ�����ȡ5g�����ǰ�����������ˮ�У������ȡ37g�Ҷ������������(���EDTA-2Na)��Լ200mlˮ�У������ܽ⡣���������ܰ���EDTA-2Na��Һ��Ϻ���25ml 0.02%�Ӻ���Һ����ˮϡ����5L��
0.1% 2,3-����������Һ��(����Һ���ڰ�������)��ȡ100mg 2,3-��������(���DAN)��200mlĥ������ƿ�У�����100ml 0.1mol/L���ᣬ��ҡ��ȫ���ܽ�(Լ15min)����Լ20ml�����飬������ҡ5min�����÷ֲ��ˮ��Ż�ԭ����ƿ�ڣ����û�������ȡ���(������DAN�����ʶ��ٶ�����һ����5��6��)�����˴�����ˮ��Һ��������ɫƿ�У���һ��Լ1cm��Ļ������Ը����������ñ����ڱ��档����ʹ����ÿ������һ��Ϊ�ˣ�������ʹ�ÿɱ���һ�ꡣ
, ��Ĵҽҩ
�����飺�ù��Ļ���������������á�
1.4 ���� ������ֻ��Ⱥ�ȷ��ȡ10g���ô�ˮϡ����100ml(��Ҫʱ���ɽ���Һ��˫�㶨����ֽ����)����ȡ10ml����Һ(�൱��1g����)��������Һ0.00,1.00,2.00,4.00,6.00,8.00,10.00ml��200mlĥ������ƿ�С���ƿ������10ml����Լ���ҡ�ȡ���1+4�����1+1��ˮ��������ɫ����ʱ��ҺpHΪ1.5��2.0����Ҫʱ��pH 0.5��5.0������ֽ���顣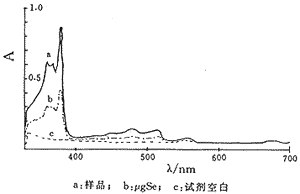
ͼ1 4��5-���������Ե���������
ע��Se4+���������������������Һ�з�Ӧ����pH 1.5��2.0Ϊ��ѣ�����ʱ��Һ���黯��̫��ʱ�ⶨ���ƫ�ߣ�����
���������ڰ��һ�ɫ�ƹ��²�������������ƿ�м���0.1%2��3-����������Һ��ҡ�ȣ��÷�ˮ�м���6min��ȡ����������ˮ����ȴ����ȡ5.00ml�������ڸ�ƿ�У��������ϣ���ҡ4min����ȫ����Һ���ڷ�Һ©���У����ֲ����ȡˮ�࣬�������������ھ����Թ��ڣ����ϴ��⡣
, ��Ĵҽҩ
�ڷֹ��ȼ��ϣ���365nm�����£���1cm��ɫ���Ի�����Ϊ�αȣ���Ũ��ֱ����ʽ���ⶨ���ع�������Ʒ������������������Ũ�ȼ�Ϊ���е�������(��λΪmg/kg)��
2 ���
2.1 �ⶨ������ѡ�� �������������Ӧ������4��5-���������ԣ��ڻ������е�����������ͼ1��ʾ��������շ���377nm������������ƫ��ȶ����ɡ��ڴδ����շ�365nm������10nm��Χ�ڣ�������ȶ������ϱȶ����ɣ���Ħ������ϵ���ż���ͼ�����������1.5�������1��ʾ��2.2 DAN������ѡ�� ȡ20ml������Һ8�ݣ����췴Ӧ����DAN���������2��ʾ��DAN����1.0mlʱ������ֵ�ӽ������һ����㶨�����Ա���ȡDAN 1.0ml��
��1 ���ֲ����ⶨ�����ļ���ָ�� ����
(nm)
, ��Ĵҽҩ
�ع�����
���ϵ��
Ħ������ϵ��
��
��ͼ����
��g
377
365
0.9984
0.9998
1.1��104
1.8��104
, http://www.100md.com
0.03
0.02
��2 DAN�����������ⶨ��Ӱ�� DAN����ml
����ֵA
0.5
1.0
1.5
2.0
2.5
3.0
4.5
5.0
0.412
, ��Ĵҽҩ
0.474
0.489
0.486
0.483
0.488
0.494
0.504
2.3 ��Ӧʱ���ѡ�� ����10%����Һ���ֱ�ȡ10.0ml 8�ݣ����첻ͬ��Ӧʱ��������ⶨ��Ӱ�졣���3��ʾ����Ӧ6min(�ڷ�ˮԡ�м���)������ֵ�ӽ�����һ����㶨�����Ա���ȡ��Ӧʱ��6min����3 ��Ӧʱ��������ⶨ��Ӱ�� ��Ӧʱ��min
����ֵA
2
, http://www.100md.com
4
6
8
10
0.242
0.295
0.333
0.338
0.337
2.4 ����Լ�������ѡ�� ȡ10.0mo 10%����Һ6�ݣ����벻ͬ������Լ������4��ʾ������Լ�����2.0ml������ֵ�ӽ�����һ����㶨��������Щ��Ʒ�������ʺ������ܽϸߣ����Ա���ѡȡ����Լ�10ml��
2.5 �������ӵĸ��� ���Ƹ��ָ���������Һ���ⶨ�������ⶨ��Ӱ�죬���5��ʾ������Ϊ1%Mg2+,2mg/L Pb2+,10mg/L Fe2+,Cu2+,Cr6+,Zn2+,20mg/L Mn2+,40mg/L Ba2+,Li+,1mol/L NO3��,100mg/L IO3���Ȳ��������IJⶨ��Sn4+Ũ��С��40mg/Lʱ�����Ų�����9%��KI���ڸ������IJⶨ(��ĿǰKIǿ��ʳ�ν���)����4 ����Լ������������ⶨ��Ӱ�� ����Լ�����ml
, ��Ĵҽҩ
����ֵA
0.00
2.00
4.00
6.00
8.00
10.00
0.271
0.319
0.321
0.299
0.304
0.311
, http://www.100md.com
��5 ��ͬ���������ⶨ�ľ��ܶ� ����
����
������
n
x��s(mg/kg)
CV%
n
x��s(mg/kg)
CV%
��
��
��
6
, ��Ĵҽҩ
6
6
2.27��0.14
4.92��0.26
14.73��0.44
6.2
5.3
3.0
5
5
5
2.36��0.23
5.26��0.79
, ��Ĵҽҩ
12.61��0.75
9.7
7.1
5.9
2.6 �ⶨ��Χ��ѡ�� ȡ��ͬ����������Һ���ֱ�ⶨ������ֵ����Ũ��Ϊ�����꣬����ֵΪ��������Ʊ����ߡ������������������0��16��g��Χ�ڣ����Թ�ϵ���ã��ع鷽��ΪC=22.32A-0.09�����ϵ��R=0.9998��ʵ�ʲⶨʱ��1g��Ʒ��������������10��g����ȡ�ⶨ��ΧΪ0��10��g��
2.7 ���ܶ���ȷ������ ȡ�͡��С�������Ũ���������ֱ�ⶨ�������ھ��ܶȺ����侫�ܶȡ����5��ʾ�����ڱ���ϵ��С��6.2%���������ϵ��С��9.7%��ȡ�͡��С�������Ũ���������ֱ����4��g�������ⶨ������ȷ�ȣ��������6������ȷ��(������)97.9%��105.6%����6 ���������ⶨ��ȷ�� ������
, ��Ĵҽҩ
n
��Ʒ��
������g
�ӱ���
��g
������%
ƽ��ֵ
��Χ
��
��
��
4
4
4
, ��Ĵҽҩ
2.36
5.26
12.61
4.00
4.00
4.00
100.5
103.0
99.7
991��102.8
99.0��105.6
97.9��100.7
, http://www.100md.com 2.8 ��ӫ��ֹ��ȷ��ıȽ� ȡ36���������ֱ��ñ�����ӫ��ֹ��ȷ�(���䷨)�ⶨ�������������ⶨ����и߶�����ԣ����ϵ��r=0.9869(P<0.001)���ع鷽��Ϊy=0.93x+0.53(yΪ�ֹ��ȷ��ⶨ�����xΪӫ�ⷨ)����t��������������ⶨ����������������Բ���(P>0.2)��
3 ����
���Ĺ�ȷ������϶࣬���ж������������ֹ��ȷ�Ӧ�ý�Ϊ�ձ飬���˷������������Է��������ûӷ���ǿ�����Խϴ�ļױ���ȡ���Բ�����Ա��һ����Σ���������������ȷ��ı�������[1��6]����Щ����������˹�ȷ��ⶨ���������ȣ���һ�㶼Ҫ�ϸ���Ʒ�Ӧ�¶ȼ�ʱ�䣬�����������ա�
2��3-��������(Ӣ����Ϊ2��3-Diaminonaphthalene,����ʽΪC10H10N2)����Se4+�������Ϸ�Ӧ������4��5-���������ԣ��ڼ�������376nm,���䲨��Ϊ520nm������ӫ�⣬����ӫ��ֹ��ȷ��ⶨ���÷������ȸߣ��Dzⶨ���ľ��䷽���������ڸ�����Ʒ�������IJⶨ7��10�����о�����Se4+�����������Ӧ�����ﱽ�������Ծ����������չ��ף�����EDTA�������ǰ��ڱ��������ӶԷ�Ӧ�ĸ��ţ����Ż�ѡ���˲ⶨ�������Լ���������Ӧʱ�估�ⶨ��Χ��ȷ���˶��������ֹ��ȷ��ⶨ���������������ɹ��Ľ����������ķֹ��ȷ���
, ��Ĵҽҩ
�÷���ͼ����Ϊ0.02��g��Ħ������ϵ��Ϊ1.8��104���Բ�ͬŨ�ȵ����������IJⶨ�����ڱ���С��6.2%���������С��9.7%��ȷ�ȷ�ΧΪ97.9%��105.6%���÷�����ӫ�ⷨ�Ƚϣ��ⶨ����������Բ���(P>0.2)���÷����м�㡢���á�������ȷ���ŵ㣬�ʺ�������(Na2SeO3-KIO3)�����������ij��������(������õ�������ʡ�ط������ΰ칫�һ�����ѧ�����Σ�������ʡ�ط��������о����¾�����������»�������ȵ�֧�֣��ڴ�һ����л!)
�����
[1] �ӱ�.���������Ĵμ�������ѧ-ӫ��ⶨ��[J].����ҽѧ����ѧ�ֲᣬ1987��3��168.
[2] ���Ͽ�ҵѧԺ������ѧ������.��ѧ�����ֲ�[M].��ѧ�����磬1984��495.
, ��Ĵҽҩ
[3] ������,�Ͻ�.������ѧ���ⶨ������[J].������ѧ��1997��25(5)��615.
[4] ���ⶫ��������.Se-KI-CTMAB-Tween-80��ϵ�������ֹ��Ȳⶨ�������о�[J].��Ԫ���뽡���о���1997��14(1)��5.
[5] Ҧ�G.����ȷ��ⶨ��������������ѧѧ��(��Ȼ��ѧ��)[J].1990��26(6)��657.
[6] ��˼��.������ѧ��ȷ��ⶨ������[J].������ѧѧ��(��Ȼ��ѧ��)��1989��13(3)��36-40.
[7] �л�����������.��������ˮ�����鷨[J].�й��������ұ�GB5750-85:58-61.
[8] �����ǣ���������ׯ����.������Ʒ��ˮ�������к�������ӫ��ⶨ��[J].Ӫ��ѧ����1985��7(1)��39.
[9] �¹��䣬�����ǣ�������.ӫ�������[J].��������ѧ�����磬1990��432-433.
[10] �����ģ������ܣ����죬��.ʹ��930��ӫ��Ʋⶨ����[J].�л�Ԥ��ҽѧ��־��1995��29(3)��180-181., ��Ĵҽҩ
��λ������ʡ�ط��������о��������� ���� 710003
�ؼ��ʣ������������������ֹ��ȷ�
�й��ط���ѧ��־990629 [ժҪ] Ŀ�� �����ʺ�������(Na2SeO3-KIO3)�������ij�����ķֹ��ȷ������� �о�Se4+�����������Ӧ�����չ������ԣ��������ʵĸ���������Բⶨ�������Լ���������Ӧʱ�䡢�ⶨ��Χ�Ƚ������Ż�ѡ��� ������ͼ����Ϊ0.02��g��Ħ������ϵ����365Ϊ1.8��104���Բ�ͬ�����������������IJⶨ�����ڱ���С��6.2%���������С��9.7%��ȷ�ȷ�ΧΪ97.9%��105.6%���÷������������ⶨ����������Բ���(P>0.2)������ �÷������м�㡢���á�������ȷ���ŵ㣬�ʺ�������(Na2SeO3-KIO3)�������ij��������
, ��Ĵҽҩ
[��ͼ�����] R115 [���ױ�ʶ��] A[���±��]1000-4955(1999)06-0480-04
Spectrophotometric determination of salt selenium with diaminonaphthalene
ZHU Can-sheng,MA Chang-an,LIU Hui-lan,et al.
(Shanxi Provincial Institute for Endemic Disease Control,Xi'an 710003,China)
[Abstract] Objective To establish a spectrophotometric method for measurement salt selenium for routine salt quality monitoring.Methods Studying the spectrophotometric features of the reaction between Se4+ and 2,3-diaminonaphthalene,and elemination of interfering substances;Optimizing measurement wavelength,reagent,reaction periods,and determination range.Results Detecting limit of this method is 0.02��g ��365 is 1.8��104;Intra CV is less than 6.2%;There is no signifi cant difference between this method and flurometric method fo salt selenium defermination (P>0.2)��inter CV is less than 9.7%;recovery ranges between 97.9%��105.6%.Conclusions This method for salt selenium is convenient,economic,sensitive,and accurate,suitable for salt selenium monitoring.
, ��Ĵҽҩ
[Key words] Diaminonaphthalene;Spectrophotometry;Salt Selenium
ʳ�μ�������Ⱥ��������㡢���еķ�����Ŀǰ���ڷ��ƿ�ɽ������ǽڲ��������������ߵ�λ��Ӧ��չ�����ij����⣬�Կ����������ĺ��������������������������Ӧ����Һ����ֵ�������������õ����Թ�ϵ���ɹ��Ľ���������(Na2SeO3-KIO3)�������ķֹ��ȷ���
1 ʵ��
1.1 ԭ�� ��pH1.5��2.0��Һ�У�2,3-��������ѡ���Ե���Se4+��Ӧ���ɻ�ɫ��4,5-���������ԣ���Ϊ��������ȡ����365nm����������Һ����ֵ����������ֱ�߹�ϵ��
1.2 ���� �����״�ʹ�õIJ�����������1+1�������5h���ϣ���������ˮ����ˮ��ϴ�ྻ�������ù��IJ�������������ˮ��ϴ����0.5%ϴ�·���Һ�н���2h���ϣ���������ˮ����ˮ��ϴ����
, ��Ĵҽҩ
200mlĥ�����ǣ�125ml��Һ©��(��������Ϳ��)��10ml�����Թܣ��ɵ�����ˮԡ����������723�ͷֹ��ȼ�(�Ϻ���������������)��
1.3 �Լ� �����Լ����ر�ָ���⣬��Ϊ��������
��������Һ����ȡ0.1000g���������������������У�����2ml�����ᡣ�ڷ�ˮԡ�ϼ�����ȥ����(Լ3��4h)����������8.4ml���ᣬ��������2min,Ȼ���ô�ˮ������100ml������Һ1.00ml��1.00mg������ȷ��ȡ���� ����������1.095g���ڴ�ˮ�У�ϡ��500ml(Se1.00mg/ml)��
������Һ������������Һ��0.1mol/L����ϡ�ͳ�1.00ml��1.000��g���������ڱ����ڱ��á�
1+4�����ȡ100ml���ᣬ����400ml��ˮ�С�
, ��Ĵҽҩ
0.02%�Ӻ���Һ����ȡ20mg�Ӻ죬����������ˮ�У���1�ΰ�ˮ��ʹ��ȫ�ܽ⣬�Ӵ�ˮϡ����100ml��
����Լ�����ȡ5g�����ǰ�����������ˮ�У������ȡ37g�Ҷ������������(���EDTA-2Na)��Լ200mlˮ�У������ܽ⡣���������ܰ���EDTA-2Na��Һ��Ϻ���25ml 0.02%�Ӻ���Һ����ˮϡ����5L��
0.1% 2,3-����������Һ��(����Һ���ڰ�������)��ȡ100mg 2,3-��������(���DAN)��200mlĥ������ƿ�У�����100ml 0.1mol/L���ᣬ��ҡ��ȫ���ܽ�(Լ15min)����Լ20ml�����飬������ҡ5min�����÷ֲ��ˮ��Ż�ԭ����ƿ�ڣ����û�������ȡ���(������DAN�����ʶ��ٶ�����һ����5��6��)�����˴�����ˮ��Һ��������ɫƿ�У���һ��Լ1cm��Ļ������Ը����������ñ����ڱ��档����ʹ����ÿ������һ��Ϊ�ˣ�������ʹ�ÿɱ���һ�ꡣ
, ��Ĵҽҩ
�����飺�ù��Ļ���������������á�
1.4 ���� ������ֻ��Ⱥ�ȷ��ȡ10g���ô�ˮϡ����100ml(��Ҫʱ���ɽ���Һ��˫�㶨����ֽ����)����ȡ10ml����Һ(�൱��1g����)��������Һ0.00,1.00,2.00,4.00,6.00,8.00,10.00ml��200mlĥ������ƿ�С���ƿ������10ml����Լ���ҡ�ȡ���1+4�����1+1��ˮ��������ɫ����ʱ��ҺpHΪ1.5��2.0����Ҫʱ��pH 0.5��5.0������ֽ���顣

ͼ1 4��5-���������Ե���������
ע��Se4+���������������������Һ�з�Ӧ����pH 1.5��2.0Ϊ��ѣ�����ʱ��Һ���黯��̫��ʱ�ⶨ���ƫ�ߣ�����
���������ڰ��һ�ɫ�ƹ��²�������������ƿ�м���0.1%2��3-����������Һ��ҡ�ȣ��÷�ˮ�м���6min��ȡ����������ˮ����ȴ����ȡ5.00ml�������ڸ�ƿ�У��������ϣ���ҡ4min����ȫ����Һ���ڷ�Һ©���У����ֲ����ȡˮ�࣬�������������ھ����Թ��ڣ����ϴ��⡣
, ��Ĵҽҩ
�ڷֹ��ȼ��ϣ���365nm�����£���1cm��ɫ���Ի�����Ϊ�αȣ���Ũ��ֱ����ʽ���ⶨ���ع�������Ʒ������������������Ũ�ȼ�Ϊ���е�������(��λΪmg/kg)��
2 ���
2.1 �ⶨ������ѡ�� �������������Ӧ������4��5-���������ԣ��ڻ������е�����������ͼ1��ʾ��������շ���377nm������������ƫ��ȶ����ɡ��ڴδ����շ�365nm������10nm��Χ�ڣ�������ȶ������ϱȶ����ɣ���Ħ������ϵ���ż���ͼ�����������1.5�������1��ʾ��2.2 DAN������ѡ�� ȡ20ml������Һ8�ݣ����췴Ӧ����DAN���������2��ʾ��DAN����1.0mlʱ������ֵ�ӽ������һ����㶨�����Ա���ȡDAN 1.0ml��
��1 ���ֲ����ⶨ�����ļ���ָ�� ����
(nm)
, ��Ĵҽҩ
�ع�����
���ϵ��
Ħ������ϵ��
��
��ͼ����
��g
377
365
0.9984
0.9998
1.1��104
1.8��104
, http://www.100md.com
0.03
0.02
��2 DAN�����������ⶨ��Ӱ�� DAN����ml
����ֵA
0.5
1.0
1.5
2.0
2.5
3.0
4.5
5.0
0.412
, ��Ĵҽҩ
0.474
0.489
0.486
0.483
0.488
0.494
0.504
2.3 ��Ӧʱ���ѡ�� ����10%����Һ���ֱ�ȡ10.0ml 8�ݣ����첻ͬ��Ӧʱ��������ⶨ��Ӱ�졣���3��ʾ����Ӧ6min(�ڷ�ˮԡ�м���)������ֵ�ӽ�����һ����㶨�����Ա���ȡ��Ӧʱ��6min����3 ��Ӧʱ��������ⶨ��Ӱ�� ��Ӧʱ��min
����ֵA
2
, http://www.100md.com
4
6
8
10
0.242
0.295
0.333
0.338
0.337
2.4 ����Լ�������ѡ�� ȡ10.0mo 10%����Һ6�ݣ����벻ͬ������Լ������4��ʾ������Լ�����2.0ml������ֵ�ӽ�����һ����㶨��������Щ��Ʒ�������ʺ������ܽϸߣ����Ա���ѡȡ����Լ�10ml��
2.5 �������ӵĸ��� ���Ƹ��ָ���������Һ���ⶨ�������ⶨ��Ӱ�죬���5��ʾ������Ϊ1%Mg2+,2mg/L Pb2+,10mg/L Fe2+,Cu2+,Cr6+,Zn2+,20mg/L Mn2+,40mg/L Ba2+,Li+,1mol/L NO3��,100mg/L IO3���Ȳ��������IJⶨ��Sn4+Ũ��С��40mg/Lʱ�����Ų�����9%��KI���ڸ������IJⶨ(��ĿǰKIǿ��ʳ�ν���)����4 ����Լ������������ⶨ��Ӱ�� ����Լ�����ml
, ��Ĵҽҩ
����ֵA
0.00
2.00
4.00
6.00
8.00
10.00
0.271
0.319
0.321
0.299
0.304
0.311
, http://www.100md.com
��5 ��ͬ���������ⶨ�ľ��ܶ� ����
����
������
n
x��s(mg/kg)
CV%
n
x��s(mg/kg)
CV%
��
��
��
6
, ��Ĵҽҩ
6
6
2.27��0.14
4.92��0.26
14.73��0.44
6.2
5.3
3.0
5
5
5
2.36��0.23
5.26��0.79
, ��Ĵҽҩ
12.61��0.75
9.7
7.1
5.9
2.6 �ⶨ��Χ��ѡ�� ȡ��ͬ����������Һ���ֱ�ⶨ������ֵ����Ũ��Ϊ�����꣬����ֵΪ��������Ʊ����ߡ������������������0��16��g��Χ�ڣ����Թ�ϵ���ã��ع鷽��ΪC=22.32A-0.09�����ϵ��R=0.9998��ʵ�ʲⶨʱ��1g��Ʒ��������������10��g����ȡ�ⶨ��ΧΪ0��10��g��
2.7 ���ܶ���ȷ������ ȡ�͡��С�������Ũ���������ֱ�ⶨ�������ھ��ܶȺ����侫�ܶȡ����5��ʾ�����ڱ���ϵ��С��6.2%���������ϵ��С��9.7%��ȡ�͡��С�������Ũ���������ֱ����4��g�������ⶨ������ȷ�ȣ��������6������ȷ��(������)97.9%��105.6%����6 ���������ⶨ��ȷ�� ������
, ��Ĵҽҩ
n
��Ʒ��
������g
�ӱ���
��g
������%
ƽ��ֵ
��Χ
��
��
��
4
4
4
, ��Ĵҽҩ
2.36
5.26
12.61
4.00
4.00
4.00
100.5
103.0
99.7
991��102.8
99.0��105.6
97.9��100.7
, http://www.100md.com 2.8 ��ӫ��ֹ��ȷ��ıȽ� ȡ36���������ֱ��ñ�����ӫ��ֹ��ȷ�(���䷨)�ⶨ�������������ⶨ����и߶�����ԣ����ϵ��r=0.9869(P<0.001)���ع鷽��Ϊy=0.93x+0.53(yΪ�ֹ��ȷ��ⶨ�����xΪӫ�ⷨ)����t��������������ⶨ����������������Բ���(P>0.2)��
3 ����
���Ĺ�ȷ������϶࣬���ж������������ֹ��ȷ�Ӧ�ý�Ϊ�ձ飬���˷������������Է��������ûӷ���ǿ�����Խϴ�ļױ���ȡ���Բ�����Ա��һ����Σ���������������ȷ��ı�������[1��6]����Щ����������˹�ȷ��ⶨ���������ȣ���һ�㶼Ҫ�ϸ���Ʒ�Ӧ�¶ȼ�ʱ�䣬�����������ա�
2��3-��������(Ӣ����Ϊ2��3-Diaminonaphthalene,����ʽΪC10H10N2)����Se4+�������Ϸ�Ӧ������4��5-���������ԣ��ڼ�������376nm,���䲨��Ϊ520nm������ӫ�⣬����ӫ��ֹ��ȷ��ⶨ���÷������ȸߣ��Dzⶨ���ľ��䷽���������ڸ�����Ʒ�������IJⶨ7��10�����о�����Se4+�����������Ӧ�����ﱽ�������Ծ����������չ��ף�����EDTA�������ǰ��ڱ��������ӶԷ�Ӧ�ĸ��ţ����Ż�ѡ���˲ⶨ�������Լ���������Ӧʱ�估�ⶨ��Χ��ȷ���˶��������ֹ��ȷ��ⶨ���������������ɹ��Ľ����������ķֹ��ȷ���
, ��Ĵҽҩ
�÷���ͼ����Ϊ0.02��g��Ħ������ϵ��Ϊ1.8��104���Բ�ͬŨ�ȵ����������IJⶨ�����ڱ���С��6.2%���������С��9.7%��ȷ�ȷ�ΧΪ97.9%��105.6%���÷�����ӫ�ⷨ�Ƚϣ��ⶨ����������Բ���(P>0.2)���÷����м�㡢���á�������ȷ���ŵ㣬�ʺ�������(Na2SeO3-KIO3)�����������ij��������(������õ�������ʡ�ط������ΰ칫�һ�����ѧ�����Σ�������ʡ�ط��������о����¾�����������»�������ȵ�֧�֣��ڴ�һ����л!)
�����
[1] �ӱ�.���������Ĵμ�������ѧ-ӫ��ⶨ��[J].����ҽѧ����ѧ�ֲᣬ1987��3��168.
[2] ���Ͽ�ҵѧԺ������ѧ������.��ѧ�����ֲ�[M].��ѧ�����磬1984��495.
, ��Ĵҽҩ
[3] ������,�Ͻ�.������ѧ���ⶨ������[J].������ѧ��1997��25(5)��615.
[4] ���ⶫ��������.Se-KI-CTMAB-Tween-80��ϵ�������ֹ��Ȳⶨ�������о�[J].��Ԫ���뽡���о���1997��14(1)��5.
[5] Ҧ�G.����ȷ��ⶨ��������������ѧѧ��(��Ȼ��ѧ��)[J].1990��26(6)��657.
[6] ��˼��.������ѧ��ȷ��ⶨ������[J].������ѧѧ��(��Ȼ��ѧ��)��1989��13(3)��36-40.
[7] �л�����������.��������ˮ�����鷨[J].�й��������ұ�GB5750-85:58-61.
[8] �����ǣ���������ׯ����.������Ʒ��ˮ�������к�������ӫ��ⶨ��[J].Ӫ��ѧ����1985��7(1)��39.
[9] �¹��䣬�����ǣ�������.ӫ�������[J].��������ѧ�����磬1990��432-433.
[10] �����ģ������ܣ����죬��.ʹ��930��ӫ��Ʋⶨ����[J].�л�Ԥ��ҽѧ��־��1995��29(3)��180-181., ��Ĵҽҩ