标准的和2周一疗程CHOP方案治疗进展型非霍奇金氏淋巴瘤的随机对照研究
作者:林桐榆,管忠震,姜文奇,何友兼,徐光川,刘冬耕,黄慧强,滕小玉,徐瑞华
单位:中山医科大学肿瘤防治中心内科(广州,510060)
关键词:非霍奇金氏淋巴瘤;进展型;CHOP;随机;治疗
癌症990621 【摘要】目的:观察缩短常规CHOP方案的化疗间隙,能否提高进展型NHL的治疗效果。方法:93例初治的进展型NHL被随机分成试验组和对照组,试验组46例患者在G-CSF的支持下使用2周的CHOP方案治疗,对照组47例病人用常规的3周CHOP方案治疗,两方案的化疗药物剂量相同。结果:试验组和对照组的CR率分别为80.4%和66.0%,2年DFS分别为52.17%和40.43%;按IPI属高中度/高度危险性的患者在试验组和对照组的CR率为76.9%和37.5%,2年DFS为38.46%和12.50%;按IPI属中低度/低度危险性者在试验组和对照组的CR率为81.8%和80.6%,2年DFS为57.88%和54.84%;两组患者的毒性反应相似,均可耐受。结论:缩短CHOP方案的化疗间隙,有可能提高按IPI属中高度/高度危险性进展型NHL患者的治疗效果,而中低度/低度危险性病人的治疗效果无明显改善。
, http://www.100md.com
中图分类号:R733.1 文献标识码:A 文章编码:1000-467X(1999)06-0697-05
Randomized clinical trial of standard CHOP regimen and biweekly intensified CHOP regimen in the treatment of aggressive non-Hodgkin's lymphoma
LIN Tong-yu,GUAN Zhong-zhen,JIANG Weng-qi,et al.
Cancer Center,Sun Yat-sen University of Medical Sciences,Guangzhou 510060,P.R.China
【Abstract】 Objective:To determine whether there were differences in the treatment of aggressive non-Hodgkin’s lymphoma (ANHL),with standard CHOP regimen (SCHOP) or biweekly CHOP regimen (BCHOP).Methods:A total of 93 previously untreated ANHL patients were enrolled and randomly assigned to study group (BCHOP group) or control group (SCHOP group).Supporting by G-CSF,BCHOP had same agent dose as SCHOP,but the interval of chemotherapy was shortened from three weeks to two weeks. Results:Thirty-seven of the 46 cases treated with BCHOP (80.4%) and 31 of the 47 cases treated with SCHOP (66.0%) had complete remissions.Two-year DFS of study group was 52.17% and 40.43% in control group.The CR rates of the high/high-intermediate risk group of international prognosis index (IPI) were 76.9% in BCHOP group versus 37.5% in SCHOP group.The CR rates of the low/low-intermediate risk group of IPI between study group and control group were similar (81.8% versus 80.6%).Two-year DFS of the high/high-intermediate risk group of IPI was 46.15% in BCHOP group versus 25.0% in SCHOP group.There was no significant difference of two-year DFS of the cases with low/low-intermediate risk group of IPI between study group and control group (57.88% versus 54.84%).The toxicity in the two groups was similar and tolerated.Conclusions:The CR rate and two-year DFS of the high/high-intermediate risk group of IPI in ANHL may be improved by BCHOP treatment compared with SCHOP treatment.There is no significant difference in CR rates or two years DFS in the low/ low-intermediate risk group of IPI between study group and control group.The toxicity of BCHOP can tolerated throngh the support of G-CSF.
, 百拇医药
Key words:Non-Hodgkin's lymphoma;Aggressive;CHOP;Randomize;Treatment
每3周为一疗程的CHOP方案(环磷酰胺、阿霉素、长春新碱和强的松)已被公认为进展型非霍奇金氏淋巴瘤(Non Hodgkin’s lymphoma NHL)的常规治疗。可是,用常规的CHOP方案治疗进展型NHL,仍有大约60%~70%的病人未能获得治愈。化疗剂量强度是影响NHL疗效的一个关键因素。增加化疗剂量强度,有可能改善其有效率和延长生存期。本研究前瞻性地随机比较常规CHOP方案(3周为一疗程)和缩短间隙的CHOP方案(2周为一疗程)治疗进展型NHL的治疗效果。
1材料和方法
1.1病例入选标准
病例入选标准:初治NHL病例,无放化疗病史;年龄≥16岁;病理组织学和免疫组化确诊的进展型NHL(美国NCI分类,按国际工作分型属弥漫性混合细胞型、弥漫性大细胞型和免疫母细胞型NHL);有可评价的病灶;重要器官功能(心、肺、肝、肾)正常;无中枢神经系统侵犯;病人同意,有随诊条件。
, http://www.100md.com
从1995年1月至1996年10月,本肿瘤中心共有93例患者符合入选标准进入本研究,随机分成试验组和对照组。随诊日期至1999年1月底止。
1.2治疗方法及评价
将符合入选条件的病例随机分为试验组和对照组两组。
CHOP方案的剂量:CTX 750mg/m2 ivd1;ADM50mg/m2 iv d1;VCR1.4mg/m2 ivd 1;Prednison 60mg/m2 po d1-5。
试验组每2周为一疗程,对照组每3周为一疗程;一般用6疗程,至少在完全缓解后加2个疗程;试验组加用粒细胞集落刺激因子(G-CSF)1.5~2μg/(kg.d),SC,d6开始,至中性粒细胞绝对数(ANC)过最低点后≥2×109/L停药,一般用药6~8天;对照组一般不用G-CSF,但如3周后血象仍不能恢复正常,可在第22天开始用G-CSF1.5~2μg/(kg.d),直到血象恢复正常。
, 百拇医药
延长化疗间隙期的指标:下一疗程到期,而ANC<2×109/L或血小板<100×109/L;心、肝、肾等重要器官的功能明显受损;除脱发以外,有Ⅲ级以上的非骨髓毒性。
观察指标:治疗前查血清的LDH水平,按AnArbor分期系统分期,身体活动能力状况用PS(Performance Status ECOG标准)评分评价;每疗程前后对病灶进行评价(包括体检、X线、CT或B超等);每周查血象2~3次;每疗程化疗前查肝肾功能、心电图;治疗前予骨髓穿刺检查,如有异常需每疗程复查;每疗程均用WHO毒性标准评价毒性反应;所有病例均密切随访追踪。
1.3统计方法
统计分析方法用SPSS电脑统计软件包,P值<0.05认为差异有显著性。疗效按实体瘤疗效标准评价,生存期从治疗日起到死亡或末次随诊日,无病生存期从完全缓解日起至复发或末次无复发随诊日止。
, 百拇医药
2结果
2.1一般临床特征
试验组46例患者中,男性39例,女性7例;中数年龄45岁(16~77),平均年龄41.65岁,超过60岁有12例;按Anarbor分期,I~II期27例,III~IV期19例;25例有结外病变,其中有10例超过一个部位;有咽淋巴环侵犯的10例,胃肠侵犯的2例,纵隔侵犯的11例,骨髓侵犯的9例;血清LDH水平超过500u/L的9例;身体状况评分(PS评分)0分13例,1分19例,2分7例,3分6例,4分1例。对照组47例患者中,男性38例,女性9例;中数年龄49岁(16~70岁),平均年龄44.18岁,超过60岁有9例;按Anarbor分期,I~II期25例,III~IV期22例;24例有结外病变,其中有8例超过一个部位;有咽淋巴环侵犯的6例,胃肠侵犯的5例,纵隔侵犯的8例,骨髓侵犯的10例;血清LDH水平超过500u/L的9例;身体状况评分0分15例,1分17例,2分9例,3分5例,4分1例。
, 百拇医药
2.2预后相关因素
NHL的国际预后指征(International prognosisindex IPI)包括年龄(>60岁)、临床分期(Ⅲ~Ⅳ)、血清LDH水平(≥500u/L)、活动能力评分(PS评分≥2)、多处结外器官侵犯(>1)等5个危险因素。按IPI分组,分低度危险组(0-1个因素)、低中度危险组(2个因素)、高中度危险组(3个因素)和高度危险组(4~5个因素)等4个组。按IPI分组,试验组中低度、低中度、高中度和高度危险者分别为18例、15例、7例和6例,高中度+高度危险患者共13例,占28.3%;对照组中低度、低中度、高中度和高度危险者分别为18例、13例、9例和7例,高中度+高度危险者共16例,占34.0%,两组中的高中度/高度危险病例比例在统计学上无明显差异(P=0.547>0.05)。
2.3缓解率
试验组有37例患者取得完全缓解(CR),完全缓解率为80.4%,4例部分缓解(PR),3例稳定(S),2例进展(PD),总有效率(CR+PR)为89.1%,试验组中按IPI分组,33例低度/低中度危险者有27例CR(81.8%),13例高中度/高度危险者有10例CR(76.9%);对照组有31例病例取得CR(66.0%),9例PR,4例S,3例PD,总有效率85.1%,对照组中按IPI分组,31例低度/低中度危险者有25例CR(80.6%),16例高中度/高度危险者有6例CR(37.5%)。试验组的CR率似乎比对照组的高,但统计学上尚无显著性意义(P=0.07>0.05);按IPI属高中度/高度危险者在试验组的CR率与对照组的比较,统计学上有显著性意义(P=0.034<0.05);而属低度/低中度危险者的CR率在两组无明显差异(P=0.904>0.05)。
, 百拇医药
表1 两组病例的毒副反应(疗程)
毒副反应
试验组(分级)
Ⅲ+Ⅳ(%)
对照组(分级)
Ⅲ+Ⅳ(%)
Ⅰ
Ⅱ
Ⅲ
Ⅳ
Ⅰ
Ⅱ
Ⅲ
, 百拇医药
Ⅳ
白细胞下降
61
49
38
7
21.7
74
70
45
6
18.7
贫血
12
, 百拇医药
12
0
18
10
0
血小板下降
3
1
0
5
0
胃肠道反应
101
86
, 百拇医药
10
3.8
87
76
10
3.8
心脏毒性
21
3
0
18
2
0
感染
, 百拇医药
18
12
5
1.9
20
11
4
1.5
肝功能损害
14
6
3
2
1.9
, 百拇医药
12
3
2
0.7
肾膀胱毒性
4
0
3
0
2.4生存情况
所有病例均随访28个月以上,试验组的2年生存率是54.35%,对照组的是51.06%,两者对比无统计学差异(P=0.753>0.05);试验组的2年无病生存率(disease-freesurvival DFS)是52.17%,而对照组的是40.43%,两者比较也无统计学差异(P=0.125>0.05);IPI属高中/高度危险者在试验组和对照组的2年DFS分别是38.46%和12.50%,两者比较有统计学显著性意义(P=0.027<0.05);IPI属低度/低中度危险者在试验组的2年DFS为57.88%,在对照组为54.84%,无显著性差异(P=0.6265>0.05)。各组的生存率情况见图1~4。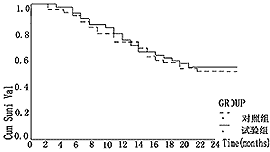
, 百拇医药
图1 试验组和对照组的生存率曲线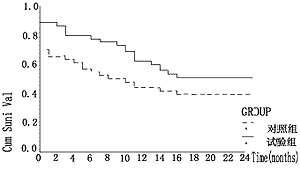
图2 试验组和对照组的无病生存率曲线
图3 两组中IPI属低度/低中度危险性者无病生存率比较
图4 两组中IPI属中高度/高度危险性者无病生存率比较
2.5毒副反应
试验组和对照组分别用了262个疗程和273疗程化疗,毒副反应按WHO标准评价(表1)。在G-CSF支持下,试验组的骨髓毒性反应与对照组的相近,Ⅲ~Ⅳ级白细胞降低在试验组为21.7%,对照组为18.7%,试验组和对照组的感染率分别是13.4%和12.8%,分别比较均无明显差异(P>0.05)。其它贫血、血小板降低、心脏毒性、肾膀胱毒性、胃肠道反应等毒性两组相似,基本能耐受。试验组有5例患者出现Ⅲ~Ⅳ级的肝功能损害,对照组也有两例Ⅲ级肝脏毒性反应,似有高剂量强度增加肝毒性的倾向,但统计学上尚未有显著性差异(P=0.383>0.05)。这部分肝功能损害的病例均为乙型肝炎病毒携带者,经治疗肝功能虽都恢复正常,但化疗间歇期明显延长。两组病例多有手指末端麻痹,无严重的神经毒性。全部病例均有2~3级的脱发。无治疗相关死亡。
, http://www.100md.com
2.6剂量强度
试验组平均每疗程为2.11周;对照组平均每疗程为3.06周。两组中各种药物的剂量强度比较见表2。试验组的平均相对剂量强度为1.42,对照组的为0.98,试验组约为对照组的1.45倍,即试验组与对照组比较,约提高了45%的化疗剂量强度。
表2 两组病例的实际化疗剂量强度比较[mg.(m2.w)-1]
药物
试验组
对照组
标准的CHOP方案
CTX
355.45
, http://www.100md.com
245.10
250
ADR
23.70
16.34
16.67
VCR
0.66
0.46
0.47
Pred
142.18
98.04
, 百拇医药
100
3讨论
70年代,由美国SWOG〔1〕首先报道用CHOP方案治疗弥漫性NHL,完全缓解率达66%,2年生存率为45%。Coltman CA.等〔2〕回顾性研究418例用CHOP方案治疗的弥漫性NHL患者,CR率为53%,30%的病例生存12年以上。中国中山医肿瘤医院用CHOP方案治疗弥漫性NHL,5年生存率也达30%左右〔3〕。近20多年来,许多研究中心在CHOP方案的基础上,将一些对淋巴瘤单药有效而骨髓毒性较低的药物加入在间隙期使用,产生了NHL的第二和第三代方案,报告了一些令人兴奋的结果〔4,5〕。但是,这些结果没有被随后的随机试验所证实〔6〕。在实际应用过程中,这些药物并没有增加原来所用药物的效果,反而增加了一些毒性反应,如BLM的肺毒性,MTX的粘膜炎等。
, 百拇医药 化疗剂量强度是影响NHL疗效的一个关键因素,提高药物剂量或缩短用药间隙,均可提高剂量强度。增加NHL的化疗剂量强度,有可能改善其有效率和延长生存期。本研究探索在G-CSF支持下,将3周为一疗程的常规CHOP方案缩短为2周治疗进展型NHL。结果,试验组的CR率为80.4%,对照组的为66.0%;2年生存率在试验组和对照组分别为54.35%和51.06%;而2年DFS在试验组和对照组分别是52.17%和40.43%。试验组的CR率、2年生存率和DFS均比对照组的高,但统计学上尚无显著性差异,这可能是病例数不够多或受预后因素影响的缘故。
NHL国际预后指征〔7〕是目前公认的对预测进展型NHL的预后有较好价值的指标。本研究结果,按IPI属高危(高中度/高度危险性)的病例在试验组和对照组的CR率分别为76.9%和37.5%,2年DFS分别是38.46%和12.50%,分别比较在统计学上均有显著性差异。提示通过缩短CHOP方案的间歇期,提高其化疗剂量强度,有可能提高按IPI分组属高危的进展型NHL的完全缓解率,近期无病生存率亦可能有所改善。ShippM等〔8〕研究在G-CSF支持下,提高CTX和ADR的剂量,用高剂量CHOP方案治疗22例按IPI分组属高危的进展型NHL,初步的治疗结果显示,CR率达86%,2年无病生存率高达79%。另一研究〔9〕,用高剂量的CHOP方案治疗高危的弥漫性大细胞NHL,也取得了72%的CR率。
, 百拇医药
本研究同时发现,按IPI分组属非高危组(低度/低中度危险性)的病例,在试验组和对照组的CR率分别是81.8%和80.6%,2年无病生存率分别是57.58%和54.84%,无明显差别,说明非高危进展型NHL患者,用常规CHOP方案治疗已可取得较好的疗效,不必忍受高剂量强度化疗所带来的毒性和经济负担。ShippM的研究〔8〕结果也显示,非高危的病例用常规的CHOP方案化疗,CR率达87%,5年生存率达73%。
在G-CSF支持下,试验组的骨髓毒性与对照组的相似,感染率也无明显差异,两组均无治疗相关死亡。证实在G-CSF的支持下,提高化疗剂量强度,使骨髓毒性可耐受是可能的。试验组和对照组分别有5例和2例病例出现3度以上的肝功能损害,均为乙型肝炎病毒携带者,提示此类病例用大剂量化疗应特别密切观察。本研究试验组的毒性反应与对照组的相似,均可耐受,证实在G-CSF支持下,缩短间歇期的高剂量强度CHOP仍为一个较为安全有效的方案。
一些中心正在研究高危的NHL病例初治时即给予较高剂量强度的化疗,或在常规治疗完全缓解后加用超大剂量化疗为巩固治疗,已取得一定的成绩。骨髓或外周血干细胞移植支持下的超大剂量化疗,在敏感复发和难治NHL的研究中已取得一定的进展,但其非骨髓毒性、昂贵的费用和特殊的设备,使其应用和推广受到限制。一些初步的研究结果显示,在G-CSF支持下的高剂量强度化疗,对初治的高危弥漫性NHL,其效果已可与超大剂量化疗的比美。如何进一步提高高危NHL患者的治疗效果,值得共同探索研究。
, 百拇医药
基金项目:广东省科研基金项目(编号:977739)资助
〔参考文献〕
〔1〕Mc Kelvey EM,Gottlieb JA,Wilson HE,et al.Hydroxylda-unomycin (Adrimycin) combination chemotherapy in malignant lymphoma〔J〕.Cancer,1976,38:1484~1493.
〔2〕Coltman CA,Dahlbertg S,Jones SE,et al. CHOP is active in thirty percent of patients with large cell lymphoma:a twelve year Southwest Oncology Group follow-up. In:Skarin AT.ed.Advances in cancer chemotherapy:update on treatment for diffuse large cell lymphoma〔M〕.New York:Park Row,1986:71~77.
, 百拇医药
〔3〕管忠震,喻丽华,何友兼,等.用“CHOP”方案治疗非霍奇金氏淋巴瘤〔J〕.癌症,1989,8(2):98~100.
〔4〕Connors JM,Klimo P.MACOP-B chemotherapy for malignant lymphomas and related conditions:1987 update and additional observations〔J〕.Semin Hematol,1988;25(2 suppl 2):41~46.
〔5〕Fisher RI,Longo DL,De Vita VT Jr,et al.Long-term follow-up of ProMACE-CytaBOM in non-Hodgkin’s lymphomas〔J〕.Ann Oncol,1991;2(suppl 1):33~35.
〔6〕Fisher RI,Gaynor ER,Dahlberg S,et al.Comparison of a standard regimen (CHOP) with three intensive chemotherapy regimens for advanced non-Hodgkin’s lymphoma 〔J〕.N Engl J Med,1993,328:1002~1006.
, 百拇医药
〔7〕A predictive model for aggressive non-Hodgkin’s lymphomas.The International Non-Hodgkin’s Lyrnphoma Prognostic Factor Project 〔J〕.N Engl J Med, 1993,329: 987~994.
〔8〕Shipp MA,Neuberg D,Janicek M,et al:High-dose CHOP as initial therapy for patients with poor-prognosis aggressive non-Hodgkin's lymphoma:a dose-finding pilot study〔J〕.J Clin Oncol,1995;13:2916~2923.
〔9〕Shipp MA,Shulman LN,Kaplan WD,et al.Intensified induction therapy for patients with“ high-risk”aggressive NHL:high dose CHOP〔J〕.Blood,1993;82(1):332.
收稿日期:1999-03-31;修回日期:1999-05-10, 百拇医药
单位:中山医科大学肿瘤防治中心内科(广州,510060)
关键词:非霍奇金氏淋巴瘤;进展型;CHOP;随机;治疗
癌症990621 【摘要】目的:观察缩短常规CHOP方案的化疗间隙,能否提高进展型NHL的治疗效果。方法:93例初治的进展型NHL被随机分成试验组和对照组,试验组46例患者在G-CSF的支持下使用2周的CHOP方案治疗,对照组47例病人用常规的3周CHOP方案治疗,两方案的化疗药物剂量相同。结果:试验组和对照组的CR率分别为80.4%和66.0%,2年DFS分别为52.17%和40.43%;按IPI属高中度/高度危险性的患者在试验组和对照组的CR率为76.9%和37.5%,2年DFS为38.46%和12.50%;按IPI属中低度/低度危险性者在试验组和对照组的CR率为81.8%和80.6%,2年DFS为57.88%和54.84%;两组患者的毒性反应相似,均可耐受。结论:缩短CHOP方案的化疗间隙,有可能提高按IPI属中高度/高度危险性进展型NHL患者的治疗效果,而中低度/低度危险性病人的治疗效果无明显改善。
, http://www.100md.com
中图分类号:R733.1 文献标识码:A 文章编码:1000-467X(1999)06-0697-05
Randomized clinical trial of standard CHOP regimen and biweekly intensified CHOP regimen in the treatment of aggressive non-Hodgkin's lymphoma
LIN Tong-yu,GUAN Zhong-zhen,JIANG Weng-qi,et al.
Cancer Center,Sun Yat-sen University of Medical Sciences,Guangzhou 510060,P.R.China
【Abstract】 Objective:To determine whether there were differences in the treatment of aggressive non-Hodgkin’s lymphoma (ANHL),with standard CHOP regimen (SCHOP) or biweekly CHOP regimen (BCHOP).Methods:A total of 93 previously untreated ANHL patients were enrolled and randomly assigned to study group (BCHOP group) or control group (SCHOP group).Supporting by G-CSF,BCHOP had same agent dose as SCHOP,but the interval of chemotherapy was shortened from three weeks to two weeks. Results:Thirty-seven of the 46 cases treated with BCHOP (80.4%) and 31 of the 47 cases treated with SCHOP (66.0%) had complete remissions.Two-year DFS of study group was 52.17% and 40.43% in control group.The CR rates of the high/high-intermediate risk group of international prognosis index (IPI) were 76.9% in BCHOP group versus 37.5% in SCHOP group.The CR rates of the low/low-intermediate risk group of IPI between study group and control group were similar (81.8% versus 80.6%).Two-year DFS of the high/high-intermediate risk group of IPI was 46.15% in BCHOP group versus 25.0% in SCHOP group.There was no significant difference of two-year DFS of the cases with low/low-intermediate risk group of IPI between study group and control group (57.88% versus 54.84%).The toxicity in the two groups was similar and tolerated.Conclusions:The CR rate and two-year DFS of the high/high-intermediate risk group of IPI in ANHL may be improved by BCHOP treatment compared with SCHOP treatment.There is no significant difference in CR rates or two years DFS in the low/ low-intermediate risk group of IPI between study group and control group.The toxicity of BCHOP can tolerated throngh the support of G-CSF.
, 百拇医药
Key words:Non-Hodgkin's lymphoma;Aggressive;CHOP;Randomize;Treatment
每3周为一疗程的CHOP方案(环磷酰胺、阿霉素、长春新碱和强的松)已被公认为进展型非霍奇金氏淋巴瘤(Non Hodgkin’s lymphoma NHL)的常规治疗。可是,用常规的CHOP方案治疗进展型NHL,仍有大约60%~70%的病人未能获得治愈。化疗剂量强度是影响NHL疗效的一个关键因素。增加化疗剂量强度,有可能改善其有效率和延长生存期。本研究前瞻性地随机比较常规CHOP方案(3周为一疗程)和缩短间隙的CHOP方案(2周为一疗程)治疗进展型NHL的治疗效果。
1材料和方法
1.1病例入选标准
病例入选标准:初治NHL病例,无放化疗病史;年龄≥16岁;病理组织学和免疫组化确诊的进展型NHL(美国NCI分类,按国际工作分型属弥漫性混合细胞型、弥漫性大细胞型和免疫母细胞型NHL);有可评价的病灶;重要器官功能(心、肺、肝、肾)正常;无中枢神经系统侵犯;病人同意,有随诊条件。
, http://www.100md.com
从1995年1月至1996年10月,本肿瘤中心共有93例患者符合入选标准进入本研究,随机分成试验组和对照组。随诊日期至1999年1月底止。
1.2治疗方法及评价
将符合入选条件的病例随机分为试验组和对照组两组。
CHOP方案的剂量:CTX 750mg/m2 ivd1;ADM50mg/m2 iv d1;VCR1.4mg/m2 ivd 1;Prednison 60mg/m2 po d1-5。
试验组每2周为一疗程,对照组每3周为一疗程;一般用6疗程,至少在完全缓解后加2个疗程;试验组加用粒细胞集落刺激因子(G-CSF)1.5~2μg/(kg.d),SC,d6开始,至中性粒细胞绝对数(ANC)过最低点后≥2×109/L停药,一般用药6~8天;对照组一般不用G-CSF,但如3周后血象仍不能恢复正常,可在第22天开始用G-CSF1.5~2μg/(kg.d),直到血象恢复正常。
, 百拇医药
延长化疗间隙期的指标:下一疗程到期,而ANC<2×109/L或血小板<100×109/L;心、肝、肾等重要器官的功能明显受损;除脱发以外,有Ⅲ级以上的非骨髓毒性。
观察指标:治疗前查血清的LDH水平,按AnArbor分期系统分期,身体活动能力状况用PS(Performance Status ECOG标准)评分评价;每疗程前后对病灶进行评价(包括体检、X线、CT或B超等);每周查血象2~3次;每疗程化疗前查肝肾功能、心电图;治疗前予骨髓穿刺检查,如有异常需每疗程复查;每疗程均用WHO毒性标准评价毒性反应;所有病例均密切随访追踪。
1.3统计方法
统计分析方法用SPSS电脑统计软件包,P值<0.05认为差异有显著性。疗效按实体瘤疗效标准评价,生存期从治疗日起到死亡或末次随诊日,无病生存期从完全缓解日起至复发或末次无复发随诊日止。
, 百拇医药
2结果
2.1一般临床特征
试验组46例患者中,男性39例,女性7例;中数年龄45岁(16~77),平均年龄41.65岁,超过60岁有12例;按Anarbor分期,I~II期27例,III~IV期19例;25例有结外病变,其中有10例超过一个部位;有咽淋巴环侵犯的10例,胃肠侵犯的2例,纵隔侵犯的11例,骨髓侵犯的9例;血清LDH水平超过500u/L的9例;身体状况评分(PS评分)0分13例,1分19例,2分7例,3分6例,4分1例。对照组47例患者中,男性38例,女性9例;中数年龄49岁(16~70岁),平均年龄44.18岁,超过60岁有9例;按Anarbor分期,I~II期25例,III~IV期22例;24例有结外病变,其中有8例超过一个部位;有咽淋巴环侵犯的6例,胃肠侵犯的5例,纵隔侵犯的8例,骨髓侵犯的10例;血清LDH水平超过500u/L的9例;身体状况评分0分15例,1分17例,2分9例,3分5例,4分1例。
, 百拇医药
2.2预后相关因素
NHL的国际预后指征(International prognosisindex IPI)包括年龄(>60岁)、临床分期(Ⅲ~Ⅳ)、血清LDH水平(≥500u/L)、活动能力评分(PS评分≥2)、多处结外器官侵犯(>1)等5个危险因素。按IPI分组,分低度危险组(0-1个因素)、低中度危险组(2个因素)、高中度危险组(3个因素)和高度危险组(4~5个因素)等4个组。按IPI分组,试验组中低度、低中度、高中度和高度危险者分别为18例、15例、7例和6例,高中度+高度危险患者共13例,占28.3%;对照组中低度、低中度、高中度和高度危险者分别为18例、13例、9例和7例,高中度+高度危险者共16例,占34.0%,两组中的高中度/高度危险病例比例在统计学上无明显差异(P=0.547>0.05)。
2.3缓解率
试验组有37例患者取得完全缓解(CR),完全缓解率为80.4%,4例部分缓解(PR),3例稳定(S),2例进展(PD),总有效率(CR+PR)为89.1%,试验组中按IPI分组,33例低度/低中度危险者有27例CR(81.8%),13例高中度/高度危险者有10例CR(76.9%);对照组有31例病例取得CR(66.0%),9例PR,4例S,3例PD,总有效率85.1%,对照组中按IPI分组,31例低度/低中度危险者有25例CR(80.6%),16例高中度/高度危险者有6例CR(37.5%)。试验组的CR率似乎比对照组的高,但统计学上尚无显著性意义(P=0.07>0.05);按IPI属高中度/高度危险者在试验组的CR率与对照组的比较,统计学上有显著性意义(P=0.034<0.05);而属低度/低中度危险者的CR率在两组无明显差异(P=0.904>0.05)。
, 百拇医药
表1 两组病例的毒副反应(疗程)
毒副反应
试验组(分级)
Ⅲ+Ⅳ(%)
对照组(分级)
Ⅲ+Ⅳ(%)
Ⅰ
Ⅱ
Ⅲ
Ⅳ
Ⅰ
Ⅱ
Ⅲ
, 百拇医药
Ⅳ
白细胞下降
61
49
38
7
21.7
74
70
45
6
18.7
贫血
12
, 百拇医药
12
0
18
10
0
血小板下降
3
1
0
5
0
胃肠道反应
101
86
, 百拇医药
10
3.8
87
76
10
3.8
心脏毒性
21
3
0
18
2
0
感染
, 百拇医药
18
12
5
1.9
20
11
4
1.5
肝功能损害
14
6
3
2
1.9
, 百拇医药
12
3
2
0.7
肾膀胱毒性
4
0
3
0
2.4生存情况
所有病例均随访28个月以上,试验组的2年生存率是54.35%,对照组的是51.06%,两者对比无统计学差异(P=0.753>0.05);试验组的2年无病生存率(disease-freesurvival DFS)是52.17%,而对照组的是40.43%,两者比较也无统计学差异(P=0.125>0.05);IPI属高中/高度危险者在试验组和对照组的2年DFS分别是38.46%和12.50%,两者比较有统计学显著性意义(P=0.027<0.05);IPI属低度/低中度危险者在试验组的2年DFS为57.88%,在对照组为54.84%,无显著性差异(P=0.6265>0.05)。各组的生存率情况见图1~4。

, 百拇医药
图1 试验组和对照组的生存率曲线

图2 试验组和对照组的无病生存率曲线

图3 两组中IPI属低度/低中度危险性者无病生存率比较

图4 两组中IPI属中高度/高度危险性者无病生存率比较
2.5毒副反应
试验组和对照组分别用了262个疗程和273疗程化疗,毒副反应按WHO标准评价(表1)。在G-CSF支持下,试验组的骨髓毒性反应与对照组的相近,Ⅲ~Ⅳ级白细胞降低在试验组为21.7%,对照组为18.7%,试验组和对照组的感染率分别是13.4%和12.8%,分别比较均无明显差异(P>0.05)。其它贫血、血小板降低、心脏毒性、肾膀胱毒性、胃肠道反应等毒性两组相似,基本能耐受。试验组有5例患者出现Ⅲ~Ⅳ级的肝功能损害,对照组也有两例Ⅲ级肝脏毒性反应,似有高剂量强度增加肝毒性的倾向,但统计学上尚未有显著性差异(P=0.383>0.05)。这部分肝功能损害的病例均为乙型肝炎病毒携带者,经治疗肝功能虽都恢复正常,但化疗间歇期明显延长。两组病例多有手指末端麻痹,无严重的神经毒性。全部病例均有2~3级的脱发。无治疗相关死亡。
, http://www.100md.com
2.6剂量强度
试验组平均每疗程为2.11周;对照组平均每疗程为3.06周。两组中各种药物的剂量强度比较见表2。试验组的平均相对剂量强度为1.42,对照组的为0.98,试验组约为对照组的1.45倍,即试验组与对照组比较,约提高了45%的化疗剂量强度。
表2 两组病例的实际化疗剂量强度比较[mg.(m2.w)-1]
药物
试验组
对照组
标准的CHOP方案
CTX
355.45
, http://www.100md.com
245.10
250
ADR
23.70
16.34
16.67
VCR
0.66
0.46
0.47
Pred
142.18
98.04
, 百拇医药
100
3讨论
70年代,由美国SWOG〔1〕首先报道用CHOP方案治疗弥漫性NHL,完全缓解率达66%,2年生存率为45%。Coltman CA.等〔2〕回顾性研究418例用CHOP方案治疗的弥漫性NHL患者,CR率为53%,30%的病例生存12年以上。中国中山医肿瘤医院用CHOP方案治疗弥漫性NHL,5年生存率也达30%左右〔3〕。近20多年来,许多研究中心在CHOP方案的基础上,将一些对淋巴瘤单药有效而骨髓毒性较低的药物加入在间隙期使用,产生了NHL的第二和第三代方案,报告了一些令人兴奋的结果〔4,5〕。但是,这些结果没有被随后的随机试验所证实〔6〕。在实际应用过程中,这些药物并没有增加原来所用药物的效果,反而增加了一些毒性反应,如BLM的肺毒性,MTX的粘膜炎等。
, 百拇医药 化疗剂量强度是影响NHL疗效的一个关键因素,提高药物剂量或缩短用药间隙,均可提高剂量强度。增加NHL的化疗剂量强度,有可能改善其有效率和延长生存期。本研究探索在G-CSF支持下,将3周为一疗程的常规CHOP方案缩短为2周治疗进展型NHL。结果,试验组的CR率为80.4%,对照组的为66.0%;2年生存率在试验组和对照组分别为54.35%和51.06%;而2年DFS在试验组和对照组分别是52.17%和40.43%。试验组的CR率、2年生存率和DFS均比对照组的高,但统计学上尚无显著性差异,这可能是病例数不够多或受预后因素影响的缘故。
NHL国际预后指征〔7〕是目前公认的对预测进展型NHL的预后有较好价值的指标。本研究结果,按IPI属高危(高中度/高度危险性)的病例在试验组和对照组的CR率分别为76.9%和37.5%,2年DFS分别是38.46%和12.50%,分别比较在统计学上均有显著性差异。提示通过缩短CHOP方案的间歇期,提高其化疗剂量强度,有可能提高按IPI分组属高危的进展型NHL的完全缓解率,近期无病生存率亦可能有所改善。ShippM等〔8〕研究在G-CSF支持下,提高CTX和ADR的剂量,用高剂量CHOP方案治疗22例按IPI分组属高危的进展型NHL,初步的治疗结果显示,CR率达86%,2年无病生存率高达79%。另一研究〔9〕,用高剂量的CHOP方案治疗高危的弥漫性大细胞NHL,也取得了72%的CR率。
, 百拇医药
本研究同时发现,按IPI分组属非高危组(低度/低中度危险性)的病例,在试验组和对照组的CR率分别是81.8%和80.6%,2年无病生存率分别是57.58%和54.84%,无明显差别,说明非高危进展型NHL患者,用常规CHOP方案治疗已可取得较好的疗效,不必忍受高剂量强度化疗所带来的毒性和经济负担。ShippM的研究〔8〕结果也显示,非高危的病例用常规的CHOP方案化疗,CR率达87%,5年生存率达73%。
在G-CSF支持下,试验组的骨髓毒性与对照组的相似,感染率也无明显差异,两组均无治疗相关死亡。证实在G-CSF的支持下,提高化疗剂量强度,使骨髓毒性可耐受是可能的。试验组和对照组分别有5例和2例病例出现3度以上的肝功能损害,均为乙型肝炎病毒携带者,提示此类病例用大剂量化疗应特别密切观察。本研究试验组的毒性反应与对照组的相似,均可耐受,证实在G-CSF支持下,缩短间歇期的高剂量强度CHOP仍为一个较为安全有效的方案。
一些中心正在研究高危的NHL病例初治时即给予较高剂量强度的化疗,或在常规治疗完全缓解后加用超大剂量化疗为巩固治疗,已取得一定的成绩。骨髓或外周血干细胞移植支持下的超大剂量化疗,在敏感复发和难治NHL的研究中已取得一定的进展,但其非骨髓毒性、昂贵的费用和特殊的设备,使其应用和推广受到限制。一些初步的研究结果显示,在G-CSF支持下的高剂量强度化疗,对初治的高危弥漫性NHL,其效果已可与超大剂量化疗的比美。如何进一步提高高危NHL患者的治疗效果,值得共同探索研究。
, 百拇医药
基金项目:广东省科研基金项目(编号:977739)资助
〔参考文献〕
〔1〕Mc Kelvey EM,Gottlieb JA,Wilson HE,et al.Hydroxylda-unomycin (Adrimycin) combination chemotherapy in malignant lymphoma〔J〕.Cancer,1976,38:1484~1493.
〔2〕Coltman CA,Dahlbertg S,Jones SE,et al. CHOP is active in thirty percent of patients with large cell lymphoma:a twelve year Southwest Oncology Group follow-up. In:Skarin AT.ed.Advances in cancer chemotherapy:update on treatment for diffuse large cell lymphoma〔M〕.New York:Park Row,1986:71~77.
, 百拇医药
〔3〕管忠震,喻丽华,何友兼,等.用“CHOP”方案治疗非霍奇金氏淋巴瘤〔J〕.癌症,1989,8(2):98~100.
〔4〕Connors JM,Klimo P.MACOP-B chemotherapy for malignant lymphomas and related conditions:1987 update and additional observations〔J〕.Semin Hematol,1988;25(2 suppl 2):41~46.
〔5〕Fisher RI,Longo DL,De Vita VT Jr,et al.Long-term follow-up of ProMACE-CytaBOM in non-Hodgkin’s lymphomas〔J〕.Ann Oncol,1991;2(suppl 1):33~35.
〔6〕Fisher RI,Gaynor ER,Dahlberg S,et al.Comparison of a standard regimen (CHOP) with three intensive chemotherapy regimens for advanced non-Hodgkin’s lymphoma 〔J〕.N Engl J Med,1993,328:1002~1006.
, 百拇医药
〔7〕A predictive model for aggressive non-Hodgkin’s lymphomas.The International Non-Hodgkin’s Lyrnphoma Prognostic Factor Project 〔J〕.N Engl J Med, 1993,329: 987~994.
〔8〕Shipp MA,Neuberg D,Janicek M,et al:High-dose CHOP as initial therapy for patients with poor-prognosis aggressive non-Hodgkin's lymphoma:a dose-finding pilot study〔J〕.J Clin Oncol,1995;13:2916~2923.
〔9〕Shipp MA,Shulman LN,Kaplan WD,et al.Intensified induction therapy for patients with“ high-risk”aggressive NHL:high dose CHOP〔J〕.Blood,1993;82(1):332.
收稿日期:1999-03-31;修回日期:1999-05-10, 百拇医药