氧自由基及其清除剂在口腔粘膜炎性损害中的作用研究
作者:周红梅 陈谦明 李秉琦 周敏
单位:610041 成都,华西医科大学口腔医学院
关键词:自由基;超氧化物歧化酶;口腔粘膜;炎症;动物,实验
中华口腔医学杂志990603 【摘要】 目的 对氧自由基(oxygen free radicals,OFRs)及其清除剂超氧化物歧化酶(superoxide dismutase,SOD)在口腔粘膜炎性损害中的作用机制进行系统研究。方法 ①建立OFRs致口腔粘膜急性炎症的动物模型,分别采用酶组织化学染色、组合导数分光光度法研究该损害中辅酶II黄递酶等酶活性以及氨基己糖、氨基葡萄糖水平的变化;②分别采用电子顺磁共振、放射免疫技术研究外源性SOD对该损害中OFRs及前列腺素E2含量的影响。结果 ①在动物模型损害中,辅酶II黄递酶等酶活性显著降低,氨基己糖和氨基葡萄糖水平显著升高;②在口腔粘膜局部注射SOD能使炎性损害中的OFRs相对含量以及前列腺素E2水平明显降低。结论 ①OFRs通过攻击上皮细胞内的重要酶类,使结缔组织中蛋白多糖分解,从而造成口腔粘膜组织的炎性损害;②SOD通过清除过量OFRs、减少炎症介质的产生而使炎性损害程度明显减轻。
, 百拇医药
The roles of oxygen free radicals and superoxide dismutase in the inflammatory injury in animal oral mucosa
ZHOU Hongmei , CHEN Qianming ,LI Bingqi ,et al.
School of Stomatology , West China University of Medical Sciences , Chengdu 610041
【Abstract】 Objective To study the roles of oxygen free radicals (OFRs) and superoxide dismutase (SOD) in the inflammatory injury in animal oral mucosa. Methods ① The animal model was established in which an acute oral mucosal inflammation was induced by OFRs. Enzyme histological methods and biochemical methods were used respectively to investigate the activities of some important enzymes such as nicotinamide adenine dinucleotide phosphate-diaphorase and the amount of aminohexoses in the lesions;②Electron spin resonance and radioimmunoassay were ultilize respectively to study the effects of exogenous SOD on the amount of OFRs and prostaglandin E2(PGE2) in the lesions. Results ① The activities of the enzymes in the oral lesions decreased and the amount of aminohexoses increased significantly; ② Local administrating SOD could reduce the amount of OFRs and PGE2 in the lesions sufficiently. Conclusion OFRs induced the inflammatory lesion by injuring some important enzymes and connective tissues in the oral mucosa. Local administrating SOD could scavenge OFRs and PGE2 in the oral mucosa sufficiently and reduce the degree of OFRs――induced oral mucosal inflammatory injury.
, 百拇医药
【Key words】 Free radicals Superoxide dismutase Mouth mucosa Inflammation Animals,laboratory
目前认为,氧自由基(oxygen free radicals,OFRs)损伤是口腔粘膜炎性疾病(如白塞综合征、复发性阿弗它溃疡等)的重要致病环节[1,2],用OFRs的天然清除剂――超氧化物歧化酶(superoxide dismutase,SOD)治疗该类疾病,效果令人满意[3]。但有关OFRs及SOD在口腔粘膜炎性损害中的作用机制尚缺乏系统研究。鉴于此,我们以甲基紫精(para -quat,PQ)诱导的金黄地鼠口腔粘膜急性炎症模型为研究对象,探讨OFRs导致以及SOD防治该模型损害的作用机制,以期为进一步阐明口腔粘膜炎性疾病的发病机制、为治疗提供新途径奠定基础。
材料和方法
, 百拇医药
一、OFRs作用机制研究
1. 实验动物:叙利亚金黄地鼠,6~8周龄,体重80~110 g。
2.建立动物模型:在靠近地鼠颊囊底部进针,准确注入0.25 ml、 5 mmol/L PQ溶液于粘膜下层。
3. 动物分组:将24只地鼠随机分成3组(8只/组)。模型组按上述方法处理动物,空白组用磷酸盐缓冲液( phosphate buffered saline ,PBS)代替PQ液处理动物,正常组不施予干预因素。
4.染色方法:于3h每组各处死3只动物,取颊囊典型病变组织行酶组织化学染色。
5.组合导数分光光度法测试:于12 h处死各组余下动物,制取颊囊干重组织,测定氨基己糖、氨基葡萄糖含量。
, 百拇医药
二、SOD作用机制研究
1.动物分组:将33只地鼠随机分成3组(11只/组)。SOD组于造模前后1.5h在颊囊粘膜下注入0.1 ml、 2.5% SOD溶液各1次,PBS组用PBS代替SOD液处理动物,正常组不施予干预因素。
2.电子自旋共振 (electron spin resonance ,ESR) 测试:于最后1次用药后8h每组各处死5只动物,立即在冷冻条件下对各颊囊标本行ESR测试。
3.放射免疫测试:于最后1次用药后6天处死各组余下动物,制取颊囊组织上清液,测定前列腺素E2(prostaglandin E2,PGE2)含量。
结果
一、OFRs作用机制研究
, 百拇医药
1.酶组织化学染色:在动物模型损害的早期(3h),上皮辅酶I黄递酶、辅酶II黄递酶及血管腺苷酸磷酸酶的活性均下降,其中以辅酶II黄递酶的下降幅度为最大,固有层酸性磷酸酶的活性升高。
2.组合导数分光光度法测试结果:见表1。
表1 氨基己糖和氨基葡萄糖含量对数转换值(mg/g干重,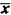 ±s) 组别
±s) 组别
例数
氨基己糖
氨基葡萄糖
模型
5
0.995 2±0.081 6*
, 百拇医药
0.891 4±0.105 7*
空白
5
0.909 9±0.061 5
0.705 2±0.092 9
正常
5
0.769 9±0.029 8
0.596 0±0.101 5
*模型组与空白组、正常组相比,差异有显著性(P<0.05)
, 百拇医药
二、SOD作用机制研究
1. ESR测试:在SOD组和PBS组的ESR波谱图中均出现OFRs的特征信号,其主要成分为超氧自由基( )。SOD组和PBS组的OFRs相对含量分别为0.242 1±0.032 9、1.087 7± 0.020 8,前者比后者低77.74%,差异有显著性 (P< 0.05)。
)。SOD组和PBS组的OFRs相对含量分别为0.242 1±0.032 9、1.087 7± 0.020 8,前者比后者低77.74%,差异有显著性 (P< 0.05)。
2.放射免疫测试: SOD、PBS及正常组的PGE2含量分别为(24.54±5.89)ng/g、(99.21±20.39)ng/g、(23.15±4.30)ng/g,SOD及正常组均低于PBS组,差异有显著性( P<0.05)。讨论
一、OFRs致口腔粘膜炎性损害的作用机制
有研究表明:在辅酶II黄递酶和氧分子存在的情况下,PQ可通过循环的氧化还原反应在生物体内产生大量 [4]。经ESR证实,在本实验动物模型损害中确实有大量主要成分为
[4]。经ESR证实,在本实验动物模型损害中确实有大量主要成分为 的OFRs产生;而酶组化研究则显示,在损害早期辅酶II黄递酶的活性即明显降低,且降低幅度最大。由此推测:本实验注入地鼠颊囊粘膜下的PQ亦是通过同一途径产生大量OFRs。
的OFRs产生;而酶组化研究则显示,在损害早期辅酶II黄递酶的活性即明显降低,且降低幅度最大。由此推测:本实验注入地鼠颊囊粘膜下的PQ亦是通过同一途径产生大量OFRs。
, 百拇医药
在短时间内产生的过量OFRs不易扩散和转移,在局部引发一系列自由基连锁反应。一方面,直接对参与电子转运的酶如本实验的辅酶I黄递酶、腺苷酸磷酸酶等进行攻击,使其活性下降,细胞的正常呼吸出现障碍,最终导致细胞结构破坏、组织损伤。另一方面,过量底物(OFRs)还可使组织中相应的酶(SOD)钝化或耗竭。SOD的活性下降,必然导致组织清除OFRs的能力下降,从而出现恶性循环,加重组织损伤。第三,伴随OFRs的产生,血管腺苷酸磷酸酶等膜相结构酶活性也下降,而溶酶体酶如酸性磷酸酶活跃,这在加重组织损伤中也起到了重要作用。
在金黄地鼠颊囊粘膜固有层基质中含有大量蛋白多糖,它由氨基半乳糖和氨基葡萄糖与糖醛酸连接成多糖链后再与蛋白质呈共价结合所形成。本实验动物模型中氨基己糖、氨基葡萄糖均升高,说明OFRs可能使结缔组织基质中含氨基葡萄糖的蛋白多糖发生分解,从而使结缔组织崩解、破坏。
二、SOD防治口腔粘膜炎性损害的作用机制
, 百拇医药
OFRs可通过攻击上皮细胞内一些重要酶类以及使结缔组织中蛋白多糖分解而造成组织的损伤,由此诱发并加重充血、渗出等炎症反应。本实验SOD组动物口腔粘膜的炎性损害程度明显减轻[5],同时,ESR证实了该组OFRs的相对含量显著减少,这说明对过量OFRs的有效清除是SOD防治口腔粘膜炎性损害的最基本的作用机制。外源性SOD进入机体后,部分进入细胞内,其余则停留于细胞外,二者协同清除细胞内、外过量的OFRs[6],从而减少了诱发和加重炎症的因素,使炎症减轻。
PGE2是高活性的炎症介质,具有使血管扩张、通透性增高等作用,其含量与炎症程度呈平行关系[7]。有关SOD拮抗PGE2产生、释放的机制作者试作如下推测:①SOD清除了大量致炎因子(OFRs),使细胞膜上磷酯酶A2不易被激活,减少了PGE2前体物质花生四烯酸的释出[7];②SOD可能清除了环加氧酶发挥正常作用所需的脂类过氧化物,从而使PGE2合成减少。可见,减少炎症介质的产生可能是SOD防治口腔粘膜炎性损害的又一重要机制。
, http://www.100md.com
通过系列实验,较全面、深入地探讨了OFRs及SOD在口腔粘膜炎性损害中的作用机制,为今后进一步阐明OFRs在口腔粘膜炎性疾病中的确切作用及应用SOD治疗该类疾病提供了较可靠的实验依据。
国家教委博士点基金资助课题(C19005)
参考文献
1 Orem A, Efe H, Deger O,et al. Relationship between lipid peroxidation and disease activity in patients with Behcet's disease. J Dermatol Sci ,1997,16:11-16.
2 Wray D, Charon J.Polymorphonuclear neutrophil function in recurrent aphthous stomatitis. J Oral Pathol Med, 1991, 20:392-394.
, 百拇医药
3 Mizushima Y, Hoshi K, Yanagawe A, et al. Topical application of superoxide dismutase cream. Drugs Exp Clin Res, 1991,17:127-131.
4 Ogata T, Manabe S. Correlation between lipid peroxidation and morphological manifestation of paraquat-induced lung injure in rats. Arch Toxicol, 1990,64:7-13.
5 周红梅,陈谦明,李秉琦,等.超氧化物歧化酶防治口腔粘膜炎性损害的动物实验研究(I).华西口腔医学杂志,1996,14:137-139.
6 Hirota M, Inoue M, Ando Y, et al. Inhibition of stress-induced gastric mucosal injury by a long acting superoxide dismutase that circulates bound to albumin. Arch Biochem Biophys, 1990,280:269-273.
7 毕涉,高骥援.炎症与抗炎症药.第1版.北京:人民卫生出版社,1993.1-20,57-59.
(收稿:1998-12-01 修回:1999-08-01), http://www.100md.com
单位:610041 成都,华西医科大学口腔医学院
关键词:自由基;超氧化物歧化酶;口腔粘膜;炎症;动物,实验
中华口腔医学杂志990603 【摘要】 目的 对氧自由基(oxygen free radicals,OFRs)及其清除剂超氧化物歧化酶(superoxide dismutase,SOD)在口腔粘膜炎性损害中的作用机制进行系统研究。方法 ①建立OFRs致口腔粘膜急性炎症的动物模型,分别采用酶组织化学染色、组合导数分光光度法研究该损害中辅酶II黄递酶等酶活性以及氨基己糖、氨基葡萄糖水平的变化;②分别采用电子顺磁共振、放射免疫技术研究外源性SOD对该损害中OFRs及前列腺素E2含量的影响。结果 ①在动物模型损害中,辅酶II黄递酶等酶活性显著降低,氨基己糖和氨基葡萄糖水平显著升高;②在口腔粘膜局部注射SOD能使炎性损害中的OFRs相对含量以及前列腺素E2水平明显降低。结论 ①OFRs通过攻击上皮细胞内的重要酶类,使结缔组织中蛋白多糖分解,从而造成口腔粘膜组织的炎性损害;②SOD通过清除过量OFRs、减少炎症介质的产生而使炎性损害程度明显减轻。
, 百拇医药
The roles of oxygen free radicals and superoxide dismutase in the inflammatory injury in animal oral mucosa
ZHOU Hongmei , CHEN Qianming ,LI Bingqi ,et al.
School of Stomatology , West China University of Medical Sciences , Chengdu 610041
【Abstract】 Objective To study the roles of oxygen free radicals (OFRs) and superoxide dismutase (SOD) in the inflammatory injury in animal oral mucosa. Methods ① The animal model was established in which an acute oral mucosal inflammation was induced by OFRs. Enzyme histological methods and biochemical methods were used respectively to investigate the activities of some important enzymes such as nicotinamide adenine dinucleotide phosphate-diaphorase and the amount of aminohexoses in the lesions;②Electron spin resonance and radioimmunoassay were ultilize respectively to study the effects of exogenous SOD on the amount of OFRs and prostaglandin E2(PGE2) in the lesions. Results ① The activities of the enzymes in the oral lesions decreased and the amount of aminohexoses increased significantly; ② Local administrating SOD could reduce the amount of OFRs and PGE2 in the lesions sufficiently. Conclusion OFRs induced the inflammatory lesion by injuring some important enzymes and connective tissues in the oral mucosa. Local administrating SOD could scavenge OFRs and PGE2 in the oral mucosa sufficiently and reduce the degree of OFRs――induced oral mucosal inflammatory injury.
, 百拇医药
【Key words】 Free radicals Superoxide dismutase Mouth mucosa Inflammation Animals,laboratory
目前认为,氧自由基(oxygen free radicals,OFRs)损伤是口腔粘膜炎性疾病(如白塞综合征、复发性阿弗它溃疡等)的重要致病环节[1,2],用OFRs的天然清除剂――超氧化物歧化酶(superoxide dismutase,SOD)治疗该类疾病,效果令人满意[3]。但有关OFRs及SOD在口腔粘膜炎性损害中的作用机制尚缺乏系统研究。鉴于此,我们以甲基紫精(para -quat,PQ)诱导的金黄地鼠口腔粘膜急性炎症模型为研究对象,探讨OFRs导致以及SOD防治该模型损害的作用机制,以期为进一步阐明口腔粘膜炎性疾病的发病机制、为治疗提供新途径奠定基础。
材料和方法
, 百拇医药
一、OFRs作用机制研究
1. 实验动物:叙利亚金黄地鼠,6~8周龄,体重80~110 g。
2.建立动物模型:在靠近地鼠颊囊底部进针,准确注入0.25 ml、 5 mmol/L PQ溶液于粘膜下层。
3. 动物分组:将24只地鼠随机分成3组(8只/组)。模型组按上述方法处理动物,空白组用磷酸盐缓冲液( phosphate buffered saline ,PBS)代替PQ液处理动物,正常组不施予干预因素。
4.染色方法:于3h每组各处死3只动物,取颊囊典型病变组织行酶组织化学染色。
5.组合导数分光光度法测试:于12 h处死各组余下动物,制取颊囊干重组织,测定氨基己糖、氨基葡萄糖含量。
, 百拇医药
二、SOD作用机制研究
1.动物分组:将33只地鼠随机分成3组(11只/组)。SOD组于造模前后1.5h在颊囊粘膜下注入0.1 ml、 2.5% SOD溶液各1次,PBS组用PBS代替SOD液处理动物,正常组不施予干预因素。
2.电子自旋共振 (electron spin resonance ,ESR) 测试:于最后1次用药后8h每组各处死5只动物,立即在冷冻条件下对各颊囊标本行ESR测试。
3.放射免疫测试:于最后1次用药后6天处死各组余下动物,制取颊囊组织上清液,测定前列腺素E2(prostaglandin E2,PGE2)含量。
结果
一、OFRs作用机制研究
, 百拇医药
1.酶组织化学染色:在动物模型损害的早期(3h),上皮辅酶I黄递酶、辅酶II黄递酶及血管腺苷酸磷酸酶的活性均下降,其中以辅酶II黄递酶的下降幅度为最大,固有层酸性磷酸酶的活性升高。
2.组合导数分光光度法测试结果:见表1。
表1 氨基己糖和氨基葡萄糖含量对数转换值(mg/g干重,
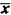 ±s) 组别
±s) 组别例数
氨基己糖
氨基葡萄糖
模型
5
0.995 2±0.081 6*
, 百拇医药
0.891 4±0.105 7*
空白
5
0.909 9±0.061 5
0.705 2±0.092 9
正常
5
0.769 9±0.029 8
0.596 0±0.101 5
*模型组与空白组、正常组相比,差异有显著性(P<0.05)
, 百拇医药
二、SOD作用机制研究
1. ESR测试:在SOD组和PBS组的ESR波谱图中均出现OFRs的特征信号,其主要成分为超氧自由基(
 )。SOD组和PBS组的OFRs相对含量分别为0.242 1±0.032 9、1.087 7± 0.020 8,前者比后者低77.74%,差异有显著性 (P< 0.05)。
)。SOD组和PBS组的OFRs相对含量分别为0.242 1±0.032 9、1.087 7± 0.020 8,前者比后者低77.74%,差异有显著性 (P< 0.05)。2.放射免疫测试: SOD、PBS及正常组的PGE2含量分别为(24.54±5.89)ng/g、(99.21±20.39)ng/g、(23.15±4.30)ng/g,SOD及正常组均低于PBS组,差异有显著性( P<0.05)。讨论
一、OFRs致口腔粘膜炎性损害的作用机制
有研究表明:在辅酶II黄递酶和氧分子存在的情况下,PQ可通过循环的氧化还原反应在生物体内产生大量
 [4]。经ESR证实,在本实验动物模型损害中确实有大量主要成分为
[4]。经ESR证实,在本实验动物模型损害中确实有大量主要成分为 的OFRs产生;而酶组化研究则显示,在损害早期辅酶II黄递酶的活性即明显降低,且降低幅度最大。由此推测:本实验注入地鼠颊囊粘膜下的PQ亦是通过同一途径产生大量OFRs。
的OFRs产生;而酶组化研究则显示,在损害早期辅酶II黄递酶的活性即明显降低,且降低幅度最大。由此推测:本实验注入地鼠颊囊粘膜下的PQ亦是通过同一途径产生大量OFRs。, 百拇医药
在短时间内产生的过量OFRs不易扩散和转移,在局部引发一系列自由基连锁反应。一方面,直接对参与电子转运的酶如本实验的辅酶I黄递酶、腺苷酸磷酸酶等进行攻击,使其活性下降,细胞的正常呼吸出现障碍,最终导致细胞结构破坏、组织损伤。另一方面,过量底物(OFRs)还可使组织中相应的酶(SOD)钝化或耗竭。SOD的活性下降,必然导致组织清除OFRs的能力下降,从而出现恶性循环,加重组织损伤。第三,伴随OFRs的产生,血管腺苷酸磷酸酶等膜相结构酶活性也下降,而溶酶体酶如酸性磷酸酶活跃,这在加重组织损伤中也起到了重要作用。
在金黄地鼠颊囊粘膜固有层基质中含有大量蛋白多糖,它由氨基半乳糖和氨基葡萄糖与糖醛酸连接成多糖链后再与蛋白质呈共价结合所形成。本实验动物模型中氨基己糖、氨基葡萄糖均升高,说明OFRs可能使结缔组织基质中含氨基葡萄糖的蛋白多糖发生分解,从而使结缔组织崩解、破坏。
二、SOD防治口腔粘膜炎性损害的作用机制
, 百拇医药
OFRs可通过攻击上皮细胞内一些重要酶类以及使结缔组织中蛋白多糖分解而造成组织的损伤,由此诱发并加重充血、渗出等炎症反应。本实验SOD组动物口腔粘膜的炎性损害程度明显减轻[5],同时,ESR证实了该组OFRs的相对含量显著减少,这说明对过量OFRs的有效清除是SOD防治口腔粘膜炎性损害的最基本的作用机制。外源性SOD进入机体后,部分进入细胞内,其余则停留于细胞外,二者协同清除细胞内、外过量的OFRs[6],从而减少了诱发和加重炎症的因素,使炎症减轻。
PGE2是高活性的炎症介质,具有使血管扩张、通透性增高等作用,其含量与炎症程度呈平行关系[7]。有关SOD拮抗PGE2产生、释放的机制作者试作如下推测:①SOD清除了大量致炎因子(OFRs),使细胞膜上磷酯酶A2不易被激活,减少了PGE2前体物质花生四烯酸的释出[7];②SOD可能清除了环加氧酶发挥正常作用所需的脂类过氧化物,从而使PGE2合成减少。可见,减少炎症介质的产生可能是SOD防治口腔粘膜炎性损害的又一重要机制。
, http://www.100md.com
通过系列实验,较全面、深入地探讨了OFRs及SOD在口腔粘膜炎性损害中的作用机制,为今后进一步阐明OFRs在口腔粘膜炎性疾病中的确切作用及应用SOD治疗该类疾病提供了较可靠的实验依据。
国家教委博士点基金资助课题(C19005)
参考文献
1 Orem A, Efe H, Deger O,et al. Relationship between lipid peroxidation and disease activity in patients with Behcet's disease. J Dermatol Sci ,1997,16:11-16.
2 Wray D, Charon J.Polymorphonuclear neutrophil function in recurrent aphthous stomatitis. J Oral Pathol Med, 1991, 20:392-394.
, 百拇医药
3 Mizushima Y, Hoshi K, Yanagawe A, et al. Topical application of superoxide dismutase cream. Drugs Exp Clin Res, 1991,17:127-131.
4 Ogata T, Manabe S. Correlation between lipid peroxidation and morphological manifestation of paraquat-induced lung injure in rats. Arch Toxicol, 1990,64:7-13.
5 周红梅,陈谦明,李秉琦,等.超氧化物歧化酶防治口腔粘膜炎性损害的动物实验研究(I).华西口腔医学杂志,1996,14:137-139.
6 Hirota M, Inoue M, Ando Y, et al. Inhibition of stress-induced gastric mucosal injury by a long acting superoxide dismutase that circulates bound to albumin. Arch Biochem Biophys, 1990,280:269-273.
7 毕涉,高骥援.炎症与抗炎症药.第1版.北京:人民卫生出版社,1993.1-20,57-59.
(收稿:1998-12-01 修回:1999-08-01), http://www.100md.com