环孢霉素A肾毒性
作者:陈惠萍 刘红
单位:南京军区南京总医院 解放军肾脏病研究所 (南京,210002)
关键词:肾移植;环孢霉素A;肾毒性
肾脏病与透析肾移植杂志990623 1 病例报告
1.1 【病例1】 男性患者,30岁,因肾移植术后1个月,肾功能延迟恢复,于1999-02-23入院。缘于1990年2月无诱因出现双下肢浮肿,尿检蛋白3+,隐血+,未予正规治疗,1996年4月发现血压升高达20/12 kPa(150/90 mmHg),复查血清肌酐(SCr)176 μmol/L。在我院行肾活检确诊为IgA肾炎(组织学类型符合局灶性节段性肾小球硬化),给予降压、纠正酸中毒、保肾等综合治疗。1998年9月疲劳后头昏、恶心加重伴呕吐,尿量减少,SCr升至800 μmol/L以上,诊断为慢性肾功能不全,尿毒症期,行血液透析治疗。于1999年1月22日在连续硬膜外麻醉下行同种异体肾移植术。术后予环孢霉素A(CsA)8 mg/kg,强的松80 mg/d(1个月内减量至20 mg/d)及双倍剂量雷公藤多甙三联免疫抑制治疗。患者病情稳定,无发热,血压波动在16~18.7/8~10.7 kPa(120~140/60~80mmHg),尿量维持在2500~3000 ml/24h,移植肾区无疼痛。但SCr始终波动在216 μmol/L左右,1999-02-25在B超引导下行抽吸式经皮移植肾活检术。
, http://www.100md.com
过去史,个人史,家庭史无特殊。
体格检查:体温36.6℃,脉搏78次/min,呼吸18次/min,血压17.3/10.7 kPa(130/80 mmHg)。重度贫血貌,无颜面浮肿,全身皮肤粘膜无黄染及出血点,未触及浅表淋巴结,双手轻度颤抖。双肺呼吸音清晰,未闻及干湿性 音,心率78次/min,律齐,各瓣膜听诊区未闻及病理性杂音。腹软,肝脾肋下未及,右下腹一长约12cm的弧形手术瘢痕,愈合良好。移植肾区无肿胀,无压痛,腹水征阴性,双下肢无浮肿,病理反射未引出。
音,心率78次/min,律齐,各瓣膜听诊区未闻及病理性杂音。腹软,肝脾肋下未及,右下腹一长约12cm的弧形手术瘢痕,愈合良好。移植肾区无肿胀,无压痛,腹水征阴性,双下肢无浮肿,病理反射未引出。
1.1.1 实验室检查
尿检:尿蛋白阴性,尿沉渣阴性,尿免疫化学检查阴性。
血清学检查:Hb 65 g/L,WBC 7.4×109/L,N 0.55,L 0.43,A/G 36.6/18.5 g/L,谷丙酶32 U/L,谷草酶16 U/L,碱性磷酸酶55 U/L,BUN 21.1 mmol/L,SCr 214 μmol/L,Ua 665 μmol/L,CH/TG 5.4/1.3 mmol/L,电解质正常。外周血CD4+细胞1.409×109/L,CD8+细胞0.745×109/L,血CsA谷值浓度617.19 μg/L(正常值<400 μg/L)
, 百拇医药
移植肾B超:105mm×49mm×48mm,彩色多谱勒超声:肾血流阻力指数增高。
1.1.2 肾活检结果
光镜:镜下1条皮质,1条皮髓交界组织,26个肾小球。肾小球体积偏大,细胞数90±/球,为肾之固有细胞,偶见节段周边袢系膜区增宽,内有2~3个系膜细胞,袢开放欠好,皱缩状,囊壁节段轻度增厚。PASM-Masson染色未见异常。肾小管无“小管炎”,灶性近端小管等立方空泡(插页图1)及细小空泡变性,间质水肿,管周毛细血管较多红细胞(插页图2)。血管未见明确异常。

图1.急性环孢霉素中毒。近端肾小管上皮细胞等立方的空泡变性(Masson三色,×400)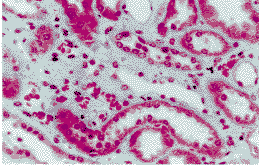
, 百拇医药
图2.急性环孢霉素中毒。管周毛细血管较多红细胞(Masson三色,×200)
电镜:电镜下未见肾小球。肾小管变化不一致,一些近曲小管上皮细胞胞浆内见大量巨大线粒体,其邻近小管则未见此改变。线粒体呈椭圆形或雪茄形,膜完整,嵴模糊。小管腔中亦见崩落的线粒体及微绒毛,小管基膜完整。管周毛细血管内大量细胞成分(红细胞、淋巴细胞、浆细胞)。
免疫荧光检查:IgM+,局灶节段分布于系膜区与血管袢。
肾组织细胞学:间质CD4+细胞16个/mm2,CD8+细胞24个/mm2,RT值0.67,IL-2R 4个/mm2,HLA-DR表达正常。
根据组织学改变特点:①肾小球轻度缺血状;②肾小管等立方及细小空泡变性;③管周毛细血管聚集。电镜巨大线粒体等改变。结合临床提示CsA肾毒性可能。
, 百拇医药
肾活检后将CsA逐渐减量,术后2个月CsA减至5.4 mg/kg,SCr降至137~147 μmol/L,复查血CsA谷值浓度为488.95 μg/L。
1.2 【病例2】 男性患者,50岁,肾移植术后10个月,于1999年12月入院行常规肾活检。缘于1996年4月体检时发现血压升高达21.3/12.7 kPa(160/95mmHg),尿检异常,蛋白2+,隐血+,未予治疗。1998年11月因恶心,纳差,口中有尿味,双肾B超示双肾萎缩(具体大小不详),结构不清,SCr升高达1000 μmol/L,诊断为慢性肾衰尿毒症期,予血液透析治疗。1999-02-09在连续硬膜外麻醉下行同种异体肾移植术,术中顺利。术后予CsA 8 mg/kg,强的松80 mg/d(1月内减至20 mg/d),霉酚酸酯(MMF)2.0 g/d及单倍剂量雷公藤多甙联合治疗。术后11天SCr降至正常,无发热,血压持续波动在14~16/10~10.7 kPa(105~120/75~80 mmHg),尿量维持在2400~3700 ml/24h,移植肾区无疼痛。肾移植术后10个月在B超引导下常规行抽吸式经皮移植肾活检术。
, http://www.100md.com
体格检查:体温36.8℃,脉搏80次/min,呼吸18次/min,血压16.6/10.7 kPa(125/80 mmHg)。轻度贫血貌,无颜面浮肿,全身皮肤粘膜无黄染及出血点,未触及浅表淋巴结。双肺呼吸音清晰,未闻及干湿性 音,心率80次/min,律齐,各瓣膜听诊区未闻及病理性杂音。腹软,肝脾肋下未及,右下腹一14cm弧形手术瘢痕,Ⅰ期愈合。移植肾区无肿胀,无压痛,腹水征阴性。双下肢无浮肿,病理反射未引出。
音,心率80次/min,律齐,各瓣膜听诊区未闻及病理性杂音。腹软,肝脾肋下未及,右下腹一14cm弧形手术瘢痕,Ⅰ期愈合。移植肾区无肿胀,无压痛,腹水征阴性。双下肢无浮肿,病理反射未引出。
过去史、个人史、家庭史无特殊。
1.2.1 实验室检查
尿检:尿蛋白阴性,尿沉渣阴性,尿免疫化学检查阴性。
血清学检查:Hb 104 g/L,WBC 11.3×109/L,N 0.74,L 0.14,A/G 39.3/19.4 g/L,谷丙酶13U/L,谷草酶17U/L,碱性磷酸酶62 U/L,BUN 9.9 mmol/L,SCr 121 μmol/L,Ua 288 μmol/L,CH/TG 4.6/1.69 mmol/L,电解质正常。外周血CD4+细胞1.169×109/L,CD8+细胞0.244×109/L。血CsA谷值浓度713.46 μg/L。(正常<400 μg/L)。
, http://www.100md.com
移植肾B超:103mm×58mm×54mm,彩色多谱勒超声:血流正常。
1.2.2 肾活检结果
光镜:镜下一小条皮质组织,11个肾小球,5条间质血管,无皮髓交界组织。肾小球细胞数100±/球,为肾之固有细胞,周边袢节段系膜区增宽,可见2~3个系膜细胞,袢开放尚好,包囊壁轻度增厚。PASM-Masson染色阴性。小管-间质病变轻度,无“小管炎”,小管上皮细胞亦未见空泡变性,间质血管入球小动脉透明变性(插页图3)。温习本例供肾切片,血管无透明变性(供肾者年龄22岁,男性)。
图3.急性环孢霉素中毒。人球小动脉壁上见透明沉积物(HE,×400)
免疫荧光检查:阴性。
, 百拇医药
肾组织细胞学:间质CD4+细胞204个/mm2,CD8+细胞144个/mm2,RT值1.42,IL-2R 28个/mm2,HLA-DR 皮质肾小管32%表达,其中阳性18%,弱阳性14%。
肾活检后将CsA逐渐减量,术后3个月CsA减至5.5 mg/kg,复查血CsA谷值浓度362.6 μg/L,SCr一直维持在正常范围。
2 讨论
环孢霉素是由一种不完全真菌属-Tolypocladium inflatum Gams在生长过程中产生的多肽混合物。将这种多肽混合物进一步纯化,即可分离出免疫抑制作用最强的一种肽―环孢霉素A(cyclosporin A,CsA),CsA的分子结构为环形十一肽,分子量1202。1978年CsA开始用于肾移植及骨髓移植临床,使移植患者的预后有了极大改观,移植肾一年成活率增加了10%~20%,尤其是高龄及高危患者受益尤其明显。
, http://www.100md.com
然而CsA也存在许多副作用,诸如毛发增生、震颤、高尿酸、高钾血症等,其肾毒性作用已成为CsA治疗中最重要的并发症。
2.1 CsA肾毒性的分类 目前常用的CsA肾毒性分类,为Thiel和Mihatsch根据发病机制所制定的一种新的分类方法(附图)。一般认为CsA的肾毒性与剂量相关,但部分患者的个体敏感性极高,或存在一些危险因素,因此即使剂量很低时,同样可出现CsA的肾毒性作用。
有作者将CsA的肾毒性分为三类,它们分别是急性CsA肾毒性,慢性CsA肾毒性和CsA相关的微血管病(表1)。我们觉得将CsA引起的肾脏病变分为肾小球病变、小管-间质性病变及微血管病变较为合适。

附图 CsA肾毒性分类
, 百拇医药
表1 CsA肾毒性的分类 急性CsA肾毒性
肾小管上皮细胞等立方的空泡
巨大线粒体
肾小管上皮细胞微钙化
肾小管周毛细血管充血
慢性CsA肾毒性
CsA所致的小动脉病变 结节状蛋白沉积
溶血尿毒综合征(HUS)/血栓性血
小板减少性紫癜(TTP)样改变
局灶间质纤维化(条纹状分布)
CsA相关的微血管病
, http://www.100md.com
HUS/TTP样改变
FSGS样病变
2.2 CsA肾损害的发生率及出现时间 Mihatsch,Thiel等和Ulrich曾对4个移植中心肾移植患者肾活检资料进行了分析,证实CsA造成肾小管中毒的发生率为9%~37%,ARF伴弥漫间质纤维化的发生率为0%~19%,条索状的间质纤维化和CsA相关的动脉病变的发生率则分别为5%~50%和5%~30%不等[1,2]。
肾移植后2周约43%的肾活检标本中可见肾小管中毒的形态学改变,移植后3年以上者检出率降至5%。CsA相关的动脉病变在移植后第一周即可出现,第2周的检出率为12%,移植后3年则可增至38%。从中可见,肾小管中毒的形态学改变多发生在急性期,而血管及间质纤维化则一般为长期用药的后果[1,2]。
2.3 肾脏病理[1~3]
, 百拇医药
2.3.1 光镜:
肾小球病变:常为小动脉病变延伸至肾小球所致。重度、中度及轻度动脉病变引发肾小球病变的发生率分别为65%,45%和25%,肾小球病变通常是局灶性,包括袢皱缩呈缺血性改变,肾小球硬化,偶见呈环状硬化,罕见病例可见典型的血栓性微血管病的特征性病变。总之,肾小球病变的形态改变多种多样,包括①纤维蛋白或血小板性血栓;②凹陷性病变(即血管极见血栓和增生性病变);③溶血性尿毒症样病变;④系膜溶解;⑤FSGS样病变等。
肾小管病变:表现为急性肾小管坏死时无特征性的形态学改变,镜下见不同程度的小管坏死、扩张及上皮细胞再生,间质水肿,T-H糖蛋白管型增多,可见广泛的钙化及刷状缘脱落,坏死的小管细胞脱落至管腔内。少尿期>2~3周,则可见间质弥漫纤维化,也可仅见小管上皮细胞等立方的空泡变性。包涵体、巨大线粒体及微钙化则为CsA肾小管病变较特征性病变。它们常出现在同一标本中,也可仅见一种肾小管病变。巨大线粒体主要见于近曲小管部(S1或S2段)。分布常不均匀,一些小管切面可见许多大线粒体,而邻近小管上皮细胞内则罕见。大线粒体常位于细胞核内,体积可为细胞核的1/2,呈圆形、卵圆形、偶尔雪茄形,常见嵴,含包涵体、巨大基质粒及脂滴,有时易误为吞噬性溶酶体,小管腔内也见巨大线粒体。
, 百拇医药
除近端小管S1,S2段外,有时S3段也可见到等立方的空泡,空泡形成与滑面内质网扩张有关,同一细胞内巨大线粒体与空泡从不同时出现。有时上皮细胞核固缩,刷状缘脱落。
光镜下微钙化呈圆形、新月形或不定形,单个发生,有时成簇出现,它们为肾小管上皮细胞坏死的痕迹,也有人提出是T-H糖蛋白管型钙化的结局。
间质病变:急性中毒常见管周毛细血管充血,慢性期肾皮质可见不规则灶性或条索状分布的小管萎缩和间质纤维化。萎缩的小管基膜常增厚(少数小管基膜也可变薄),纤维化的间质中可见单核细胞浸润。重度小管萎缩及间质纤维化时,常见小球球性废弃。
血管病变:动脉和小动脉平滑肌细胞常见非特异性的空泡变性。典型的血管病变分为二种,一种为环形或结节状的“内渗”透明物,沉积於小动脉壁,替代坏死的平滑肌细胞,内渗的透明样蛋白常常突向外膜或血管壁的外侧,似珍珠或戒指状,有的则可穿透小动脉壁引起血管腔狭窄或闭锁。第二种病变较罕见,动脉和小动脉内皮下粘液样增宽,电镜观察可见增宽的内膜下区域中见无定形样物质沉积。弓状动脉以上的血管多不受累,罕见病例可见动脉和小动脉栓塞性病变。
, 百拇医药
重复活检证实,停用或减撤CsA后小动脉病变仍继续进展,若血管全层受累,则由瘢痕替代,并逐渐融合消失伴间质纤维化,若小动脉不全受累则蛋白沉积逐渐减少,小动脉管腔通畅,重建,仅见管壁增厚,基膜样物质增加。
2.3.2 免疫荧光:无助于诊断,多为非特异性沉积。
2.3.3 电镜:肾小管病变如巨大线粒体,包涵体等可在电镜下观察,然而由于电镜制作、观察较费时,只能做为研究的一种手段。
2.4 鉴别诊断[1,3,4] 肾小管病变如等立方的空泡变性需与肾脏缺血性损伤时出现的粗大、不规则的空泡变性相区别。如活检前患者曾接受渗透性利尿剂如甘露醇、葡聚糖等治疗或曾使用造影剂时,则等立方的空泡变性不能作为CsA中毒的指标。急性肾小管坏死所致小管上皮细胞坏死的微钙化较CsA所致的微钙化灶大,如果肾组织中单独见微钙化,不能做为肾小管中毒性病变的依据。
, 百拇医药
CsA相关的小动脉病变应注意与高血压或糖尿病小动脉透明样变性相鉴别。后二者在完整的平滑肌细胞内可见局灶的结节状沉积物,而CsA相关的小动脉病变,环状或结节状的透明物取代坏死的平滑肌细胞(电镜下最为清晰)。CsA中毒所致的肾脏病变,不仅要与慢性排斥反应相鉴别,还应与移植排斥所致的血管病变相鉴别(表2,3)[3,4]表2 慢性排斥和慢性CsA毒性的区别
慢性排斥
CsA中毒
肾小球
大小
正常
缩小
基膜
分层
, 百拇医药
增厚或正常
毛细血管袢
开放
血栓、局灶硬化
免疫荧光
非特异性线状IgG
沿袢分布
非特异性线性IgG
沿袢分布
间质
间质纤维化
条索状纤维化
小管
, 百拇医药
小管减少
斑片状小管萎缩
血管
内膜增厚
透明样结节(蛋白渗出物)
中膜增厚
沉积于中膜和外膜
腔狭窄
表3 CsA中毒与排斥反应的鉴别
排斥反应
排斥反应/
CsA毒性
, 百拇医药
CsA毒性
动脉*
血管内凝血,坏死,增殖,浸润
内膜纤维化
小动
脉**
与血管排斥相关的小动脉病变
小动脉透明变性
无血管排斥证据的CsA动脉病变
肾小球
肾小球炎,弥漫球性肾小球病变
, 百拇医药 塌陷,局灶节段肾小球硬化,纤维蛋白血栓
类似HUS样血栓性微血管病,无血管排斥证据
肾小管
小管炎,HLA-Ⅱ类抗原局灶/弥漫阳性表达
坏死,粗的不规则空泡
巨大线粒体,等体积的小空泡,小管HLA-Ⅱ类抗原表达阴性
间质
出血,伴小管炎的弥漫细胞浸润
间质纤维化,限于纤维化区域中的细胞浸润
局灶或条纹状间质纤维化,伴CsA中毒的微血管病
, 百拇医药
*弓形、叶间;**至少二层平滑肌细胞
总之,在鉴别移植后肾功能延迟恢复的病因时,应考虑到CsA中毒的可能性,肾活检是可靠的方法之一。 参考文献
1 Mihatsch MJ,Ryffel B,Gudat F et al.Cyclosporine Nephropathy.In:Tisher CL,Brenner BM(eds):Renal pathology with clinical and functional correlations,2nd,ed,Philadelphia:JBL ippincott,1994.P1641
2 Mihatsch MJ,Thiel G,Basler V et al.Morphologic patterns in cyclosporin A treated renal transplant recipients.Transplant Proc,1985,17:101
3 Jindal RM,Hariharan S.Chronic rejection in kidney transplants.Nephron,1999,83:13
4 Ulrich W.Morphololgic von Nierentransplantation.Wien:Springer verlag,1986.
(1999-10-29收稿), http://www.100md.com
单位:南京军区南京总医院 解放军肾脏病研究所 (南京,210002)
关键词:肾移植;环孢霉素A;肾毒性
肾脏病与透析肾移植杂志990623 1 病例报告
1.1 【病例1】 男性患者,30岁,因肾移植术后1个月,肾功能延迟恢复,于1999-02-23入院。缘于1990年2月无诱因出现双下肢浮肿,尿检蛋白3+,隐血+,未予正规治疗,1996年4月发现血压升高达20/12 kPa(150/90 mmHg),复查血清肌酐(SCr)176 μmol/L。在我院行肾活检确诊为IgA肾炎(组织学类型符合局灶性节段性肾小球硬化),给予降压、纠正酸中毒、保肾等综合治疗。1998年9月疲劳后头昏、恶心加重伴呕吐,尿量减少,SCr升至800 μmol/L以上,诊断为慢性肾功能不全,尿毒症期,行血液透析治疗。于1999年1月22日在连续硬膜外麻醉下行同种异体肾移植术。术后予环孢霉素A(CsA)8 mg/kg,强的松80 mg/d(1个月内减量至20 mg/d)及双倍剂量雷公藤多甙三联免疫抑制治疗。患者病情稳定,无发热,血压波动在16~18.7/8~10.7 kPa(120~140/60~80mmHg),尿量维持在2500~3000 ml/24h,移植肾区无疼痛。但SCr始终波动在216 μmol/L左右,1999-02-25在B超引导下行抽吸式经皮移植肾活检术。
, http://www.100md.com
过去史,个人史,家庭史无特殊。
体格检查:体温36.6℃,脉搏78次/min,呼吸18次/min,血压17.3/10.7 kPa(130/80 mmHg)。重度贫血貌,无颜面浮肿,全身皮肤粘膜无黄染及出血点,未触及浅表淋巴结,双手轻度颤抖。双肺呼吸音清晰,未闻及干湿性
 音,心率78次/min,律齐,各瓣膜听诊区未闻及病理性杂音。腹软,肝脾肋下未及,右下腹一长约12cm的弧形手术瘢痕,愈合良好。移植肾区无肿胀,无压痛,腹水征阴性,双下肢无浮肿,病理反射未引出。
音,心率78次/min,律齐,各瓣膜听诊区未闻及病理性杂音。腹软,肝脾肋下未及,右下腹一长约12cm的弧形手术瘢痕,愈合良好。移植肾区无肿胀,无压痛,腹水征阴性,双下肢无浮肿,病理反射未引出。1.1.1 实验室检查
尿检:尿蛋白阴性,尿沉渣阴性,尿免疫化学检查阴性。
血清学检查:Hb 65 g/L,WBC 7.4×109/L,N 0.55,L 0.43,A/G 36.6/18.5 g/L,谷丙酶32 U/L,谷草酶16 U/L,碱性磷酸酶55 U/L,BUN 21.1 mmol/L,SCr 214 μmol/L,Ua 665 μmol/L,CH/TG 5.4/1.3 mmol/L,电解质正常。外周血CD4+细胞1.409×109/L,CD8+细胞0.745×109/L,血CsA谷值浓度617.19 μg/L(正常值<400 μg/L)
, 百拇医药
移植肾B超:105mm×49mm×48mm,彩色多谱勒超声:肾血流阻力指数增高。
1.1.2 肾活检结果
光镜:镜下1条皮质,1条皮髓交界组织,26个肾小球。肾小球体积偏大,细胞数90±/球,为肾之固有细胞,偶见节段周边袢系膜区增宽,内有2~3个系膜细胞,袢开放欠好,皱缩状,囊壁节段轻度增厚。PASM-Masson染色未见异常。肾小管无“小管炎”,灶性近端小管等立方空泡(插页图1)及细小空泡变性,间质水肿,管周毛细血管较多红细胞(插页图2)。血管未见明确异常。


图1.急性环孢霉素中毒。近端肾小管上皮细胞等立方的空泡变性(Masson三色,×400)

, 百拇医药
图2.急性环孢霉素中毒。管周毛细血管较多红细胞(Masson三色,×200)
电镜:电镜下未见肾小球。肾小管变化不一致,一些近曲小管上皮细胞胞浆内见大量巨大线粒体,其邻近小管则未见此改变。线粒体呈椭圆形或雪茄形,膜完整,嵴模糊。小管腔中亦见崩落的线粒体及微绒毛,小管基膜完整。管周毛细血管内大量细胞成分(红细胞、淋巴细胞、浆细胞)。
免疫荧光检查:IgM+,局灶节段分布于系膜区与血管袢。
肾组织细胞学:间质CD4+细胞16个/mm2,CD8+细胞24个/mm2,RT值0.67,IL-2R 4个/mm2,HLA-DR表达正常。
根据组织学改变特点:①肾小球轻度缺血状;②肾小管等立方及细小空泡变性;③管周毛细血管聚集。电镜巨大线粒体等改变。结合临床提示CsA肾毒性可能。
, 百拇医药
肾活检后将CsA逐渐减量,术后2个月CsA减至5.4 mg/kg,SCr降至137~147 μmol/L,复查血CsA谷值浓度为488.95 μg/L。
1.2 【病例2】 男性患者,50岁,肾移植术后10个月,于1999年12月入院行常规肾活检。缘于1996年4月体检时发现血压升高达21.3/12.7 kPa(160/95mmHg),尿检异常,蛋白2+,隐血+,未予治疗。1998年11月因恶心,纳差,口中有尿味,双肾B超示双肾萎缩(具体大小不详),结构不清,SCr升高达1000 μmol/L,诊断为慢性肾衰尿毒症期,予血液透析治疗。1999-02-09在连续硬膜外麻醉下行同种异体肾移植术,术中顺利。术后予CsA 8 mg/kg,强的松80 mg/d(1月内减至20 mg/d),霉酚酸酯(MMF)2.0 g/d及单倍剂量雷公藤多甙联合治疗。术后11天SCr降至正常,无发热,血压持续波动在14~16/10~10.7 kPa(105~120/75~80 mmHg),尿量维持在2400~3700 ml/24h,移植肾区无疼痛。肾移植术后10个月在B超引导下常规行抽吸式经皮移植肾活检术。
, http://www.100md.com
体格检查:体温36.8℃,脉搏80次/min,呼吸18次/min,血压16.6/10.7 kPa(125/80 mmHg)。轻度贫血貌,无颜面浮肿,全身皮肤粘膜无黄染及出血点,未触及浅表淋巴结。双肺呼吸音清晰,未闻及干湿性
 音,心率80次/min,律齐,各瓣膜听诊区未闻及病理性杂音。腹软,肝脾肋下未及,右下腹一14cm弧形手术瘢痕,Ⅰ期愈合。移植肾区无肿胀,无压痛,腹水征阴性。双下肢无浮肿,病理反射未引出。
音,心率80次/min,律齐,各瓣膜听诊区未闻及病理性杂音。腹软,肝脾肋下未及,右下腹一14cm弧形手术瘢痕,Ⅰ期愈合。移植肾区无肿胀,无压痛,腹水征阴性。双下肢无浮肿,病理反射未引出。过去史、个人史、家庭史无特殊。
1.2.1 实验室检查
尿检:尿蛋白阴性,尿沉渣阴性,尿免疫化学检查阴性。
血清学检查:Hb 104 g/L,WBC 11.3×109/L,N 0.74,L 0.14,A/G 39.3/19.4 g/L,谷丙酶13U/L,谷草酶17U/L,碱性磷酸酶62 U/L,BUN 9.9 mmol/L,SCr 121 μmol/L,Ua 288 μmol/L,CH/TG 4.6/1.69 mmol/L,电解质正常。外周血CD4+细胞1.169×109/L,CD8+细胞0.244×109/L。血CsA谷值浓度713.46 μg/L。(正常<400 μg/L)。
, http://www.100md.com
移植肾B超:103mm×58mm×54mm,彩色多谱勒超声:血流正常。
1.2.2 肾活检结果
光镜:镜下一小条皮质组织,11个肾小球,5条间质血管,无皮髓交界组织。肾小球细胞数100±/球,为肾之固有细胞,周边袢节段系膜区增宽,可见2~3个系膜细胞,袢开放尚好,包囊壁轻度增厚。PASM-Masson染色阴性。小管-间质病变轻度,无“小管炎”,小管上皮细胞亦未见空泡变性,间质血管入球小动脉透明变性(插页图3)。温习本例供肾切片,血管无透明变性(供肾者年龄22岁,男性)。

图3.急性环孢霉素中毒。人球小动脉壁上见透明沉积物(HE,×400)
免疫荧光检查:阴性。
, 百拇医药
肾组织细胞学:间质CD4+细胞204个/mm2,CD8+细胞144个/mm2,RT值1.42,IL-2R 28个/mm2,HLA-DR 皮质肾小管32%表达,其中阳性18%,弱阳性14%。
肾活检后将CsA逐渐减量,术后3个月CsA减至5.5 mg/kg,复查血CsA谷值浓度362.6 μg/L,SCr一直维持在正常范围。
2 讨论
环孢霉素是由一种不完全真菌属-Tolypocladium inflatum Gams在生长过程中产生的多肽混合物。将这种多肽混合物进一步纯化,即可分离出免疫抑制作用最强的一种肽―环孢霉素A(cyclosporin A,CsA),CsA的分子结构为环形十一肽,分子量1202。1978年CsA开始用于肾移植及骨髓移植临床,使移植患者的预后有了极大改观,移植肾一年成活率增加了10%~20%,尤其是高龄及高危患者受益尤其明显。
, http://www.100md.com
然而CsA也存在许多副作用,诸如毛发增生、震颤、高尿酸、高钾血症等,其肾毒性作用已成为CsA治疗中最重要的并发症。
2.1 CsA肾毒性的分类 目前常用的CsA肾毒性分类,为Thiel和Mihatsch根据发病机制所制定的一种新的分类方法(附图)。一般认为CsA的肾毒性与剂量相关,但部分患者的个体敏感性极高,或存在一些危险因素,因此即使剂量很低时,同样可出现CsA的肾毒性作用。
有作者将CsA的肾毒性分为三类,它们分别是急性CsA肾毒性,慢性CsA肾毒性和CsA相关的微血管病(表1)。我们觉得将CsA引起的肾脏病变分为肾小球病变、小管-间质性病变及微血管病变较为合适。


附图 CsA肾毒性分类
, 百拇医药
表1 CsA肾毒性的分类 急性CsA肾毒性
肾小管上皮细胞等立方的空泡
巨大线粒体
肾小管上皮细胞微钙化
肾小管周毛细血管充血
慢性CsA肾毒性
CsA所致的小动脉病变 结节状蛋白沉积
溶血尿毒综合征(HUS)/血栓性血
小板减少性紫癜(TTP)样改变
局灶间质纤维化(条纹状分布)
CsA相关的微血管病
, http://www.100md.com
HUS/TTP样改变
FSGS样病变
2.2 CsA肾损害的发生率及出现时间 Mihatsch,Thiel等和Ulrich曾对4个移植中心肾移植患者肾活检资料进行了分析,证实CsA造成肾小管中毒的发生率为9%~37%,ARF伴弥漫间质纤维化的发生率为0%~19%,条索状的间质纤维化和CsA相关的动脉病变的发生率则分别为5%~50%和5%~30%不等[1,2]。
肾移植后2周约43%的肾活检标本中可见肾小管中毒的形态学改变,移植后3年以上者检出率降至5%。CsA相关的动脉病变在移植后第一周即可出现,第2周的检出率为12%,移植后3年则可增至38%。从中可见,肾小管中毒的形态学改变多发生在急性期,而血管及间质纤维化则一般为长期用药的后果[1,2]。
2.3 肾脏病理[1~3]
, 百拇医药
2.3.1 光镜:
肾小球病变:常为小动脉病变延伸至肾小球所致。重度、中度及轻度动脉病变引发肾小球病变的发生率分别为65%,45%和25%,肾小球病变通常是局灶性,包括袢皱缩呈缺血性改变,肾小球硬化,偶见呈环状硬化,罕见病例可见典型的血栓性微血管病的特征性病变。总之,肾小球病变的形态改变多种多样,包括①纤维蛋白或血小板性血栓;②凹陷性病变(即血管极见血栓和增生性病变);③溶血性尿毒症样病变;④系膜溶解;⑤FSGS样病变等。
肾小管病变:表现为急性肾小管坏死时无特征性的形态学改变,镜下见不同程度的小管坏死、扩张及上皮细胞再生,间质水肿,T-H糖蛋白管型增多,可见广泛的钙化及刷状缘脱落,坏死的小管细胞脱落至管腔内。少尿期>2~3周,则可见间质弥漫纤维化,也可仅见小管上皮细胞等立方的空泡变性。包涵体、巨大线粒体及微钙化则为CsA肾小管病变较特征性病变。它们常出现在同一标本中,也可仅见一种肾小管病变。巨大线粒体主要见于近曲小管部(S1或S2段)。分布常不均匀,一些小管切面可见许多大线粒体,而邻近小管上皮细胞内则罕见。大线粒体常位于细胞核内,体积可为细胞核的1/2,呈圆形、卵圆形、偶尔雪茄形,常见嵴,含包涵体、巨大基质粒及脂滴,有时易误为吞噬性溶酶体,小管腔内也见巨大线粒体。
, 百拇医药
除近端小管S1,S2段外,有时S3段也可见到等立方的空泡,空泡形成与滑面内质网扩张有关,同一细胞内巨大线粒体与空泡从不同时出现。有时上皮细胞核固缩,刷状缘脱落。
光镜下微钙化呈圆形、新月形或不定形,单个发生,有时成簇出现,它们为肾小管上皮细胞坏死的痕迹,也有人提出是T-H糖蛋白管型钙化的结局。
间质病变:急性中毒常见管周毛细血管充血,慢性期肾皮质可见不规则灶性或条索状分布的小管萎缩和间质纤维化。萎缩的小管基膜常增厚(少数小管基膜也可变薄),纤维化的间质中可见单核细胞浸润。重度小管萎缩及间质纤维化时,常见小球球性废弃。
血管病变:动脉和小动脉平滑肌细胞常见非特异性的空泡变性。典型的血管病变分为二种,一种为环形或结节状的“内渗”透明物,沉积於小动脉壁,替代坏死的平滑肌细胞,内渗的透明样蛋白常常突向外膜或血管壁的外侧,似珍珠或戒指状,有的则可穿透小动脉壁引起血管腔狭窄或闭锁。第二种病变较罕见,动脉和小动脉内皮下粘液样增宽,电镜观察可见增宽的内膜下区域中见无定形样物质沉积。弓状动脉以上的血管多不受累,罕见病例可见动脉和小动脉栓塞性病变。
, 百拇医药
重复活检证实,停用或减撤CsA后小动脉病变仍继续进展,若血管全层受累,则由瘢痕替代,并逐渐融合消失伴间质纤维化,若小动脉不全受累则蛋白沉积逐渐减少,小动脉管腔通畅,重建,仅见管壁增厚,基膜样物质增加。
2.3.2 免疫荧光:无助于诊断,多为非特异性沉积。
2.3.3 电镜:肾小管病变如巨大线粒体,包涵体等可在电镜下观察,然而由于电镜制作、观察较费时,只能做为研究的一种手段。
2.4 鉴别诊断[1,3,4] 肾小管病变如等立方的空泡变性需与肾脏缺血性损伤时出现的粗大、不规则的空泡变性相区别。如活检前患者曾接受渗透性利尿剂如甘露醇、葡聚糖等治疗或曾使用造影剂时,则等立方的空泡变性不能作为CsA中毒的指标。急性肾小管坏死所致小管上皮细胞坏死的微钙化较CsA所致的微钙化灶大,如果肾组织中单独见微钙化,不能做为肾小管中毒性病变的依据。
, 百拇医药
CsA相关的小动脉病变应注意与高血压或糖尿病小动脉透明样变性相鉴别。后二者在完整的平滑肌细胞内可见局灶的结节状沉积物,而CsA相关的小动脉病变,环状或结节状的透明物取代坏死的平滑肌细胞(电镜下最为清晰)。CsA中毒所致的肾脏病变,不仅要与慢性排斥反应相鉴别,还应与移植排斥所致的血管病变相鉴别(表2,3)[3,4]表2 慢性排斥和慢性CsA毒性的区别
慢性排斥
CsA中毒
肾小球
大小
正常
缩小
基膜
分层
, 百拇医药
增厚或正常
毛细血管袢
开放
血栓、局灶硬化
免疫荧光
非特异性线状IgG
沿袢分布
非特异性线性IgG
沿袢分布
间质
间质纤维化
条索状纤维化
小管
, 百拇医药
小管减少
斑片状小管萎缩
血管
内膜增厚
透明样结节(蛋白渗出物)
中膜增厚
沉积于中膜和外膜
腔狭窄
表3 CsA中毒与排斥反应的鉴别
排斥反应
排斥反应/
CsA毒性
, 百拇医药
CsA毒性
动脉*
血管内凝血,坏死,增殖,浸润
内膜纤维化
小动
脉**
与血管排斥相关的小动脉病变
小动脉透明变性
无血管排斥证据的CsA动脉病变
肾小球
肾小球炎,弥漫球性肾小球病变
, 百拇医药 塌陷,局灶节段肾小球硬化,纤维蛋白血栓
类似HUS样血栓性微血管病,无血管排斥证据
肾小管
小管炎,HLA-Ⅱ类抗原局灶/弥漫阳性表达
坏死,粗的不规则空泡
巨大线粒体,等体积的小空泡,小管HLA-Ⅱ类抗原表达阴性
间质
出血,伴小管炎的弥漫细胞浸润
间质纤维化,限于纤维化区域中的细胞浸润
局灶或条纹状间质纤维化,伴CsA中毒的微血管病
, 百拇医药
*弓形、叶间;**至少二层平滑肌细胞
总之,在鉴别移植后肾功能延迟恢复的病因时,应考虑到CsA中毒的可能性,肾活检是可靠的方法之一。 参考文献
1 Mihatsch MJ,Ryffel B,Gudat F et al.Cyclosporine Nephropathy.In:Tisher CL,Brenner BM(eds):Renal pathology with clinical and functional correlations,2nd,ed,Philadelphia:JBL ippincott,1994.P1641
2 Mihatsch MJ,Thiel G,Basler V et al.Morphologic patterns in cyclosporin A treated renal transplant recipients.Transplant Proc,1985,17:101
3 Jindal RM,Hariharan S.Chronic rejection in kidney transplants.Nephron,1999,83:13
4 Ulrich W.Morphololgic von Nierentransplantation.Wien:Springer verlag,1986.
(1999-10-29收稿), http://www.100md.com