竞争性聚合酶链反应定量检测HBV DNA及对干扰素治疗的初步评价
作者:田小平 朱崇尧 何浩明 郝志强
单位:连云港市第一人民医院邮政编码:222002
关键词:定量聚合酶链反应 乙型肝炎病毒脱氧核糖核酸 干扰素
江苏医药991208 摘要 目的:研究HBV DNA浓度与临床疾病关系及对干扰素治疗效果进行评价。方法:应用竞争性聚合酶链反应技术检测42例慢性乙型肝炎(慢乙肝)患者血清HBV DNA含量,并对26例患者进行了人白细胞干扰素治疗前后循环血中HBV DNA浓度的动态观察。结果:慢乙肝患者血清HBV DNA含量在5×100~5×108拷贝/μl之间;血清HBV DNA含量与ALT活性相关关系不明显(r=0.2862,P>0.05);干扰素治疗前完全反应组HBV DNA浓度显著低于部分反应组(t=4.84,P<0.01)和无反应组(t=6.26,P<0.01)。结论:HBV感染后产生的各种临床疾病类型可能主要归于宿主免疫应答的不同,HBV DNA浓度较低的患者(小于10000拷贝/μl)干扰素治疗效果较好,定量检测HBV DNA浓度在抗病毒药物疗效预测和评价中是一个有重要意义的参考指标。
, http://www.100md.com
干扰素已广泛地应用于慢性乙型肝炎(慢乙肝)的治疗,取得了较好的治疗效果。国外研究显示,治疗前循环血中的乙型肝炎病毒DNA含量和ALT活性是影响治疗效果的重要因素,检测血清HBV DNA水平可作为干扰素治疗反应的一个预测因素[1,2]。聚合酶链反应(PCR)是检测乙型肝炎病毒的最敏感技术,应用定量PCR技术检测病毒基因水平国外已有报道[3]。我们用竞争性PCR技术检测慢乙肝血清HBV DNA浓度,探讨HBV DNA浓度与临床疾病关系并对干扰素治疗进行初步评价。
资料与方法
一、一般情况 42例慢乙肝患者为1995年~1997年我院门诊及住院患者,男26例,女16例,平均年龄34.6±15.0岁。诊断符合1995年5月北京会议[4]标准。患者空腹采血即分离血清,-20℃冰冻待检。
二、干扰素治疗和效果判定 26例HBV DNA阳性的慢乙肝患者接受300万单位人白细胞干扰素肌注治疗,每周三次,共24周。治疗前、治疗期间,每4周检测HBV DNA含量及ALT活性,并随访24周。用药24周内HBV DNA转阴,ALT降至正常,且随访后指标无反跳者为完全有效;用药后ALT明显下降或复常,HBV DNA浓度降低,治疗结束后又反跳者为部分有效;用药后ALT无明显下降,HBV DNA浓度无变化者为无效。
, 百拇医药
三、定量PCR测定HBV DNA 试剂由宏达生物技术公司提供,结果以血清每μl拷贝的对数值表示,每次实验中均设阴阳性对照,参照Kwok[5]等提出的防污染措施进行实验。
结果
一、慢乙肝患者血清HBV DNA含量检测结果见表1。表1显示:慢乙肝患者血清HBV DNA含量范围在5×100~5×108拷贝/μl之间。HBVM模式转换中HBsAg、HBeAg阳性组血清HBV DNA含量显著高于HBsAg、抗-HBe阳性组(t=6.56,P<0.01)和抗-HBs、抗-HBc阳性组(t=7.14,P<0.01)。
表1 慢乙肝患者血清HBV DNA含量(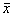 ±s)
±s)
, http://www.100md.com
例数
阳性数
(%)
HBV DNA
(拷贝/μl)
HBsAg、HBeAg(+)组
22
22(100.0)
6.22±4.95
HBsAg、抗-HBe(+)组
14
8(57.1)
, 百拇医药
3.74±2.64
抗-HBs、抗-HBc(+)组
6
2(33.3)
1.79±1.47
二、相关分析显示慢乙肝患者血清HBVDNA含量与ALT活性无明显相关性(r=0.2862,P>0.05)。
三、干扰素治疗前后血清HBV DNA含量见表2。表2显示,在干扰素治疗期间动态观察HBV DNA浓度,完全有效者在治疗6~10周后HBV DNA浓度显著下降,伴随ALT活性降低,在24周内HBV DNA全部转阴,ALT恢复至正常;部分有反应者治疗6~10周后血清HBV DNA含量开始下降,ALT发生波动,治疗结束时HBV DNA降至较低水平,随访24周恢复到原来水平;无反应者治疗前后血清HBV DNA含量无明显变化,ALT无明显下降。干扰素治疗前完全反应组HBV DNA浓度显著低于部分反应组(t=4.84,P<0.01)和无反应组(t=6.26,P<0.01)。表2干扰素治疗前后血清HBV DNA含量(拷贝/μl,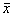 ±s)
±s)
, http://www.100md.com
例数
完 全 反 应
部 分 反 应
无 反 应
例数
HBV DNA
例数
HBV DNA
例数
HBV DNA
治疗前
26
10
, http://www.100md.com
3.21±2.25
4
5.84±3.71
12
6.73±4.36
治疗后
26
10
0
4
4.46±2.08
12
6.04±3.97
, http://www.100md.com
随访24周
26
10
0
4
5.77±3.30
12
6.92±4.15
讨论 PCR技术具有极高的特异性和灵敏度,已被广泛用于血清、肝组织和白细胞中HBV DNA的检测。竞争性PCR是将待测靶序列与已知量的竞争模板加入同一管同一反应体系中进行共同扩增,保证两者处在同等反应条件,避免了管与管之间的差别;由于使用同一引物、参与同一反应,所以两者扩增产物量的相对变化反应了竞争模板与靶序列在初始反应混合液中的相对浓度。当然,由于内参照模板与标本模板长度有差异、二级结构不完全相同等因素,两者扩增效率也不可能完全一致。但其影响已减至最小,使实验结果的可信度极大地提高。
, 百拇医药
用该方法检测慢乙肝患者血清HBV DNA含量,在出现抗-HBe、抗-HBc及抗-HBs血清中有不少病例可检出HBV DNA,但含量显著低于HBeAg阳性组,说明这些抗体的出现并不是HBV DNA复制的停止,而只是复制水平的降低,显然对于这些患者的传染性及潜在复发不容忽视。
通过动态观察干扰素治疗期间患者病毒浓度,表明治疗前血清HBV DNA浓度较低的患者治疗效果较好,反之则较差。治疗有效组中ALT随HBV DNA的清除而转至正常,无效者或部分有效者的病毒虽也有下降,但仍处于可检测水平或上升,ALT也始终异常或波动,提示干扰素在这部分患者中可以抑制病毒的复制,从而使病程向好的方向转化。从有效组的反应来看,治疗前循环血中HBV DNA的水平较部分有效及无效组为低,提示治疗前循环血中HBV DNA水平是影响治疗效果的重要因素,说明在治疗前检测并比较循环血中核酸含量对临床治疗有重要参考价值。循环血中HBV DNA含量小于10 000拷贝/μl的患者可能对干扰素治疗有积极反应,可能反应出宿主免疫状态对HBV耐受较轻而易于激活。慢乙肝患者在进行治疗前有必要考虑并比较血中核酸浓度,以预测和评价干扰素治疗效果,并可参考此浓度调整剂量及决定疗程。
, http://www.100md.com
值得注意的是,HBV DNA浓度与肝细胞损害程度无关,HBV感染后产生的各种临床疾病类型可能主要归于宿主免疫应答的不同,HBV变异与临床也密切相关[6],可以看出影响抗病毒疗效的因素是多方面的和复杂的,抗病毒治疗中病毒的量及其变异和患者免疫功能对疗效的影响及相互作用需进一步深入研究。
参考文献
[1] Brook MG,et al.Hepatology 1989;10:761.
[2] Perrillo RP,et al.J Hepatol 1993;17(Suppl):56S.
[3] Wu JW,et al.J Virol Methods 1994;49:331.
[4] 病毒性肝炎防治方案(试行).中华传染病杂志 1995;13(4):241.
[5] Kwok S,et al.Nature 1989;339:237.
[6] Brunetto MR,et al.Hepatology 1989;10:198.
(1998年12月23日收稿 1999年6月18日修回), 百拇医药
单位:连云港市第一人民医院邮政编码:222002
关键词:定量聚合酶链反应 乙型肝炎病毒脱氧核糖核酸 干扰素
江苏医药991208 摘要 目的:研究HBV DNA浓度与临床疾病关系及对干扰素治疗效果进行评价。方法:应用竞争性聚合酶链反应技术检测42例慢性乙型肝炎(慢乙肝)患者血清HBV DNA含量,并对26例患者进行了人白细胞干扰素治疗前后循环血中HBV DNA浓度的动态观察。结果:慢乙肝患者血清HBV DNA含量在5×100~5×108拷贝/μl之间;血清HBV DNA含量与ALT活性相关关系不明显(r=0.2862,P>0.05);干扰素治疗前完全反应组HBV DNA浓度显著低于部分反应组(t=4.84,P<0.01)和无反应组(t=6.26,P<0.01)。结论:HBV感染后产生的各种临床疾病类型可能主要归于宿主免疫应答的不同,HBV DNA浓度较低的患者(小于10000拷贝/μl)干扰素治疗效果较好,定量检测HBV DNA浓度在抗病毒药物疗效预测和评价中是一个有重要意义的参考指标。
, http://www.100md.com
干扰素已广泛地应用于慢性乙型肝炎(慢乙肝)的治疗,取得了较好的治疗效果。国外研究显示,治疗前循环血中的乙型肝炎病毒DNA含量和ALT活性是影响治疗效果的重要因素,检测血清HBV DNA水平可作为干扰素治疗反应的一个预测因素[1,2]。聚合酶链反应(PCR)是检测乙型肝炎病毒的最敏感技术,应用定量PCR技术检测病毒基因水平国外已有报道[3]。我们用竞争性PCR技术检测慢乙肝血清HBV DNA浓度,探讨HBV DNA浓度与临床疾病关系并对干扰素治疗进行初步评价。
资料与方法
一、一般情况 42例慢乙肝患者为1995年~1997年我院门诊及住院患者,男26例,女16例,平均年龄34.6±15.0岁。诊断符合1995年5月北京会议[4]标准。患者空腹采血即分离血清,-20℃冰冻待检。
二、干扰素治疗和效果判定 26例HBV DNA阳性的慢乙肝患者接受300万单位人白细胞干扰素肌注治疗,每周三次,共24周。治疗前、治疗期间,每4周检测HBV DNA含量及ALT活性,并随访24周。用药24周内HBV DNA转阴,ALT降至正常,且随访后指标无反跳者为完全有效;用药后ALT明显下降或复常,HBV DNA浓度降低,治疗结束后又反跳者为部分有效;用药后ALT无明显下降,HBV DNA浓度无变化者为无效。
, 百拇医药
三、定量PCR测定HBV DNA 试剂由宏达生物技术公司提供,结果以血清每μl拷贝的对数值表示,每次实验中均设阴阳性对照,参照Kwok[5]等提出的防污染措施进行实验。
结果
一、慢乙肝患者血清HBV DNA含量检测结果见表1。表1显示:慢乙肝患者血清HBV DNA含量范围在5×100~5×108拷贝/μl之间。HBVM模式转换中HBsAg、HBeAg阳性组血清HBV DNA含量显著高于HBsAg、抗-HBe阳性组(t=6.56,P<0.01)和抗-HBs、抗-HBc阳性组(t=7.14,P<0.01)。
表1 慢乙肝患者血清HBV DNA含量(
, http://www.100md.com
例数
阳性数
(%)
HBV DNA
(拷贝/μl)
HBsAg、HBeAg(+)组
22
22(100.0)
6.22±4.95
HBsAg、抗-HBe(+)组
14
8(57.1)
, 百拇医药
3.74±2.64
抗-HBs、抗-HBc(+)组
6
2(33.3)
1.79±1.47
二、相关分析显示慢乙肝患者血清HBVDNA含量与ALT活性无明显相关性(r=0.2862,P>0.05)。
三、干扰素治疗前后血清HBV DNA含量见表2。表2显示,在干扰素治疗期间动态观察HBV DNA浓度,完全有效者在治疗6~10周后HBV DNA浓度显著下降,伴随ALT活性降低,在24周内HBV DNA全部转阴,ALT恢复至正常;部分有反应者治疗6~10周后血清HBV DNA含量开始下降,ALT发生波动,治疗结束时HBV DNA降至较低水平,随访24周恢复到原来水平;无反应者治疗前后血清HBV DNA含量无明显变化,ALT无明显下降。干扰素治疗前完全反应组HBV DNA浓度显著低于部分反应组(t=4.84,P<0.01)和无反应组(t=6.26,P<0.01)。表2干扰素治疗前后血清HBV DNA含量(拷贝/μl,
, http://www.100md.com
例数
完 全 反 应
部 分 反 应
无 反 应
例数
HBV DNA
例数
HBV DNA
例数
HBV DNA
治疗前
26
10
, http://www.100md.com
3.21±2.25
4
5.84±3.71
12
6.73±4.36
治疗后
26
10
0
4
4.46±2.08
12
6.04±3.97
, http://www.100md.com
随访24周
26
10
0
4
5.77±3.30
12
6.92±4.15
讨论 PCR技术具有极高的特异性和灵敏度,已被广泛用于血清、肝组织和白细胞中HBV DNA的检测。竞争性PCR是将待测靶序列与已知量的竞争模板加入同一管同一反应体系中进行共同扩增,保证两者处在同等反应条件,避免了管与管之间的差别;由于使用同一引物、参与同一反应,所以两者扩增产物量的相对变化反应了竞争模板与靶序列在初始反应混合液中的相对浓度。当然,由于内参照模板与标本模板长度有差异、二级结构不完全相同等因素,两者扩增效率也不可能完全一致。但其影响已减至最小,使实验结果的可信度极大地提高。
, 百拇医药
用该方法检测慢乙肝患者血清HBV DNA含量,在出现抗-HBe、抗-HBc及抗-HBs血清中有不少病例可检出HBV DNA,但含量显著低于HBeAg阳性组,说明这些抗体的出现并不是HBV DNA复制的停止,而只是复制水平的降低,显然对于这些患者的传染性及潜在复发不容忽视。
通过动态观察干扰素治疗期间患者病毒浓度,表明治疗前血清HBV DNA浓度较低的患者治疗效果较好,反之则较差。治疗有效组中ALT随HBV DNA的清除而转至正常,无效者或部分有效者的病毒虽也有下降,但仍处于可检测水平或上升,ALT也始终异常或波动,提示干扰素在这部分患者中可以抑制病毒的复制,从而使病程向好的方向转化。从有效组的反应来看,治疗前循环血中HBV DNA的水平较部分有效及无效组为低,提示治疗前循环血中HBV DNA水平是影响治疗效果的重要因素,说明在治疗前检测并比较循环血中核酸含量对临床治疗有重要参考价值。循环血中HBV DNA含量小于10 000拷贝/μl的患者可能对干扰素治疗有积极反应,可能反应出宿主免疫状态对HBV耐受较轻而易于激活。慢乙肝患者在进行治疗前有必要考虑并比较血中核酸浓度,以预测和评价干扰素治疗效果,并可参考此浓度调整剂量及决定疗程。
, http://www.100md.com
值得注意的是,HBV DNA浓度与肝细胞损害程度无关,HBV感染后产生的各种临床疾病类型可能主要归于宿主免疫应答的不同,HBV变异与临床也密切相关[6],可以看出影响抗病毒疗效的因素是多方面的和复杂的,抗病毒治疗中病毒的量及其变异和患者免疫功能对疗效的影响及相互作用需进一步深入研究。
参考文献
[1] Brook MG,et al.Hepatology 1989;10:761.
[2] Perrillo RP,et al.J Hepatol 1993;17(Suppl):56S.
[3] Wu JW,et al.J Virol Methods 1994;49:331.
[4] 病毒性肝炎防治方案(试行).中华传染病杂志 1995;13(4):241.
[5] Kwok S,et al.Nature 1989;339:237.
[6] Brunetto MR,et al.Hepatology 1989;10:198.
(1998年12月23日收稿 1999年6月18日修回), 百拇医药