一氧化氮诱导VSMC凋亡观察
作者:田雪梅 马晓东 李进
单位:田雪梅(第一军医大学组织胚胎学教研室,广东 广州 510515);马晓东(第一军医大学中心实验室,广东 广州 510515);李进(第一军医大学组织胚胎学教研室,广东 广州 510515)
关键词:一氧化氮;血管平滑肌细胞;细胞凋亡
第一军医大学学报000105 摘要:目的 研究动脉粥样硬化和冠脉气囊成形术后再狭窄中血管平滑肌细胞数量异常增多的机制,并初步探讨NO诱导血管平滑肌细胞凋亡的作用。材料和方法 以SNAP作为NO供体,采用HE,TUNEL,荧光双染后光镜观察以及电镜、流式细胞术、细胞DNA的琼脂糖凝胶电泳对SNAP作用下的细胞凋亡进行鉴定和检测。结果 观察发现,0.4 mmol/L SNAP作用8~10 h即能明显地诱导培养的血管平滑肌细胞凋亡。结论 SNAP以浓度依赖方式诱导血管平滑肌细胞凋亡,细胞爬片的HE染色结合TUNEL标记是检测凋亡的较为准确且简单的方法。
, http://www.100md.com
中图分类号:Q571; Q461 文献标识码:A 文章编号:1000-2500(2000)01-0015-04
Nitric oxide induced apoptosis in vascular smooth muscle cells
TIAN Xue-mei LI Jin
(Department of Histology and Embryology, First Military Medical University, Guangzhou 510515, China)
MA Xiao-dong
(Central Laboratory, First Military Medical University, Guangzhou 510515, China)
, 百拇医药
Abstract: Objective To further study the significant number increase of vascular smooth muscle cells in atherosclerosis and resterosis. We investigated the effect of NO on the induction of apoptosis in cultured vascular smooth muscle cells. Methods SNAP was used as NO donor. HE, TUNEL, double fluorescent staining and electronic microscopy, flow cytometry, agarose gel electrophoresis of DNA were employed to detect and observe cell apoptosis. Result Vascular smooth muscle cells showed apoptosis when treated with 0.4 mmol/L SNAP for 8 to 10 hours. Conclusions The results indicated that SNAP dose-dependently induce apoptosis in VSMC, and HE staining along with TUNEL was a simple method to observe and detect apoptosis in cells cultured on slide. To further study the significant number increase of vascular smooth muscle cells in atherosclerosis and resterosis. We investigated the effect of NO on the induction of apoptosis in cultured vascular smooth muscle cells. Methods SNAP was used as NO donor. HE, TUNEL, double fluorescent staining and electronic microscopy, flow cytometry, agarose gel electrophoresis of DNA were employed to detect and observe cell apoptosis. Result Vascular smooth muscle cells showed apoptosis when treated with 0.4 mmol/L SNAP for 8 to 10 hours. Conclusions The results indicated that SNAP dose-dependently induce apoptosis in VSMC, and HE staining along with TUNEL was a simple method to observe and detect apoptosis in cells cultured on slide.
, 百拇医药
Key words: nitric oxide; vascular smooth muscle cell; apoptosis
动脉粥样硬化(Atherosclerosis,AS)病变中,血管平滑肌细胞(Vascular smooth muscle cell,VSMC)异常增殖是血管壁增厚的主要原因。在VSMC增殖的同时,VSMC也有凋亡发生。两者间的平衡状态直接影响VSMC的数量,并最终决定血管壁的厚度和血管腔的大小[1]。VSMC 凋亡又能引起AS斑块的不稳定。此外,凋亡的VSMC可激活凝血酶等血栓形成物质,促进血栓形成。一氧化氮(Nitric oxide,NO)广泛存在于心血管系统中,具有多种生物效应[2-5]。NO诱导细胞凋亡是对NO作用的新认识[6]。本实验拟从NO诱导VSMC凋亡的作用方面进行研究。而VSMC凋亡模型的建立及检测方法的确定是进行VSMC凋亡研究的前提。因此,本实验建立NO诱导VSMC凋亡的模型,并通过HE染色、荧光双染法、流式细胞术、原位末端标记、透射电镜观察、DNA琼脂糖凝胶电泳几种方法,对VSMC凋亡进行观察和检测。
, 百拇医药
1 材料和方法
1.1 材料
Sprague Dawley(SD)大鼠;DMEM培养基(GIBCO BRL公司),小牛血清(杭州四季青生物工程材料研究所),牛血清白蛋白(天象人生物工程有限公司),胰蛋白酶(国产),亚硝基乙酰青霉胺(S-Nitroso-N-acetylpenicillamine, SNAP,Sigma),硝普钠(Sodium nitroprusside, SNP,国产), 丫啶橙(AO)、溴化乙锭(EB)、碘化丙锭(PI)(国产),TUNEL试剂盒(Boehringer Mannheim)。
1.2 方法1.2 方法
1.2.1 VSMC培养 采用贴块法[1]。无菌条件下分离大鼠的胸主动脉,去除内外膜,将中膜平滑肌组织块剪碎,接种于培养瓶内,加入含20% 小牛血清的DMEM培养液,在37℃、5% CO2 培养箱中静置培养。待细胞生长达汇合,用0.25% 胰蛋白酶消化传代,用含10~15%小牛血清的培养液继续培养。第4、5代细胞用抗α-actin肌动蛋白抗体免疫组化法进行鉴定。实验用第5~8代细胞。
, 百拇医药
1.2.2 细胞爬片制作 将5~10代细胞用胰蛋白酶消化,制成密度为104~105/ml的细胞悬液。滴加细胞悬液于盖玻片上。2~6 h后,细胞贴壁,补加培养基。待细胞生长达50%~60%,用无血清DMEM培养液洗2次,再加条件培养液,继续培养24~48 h,然后加含0.08~1.0 mmol/L SNAP或SNP的条件培养液。继续培养2~24 h (2 h,6 h,8 h,10 h,12 h,24 h),收集盖片,4%多聚甲醛固定,存放。
1.2.3 细胞爬片进行常规HE染色。
1.2.4 荧光双染色 细胞爬片经PBS洗后,滴加100 mg/L AO染液和100 mg/L EB染液,避光染色,PBS漂洗,湿封盖片于载玻片上。荧光显微镜下,388 nm紫外光激发进行观察。
1.2.5 原位末端标记 按TUNEL试剂盒说明书操作。
, 百拇医药
1.2.6 透射电镜样品制备 细胞接种于培养瓶中,生长达50%~60% 时,换成条件培养液培养24~48 h后,加含SNAP的条件培养液,使SNAP终浓度为1.0 mmol/L,培养8~10 h,收集细胞;按常规透射电镜样品制作法做透射电镜切片并观察。
1.2.7 凋亡细胞DNA的琼脂糖凝胶电泳 细胞接种于培养瓶中,分别经1.0 mmol/L的SNAP和 SNP处理,方法同前。收集细胞,提取细胞DNA。
1.2.8 流式细胞仪(FCM)检测 细胞接种于培养瓶中,经不同浓度的SNAP分别作用8 h、12 h后,收集细胞;800~1000 r/min离心10 min;75% 的冷乙醇固定,4℃冰箱或-20℃存放。经固定的细胞,离心,弃去固定液;用PBS洗2遍;加RNase(终浓度为2 μg/ml),于37℃水浴30 min加入含50 mg/L PI的PBS溶液 1 ml,37℃下孵育30 min;细胞悬液过400目尼龙膜以除去杂质及细胞团,上机检测。FCM自动去本底,选用488 nm波长激发光激发荧光,测定样品。LysysⅡ软件分析结果。
, 百拇医药
2 结果
2.1 VSMC培养
贴块法培养的VSMC,倒置显微镜观察,4~7 d即有细胞从组织快周围爬出,并且细胞生长呈典型的“谷和峰”状态,第4、5代细胞,抗α-actin抗体组化检测鉴定95%以上为VSMC。
2.2 VSMC凋亡的形态观察
2.2.1 培养过程中细胞的形态变化 0.04~1 mol/ L范围内不同浓度的SNAP处理细胞。1 h后,倒置显微镜下即可见,有的细胞开始与相邻细胞脱离联系,逐渐变圆,胞质凝集,体积缩小。随时间延长,变圆的细胞皱缩,体积更小,最终脱离附着面,漂浮于培养液中,但始终保持完整的形状。
图1 细胞爬片的HE染色
, 百拇医药
Fig.1 VSMCS cultured on glass slides were stained with HE. Cells exhibit neclear chromatin condensation, cell rounding, membrane blebbing and fragmented nuclear. ×200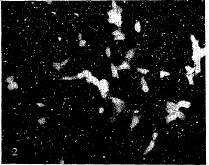
图2 细胞爬片的AO和EB染色
Fig. 2 Cell slide stained with AO and EB. Showing apoptotic cells and normal cells. ×40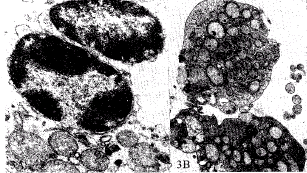
图3 VSMC的电镜观察
, http://www.100md.com
Fig.3 Electron microscopic appearance of apoptosis or necrosis in VSMCs. A .chromatin condensation at the periphery of the nucleus;B. Formation of membrane-bound vesicles
图4 细胞爬片的TUNEL染色
Fig.4 Detection of apoptotic VSMCs with TUNEL VSMCs cultured on glass slide were treated with 0.4 mmol/L SNAP for 8 to 10 h. ×100
2.2.2 HE染色显示凋亡细胞的形态变化 细胞爬片经HE染色,SNAP处理后的VSMC,可以看到染色质边集,核固缩,核碎裂等凋亡细胞核的特征性变化(图1)。
, http://www.100md.com
2.2.3 荧光双染色区分死亡细胞与凋亡细胞 经AO和EB双染后,能够区分3种不同状态的细胞。正常活细胞,细胞核染成绿色,核呈椭圆,核质均匀,核仁黄色或橙红色清晰可见,胞质为橙色或黄色;死亡细胞显橙色;凋亡细胞可见两种状态:一种细胞核固缩成球状,呈绿色、黄色或橙色,胞质黄色,细胞尚未变圆;另一种细胞发橙黄色荧光,细胞内可见1至数个大小不等的球状小体,为碎裂的细胞核(图2)。
2.2.4 VSMC的超微结构 电镜观察(图3),凋亡细胞的核染色质边集、凝集及核碎裂。胞质内分布着大小不同的腔扩大了的内质网,其中含有均质的内容物,仍可见粗面内质网膜上均匀分布着的核糖体颗粒,线粒体的形态也保持完整,线粒体嵴清晰可见。可见凋亡小体形成,线粒体等细胞内容物被膜包裹。
2.3 凋亡细胞DNA断裂分析2.3 凋亡细胞DNA断裂分析
2.3.1原位末端标记 经TUNEL染色,凋亡细胞呈黄色/棕黄色,核着色深,大部细胞的胞质也有着色。收缩变圆的细胞几乎均呈阳性染色,为凋亡细胞(图4)。SNP处理的细胞TUNEL染色为阳性的少。TUNEL染色结果及前述形态观察都显示,凋亡细胞的数量随SNAP浓度升高,有较为显著的增加;而同一浓度SNAP作用下,2~8 h孵育,凋亡细胞数量渐增加。但8 h、10 h与12 h处理相比,凋亡细胞增加不明显。
, 百拇医药
2.3.2 琼脂糖凝胶电泳 SNP处理,细胞DNA电泳呈弥散状的细胞坏死特征,1.0 mmol/L SNAP 处理后,DNA电泳呈凋亡细胞特有的梯状带;而0.08 mmol/L SNAP处理后,大多数细胞DNA仍完整(图5)。
2.4流式细胞仪检测2.4流式细胞仪检测
流式细胞仪检测结果发现,0.08、0.10、0.30、0.50、1.0 mmol/L SNAP作用8 h后,细胞凋亡率分别为5.9%、8.1%、13.5%、22.5%、42.7%, 随浓度增加,凋亡细胞的数量增多;12 h作用,结果相似。而同一浓度SNAP处理8 h、12 h,凋亡细胞数量差别不明显,如0.08 mmol/L SNAP作用8 、12 h后,细胞凋亡率分别为5.9%,6.3% 。表明8 h以后,细胞凋亡不再随作用时间增加而明显增多,与形态观察的结果一致。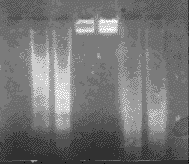
, 百拇医药
图5 死亡细胞DNA的琼脂糖凝胶电泳结果
Fig.5 Agarose gel electrophoresis of DNA isolated from dying cells treated with SNAP or SNP for 8 h
3 讨论
组织贴块法培养VSMC是一种经济方便的方法。但缺点在于培养过程中血管外膜不能绝对被去除干净,因而有一些成纤维细胞混杂于VSMC中长出。但由于成纤维细胞易于脱壁,在连续的传代培养过程中可以不断地被清除。一般到第5代时,成纤维细胞几近绝迹,此时,VSMC的性状较为稳定。而当传代培养10代以上,部分VSMC将会转变为多倍体。因此,本实验选择5~8代细胞进行实验。
检测细胞凋亡的方法有多种。其中HE染色最为简便。经HE染色能清晰地观察到凋亡过程中细胞变圆、皱缩,细胞核染色质边集、核固缩、核碎裂形成凋亡小体等形态变化。凋亡早期的细胞和某些处于分裂期的细胞有相似的形态变化:细胞变圆,染色质浓缩聚集而使核深染。荧光染料染色则能够更突出的显示细胞核的形态,但是,使用一种荧光染料染色,不易分辨坏死细胞与凋亡细胞。经过使用AO与EB两种DNA染料混合染色,根据细胞的着色情况,能分辩正常细胞、坏死细胞和凋亡细胞。AO为膜通透性染料,它能进入活细胞,与细胞核内DNA结合,发出绿色荧光,与胞质内RNA结合发出橙色或黄色荧光;而EB只能进入膜结构改变了的坏死细胞,将细胞核染成红色;凋亡早期的细胞,膜结构完整,EB不能进入,核显绿色;而凋亡晚期的细胞,细胞膜受损,被AO和EB复合染色,细胞核被染成橙色、橙红色。但是荧光染色不易控制。透射电镜能最清楚地观察到凋亡细胞的形态,特别是胞核的形态变化。
, 百拇医药
经PI使细胞内DNA染色后,借助流式细胞仪进行检测,可以根据G1期峰旁是否出现一个不连续的亚(次)二倍体峰来确定细胞凋亡,并可得出细胞凋亡率。
细胞核内DNA被内源性核酸内切酶降解,形成180~200 bp及其倍数的DNA片段,在琼脂糖凝胶电泳中表现为DNA梯状带,为细胞凋亡最具特征性的变化[7]。DNA断裂为核苷片段常发生于细胞核形态变化之前[8]。原位末端标记法则能灵敏地检测到DNA链的轻微损伤。细胞凋亡时,核DNA被切割而断裂,产生3’-OH末端,TUNEL法则借助dT将标记的dUTP掺入3’-OH,其特异性高,优先标记凋亡细胞并能够识别凋亡早期的细胞,弥补了HE染色和荧光染色等方法的不足。实验中发现HE染色显示凋亡细胞形态,并结合TUNEL法鉴定是检测细胞凋亡最简便可靠的方法。
SNAP在溶解状态下能自发地释放NO。荧光双染色、TUNEL及DNA电泳结果指出,SNAP作用下细胞主要以凋亡形式死亡。SNAP在溶解状态下不稳定,半衰期在5 h以内,它最终降解为青霉胺、NaNO2和NaNO3[8]。1 mmol/L溶液中的SNAP,3 d后就会完全降解[9]。这可以解释SNAP处理过程中,8~10 h以后,VSMC凋亡不再随时间延长而有明显增加的现象。实验中观察到SNAP诱导VSMC凋亡具有浓度依赖性。经形态学观察及DNA断裂检测,实验中选择SNAP为诱导VSMC凋亡的NO供体,8~10 h为最佳作用时间。实验中还发现高浓度的SNAP诱导VSMC凋亡的效果更明显。这可能是因为NO在高氧环境中易于氧化而损耗所致。但在体内组织中O2浓度低,并且周围细胞能持续地释放NO,可能使局部保持较高的NO浓度。因此,在体内有存在高浓度NO的可能性。
, http://www.100md.com
参考文献
[1]Han DK, Haudenschild CC, Hong MK et al. Evidence for apoptosis inhuman atherogensis and in a rat vascular injury model[J]. Am J Pathol, 1995, 147(2):267~77.
[2]Naito M, Hayashi H, Iguchi A. New approaches to the prevention of atherosclerosis[J]. Drugs, 1995, 50(3):440~53.
[3]Loscalzo J, Welch G. Nitric oxide and its role in the cardiovascular system[J]. Progress in cardiovascular Disease, 1995, 38(2):87~104.
, 百拇医药
[4]Sarker R, Meinberg EG, James G et al. Nitric oxide reversibly inhibits the migration of cultured vascular smooth muscle cells[J]. Circ Res, 1996, 78:225~30.
[5]Fukuo K, Hata S Suhara T et al. Nitric oxide mduces upregulation of Fas and apoptosis in vascular smooth muscle[J]. Hypertension, 1996, 27(Part 2):823~6.
[6]Ross R. The smooth muscle cell. Ⅱ. Growth of smooth muscle in culture and formation of elastic fibers[J]. J Cell Biol, 1971, 50(1):63~8.
, 百拇医药
[7]Compton MA. Biochemical hallmark of apoptosis: internucleosomal degradation of the genome[J]. Cancer Metastasis Rev, 1992, 11(1): 105~9.
[8]Ignarro LJ, H. Lippton JC, Edwards et al. Mechanism of vascular smooth muscle relaxation by organic nitrates, nitrites, nitroprusside and nitric oxide: Evidence for the involvement of 9-nitriosothiols as active intermediates[J]. J Pharmacol Exp Ther, 1981, 218(3):739~49.
[9]Garg UC, Hassid A. Nitric oxide-generating vasodilators and 8-Bromo-cyclic guanosine monophosphate inhibit mitogenesis and proliferation of cultured rat vascular smooth muscle cells[J]. J Clin Invest, 1989, 83(5):1774~7.
1999-02-20, 百拇医药
单位:田雪梅(第一军医大学组织胚胎学教研室,广东 广州 510515);马晓东(第一军医大学中心实验室,广东 广州 510515);李进(第一军医大学组织胚胎学教研室,广东 广州 510515)
关键词:一氧化氮;血管平滑肌细胞;细胞凋亡
第一军医大学学报000105 摘要:目的 研究动脉粥样硬化和冠脉气囊成形术后再狭窄中血管平滑肌细胞数量异常增多的机制,并初步探讨NO诱导血管平滑肌细胞凋亡的作用。材料和方法 以SNAP作为NO供体,采用HE,TUNEL,荧光双染后光镜观察以及电镜、流式细胞术、细胞DNA的琼脂糖凝胶电泳对SNAP作用下的细胞凋亡进行鉴定和检测。结果 观察发现,0.4 mmol/L SNAP作用8~10 h即能明显地诱导培养的血管平滑肌细胞凋亡。结论 SNAP以浓度依赖方式诱导血管平滑肌细胞凋亡,细胞爬片的HE染色结合TUNEL标记是检测凋亡的较为准确且简单的方法。
, http://www.100md.com
中图分类号:Q571; Q461 文献标识码:A 文章编号:1000-2500(2000)01-0015-04
Nitric oxide induced apoptosis in vascular smooth muscle cells
TIAN Xue-mei LI Jin
(Department of Histology and Embryology, First Military Medical University, Guangzhou 510515, China)
MA Xiao-dong
(Central Laboratory, First Military Medical University, Guangzhou 510515, China)
, 百拇医药
Abstract: Objective To further study the significant number increase of vascular smooth muscle cells in atherosclerosis and resterosis. We investigated the effect of NO on the induction of apoptosis in cultured vascular smooth muscle cells. Methods SNAP was used as NO donor. HE, TUNEL, double fluorescent staining and electronic microscopy, flow cytometry, agarose gel electrophoresis of DNA were employed to detect and observe cell apoptosis. Result Vascular smooth muscle cells showed apoptosis when treated with 0.4 mmol/L SNAP for 8 to 10 hours. Conclusions The results indicated that SNAP dose-dependently induce apoptosis in VSMC, and HE staining along with TUNEL was a simple method to observe and detect apoptosis in cells cultured on slide. To further study the significant number increase of vascular smooth muscle cells in atherosclerosis and resterosis. We investigated the effect of NO on the induction of apoptosis in cultured vascular smooth muscle cells. Methods SNAP was used as NO donor. HE, TUNEL, double fluorescent staining and electronic microscopy, flow cytometry, agarose gel electrophoresis of DNA were employed to detect and observe cell apoptosis. Result Vascular smooth muscle cells showed apoptosis when treated with 0.4 mmol/L SNAP for 8 to 10 hours. Conclusions The results indicated that SNAP dose-dependently induce apoptosis in VSMC, and HE staining along with TUNEL was a simple method to observe and detect apoptosis in cells cultured on slide.
, 百拇医药
Key words: nitric oxide; vascular smooth muscle cell; apoptosis
动脉粥样硬化(Atherosclerosis,AS)病变中,血管平滑肌细胞(Vascular smooth muscle cell,VSMC)异常增殖是血管壁增厚的主要原因。在VSMC增殖的同时,VSMC也有凋亡发生。两者间的平衡状态直接影响VSMC的数量,并最终决定血管壁的厚度和血管腔的大小[1]。VSMC 凋亡又能引起AS斑块的不稳定。此外,凋亡的VSMC可激活凝血酶等血栓形成物质,促进血栓形成。一氧化氮(Nitric oxide,NO)广泛存在于心血管系统中,具有多种生物效应[2-5]。NO诱导细胞凋亡是对NO作用的新认识[6]。本实验拟从NO诱导VSMC凋亡的作用方面进行研究。而VSMC凋亡模型的建立及检测方法的确定是进行VSMC凋亡研究的前提。因此,本实验建立NO诱导VSMC凋亡的模型,并通过HE染色、荧光双染法、流式细胞术、原位末端标记、透射电镜观察、DNA琼脂糖凝胶电泳几种方法,对VSMC凋亡进行观察和检测。
, 百拇医药
1 材料和方法
1.1 材料
Sprague Dawley(SD)大鼠;DMEM培养基(GIBCO BRL公司),小牛血清(杭州四季青生物工程材料研究所),牛血清白蛋白(天象人生物工程有限公司),胰蛋白酶(国产),亚硝基乙酰青霉胺(S-Nitroso-N-acetylpenicillamine, SNAP,Sigma),硝普钠(Sodium nitroprusside, SNP,国产), 丫啶橙(AO)、溴化乙锭(EB)、碘化丙锭(PI)(国产),TUNEL试剂盒(Boehringer Mannheim)。
1.2 方法1.2 方法
1.2.1 VSMC培养 采用贴块法[1]。无菌条件下分离大鼠的胸主动脉,去除内外膜,将中膜平滑肌组织块剪碎,接种于培养瓶内,加入含20% 小牛血清的DMEM培养液,在37℃、5% CO2 培养箱中静置培养。待细胞生长达汇合,用0.25% 胰蛋白酶消化传代,用含10~15%小牛血清的培养液继续培养。第4、5代细胞用抗α-actin肌动蛋白抗体免疫组化法进行鉴定。实验用第5~8代细胞。
, 百拇医药
1.2.2 细胞爬片制作 将5~10代细胞用胰蛋白酶消化,制成密度为104~105/ml的细胞悬液。滴加细胞悬液于盖玻片上。2~6 h后,细胞贴壁,补加培养基。待细胞生长达50%~60%,用无血清DMEM培养液洗2次,再加条件培养液,继续培养24~48 h,然后加含0.08~1.0 mmol/L SNAP或SNP的条件培养液。继续培养2~24 h (2 h,6 h,8 h,10 h,12 h,24 h),收集盖片,4%多聚甲醛固定,存放。
1.2.3 细胞爬片进行常规HE染色。
1.2.4 荧光双染色 细胞爬片经PBS洗后,滴加100 mg/L AO染液和100 mg/L EB染液,避光染色,PBS漂洗,湿封盖片于载玻片上。荧光显微镜下,388 nm紫外光激发进行观察。
1.2.5 原位末端标记 按TUNEL试剂盒说明书操作。
, 百拇医药
1.2.6 透射电镜样品制备 细胞接种于培养瓶中,生长达50%~60% 时,换成条件培养液培养24~48 h后,加含SNAP的条件培养液,使SNAP终浓度为1.0 mmol/L,培养8~10 h,收集细胞;按常规透射电镜样品制作法做透射电镜切片并观察。
1.2.7 凋亡细胞DNA的琼脂糖凝胶电泳 细胞接种于培养瓶中,分别经1.0 mmol/L的SNAP和 SNP处理,方法同前。收集细胞,提取细胞DNA。
1.2.8 流式细胞仪(FCM)检测 细胞接种于培养瓶中,经不同浓度的SNAP分别作用8 h、12 h后,收集细胞;800~1000 r/min离心10 min;75% 的冷乙醇固定,4℃冰箱或-20℃存放。经固定的细胞,离心,弃去固定液;用PBS洗2遍;加RNase(终浓度为2 μg/ml),于37℃水浴30 min加入含50 mg/L PI的PBS溶液 1 ml,37℃下孵育30 min;细胞悬液过400目尼龙膜以除去杂质及细胞团,上机检测。FCM自动去本底,选用488 nm波长激发光激发荧光,测定样品。LysysⅡ软件分析结果。
, 百拇医药
2 结果
2.1 VSMC培养
贴块法培养的VSMC,倒置显微镜观察,4~7 d即有细胞从组织快周围爬出,并且细胞生长呈典型的“谷和峰”状态,第4、5代细胞,抗α-actin抗体组化检测鉴定95%以上为VSMC。
2.2 VSMC凋亡的形态观察
2.2.1 培养过程中细胞的形态变化 0.04~1 mol/ L范围内不同浓度的SNAP处理细胞。1 h后,倒置显微镜下即可见,有的细胞开始与相邻细胞脱离联系,逐渐变圆,胞质凝集,体积缩小。随时间延长,变圆的细胞皱缩,体积更小,最终脱离附着面,漂浮于培养液中,但始终保持完整的形状。

图1 细胞爬片的HE染色
, 百拇医药
Fig.1 VSMCS cultured on glass slides were stained with HE. Cells exhibit neclear chromatin condensation, cell rounding, membrane blebbing and fragmented nuclear. ×200

图2 细胞爬片的AO和EB染色
Fig. 2 Cell slide stained with AO and EB. Showing apoptotic cells and normal cells. ×40

图3 VSMC的电镜观察
, http://www.100md.com
Fig.3 Electron microscopic appearance of apoptosis or necrosis in VSMCs. A .chromatin condensation at the periphery of the nucleus;B. Formation of membrane-bound vesicles

图4 细胞爬片的TUNEL染色
Fig.4 Detection of apoptotic VSMCs with TUNEL VSMCs cultured on glass slide were treated with 0.4 mmol/L SNAP for 8 to 10 h. ×100
2.2.2 HE染色显示凋亡细胞的形态变化 细胞爬片经HE染色,SNAP处理后的VSMC,可以看到染色质边集,核固缩,核碎裂等凋亡细胞核的特征性变化(图1)。
, http://www.100md.com
2.2.3 荧光双染色区分死亡细胞与凋亡细胞 经AO和EB双染后,能够区分3种不同状态的细胞。正常活细胞,细胞核染成绿色,核呈椭圆,核质均匀,核仁黄色或橙红色清晰可见,胞质为橙色或黄色;死亡细胞显橙色;凋亡细胞可见两种状态:一种细胞核固缩成球状,呈绿色、黄色或橙色,胞质黄色,细胞尚未变圆;另一种细胞发橙黄色荧光,细胞内可见1至数个大小不等的球状小体,为碎裂的细胞核(图2)。
2.2.4 VSMC的超微结构 电镜观察(图3),凋亡细胞的核染色质边集、凝集及核碎裂。胞质内分布着大小不同的腔扩大了的内质网,其中含有均质的内容物,仍可见粗面内质网膜上均匀分布着的核糖体颗粒,线粒体的形态也保持完整,线粒体嵴清晰可见。可见凋亡小体形成,线粒体等细胞内容物被膜包裹。
2.3 凋亡细胞DNA断裂分析2.3 凋亡细胞DNA断裂分析
2.3.1原位末端标记 经TUNEL染色,凋亡细胞呈黄色/棕黄色,核着色深,大部细胞的胞质也有着色。收缩变圆的细胞几乎均呈阳性染色,为凋亡细胞(图4)。SNP处理的细胞TUNEL染色为阳性的少。TUNEL染色结果及前述形态观察都显示,凋亡细胞的数量随SNAP浓度升高,有较为显著的增加;而同一浓度SNAP作用下,2~8 h孵育,凋亡细胞数量渐增加。但8 h、10 h与12 h处理相比,凋亡细胞增加不明显。
, 百拇医药
2.3.2 琼脂糖凝胶电泳 SNP处理,细胞DNA电泳呈弥散状的细胞坏死特征,1.0 mmol/L SNAP 处理后,DNA电泳呈凋亡细胞特有的梯状带;而0.08 mmol/L SNAP处理后,大多数细胞DNA仍完整(图5)。
2.4流式细胞仪检测2.4流式细胞仪检测
流式细胞仪检测结果发现,0.08、0.10、0.30、0.50、1.0 mmol/L SNAP作用8 h后,细胞凋亡率分别为5.9%、8.1%、13.5%、22.5%、42.7%, 随浓度增加,凋亡细胞的数量增多;12 h作用,结果相似。而同一浓度SNAP处理8 h、12 h,凋亡细胞数量差别不明显,如0.08 mmol/L SNAP作用8 、12 h后,细胞凋亡率分别为5.9%,6.3% 。表明8 h以后,细胞凋亡不再随作用时间增加而明显增多,与形态观察的结果一致。

, 百拇医药
图5 死亡细胞DNA的琼脂糖凝胶电泳结果
Fig.5 Agarose gel electrophoresis of DNA isolated from dying cells treated with SNAP or SNP for 8 h
3 讨论
组织贴块法培养VSMC是一种经济方便的方法。但缺点在于培养过程中血管外膜不能绝对被去除干净,因而有一些成纤维细胞混杂于VSMC中长出。但由于成纤维细胞易于脱壁,在连续的传代培养过程中可以不断地被清除。一般到第5代时,成纤维细胞几近绝迹,此时,VSMC的性状较为稳定。而当传代培养10代以上,部分VSMC将会转变为多倍体。因此,本实验选择5~8代细胞进行实验。
检测细胞凋亡的方法有多种。其中HE染色最为简便。经HE染色能清晰地观察到凋亡过程中细胞变圆、皱缩,细胞核染色质边集、核固缩、核碎裂形成凋亡小体等形态变化。凋亡早期的细胞和某些处于分裂期的细胞有相似的形态变化:细胞变圆,染色质浓缩聚集而使核深染。荧光染料染色则能够更突出的显示细胞核的形态,但是,使用一种荧光染料染色,不易分辨坏死细胞与凋亡细胞。经过使用AO与EB两种DNA染料混合染色,根据细胞的着色情况,能分辩正常细胞、坏死细胞和凋亡细胞。AO为膜通透性染料,它能进入活细胞,与细胞核内DNA结合,发出绿色荧光,与胞质内RNA结合发出橙色或黄色荧光;而EB只能进入膜结构改变了的坏死细胞,将细胞核染成红色;凋亡早期的细胞,膜结构完整,EB不能进入,核显绿色;而凋亡晚期的细胞,细胞膜受损,被AO和EB复合染色,细胞核被染成橙色、橙红色。但是荧光染色不易控制。透射电镜能最清楚地观察到凋亡细胞的形态,特别是胞核的形态变化。
, 百拇医药
经PI使细胞内DNA染色后,借助流式细胞仪进行检测,可以根据G1期峰旁是否出现一个不连续的亚(次)二倍体峰来确定细胞凋亡,并可得出细胞凋亡率。
细胞核内DNA被内源性核酸内切酶降解,形成180~200 bp及其倍数的DNA片段,在琼脂糖凝胶电泳中表现为DNA梯状带,为细胞凋亡最具特征性的变化[7]。DNA断裂为核苷片段常发生于细胞核形态变化之前[8]。原位末端标记法则能灵敏地检测到DNA链的轻微损伤。细胞凋亡时,核DNA被切割而断裂,产生3’-OH末端,TUNEL法则借助dT将标记的dUTP掺入3’-OH,其特异性高,优先标记凋亡细胞并能够识别凋亡早期的细胞,弥补了HE染色和荧光染色等方法的不足。实验中发现HE染色显示凋亡细胞形态,并结合TUNEL法鉴定是检测细胞凋亡最简便可靠的方法。
SNAP在溶解状态下能自发地释放NO。荧光双染色、TUNEL及DNA电泳结果指出,SNAP作用下细胞主要以凋亡形式死亡。SNAP在溶解状态下不稳定,半衰期在5 h以内,它最终降解为青霉胺、NaNO2和NaNO3[8]。1 mmol/L溶液中的SNAP,3 d后就会完全降解[9]。这可以解释SNAP处理过程中,8~10 h以后,VSMC凋亡不再随时间延长而有明显增加的现象。实验中观察到SNAP诱导VSMC凋亡具有浓度依赖性。经形态学观察及DNA断裂检测,实验中选择SNAP为诱导VSMC凋亡的NO供体,8~10 h为最佳作用时间。实验中还发现高浓度的SNAP诱导VSMC凋亡的效果更明显。这可能是因为NO在高氧环境中易于氧化而损耗所致。但在体内组织中O2浓度低,并且周围细胞能持续地释放NO,可能使局部保持较高的NO浓度。因此,在体内有存在高浓度NO的可能性。
, http://www.100md.com
参考文献
[1]Han DK, Haudenschild CC, Hong MK et al. Evidence for apoptosis inhuman atherogensis and in a rat vascular injury model[J]. Am J Pathol, 1995, 147(2):267~77.
[2]Naito M, Hayashi H, Iguchi A. New approaches to the prevention of atherosclerosis[J]. Drugs, 1995, 50(3):440~53.
[3]Loscalzo J, Welch G. Nitric oxide and its role in the cardiovascular system[J]. Progress in cardiovascular Disease, 1995, 38(2):87~104.
, 百拇医药
[4]Sarker R, Meinberg EG, James G et al. Nitric oxide reversibly inhibits the migration of cultured vascular smooth muscle cells[J]. Circ Res, 1996, 78:225~30.
[5]Fukuo K, Hata S Suhara T et al. Nitric oxide mduces upregulation of Fas and apoptosis in vascular smooth muscle[J]. Hypertension, 1996, 27(Part 2):823~6.
[6]Ross R. The smooth muscle cell. Ⅱ. Growth of smooth muscle in culture and formation of elastic fibers[J]. J Cell Biol, 1971, 50(1):63~8.
, 百拇医药
[7]Compton MA. Biochemical hallmark of apoptosis: internucleosomal degradation of the genome[J]. Cancer Metastasis Rev, 1992, 11(1): 105~9.
[8]Ignarro LJ, H. Lippton JC, Edwards et al. Mechanism of vascular smooth muscle relaxation by organic nitrates, nitrites, nitroprusside and nitric oxide: Evidence for the involvement of 9-nitriosothiols as active intermediates[J]. J Pharmacol Exp Ther, 1981, 218(3):739~49.
[9]Garg UC, Hassid A. Nitric oxide-generating vasodilators and 8-Bromo-cyclic guanosine monophosphate inhibit mitogenesis and proliferation of cultured rat vascular smooth muscle cells[J]. J Clin Invest, 1989, 83(5):1774~7.
1999-02-20, 百拇医药