葛黄注射液质量控制研究
作者:黄亚非 张永明 陈建萍
单位:黄亚非 张永明(中山医科大学第三附属医院 广州 510630);陈建萍(中山医科大学中西医结合研究所)
关键词:葛黄注射液;质量控制;大黄素
中草药000111摘 要 采用薄层鉴别法对葛黄注射液进行定性,并采用分光光度法测定该药中大黄素的含量。回收率为102.29 %,RSD为0.20 %。此方法的重现性好,可作本品的质量控制标准。
Studies on the Quality Control of Gehuang Injection
Huang Yafei and Zhang Yongming
The Third Hospital Affiliated in Sun Yat-sen University of Medical Sciences (Guangzhou 510630)
, 百拇医药
Chen Jianping
Institute of Combination of Chinese Traditional and Western Medicine in Sun Yat-sen University of Medical Sciences
Abstract TLC was used to determine the chemical compostition of Gehuang injection, and spectrophotometry was used for quantitative determination of emodin in Gehuang injection. The recovery was 102.29 %, and RSD 0.20 %, with good reproducibility and can be used for the quality control of the injection.
, 百拇医药
Key words Gehuang injection quality control emodin▲
葛黄注射液由大黄、葛根等药物组成,具有清热解毒,通腑泻热,兼有活血化瘀的作用。可用于治疗各种温热性疾病,我院临床上用于以发热为主的温热性疾病,症见发热、口角生疮、大便秘结、舌质红或有瘀点或瘀斑、脉数等。
方中主要药物为大黄,其具有生物活性的成分主要有[1]:蒽醌衍生物类包括游离蒽醌类(大黄素、大黄酸、大黄酚、大黄素甲醚、芦荟大黄素)和结合蒽醌类(番泻苷A,B,C,D,E,F以及大黄苷A,B,C,D)等。本实验以大黄素为定性及含量测定的对象,作为质控指标。
1 仪器与试药
GW-752紫外分光光度仪,硅胶G(青岛海洋化工厂),葛黄注射液(自制品),对照品由中国药品生物制品检定所提供。所用试剂均为分析纯。
, 百拇医药
2 方法与结果
2.1 定性鉴别[2]:取葛黄注射液4 mL蒸干,用适量的甲醇充分振摇溶解,滤过,取滤液定容作供试品;取大黄对照药材、大黄素、大黄酸、大黄酚为对照品,用甲醇提取定容,吸取一定量上述溶液,点于硅胶G板上(自制)。展开剂:正己烷-乙酸乙酯-甲酸(26∶10∶0.5)上行展开,展距为8 cm,展开后取出,晾干,置紫外灯(365 nm)下检视,供试品色谱在对照品色谱相应的位置上显相同颜色的荧光斑点,结果如图1。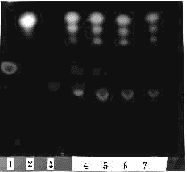
1-大黄素 2-大黄酚 3-大黄酸 4-大黄对照药材 5-样1 6-样2 7-样3
图1 样品TLC图
2.2 含量测定[3]:比色波长的选择:按标准曲线制备项下方法,将待测液于GW-752紫外分光光度仪在495,500,505,510,520,535 nm处测定其吸收度,结果表明λmax为510 nm。
, 百拇医药
2.2.1 标准曲线的制备[4]:精密称取在105 ℃干燥至恒重的大黄素对照品10 mg,置100 mL量瓶中,加甲醇使溶解,并稀释至刻度,摇匀,即得0.1 mg/mL的对照溶液。精密吸取对照溶液1.0,2.0,3.0,4.0,5.0 mL分别置于25 mL容量瓶中,加1%醋酸镁甲醇溶液10 mL,加甲醇至刻度,以甲醇做空白,510 nm波长处测定吸光度,测定结果见表1。
表1 不同量的对照溶液吸光值变化 取样量(mL)
含量(μg/mL)
吸光值
1.0
4.0
0.164 3
2.0
, http://www.100md.com
8.0
0.296 6
3.0
12.0
0.458 7
4.0
16.0
0.602 0
5.0
20.0
0.762 7
大黄素浓度与吸光度关系方程为C=26.601 5X-0.153 2,r=0.999 5,线性范围2.0~40.0 μg/mL。
, 百拇医药
2.2.2 半成品中大黄素的含量测定:从3批半成品中分别精密称取该品一定量,蒸干,加入适量(约20 mL)的甲醇使之溶解,再置分液漏斗中,用30,20,10 mL氯仿数次萃取至氯仿层无色,收集氯仿层,回收氯仿,然后用少量甲醇洗涤残渣数次,转移入100 mL容量瓶中,再加50 mL 1 %醋酸镁甲醇液,再用甲醇定容至刻度,用力摇匀。放置30 min后,以甲醇作空白对照,于510 nm处测定吸光度,将吸光度值代入标准曲线计算含量,结果见表2。表2 大黄提取物总固体量和大黄素含量 试验号
总固体(g/100 g生药)
大黄素含量(μg)
(%)
1
2.271 3
237 307.266 4
, 百拇医药
10.448
2
2.692 1
285 042.386 7
10.588
3
2.531 5
265 035.353 3
10.469
2.2.3 回收率测定:准确称取该品,蒸干,再准确取1.1 mg大黄素对照品加入其中混和,用适量甲醇溶解,后按照上述含量测定方法测定大黄素含量。结果3批实验平均回收率为109.39%,RSD=0.36%;94.60%,RSD=0.11%;102.97%,RSD=0.14%。
, 百拇医药
2.2.4 精密度、重复性试验:准确称取该品,蒸干,按上述含量测定方法测定吸光度,计算大黄素含量。平行操作6次,结果RSD=1.13%;仪器精密度RSD=0.29%,表明取样精密度、仪器精密度、重复性良好。
2.2.5 稳定性试验:准确称取该品,蒸干,按含量测定方法测定吸光度。每隔30 min测定一次,结果3 h内稳定,RSD=0.13%。说明大黄成分稳定,在此时间范围内测定误差较小。
从以上对半成品的鉴别和检查认为半成品已经符合配液要求,可用于下一步的配液研究。
3 讨论
3.1 此注射液主要用于治疗温热性疾病的初、中期,清热解毒、退高热。其中的游离蒽醌类成分特别是大黄素、大黄酸、芦荟大黄素的药理作用较强,因此可用大黄素含量来代表这类成分的含量。
, http://www.100md.com 3.2 质量控制用紫外分光光度法进行,方法简便易行,可作为生产单位应用。■
黄亚非:Address:Huang Yafei, Affiliated Third Hospital, Sun Yatsen University of Med
ical Sciences, Guangzhou
参考文献
1,楼之岑.北京医科大学学报,1993,(增刊):2
2,中华人民共和国药典中药薄层色谱色图集.1993:23
3,芦喜珍.中国医院药学杂志,1994,14(8):376
4,徐韧柳,等.中国实验方剂学杂志,1998,4(3):9
(1999-06-25 收稿), http://www.100md.com
单位:黄亚非 张永明(中山医科大学第三附属医院 广州 510630);陈建萍(中山医科大学中西医结合研究所)
关键词:葛黄注射液;质量控制;大黄素
中草药000111摘 要 采用薄层鉴别法对葛黄注射液进行定性,并采用分光光度法测定该药中大黄素的含量。回收率为102.29 %,RSD为0.20 %。此方法的重现性好,可作本品的质量控制标准。
Studies on the Quality Control of Gehuang Injection
Huang Yafei and Zhang Yongming
The Third Hospital Affiliated in Sun Yat-sen University of Medical Sciences (Guangzhou 510630)
, 百拇医药
Chen Jianping
Institute of Combination of Chinese Traditional and Western Medicine in Sun Yat-sen University of Medical Sciences
Abstract TLC was used to determine the chemical compostition of Gehuang injection, and spectrophotometry was used for quantitative determination of emodin in Gehuang injection. The recovery was 102.29 %, and RSD 0.20 %, with good reproducibility and can be used for the quality control of the injection.
, 百拇医药
Key words Gehuang injection quality control emodin▲
葛黄注射液由大黄、葛根等药物组成,具有清热解毒,通腑泻热,兼有活血化瘀的作用。可用于治疗各种温热性疾病,我院临床上用于以发热为主的温热性疾病,症见发热、口角生疮、大便秘结、舌质红或有瘀点或瘀斑、脉数等。
方中主要药物为大黄,其具有生物活性的成分主要有[1]:蒽醌衍生物类包括游离蒽醌类(大黄素、大黄酸、大黄酚、大黄素甲醚、芦荟大黄素)和结合蒽醌类(番泻苷A,B,C,D,E,F以及大黄苷A,B,C,D)等。本实验以大黄素为定性及含量测定的对象,作为质控指标。
1 仪器与试药
GW-752紫外分光光度仪,硅胶G(青岛海洋化工厂),葛黄注射液(自制品),对照品由中国药品生物制品检定所提供。所用试剂均为分析纯。
, 百拇医药
2 方法与结果
2.1 定性鉴别[2]:取葛黄注射液4 mL蒸干,用适量的甲醇充分振摇溶解,滤过,取滤液定容作供试品;取大黄对照药材、大黄素、大黄酸、大黄酚为对照品,用甲醇提取定容,吸取一定量上述溶液,点于硅胶G板上(自制)。展开剂:正己烷-乙酸乙酯-甲酸(26∶10∶0.5)上行展开,展距为8 cm,展开后取出,晾干,置紫外灯(365 nm)下检视,供试品色谱在对照品色谱相应的位置上显相同颜色的荧光斑点,结果如图1。

1-大黄素 2-大黄酚 3-大黄酸 4-大黄对照药材 5-样1 6-样2 7-样3
图1 样品TLC图
2.2 含量测定[3]:比色波长的选择:按标准曲线制备项下方法,将待测液于GW-752紫外分光光度仪在495,500,505,510,520,535 nm处测定其吸收度,结果表明λmax为510 nm。
, 百拇医药
2.2.1 标准曲线的制备[4]:精密称取在105 ℃干燥至恒重的大黄素对照品10 mg,置100 mL量瓶中,加甲醇使溶解,并稀释至刻度,摇匀,即得0.1 mg/mL的对照溶液。精密吸取对照溶液1.0,2.0,3.0,4.0,5.0 mL分别置于25 mL容量瓶中,加1%醋酸镁甲醇溶液10 mL,加甲醇至刻度,以甲醇做空白,510 nm波长处测定吸光度,测定结果见表1。
表1 不同量的对照溶液吸光值变化 取样量(mL)
含量(μg/mL)
吸光值
1.0
4.0
0.164 3
2.0
, http://www.100md.com
8.0
0.296 6
3.0
12.0
0.458 7
4.0
16.0
0.602 0
5.0
20.0
0.762 7
大黄素浓度与吸光度关系方程为C=26.601 5X-0.153 2,r=0.999 5,线性范围2.0~40.0 μg/mL。
, 百拇医药
2.2.2 半成品中大黄素的含量测定:从3批半成品中分别精密称取该品一定量,蒸干,加入适量(约20 mL)的甲醇使之溶解,再置分液漏斗中,用30,20,10 mL氯仿数次萃取至氯仿层无色,收集氯仿层,回收氯仿,然后用少量甲醇洗涤残渣数次,转移入100 mL容量瓶中,再加50 mL 1 %醋酸镁甲醇液,再用甲醇定容至刻度,用力摇匀。放置30 min后,以甲醇作空白对照,于510 nm处测定吸光度,将吸光度值代入标准曲线计算含量,结果见表2。表2 大黄提取物总固体量和大黄素含量 试验号
总固体(g/100 g生药)
大黄素含量(μg)
(%)
1
2.271 3
237 307.266 4
, 百拇医药
10.448
2
2.692 1
285 042.386 7
10.588
3
2.531 5
265 035.353 3
10.469
2.2.3 回收率测定:准确称取该品,蒸干,再准确取1.1 mg大黄素对照品加入其中混和,用适量甲醇溶解,后按照上述含量测定方法测定大黄素含量。结果3批实验平均回收率为109.39%,RSD=0.36%;94.60%,RSD=0.11%;102.97%,RSD=0.14%。
, 百拇医药
2.2.4 精密度、重复性试验:准确称取该品,蒸干,按上述含量测定方法测定吸光度,计算大黄素含量。平行操作6次,结果RSD=1.13%;仪器精密度RSD=0.29%,表明取样精密度、仪器精密度、重复性良好。
2.2.5 稳定性试验:准确称取该品,蒸干,按含量测定方法测定吸光度。每隔30 min测定一次,结果3 h内稳定,RSD=0.13%。说明大黄成分稳定,在此时间范围内测定误差较小。
从以上对半成品的鉴别和检查认为半成品已经符合配液要求,可用于下一步的配液研究。
3 讨论
3.1 此注射液主要用于治疗温热性疾病的初、中期,清热解毒、退高热。其中的游离蒽醌类成分特别是大黄素、大黄酸、芦荟大黄素的药理作用较强,因此可用大黄素含量来代表这类成分的含量。
, http://www.100md.com 3.2 质量控制用紫外分光光度法进行,方法简便易行,可作为生产单位应用。■
黄亚非:Address:Huang Yafei, Affiliated Third Hospital, Sun Yatsen University of Med
ical Sciences, Guangzhou
参考文献
1,楼之岑.北京医科大学学报,1993,(增刊):2
2,中华人民共和国药典中药薄层色谱色图集.1993:23
3,芦喜珍.中国医院药学杂志,1994,14(8):376
4,徐韧柳,等.中国实验方剂学杂志,1998,4(3):9
(1999-06-25 收稿), http://www.100md.com