p14ARF������������ϸ����ֳ���о������������ڡ�л������������
���ߣ�
��λ��������(����ҽѧ��ѧԺ����ҽѧ�о���,���� 100850)������(��ž���ҽԺ���Ǻ���,���� 100853)��л����(������ͯҽԺѪ����,���� 100045)��������(����ҽѧ��ѧԺ����ҽѧ�о���,���� 100850)
�ؼ��ʣ�p14ARF���������ƣ�p53����ҩ����ϸ��
��֢000202
��ժ Ҫ��Ŀ��:�������˸�ϸ��ϵL02ϸ���������˵��������ƻ���p14ARF�����о�����˵Ķ�������ϸ��������Ӱ�졣����:Ӧ��RT-PCR�������������������˸�ϸ��ϵL02ϸ����������0.4Kb��p14ARFcDNAƬ�Σ�������ȷ�������˱�������pcDNA3�ϵ�BamHI��EcoRIλ�㣬����ΪpcDNA3ARF����������֬����LipofectamineTM�鵼תȾ����ϸ��Hep2��KB��KB-v200��HepG2��HLE��Huh7�Լ�MCF7��MCF7/ADR����G418ɸѡ2�ܺ�ͳ���γɵļ����������:��������G418ɸѡ2�ܺ���p53���Ե�����ϸ��HepG2��Hep2��MCF7�γɵļ��������٣��ֱ�Ϊ59��2.1,60��2.1��66��7.0��ռ���Զ������47%��57%��58%����p53�쳣������ϸ��KB,HLE,Huh-7�����γ���Խ϶�ļ��䣬�ֱ�Ϊ91��2.5,48��2.0,41��2.0��ռ���Զ������74%��65%��80%,���Ƕ���p53�쳣����ҩ����ϸ����KB-v200��MCF7/ADR,�γɵļ��������٣��ֱ�Ϊ13��2.0��21��1.5��ռ����תȾ������pcDNA3�Ķ������15%��17%������:p14ARF����������p53��������ϸ��������������p53�����;Ȼ��p14ARF��p53���Ե���ҩ����ϸ��ȴ����ǿ�ҵ��������ã��ɴ���ʾ:p14ARF������ҩ����ϸ����������p53�������Ե�(��������������ҩ����ϸ����)��
, http://www.100md.com
��ͼ����ţ�R735.5 ���ױ�ʶ�룺A
���±�ţ�1000-467X(2000)02-0104-04
Transfer of p14ARF gene in human tumor cell lines inhibits cell proliferation
FAN Guo-chang
(Beijing Institute of Radiation Medicine,Beijing 100850, P.R.China)
LEI Lei
(PLA General Hospital,Beijing 100853, P.R.China)
, http://www.100md.com
XIE Jian-jun
(Beijing Children Hospital,Beijing 100045, P.R.China)
��Abstract�� Objective: To clone p14ARF gene from cells of the human normal liver cell line L02 and explore its inhibitory effect on tumor cell proliferation. Methods: p14ARF cDNA was cloned from L02 cells by using RT- PCR method and inserted into the BamHI and EcoRI sites of pcDNA3 (called pcDNA3ARF). Lipofectamine mediated pcDNA3ARF was transferred into tumor cell lines, such as Hep2, KB, KB- v200, HepG2, HLE, Huh7, MCF7 and MCF7/ADR. The number of colonies of these tumor cell lines were calculated after more than two weeks' screening in DMEM medium containing G418. Results:The colony-forming efficiency of the p14ARF -transfected KB-v200 and MCF7/ADR drug-resistant cells was 13�� 2.0 and 21�� 1.5 , respectively, compared with 86�� 3.1(15% )and 126�� 7.5(17% )in the cells transfected with empty vector pcDNA3, and in the p53 positive tumor cell lines, such as HepG2(47% ), Hep2(57% ), MCF7(58% ) cells, the inhibition was also found�� whereas in the p53 negative tumor cell lines, such as KB(74% ), HLE(65% ), Huh-7(80% ) cells, the inhibitory effect was milder. Conclusions: p14ARF can suppress the growth of the p53 positive tumor cell lines in a p53-relevant manner, while in the p53 negative, drug-resistant tumor cells, p14ARF has strong inhibitory effect, indicating the inhibitory effect of p14ARF on growth of drug-resistant tumor cells is independent on p53, at least in KB-v200 and MCF7/ADR drug-resistant cells.
, http://www.100md.com
Key words��p14ARF; Tumor growth suppress; p53; Drug-resistant tumor cells
ϸ�����ڵĵ����������ͬ������ɵĶ���ͨ·����ɵġ�����������ϸ���У������ļ��ֻ�������ͻ�䣬��Щ�������p53,RB,INK4��/ARF�ȡ�Ȼ��,�������ǹ��ɵ���������ͨ·��RBͨ·(p16INK4��-RB)��p53ͨ·(ARF-p53)�ڵ����������������Ĺ��������Źؼ������ã�����RBͨ·�е�INK4��(p16INK4��)��p53ͨ·�е�p53�Ǿ��������ı����������[1,2]��RBͨ·�����������ƹ��ܣ���ͨ������ϸ��G1-S�ڱ�������ת¼���Ӷ���ϸ��������G1�ڣ�p53ͨ·��������������ϸ������������ϸ����G1�ڣ�����Ҫ������ϸ�����ͺ�ϸ��״̬��p53��Ϊ˳ʽ�������Ӻ�ϸ����������������ã����ղ����������ƹ��ܡ�����о�����[3]��������;��ͨ��INK4��/ARF(9p21)λ�����ϵ��������λ��ͨ����ͬ���Ķ���ܶ��������ֲ�ͬ���������Ƶ��ף�p16��p14ARF(���ͬԴ��Ϊp19ARF)������p16INK4����������ϸ����ֳ������Ƶ��о������кܶ౨������Ŀǰ�й�p14ARF����ʶ����Դ�����p19ARF[4]����˱��Ĵ������˸�ϸ��ϵL02ϸ���У�RT-PCR������0.4kb����p14ARF�������о�����˵Ķ�������ϸ��������Ӱ�졣
, ��Ĵҽҩ
1 �����뷽��
1.1 ϸ��ϵ
L02����������ϸ��ϵ��Hep2���˺��۰�ϸ��ϵ��KB���˱��ʰ�ϸ��ϵ��KB-v200�����ʰ������¼���ҩ�ꣻHepG2��HLE��Huh-7���˸ΰ�ϸ��ϵ��MCF-7�������ٰ�ϸ��ϵ��MCF-7/ADR�����ٰ���ù����ҩ�ꡣ����ϸ��ϵ����ҩϸ�������������37�桢5%CO2������,��10%̥ţѪ��ĸ���DMEM������(Gibco/BRL)��;KB-v200ϸ������������Ҫ����������Һ������80nmol/ml�����¼�,MCF-7/ADRϸ������������Ҫ����8��g/ml��ù��,ʵ��ǰһ�ܳ�ȥҩ�
1.2 p14ARF����Ŀ�¡����˱�������Ĺ���
1.2.1 һ���������ѧ��������:�����淽��[5]���У�һЩ��������ѧ����ø��ΪPromega��˾��Ʒ������ĺϳɼ����вⶨ�ɴ��������﹤�̹�˾��ɡ�
, http://www.100md.com
1.2.2 RNA����ȡ��RT-PCR��Ӧ:��ø��������״̬���õ�L02ϸ���������ռ��������PBSϴ���Σ��ٰ�RNA��ȡ�Լ��в���������ȡϸ����RNA��ȡ��RNA1��g������Oligo(dT)����1��g����20��l�����42������ת¼��Ӧ��ȡ5��l��ת¼����Ϊģ�壬����PCR��Ӧ������PCR��Ӧ�������£�94�棬1min;50��,1min;72��,1.5min;5��ѭ����94�棬1min;60��,1min;72��,1.5min;35��ѭ����72������10min��AMV��ת¼ø��Taqø��ΪPromega��˾��Ʒ��p14ARF������������£�
�������5'��GGC GGA TCC ATG GTG CGC AGG TTC T-3'
�������5'��CCG AAT TCT CAG CCA GGT CCA CG-3'
1.2.3 p14ARFcDNA�������弰��˱�������Ĺ���:����RT��PCR������Wizard Plus Minipreps DNA Purification System(Promega��˾)���մ���������BamHI��EcoRIø�У�1.5%����֬��������Ӿ���մ�ø�е�0.4kbp14ARF cDNA����¡������pSK��BamHI��EcoRIλ�㣬����ΪpSKARF��������ȷ������ٽ�0.4kbp14ARF cDNA���������˱�������pcDNA3�ϵ�BamHI��EcoRIλ�㣬����ΪpcDNA3ARF��
, http://www.100md.com
1.3 pcDNA3ARFתȾ����ϸ��
����״̬���õ�����ϸ������ø����������6�װ��У�ÿ��3��105ϸ����������80%��Ϻ�֬�����Լ�LipofectamineTM(Gibco/BRL)תȾ����תȾpcDNA3ARF�Ͷ�������pcDNA3��ÿ����1��g������6��l֬���壬תȾ���Һ���뵽����ϸ����37�棬5%CO2����6h���ټ��뺬20%̥ţѪ���DMEM����Һ����������72h����ø������ת��25cm2������ƿ�ڣ�ÿƿ5��105ϸ����ͬʱ������ӦŨ�ȵĿ�����G418(Gibco/BRL)��Hep2��HepG2��MCF7��KBϸ��������Ŀ�����Ũ��Ϊ800��g/ml,HLE��Huh7ϸ��Ϊ400��g/ml��KB-v200��MCF7/ADRϸ��Ϊ300��g/ml��ÿ��3��4�컻һ������Һ��G418ɸѡ2��(Huh7ϸ��������������ɸѡ3��4��)��4%��ȩ�̶����ᾧ��Ⱦɫ��ͳ���γɵļ�������
, http://www.100md.com
2 ���
2.1 p14ARFcDNA�������ͼ���
Ӧ��RT-PCR�������������������˸�ϸ��ϵL02ϸ����������0.4Kb��cDNAƬ��(ͼ1)��BamHI��EcoRIø�л��մ�Ƭ�Σ���¡������pSK��BamHI��EcoRIλ���ϣ�����ΪpSKARF�����к��������вⶨ���������֤ʵ������[6,7]����������һ�¡�
ͼ1 p14ARFcDNA��RT-PCR����
1.DL2000 DNA Marker 2.p14ARFcDNA
GGC GGA TCC ATG GTG CGC AGG TTC TTG GTG ACC CTC CGG ATT CGG CGC GCG TGC GGC CCG
, ��Ĵҽҩ
CCG CGA GTG AGG GTT TTC GTG GTT CAC ATC CCG CGG CTC ACG GGG GAG TGG GCA GCG CCA
GGG GCG CCC GCC GCT GTG GCC CTC GTG CTG ATG CTA CTG AGG AGC CAG CGT CTA GGG CAG
CAG CCG CTT CCT AGA AGA CCA GGT CAT GAT GAT GGG CAG CGC CCG AGT GGC GGA GCT GCT
GCT GCT CCA CGG CGC GGA GCC CAA CTG CGC CGA CCC CGC CAC TCT CAC CCG ACC CGT GCA
CGA CGC TGC CCG GGA GGG CTT CCT GGA CAC GCT GGT GGT GCT GCA CCG GGC CGG GGC GCG
, http://www.100md.com
GCT GGA CGT GCG CGA TGC CTG GGG CCG CCG TCT GCC CGT GGA CCT GGC TGA GAA TTC
2.2 p14ARF��˱�������Ĺ���
�����������ȷ���������BamHI��EcoRIø������pSKARF���õ�0.4Kb��ARF����Ƭ�Σ�������˱�������pcDNA3��BamHI��EcoRIλ�㣬����ΪpcDNA3ARF,���幹��������ͼ2��ø�м���֤ʵp14ARF��˱������幹����ȷ(ͼ3)��
ͼ2 p14ARF��˱�������Ĺ���
, ��Ĵҽҩ
ͼ3 pcDNA3ARF��ø�м���
1.DL2000DNAMarker;2.pcDNA3ARF/EcoRI;
3.pcDNA3ARF/BamHI;4.pcDNA3ARF/EcoRI+BamHI;
5.pcDNA3ARF
2.3 p14ARF������ϸ������������Ӱ��
pcDNA3ARF��֬����鵼תȾ����ϸ����������G418ɸѡ2��(Huh7ϸ��������������ɸѡ3��4��)�����ü�ȩ�̶����ᾧ��Ⱦɫ������������ϸ���ļ���(��1)��������ֶ�����ҩ����ϸ����KB-v200��MCF7/ADR�ļ��������٣��ֱ�Ϊ13��2.0��21��1.5��ռ����תȾ������pcDNA3�������15%��17%����p53���Ե�����ϸ��HepG2��Hep2��MCF7�γɵļ�����Ҳ���٣��ֱ�Ϊ59��2.1,60��2.1��66��7.0��ռ���Զ������47%��57%��58%��p53�쳣������ϸ��KB,HLE,Huh-7�����γ���Խ϶�ļ��䣬�ֱ�Ϊ91��2.5,48��2.0,41��2.0��ռ���Զ������74%��65%��80%���ɴ˿ɼ���p14ARF����������p53��������ϸ��������������p53���Ե�����ϸ��������Ӱ������Խ��٣�����p14ARF����������ϸ������������p53����ԡ����DZ���ʵ����Ҳ��ʾ����p14ARF����ҩ����ϸ������ǿ�ҵ��������ã�����������ҩϸ���궼��p53�쳣�ģ���˵��p14ARF������ҩ����ϸ����������p53�������Եġ�
, http://www.100md.com
��1 תȾp14ARF���������ϸ����¡�γ��� ϸ��ϵ
ϸ������
��Դ��
p53״��
תȾpcDNA3ARF
(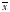 ��s)
��s)
תȾpcDNA3
(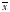 ��s)
��s)
���������
, ��Ĵҽҩ pcDNA3ARF/pcDNA3)
Hep2
���۰�
+
60��2.1
105��2.0
57%
KB
���ʰ�
-
91��2.5
123��5.5
74%
, http://www.100md.com
KB-v200
���ʰ�/VCR
-
13��2.0
86��3.1
15%
��ҩ��
HepG2
�ΰ�
+
59��2.1
126��6.2
47%
, ��Ĵҽҩ
HLE
�ΰ�
-
48��2.0
74��4.2
65%
Hle
�ΰ�
-
41��2.0
50��3.1
80%
Huh-7
, ��Ĵҽҩ
���ٰ�
+
66��7.0
114��6.7
58%
MCF-7
���ٰ�/ADR
-
21��1.5
126��7.5
17%
MCF-7/ADR
��ҩ��
, ��Ĵҽҩ
3 ����
Ŀǰ��ϸ�����ڵ��غ�ϸ�������ķ��ӻ�������ʶ����ٽ����������������о��ķ�չ������Ϊֹ�������Ѷ�p53,p16,RB,Mda-7���ְ�����ͨ���������嵼���������ϸ���������ڡ������飬�������һ����Ԥ��Ч��[8]���������ְ����������³�Աp14ARF���о����٣��Դ˻����ܵ���ʶ�����϶���Դ�����p19ARF�����ڴˣ����Ĵ������˸�ϸ��ϵL02ϸ����RT-PCR������0.4Kb������¡����˱�������pcDNA3�ϣ�תȾ��������ϸ���������ʾ��p14ARF����������p53��������ϸ��������γɡ���ȥ���б������p19ARF������ϸ����G1�ں�G2/M��(Quelle�ȣ�1995)[9],��Stott[10]����(1998)���о����Ҳ˵����p14ARF�ı�����������p53���Ե����ٰ�ϸ��ϵMCF7��G1�ڣ���ȴ�����յ�p53���Ե��˷ΰ�ϸ��ϵH1299ϸ��������SOAS2ϸ�����������ͣ��ɴ���ʾ�ˣ�p14ARF����������ϸ��������p53����ԡ����ǵ��о������һ��֧������һ�۵㣻������һ���棬���Ĵ�p14ARFתȾ��ҩ����ϸ����ʵ������ȴ�ó����෴�Ĺ۵㣬������KB-V200��MCF7/ADR����p53�쳣������p14ARFȴǿ���������ǵ�����������ʾp14ARF������ҩ����ϸ���������Ƕ�����p53;���ġ����ڴ�����������߾���λ��ƺ����������ϸ���Ի���ҩ�����ҩ��,�������������������,p14ARF��Ӧ�ý��Ǽ�p53֮���һ����Ҫ��չ����,��һ���ֵķ��ӻ������������о�֮�С�
, http://www.100md.com
[�༭ :�Ӿ��� ;У�� :�ʿɽ� ]
ͨѶ���ߣ�������Tel��86-10-68158311
Fax��86-10-68158311
E-mail��wuct@nic.bmi.ac.cn
[�����]
[1] Levine AJ. p53,the cellular gatekeeper for growth and division [J]. Cell, 1997,88(3):323��331.
[2] Sheer CJ. Cancer cell cycle [J]. Science, 1996,274:1672��1677.
, ��Ĵҽҩ
[3] Chin L, Pomerantz J, DePinho RA. The INK4��/ARF tumor suppressor: one gene-two products-two pathways [J]. Trends Biochem Sci, 1998,23(8):291��296.
[4] Sheer CJ. Tumor surveillance via the ARF- p53 pathway [J]. Genes �� Development, 1998,12(19):2984��2991.
[5] ��˹�� F ,��˹�� RE�������� JG,��,����. ����������,��.�����������ѧʵ��ָ��[M].��������ѧ�����磬1998:29��108.
[6] Duro D, Bernard O, Della Valle V, et al. A new type of p16INK4/MTS1 gene transcript expressed in B-cell malignancies [J]. Oncogene,1995,11(1):21��29.
, ��Ĵҽҩ
[7] Mao L, Merlo A, Bedi G, et al. A novel p16INK4A transcript [J]. Cancer Res. 1995,55(14):2995��2997.
[8] Paillard F. Cancer gene therapy annual conference 1997:Trends and News [J]. Human Gene Therapy,1998,9(3):283��286.
[9] Quelle DE, Zindy F, Ashmun RA, et al. Alternative reading frames of the INK4a tumor suppressor gene encode two unrelated proteins capable of inducing cell cycle arrest [J]. Cell, 1995,83(6):993��1000.
[10] Stott FJ, Bates SA, James MC, et al. The alternative product from the human CDKN2A locus, p14ARF, participates in a regulatory feedback loop with p53 and MDM2 [J]. EMBO J, 1998,17(17):5001��5014.
�ո����ڣ�1999-12-02;�����ڣ�1999-12-24, http://www.100md.com
��λ��������(����ҽѧ��ѧԺ����ҽѧ�о���,���� 100850)������(��ž���ҽԺ���Ǻ���,���� 100853)��л����(������ͯҽԺѪ����,���� 100045)��������(����ҽѧ��ѧԺ����ҽѧ�о���,���� 100850)
�ؼ��ʣ�p14ARF���������ƣ�p53����ҩ����ϸ��
��֢000202
��ժ Ҫ��Ŀ��:�������˸�ϸ��ϵL02ϸ���������˵��������ƻ���p14ARF�����о�����˵Ķ�������ϸ��������Ӱ�졣����:Ӧ��RT-PCR�������������������˸�ϸ��ϵL02ϸ����������0.4Kb��p14ARFcDNAƬ�Σ�������ȷ�������˱�������pcDNA3�ϵ�BamHI��EcoRIλ�㣬����ΪpcDNA3ARF����������֬����LipofectamineTM�鵼תȾ����ϸ��Hep2��KB��KB-v200��HepG2��HLE��Huh7�Լ�MCF7��MCF7/ADR����G418ɸѡ2�ܺ�ͳ���γɵļ����������:��������G418ɸѡ2�ܺ���p53���Ե�����ϸ��HepG2��Hep2��MCF7�γɵļ��������٣��ֱ�Ϊ59��2.1,60��2.1��66��7.0��ռ���Զ������47%��57%��58%����p53�쳣������ϸ��KB,HLE,Huh-7�����γ���Խ϶�ļ��䣬�ֱ�Ϊ91��2.5,48��2.0,41��2.0��ռ���Զ������74%��65%��80%,���Ƕ���p53�쳣����ҩ����ϸ����KB-v200��MCF7/ADR,�γɵļ��������٣��ֱ�Ϊ13��2.0��21��1.5��ռ����תȾ������pcDNA3�Ķ������15%��17%������:p14ARF����������p53��������ϸ��������������p53�����;Ȼ��p14ARF��p53���Ե���ҩ����ϸ��ȴ����ǿ�ҵ��������ã��ɴ���ʾ:p14ARF������ҩ����ϸ����������p53�������Ե�(��������������ҩ����ϸ����)��
, http://www.100md.com
��ͼ����ţ�R735.5 ���ױ�ʶ�룺A
���±�ţ�1000-467X(2000)02-0104-04
Transfer of p14ARF gene in human tumor cell lines inhibits cell proliferation
FAN Guo-chang
(Beijing Institute of Radiation Medicine,Beijing 100850, P.R.China)
LEI Lei
(PLA General Hospital,Beijing 100853, P.R.China)
, http://www.100md.com
XIE Jian-jun
(Beijing Children Hospital,Beijing 100045, P.R.China)
��Abstract�� Objective: To clone p14ARF gene from cells of the human normal liver cell line L02 and explore its inhibitory effect on tumor cell proliferation. Methods: p14ARF cDNA was cloned from L02 cells by using RT- PCR method and inserted into the BamHI and EcoRI sites of pcDNA3 (called pcDNA3ARF). Lipofectamine mediated pcDNA3ARF was transferred into tumor cell lines, such as Hep2, KB, KB- v200, HepG2, HLE, Huh7, MCF7 and MCF7/ADR. The number of colonies of these tumor cell lines were calculated after more than two weeks' screening in DMEM medium containing G418. Results:The colony-forming efficiency of the p14ARF -transfected KB-v200 and MCF7/ADR drug-resistant cells was 13�� 2.0 and 21�� 1.5 , respectively, compared with 86�� 3.1(15% )and 126�� 7.5(17% )in the cells transfected with empty vector pcDNA3, and in the p53 positive tumor cell lines, such as HepG2(47% ), Hep2(57% ), MCF7(58% ) cells, the inhibition was also found�� whereas in the p53 negative tumor cell lines, such as KB(74% ), HLE(65% ), Huh-7(80% ) cells, the inhibitory effect was milder. Conclusions: p14ARF can suppress the growth of the p53 positive tumor cell lines in a p53-relevant manner, while in the p53 negative, drug-resistant tumor cells, p14ARF has strong inhibitory effect, indicating the inhibitory effect of p14ARF on growth of drug-resistant tumor cells is independent on p53, at least in KB-v200 and MCF7/ADR drug-resistant cells.
, http://www.100md.com
Key words��p14ARF; Tumor growth suppress; p53; Drug-resistant tumor cells
ϸ�����ڵĵ����������ͬ������ɵĶ���ͨ·����ɵġ�����������ϸ���У������ļ��ֻ�������ͻ�䣬��Щ�������p53,RB,INK4��/ARF�ȡ�Ȼ��,�������ǹ��ɵ���������ͨ·��RBͨ·(p16INK4��-RB)��p53ͨ·(ARF-p53)�ڵ����������������Ĺ��������Źؼ������ã�����RBͨ·�е�INK4��(p16INK4��)��p53ͨ·�е�p53�Ǿ��������ı����������[1,2]��RBͨ·�����������ƹ��ܣ���ͨ������ϸ��G1-S�ڱ�������ת¼���Ӷ���ϸ��������G1�ڣ�p53ͨ·��������������ϸ������������ϸ����G1�ڣ�����Ҫ������ϸ�����ͺ�ϸ��״̬��p53��Ϊ˳ʽ�������Ӻ�ϸ����������������ã����ղ����������ƹ��ܡ�����о�����[3]��������;��ͨ��INK4��/ARF(9p21)λ�����ϵ��������λ��ͨ����ͬ���Ķ���ܶ��������ֲ�ͬ���������Ƶ��ף�p16��p14ARF(���ͬԴ��Ϊp19ARF)������p16INK4����������ϸ����ֳ������Ƶ��о������кܶ౨������Ŀǰ�й�p14ARF����ʶ����Դ�����p19ARF[4]����˱��Ĵ������˸�ϸ��ϵL02ϸ���У�RT-PCR������0.4kb����p14ARF�������о�����˵Ķ�������ϸ��������Ӱ�졣
, ��Ĵҽҩ
1 �����뷽��
1.1 ϸ��ϵ
L02����������ϸ��ϵ��Hep2���˺��۰�ϸ��ϵ��KB���˱��ʰ�ϸ��ϵ��KB-v200�����ʰ������¼���ҩ�ꣻHepG2��HLE��Huh-7���˸ΰ�ϸ��ϵ��MCF-7�������ٰ�ϸ��ϵ��MCF-7/ADR�����ٰ���ù����ҩ�ꡣ����ϸ��ϵ����ҩϸ�������������37�桢5%CO2������,��10%̥ţѪ��ĸ���DMEM������(Gibco/BRL)��;KB-v200ϸ������������Ҫ����������Һ������80nmol/ml�����¼�,MCF-7/ADRϸ������������Ҫ����8��g/ml��ù��,ʵ��ǰһ�ܳ�ȥҩ�
1.2 p14ARF����Ŀ�¡����˱�������Ĺ���
1.2.1 һ���������ѧ��������:�����淽��[5]���У�һЩ��������ѧ����ø��ΪPromega��˾��Ʒ������ĺϳɼ����вⶨ�ɴ��������﹤�̹�˾��ɡ�
, http://www.100md.com
1.2.2 RNA����ȡ��RT-PCR��Ӧ:��ø��������״̬���õ�L02ϸ���������ռ��������PBSϴ���Σ��ٰ�RNA��ȡ�Լ��в���������ȡϸ����RNA��ȡ��RNA1��g������Oligo(dT)����1��g����20��l�����42������ת¼��Ӧ��ȡ5��l��ת¼����Ϊģ�壬����PCR��Ӧ������PCR��Ӧ�������£�94�棬1min;50��,1min;72��,1.5min;5��ѭ����94�棬1min;60��,1min;72��,1.5min;35��ѭ����72������10min��AMV��ת¼ø��Taqø��ΪPromega��˾��Ʒ��p14ARF������������£�
�������5'��GGC GGA TCC ATG GTG CGC AGG TTC T-3'
�������5'��CCG AAT TCT CAG CCA GGT CCA CG-3'
1.2.3 p14ARFcDNA�������弰��˱�������Ĺ���:����RT��PCR������Wizard Plus Minipreps DNA Purification System(Promega��˾)���մ���������BamHI��EcoRIø�У�1.5%����֬��������Ӿ���մ�ø�е�0.4kbp14ARF cDNA����¡������pSK��BamHI��EcoRIλ�㣬����ΪpSKARF��������ȷ������ٽ�0.4kbp14ARF cDNA���������˱�������pcDNA3�ϵ�BamHI��EcoRIλ�㣬����ΪpcDNA3ARF��
, http://www.100md.com
1.3 pcDNA3ARFתȾ����ϸ��
����״̬���õ�����ϸ������ø����������6�װ��У�ÿ��3��105ϸ����������80%��Ϻ�֬�����Լ�LipofectamineTM(Gibco/BRL)תȾ����תȾpcDNA3ARF�Ͷ�������pcDNA3��ÿ����1��g������6��l֬���壬תȾ���Һ���뵽����ϸ����37�棬5%CO2����6h���ټ��뺬20%̥ţѪ���DMEM����Һ����������72h����ø������ת��25cm2������ƿ�ڣ�ÿƿ5��105ϸ����ͬʱ������ӦŨ�ȵĿ�����G418(Gibco/BRL)��Hep2��HepG2��MCF7��KBϸ��������Ŀ�����Ũ��Ϊ800��g/ml,HLE��Huh7ϸ��Ϊ400��g/ml��KB-v200��MCF7/ADRϸ��Ϊ300��g/ml��ÿ��3��4�컻һ������Һ��G418ɸѡ2��(Huh7ϸ��������������ɸѡ3��4��)��4%��ȩ�̶����ᾧ��Ⱦɫ��ͳ���γɵļ�������
, http://www.100md.com
2 ���
2.1 p14ARFcDNA�������ͼ���
Ӧ��RT-PCR�������������������˸�ϸ��ϵL02ϸ����������0.4Kb��cDNAƬ��(ͼ1)��BamHI��EcoRIø�л��մ�Ƭ�Σ���¡������pSK��BamHI��EcoRIλ���ϣ�����ΪpSKARF�����к��������вⶨ���������֤ʵ������[6,7]����������һ�¡�

ͼ1 p14ARFcDNA��RT-PCR����
1.DL2000 DNA Marker 2.p14ARFcDNA
GGC GGA TCC ATG GTG CGC AGG TTC TTG GTG ACC CTC CGG ATT CGG CGC GCG TGC GGC CCG
, ��Ĵҽҩ
CCG CGA GTG AGG GTT TTC GTG GTT CAC ATC CCG CGG CTC ACG GGG GAG TGG GCA GCG CCA
GGG GCG CCC GCC GCT GTG GCC CTC GTG CTG ATG CTA CTG AGG AGC CAG CGT CTA GGG CAG
CAG CCG CTT CCT AGA AGA CCA GGT CAT GAT GAT GGG CAG CGC CCG AGT GGC GGA GCT GCT
GCT GCT CCA CGG CGC GGA GCC CAA CTG CGC CGA CCC CGC CAC TCT CAC CCG ACC CGT GCA
CGA CGC TGC CCG GGA GGG CTT CCT GGA CAC GCT GGT GGT GCT GCA CCG GGC CGG GGC GCG
, http://www.100md.com
GCT GGA CGT GCG CGA TGC CTG GGG CCG CCG TCT GCC CGT GGA CCT GGC TGA GAA TTC
2.2 p14ARF��˱�������Ĺ���
�����������ȷ���������BamHI��EcoRIø������pSKARF���õ�0.4Kb��ARF����Ƭ�Σ�������˱�������pcDNA3��BamHI��EcoRIλ�㣬����ΪpcDNA3ARF,���幹��������ͼ2��ø�м���֤ʵp14ARF��˱������幹����ȷ(ͼ3)��

ͼ2 p14ARF��˱�������Ĺ���

, ��Ĵҽҩ
ͼ3 pcDNA3ARF��ø�м���
1.DL2000DNAMarker;2.pcDNA3ARF/EcoRI;
3.pcDNA3ARF/BamHI;4.pcDNA3ARF/EcoRI+BamHI;
5.pcDNA3ARF
2.3 p14ARF������ϸ������������Ӱ��
pcDNA3ARF��֬����鵼תȾ����ϸ����������G418ɸѡ2��(Huh7ϸ��������������ɸѡ3��4��)�����ü�ȩ�̶����ᾧ��Ⱦɫ������������ϸ���ļ���(��1)��������ֶ�����ҩ����ϸ����KB-v200��MCF7/ADR�ļ��������٣��ֱ�Ϊ13��2.0��21��1.5��ռ����תȾ������pcDNA3�������15%��17%����p53���Ե�����ϸ��HepG2��Hep2��MCF7�γɵļ�����Ҳ���٣��ֱ�Ϊ59��2.1,60��2.1��66��7.0��ռ���Զ������47%��57%��58%��p53�쳣������ϸ��KB,HLE,Huh-7�����γ���Խ϶�ļ��䣬�ֱ�Ϊ91��2.5,48��2.0,41��2.0��ռ���Զ������74%��65%��80%���ɴ˿ɼ���p14ARF����������p53��������ϸ��������������p53���Ե�����ϸ��������Ӱ������Խ��٣�����p14ARF����������ϸ������������p53����ԡ����DZ���ʵ����Ҳ��ʾ����p14ARF����ҩ����ϸ������ǿ�ҵ��������ã�����������ҩϸ���궼��p53�쳣�ģ���˵��p14ARF������ҩ����ϸ����������p53�������Եġ�
, http://www.100md.com
��1 תȾp14ARF���������ϸ����¡�γ��� ϸ��ϵ
ϸ������
��Դ��
p53״��
תȾpcDNA3ARF
(
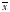 ��s)
��s)תȾpcDNA3
(
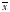 ��s)
��s)���������
, ��Ĵҽҩ pcDNA3ARF/pcDNA3)
Hep2
���۰�
+
60��2.1
105��2.0
57%
KB
���ʰ�
-
91��2.5
123��5.5
74%
, http://www.100md.com
KB-v200
���ʰ�/VCR
-
13��2.0
86��3.1
15%
��ҩ��
HepG2
�ΰ�
+
59��2.1
126��6.2
47%
, ��Ĵҽҩ
HLE
�ΰ�
-
48��2.0
74��4.2
65%
Hle
�ΰ�
-
41��2.0
50��3.1
80%
Huh-7
, ��Ĵҽҩ
���ٰ�
+
66��7.0
114��6.7
58%
MCF-7
���ٰ�/ADR
-
21��1.5
126��7.5
17%
MCF-7/ADR
��ҩ��
, ��Ĵҽҩ
3 ����
Ŀǰ��ϸ�����ڵ��غ�ϸ�������ķ��ӻ�������ʶ����ٽ����������������о��ķ�չ������Ϊֹ�������Ѷ�p53,p16,RB,Mda-7���ְ�����ͨ���������嵼���������ϸ���������ڡ������飬�������һ����Ԥ��Ч��[8]���������ְ����������³�Աp14ARF���о����٣��Դ˻����ܵ���ʶ�����϶���Դ�����p19ARF�����ڴˣ����Ĵ������˸�ϸ��ϵL02ϸ����RT-PCR������0.4Kb������¡����˱�������pcDNA3�ϣ�תȾ��������ϸ���������ʾ��p14ARF����������p53��������ϸ��������γɡ���ȥ���б������p19ARF������ϸ����G1�ں�G2/M��(Quelle�ȣ�1995)[9],��Stott[10]����(1998)���о����Ҳ˵����p14ARF�ı�����������p53���Ե����ٰ�ϸ��ϵMCF7��G1�ڣ���ȴ�����յ�p53���Ե��˷ΰ�ϸ��ϵH1299ϸ��������SOAS2ϸ�����������ͣ��ɴ���ʾ�ˣ�p14ARF����������ϸ��������p53����ԡ����ǵ��о������һ��֧������һ�۵㣻������һ���棬���Ĵ�p14ARFתȾ��ҩ����ϸ����ʵ������ȴ�ó����෴�Ĺ۵㣬������KB-V200��MCF7/ADR����p53�쳣������p14ARFȴǿ���������ǵ�����������ʾp14ARF������ҩ����ϸ���������Ƕ�����p53;���ġ����ڴ�����������߾���λ��ƺ����������ϸ���Ի���ҩ�����ҩ��,�������������������,p14ARF��Ӧ�ý��Ǽ�p53֮���һ����Ҫ��չ����,��һ���ֵķ��ӻ������������о�֮�С�
, http://www.100md.com
[�༭ :�Ӿ��� ;У�� :�ʿɽ� ]
ͨѶ���ߣ�������Tel��86-10-68158311
Fax��86-10-68158311
E-mail��wuct@nic.bmi.ac.cn
[�����]
[1] Levine AJ. p53,the cellular gatekeeper for growth and division [J]. Cell, 1997,88(3):323��331.
[2] Sheer CJ. Cancer cell cycle [J]. Science, 1996,274:1672��1677.
, ��Ĵҽҩ
[3] Chin L, Pomerantz J, DePinho RA. The INK4��/ARF tumor suppressor: one gene-two products-two pathways [J]. Trends Biochem Sci, 1998,23(8):291��296.
[4] Sheer CJ. Tumor surveillance via the ARF- p53 pathway [J]. Genes �� Development, 1998,12(19):2984��2991.
[5] ��˹�� F ,��˹�� RE�������� JG,��,����. ����������,��.�����������ѧʵ��ָ��[M].��������ѧ�����磬1998:29��108.
[6] Duro D, Bernard O, Della Valle V, et al. A new type of p16INK4/MTS1 gene transcript expressed in B-cell malignancies [J]. Oncogene,1995,11(1):21��29.
, ��Ĵҽҩ
[7] Mao L, Merlo A, Bedi G, et al. A novel p16INK4A transcript [J]. Cancer Res. 1995,55(14):2995��2997.
[8] Paillard F. Cancer gene therapy annual conference 1997:Trends and News [J]. Human Gene Therapy,1998,9(3):283��286.
[9] Quelle DE, Zindy F, Ashmun RA, et al. Alternative reading frames of the INK4a tumor suppressor gene encode two unrelated proteins capable of inducing cell cycle arrest [J]. Cell, 1995,83(6):993��1000.
[10] Stott FJ, Bates SA, James MC, et al. The alternative product from the human CDKN2A locus, p14ARF, participates in a regulatory feedback loop with p53 and MDM2 [J]. EMBO J, 1998,17(17):5001��5014.
�ո����ڣ�1999-12-02;�����ڣ�1999-12-24, http://www.100md.com