高效液相色谱法测定人血浆中黄芩苷与血浆蛋白的结合率
作者:王弘 陈济民 张清民
单位:沈阳药科大学药学系,沈阳 110015
关键词:高效液相色谱法;黄芩苷;蛋白结合率
沈阳药科大学学报000210 摘 要:用高效液相色谱法对人血浆中黄芩苷进行了测定.在5、15、25 μg/mL范围的回收率为95.0%、88.7%、94.2%.人血浆中黄芩苷与血浆蛋白的结合率测定,为设计合理的给药方案提供了实验依据.
分类号;R963
High-Performance Liquid Chromatographic Determination of Baicalin in Human Plasma
Wang Hong Chen Jimin Zhang Qingmin
, http://www.100md.com
(Department of Pharmacy,Shenyang Pharmaceutical University, Shenyang 110015)
Abstract:A high-performance liquid chromatographic method for the quantitative determination of baicalin in human plasma is presented. The method has been carried out by using the NUCLeosil-C18 column and methanol-water-acetic acid as the mobile phase. The method proved to be simple and sensitive with good specificity, precision and accuracy. 95.0%,88.7% and 94.2% at three different concentrations of baicalin were the recoveries. The determination of combining percentage of protein with baicalin provided experimental evidence for suggestion of rational administration.
, 百拇医药
Key words:high-performance liquid chromatography; baicalin; combining percentage of protein▲
药物进入机体后能与体内多种生物高分子发生结合,比如药物与受体的结合,药物与核酸的结合等.药物与血浆蛋白的结合,也是药物与生物高分子的结合,与上述其它类型的结合之间存在一定的相关性,因此药物与血浆蛋白的结合,是药理学基础理论研究,特别是分子药理学的重要研究内容之一.
高度结合时(一般指80%以上)还具有下列临床意义:延缓药物经肾排泄;延缓进入细胞外液,从而影响药物体内分布;药物的药理作用强度常常只与血浆中未与蛋白结合的游离浓度成线性关系,故在设计最适给药方案时,常需考虑血浆蛋白结合率〔1,2〕.
1 实验材料与条件
, 百拇医药 1.1 仪器、样品、试剂与材料
仪器:635高效液相色谱仪;200-10型UV-VIS分光光度计.
样品:黄芩苷(深圳南方药厂提供);黄芩苷对照品(中国药品生物制品检定所);呋喃苯胺酸(沈阳第一制药厂).
试剂:3%磺酸水杨酸试剂;透析液(pH7.4的0.02 mol/L磷酸盐缓冲液,内含0.15 mol/L NaCl).
材料:正常人血浆(沈阳军区总医院血液科提供);管状半透膜(周长5 cm,长10 cm).
1.2 色谱条件
色谱柱: C18(5 μm) 4 mm×250 mm ;流动相:甲醇-水-乙酸(体积比为60∶39∶1);流速:0.9 mL/min; 柱温:室温;检测器:276 nm(UV-VIS分光光度计).
, 百拇医药
1.3 实验条件
1.3.1 最大吸收波长的选择
经紫外全波长扫描,黄芩苷在276 nm处有最大吸收,故选用276 nm处测定.
1.3.2 流动相选择
经比较选择,作者所用流动相分离完全,血浆杂质无干扰,见图1.
Fig.1 The chart of chromatography
A—Blank plasma;B—Baicalin+furosemide;
C—Blank plasma+baicalin +furosemide;
, 百拇医药
1—Furosemide(tR=3.93 min);
2—Baicalin(tR=5.98 min)
2 实验方法
2.1 线性关系的考察
精密吸取黄芩苷对照品甲醇溶液(10.0 mg→100 mL)0.25、0.5、0.75、1、1.25、1.50、1.75、2.00、2.25、2.50、2.75、3 mL,置于10 mL容量瓶中,加甲醇液至刻度,配成5、10、15、20、25、30、35、40、45、50、55、60 μg/μL系列对照溶液.精取内标呋喃苯胺酸(250 mg→25 mL) 贮备液适量,加甲醇得到0.125 μg/μL内标溶液.用甲醇配制黄芩苷系列标准液,精密加内标溶液80 μL,混匀振荡10 min,放置0.5 h, HPLC分析测定峰高,以黄芩苷与速尿峰高比为横坐标,以黄芩苷进样浓度为纵坐标,绘制标准曲线.回归方程为:C=0.015 28A-3.333×10-3 (r=0.999 0,n=10).
, 百拇医药
结果表明:黄芩苷的浓度测定值在5~60 μg/mL范围内呈线性关系.
2.2 回收率与精密度试验
精密吸取黄芩苷样品溶液在5 μg/mL、15 μg/mL、25 μg/mL 3个水平上重复进样5次, 结果见表1.
Tab.1 Recoveries and RSD of baicalin by HPLC assay Add value/μg。mL-1
Assay value /μg。mL-1
n
Recovery/%
RSD/%
, http://www.100md.com
5
4.998
±0.132
5
99.9
3.25
15
14.89
±0.291
5
99.3
2.39
25
, http://www.100md.com
24.96
±0.106
5
99.9
4.23
2.3 稳定性试验 一份样品(含有黄芩苷)经甲醇沉淀后,各取1 mL上清液于6支试管中,其中3管于90℃水浴空气吹干,另3支管于25℃下氮气吹干,结果:SX1-X2=0.292 4,t=0.167 5(t0.05=2.776 4, t0.1=2.131 8),P>0.1,所以经两种不同方法处理黄芩苷浓度测定值无显著差异,见表2.
Tab.2 Assay values of concentration of baicalin No.
, 百拇医药
Group by N2 at 25℃
Group by air at 90℃
1
5.074
4.268
2
4.438
5.048
3
4.652
4.702
Mean
, http://www.100md.com
4.721
4.672
2.4 空白试验
取血浆1 mL加甲醇4 mL,混匀振荡15 min,然后以2 500 r/min离心10 min,取20 L进行HPLC分析,结果表明:空白血浆无干扰.采用本法可将黄芩苷、呋喃苯胺酸与血浆杂质完全分离.
2.5 人血浆中的线性范围考察
在1 mL空白血浆中定量加入黄芩苷,精密加入内标物呋喃苯胺酸15 μg、甲醇4 mL,沉淀蛋白,配成5、10、15、20、25、30、35、40、45、50 μg/mL.于混合振荡器上振荡10 min,以2 500 r/min离心8 min.取上清液,90℃水浴空气吹至0.25 mL左右,HPLC进样测定.
, 百拇医药 将浓度与黄芩苷和速尿峰高之比作线性回归,在黄芩苷浓度为5~35 μg/mL范围内线性关系良好.回归直线方程:C=0.015 23A+1.066×10-3(r=0.998 0).
2.6 血浆中的回收率与精密度试验
在3个黄芩苷浓度(5 μg/mL、15 μg/mL、25 μg/mL)水平上测定了回收率与精密度,结果见表3.
Tab.3 Recoveries and RSD of baicalin in plasma Add/μg。mL-1
Found /μg。mL-1
n
Recovery/%
, 百拇医药
RSD/%
5
4.75±0.302
5
95.0
4.81
15
13.31±0.177
5
88.7
1.66
25
23.54±0.180
, 百拇医药
5
94.2
4.32
2.7 蛋白结合率的测定2.7.1 方法
将管状半透膜一端用线扎紧,保证不漏,保留结扎线段10 cm左右,以便调节袋内外液面之用.用吸管加入血浆样本2.5 mL到上述半透膜袋内;折叠并结扎袋口,使袋内保留少量空气,使透析袋能悬浮在缓冲液内,不致沉入底部.将两端结扎的半透膜袋置于盛有10 mL透析液的30 mL广口瓶中,用袋两端残留线段调节袋内外液体,使保持同一水平,排除因液面相差引起液体流动.除实验样本外,另外用2.5 mL透析液代替血浆,操作同上,作为时间对照样本,以确定药物从袋内外自由扩散达到平衡所需时间.加所试药物(150 μg)至袋外透析液中;置广口瓶于冰箱中平衡透析72 h.达到平衡透析时间后,吸出袋外透析液少许,加等量磺酸水杨酸试剂,检查有无血浆蛋白漏出.取出半透膜袋,用滤纸吸干附着于袋外壁的透析液,小心剪破透析袋,使袋内血浆流入干净试管中,测定袋内袋外的溶液中药物浓度, 加入袋外黄芩苷药液体积分别为:0.1、0.2、0.3、0.4、0.5、0.6、0.7、 0.8、0.9 mL,加入袋外黄芩苷量分别为: 6、12、18、24、30、36、42、50、54 μg/mL. 黄芩苷(600 μg/mL)于10 mL袋内透析液中,袋内血浆均为2.5 mL,另一袋内盛有2.5 mL透析液.
, 百拇医药
2.7.2 计算蛋白结合率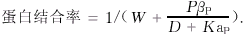
W为血液含水率;P为血浆蛋白浓度,以g/L表示;βP为白蛋白结合药物表观最大能力;D为黄芩苷的测定值;Kap为药物蛋白复合物的解离常数,以μmol/L表示.求得βP及Kap后利用上式计算任一浓度时蛋白结合率.
2.7.3 计算βp及Kap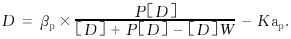
[D]为测定的药物浓度.
令[D]为纵轴,P[D]/([D]+P[D]-[D]W)为横轴,利用直线回归求斜率βp、纵轴截距KaP.
, 百拇医药
取平衡透析后袋内血浆1 mL、袋外透析液1 mL,处理方法同上,HPLC测定(血清蛋白总量为70.7 g/L,血清水含量为99.25%),计算,结果βp值为0.213;Kap值为21.31.
回归方程:Y=21.31-0.213 0X (r=0.927 3),对不同黄芩苷浓度(10、20、30、40、50 μg/mL)进行线性回归.
结果表明,黄芩苷蛋白结合率分别为:67.9%、73.7%、77.8%、80.8%、83.1%
3 讨论
根据黄芩苷含有羧基,采用C18柱分离黄芩苷,并用HPLC法进行人血浆中黄芩苷的蛋白结合率测定,目前尚未见报道.本法回收率、精密度较高,是一种准确、快速的方法.
, 百拇医药
参照文献〔1〕,选用甲醇作溶剂、呋喃苯胺酸为内标,测定黄芩苷浓度,所得结果良好.
90℃水浴空气吹干与25℃下氮气吹干所测结果基本一致,选择90℃水浴空气吹干.
本实验测定不同浓度下黄芩苷的蛋白结合率,为临床设计合理的给药方案提供了参考.黄芩苷与蛋白在高度结合(80%以上)时,或者当病理状态或其它伍用药物的交互作用影响结合率时,可使游离药物浓度增高,此时蛋白结合率的测定,是必须的临床检验项目.
参考文献:
[1]毛凤斐,朱家璧,屠锡德,等. 黄芩苷在人体内吸收的研究. 南京药学院学报,1983,21(1):61~66
[2] 徐叔云,卞如濂,陈修主编.药理学实验方法.北京:人民卫生出版社,1982.441~445
收稿日期:1999-07-09
, 百拇医药
单位:沈阳药科大学药学系,沈阳 110015
关键词:高效液相色谱法;黄芩苷;蛋白结合率
沈阳药科大学学报000210 摘 要:用高效液相色谱法对人血浆中黄芩苷进行了测定.在5、15、25 μg/mL范围的回收率为95.0%、88.7%、94.2%.人血浆中黄芩苷与血浆蛋白的结合率测定,为设计合理的给药方案提供了实验依据.
分类号;R963
High-Performance Liquid Chromatographic Determination of Baicalin in Human Plasma
Wang Hong Chen Jimin Zhang Qingmin
, http://www.100md.com
(Department of Pharmacy,Shenyang Pharmaceutical University, Shenyang 110015)
Abstract:A high-performance liquid chromatographic method for the quantitative determination of baicalin in human plasma is presented. The method has been carried out by using the NUCLeosil-C18 column and methanol-water-acetic acid as the mobile phase. The method proved to be simple and sensitive with good specificity, precision and accuracy. 95.0%,88.7% and 94.2% at three different concentrations of baicalin were the recoveries. The determination of combining percentage of protein with baicalin provided experimental evidence for suggestion of rational administration.
, 百拇医药
Key words:high-performance liquid chromatography; baicalin; combining percentage of protein▲
药物进入机体后能与体内多种生物高分子发生结合,比如药物与受体的结合,药物与核酸的结合等.药物与血浆蛋白的结合,也是药物与生物高分子的结合,与上述其它类型的结合之间存在一定的相关性,因此药物与血浆蛋白的结合,是药理学基础理论研究,特别是分子药理学的重要研究内容之一.
高度结合时(一般指80%以上)还具有下列临床意义:延缓药物经肾排泄;延缓进入细胞外液,从而影响药物体内分布;药物的药理作用强度常常只与血浆中未与蛋白结合的游离浓度成线性关系,故在设计最适给药方案时,常需考虑血浆蛋白结合率〔1,2〕.
1 实验材料与条件
, 百拇医药 1.1 仪器、样品、试剂与材料
仪器:635高效液相色谱仪;200-10型UV-VIS分光光度计.
样品:黄芩苷(深圳南方药厂提供);黄芩苷对照品(中国药品生物制品检定所);呋喃苯胺酸(沈阳第一制药厂).
试剂:3%磺酸水杨酸试剂;透析液(pH7.4的0.02 mol/L磷酸盐缓冲液,内含0.15 mol/L NaCl).
材料:正常人血浆(沈阳军区总医院血液科提供);管状半透膜(周长5 cm,长10 cm).
1.2 色谱条件
色谱柱: C18(5 μm) 4 mm×250 mm ;流动相:甲醇-水-乙酸(体积比为60∶39∶1);流速:0.9 mL/min; 柱温:室温;检测器:276 nm(UV-VIS分光光度计).
, 百拇医药
1.3 实验条件
1.3.1 最大吸收波长的选择
经紫外全波长扫描,黄芩苷在276 nm处有最大吸收,故选用276 nm处测定.
1.3.2 流动相选择
经比较选择,作者所用流动相分离完全,血浆杂质无干扰,见图1.

Fig.1 The chart of chromatography
A—Blank plasma;B—Baicalin+furosemide;
C—Blank plasma+baicalin +furosemide;
, 百拇医药
1—Furosemide(tR=3.93 min);
2—Baicalin(tR=5.98 min)
2 实验方法
2.1 线性关系的考察
精密吸取黄芩苷对照品甲醇溶液(10.0 mg→100 mL)0.25、0.5、0.75、1、1.25、1.50、1.75、2.00、2.25、2.50、2.75、3 mL,置于10 mL容量瓶中,加甲醇液至刻度,配成5、10、15、20、25、30、35、40、45、50、55、60 μg/μL系列对照溶液.精取内标呋喃苯胺酸(250 mg→25 mL) 贮备液适量,加甲醇得到0.125 μg/μL内标溶液.用甲醇配制黄芩苷系列标准液,精密加内标溶液80 μL,混匀振荡10 min,放置0.5 h, HPLC分析测定峰高,以黄芩苷与速尿峰高比为横坐标,以黄芩苷进样浓度为纵坐标,绘制标准曲线.回归方程为:C=0.015 28A-3.333×10-3 (r=0.999 0,n=10).
, 百拇医药
结果表明:黄芩苷的浓度测定值在5~60 μg/mL范围内呈线性关系.
2.2 回收率与精密度试验
精密吸取黄芩苷样品溶液在5 μg/mL、15 μg/mL、25 μg/mL 3个水平上重复进样5次, 结果见表1.
Tab.1 Recoveries and RSD of baicalin by HPLC assay Add value/μg。mL-1
Assay value /μg。mL-1
n
Recovery/%
RSD/%
, http://www.100md.com
5
4.998
±0.132
5
99.9
3.25
15
14.89
±0.291
5
99.3
2.39
25
, http://www.100md.com
24.96
±0.106
5
99.9
4.23
2.3 稳定性试验 一份样品(含有黄芩苷)经甲醇沉淀后,各取1 mL上清液于6支试管中,其中3管于90℃水浴空气吹干,另3支管于25℃下氮气吹干,结果:SX1-X2=0.292 4,t=0.167 5(t0.05=2.776 4, t0.1=2.131 8),P>0.1,所以经两种不同方法处理黄芩苷浓度测定值无显著差异,见表2.
Tab.2 Assay values of concentration of baicalin No.
, 百拇医药
Group by N2 at 25℃
Group by air at 90℃
1
5.074
4.268
2
4.438
5.048
3
4.652
4.702
Mean
, http://www.100md.com
4.721
4.672
2.4 空白试验
取血浆1 mL加甲醇4 mL,混匀振荡15 min,然后以2 500 r/min离心10 min,取20 L进行HPLC分析,结果表明:空白血浆无干扰.采用本法可将黄芩苷、呋喃苯胺酸与血浆杂质完全分离.
2.5 人血浆中的线性范围考察
在1 mL空白血浆中定量加入黄芩苷,精密加入内标物呋喃苯胺酸15 μg、甲醇4 mL,沉淀蛋白,配成5、10、15、20、25、30、35、40、45、50 μg/mL.于混合振荡器上振荡10 min,以2 500 r/min离心8 min.取上清液,90℃水浴空气吹至0.25 mL左右,HPLC进样测定.
, 百拇医药 将浓度与黄芩苷和速尿峰高之比作线性回归,在黄芩苷浓度为5~35 μg/mL范围内线性关系良好.回归直线方程:C=0.015 23A+1.066×10-3(r=0.998 0).
2.6 血浆中的回收率与精密度试验
在3个黄芩苷浓度(5 μg/mL、15 μg/mL、25 μg/mL)水平上测定了回收率与精密度,结果见表3.
Tab.3 Recoveries and RSD of baicalin in plasma Add/μg。mL-1
Found /μg。mL-1
n
Recovery/%
, 百拇医药
RSD/%
5
4.75±0.302
5
95.0
4.81
15
13.31±0.177
5
88.7
1.66
25
23.54±0.180
, 百拇医药
5
94.2
4.32
2.7 蛋白结合率的测定2.7.1 方法
将管状半透膜一端用线扎紧,保证不漏,保留结扎线段10 cm左右,以便调节袋内外液面之用.用吸管加入血浆样本2.5 mL到上述半透膜袋内;折叠并结扎袋口,使袋内保留少量空气,使透析袋能悬浮在缓冲液内,不致沉入底部.将两端结扎的半透膜袋置于盛有10 mL透析液的30 mL广口瓶中,用袋两端残留线段调节袋内外液体,使保持同一水平,排除因液面相差引起液体流动.除实验样本外,另外用2.5 mL透析液代替血浆,操作同上,作为时间对照样本,以确定药物从袋内外自由扩散达到平衡所需时间.加所试药物(150 μg)至袋外透析液中;置广口瓶于冰箱中平衡透析72 h.达到平衡透析时间后,吸出袋外透析液少许,加等量磺酸水杨酸试剂,检查有无血浆蛋白漏出.取出半透膜袋,用滤纸吸干附着于袋外壁的透析液,小心剪破透析袋,使袋内血浆流入干净试管中,测定袋内袋外的溶液中药物浓度, 加入袋外黄芩苷药液体积分别为:0.1、0.2、0.3、0.4、0.5、0.6、0.7、 0.8、0.9 mL,加入袋外黄芩苷量分别为: 6、12、18、24、30、36、42、50、54 μg/mL. 黄芩苷(600 μg/mL)于10 mL袋内透析液中,袋内血浆均为2.5 mL,另一袋内盛有2.5 mL透析液.
, 百拇医药
2.7.2 计算蛋白结合率
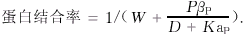
W为血液含水率;P为血浆蛋白浓度,以g/L表示;βP为白蛋白结合药物表观最大能力;D为黄芩苷的测定值;Kap为药物蛋白复合物的解离常数,以μmol/L表示.求得βP及Kap后利用上式计算任一浓度时蛋白结合率.
2.7.3 计算βp及Kap
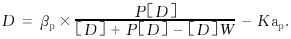
[D]为测定的药物浓度.
令[D]为纵轴,P[D]/([D]+P[D]-[D]W)为横轴,利用直线回归求斜率βp、纵轴截距KaP.
, 百拇医药
取平衡透析后袋内血浆1 mL、袋外透析液1 mL,处理方法同上,HPLC测定(血清蛋白总量为70.7 g/L,血清水含量为99.25%),计算,结果βp值为0.213;Kap值为21.31.
回归方程:Y=21.31-0.213 0X (r=0.927 3),对不同黄芩苷浓度(10、20、30、40、50 μg/mL)进行线性回归.
结果表明,黄芩苷蛋白结合率分别为:67.9%、73.7%、77.8%、80.8%、83.1%
3 讨论
根据黄芩苷含有羧基,采用C18柱分离黄芩苷,并用HPLC法进行人血浆中黄芩苷的蛋白结合率测定,目前尚未见报道.本法回收率、精密度较高,是一种准确、快速的方法.
, 百拇医药
参照文献〔1〕,选用甲醇作溶剂、呋喃苯胺酸为内标,测定黄芩苷浓度,所得结果良好.
90℃水浴空气吹干与25℃下氮气吹干所测结果基本一致,选择90℃水浴空气吹干.
本实验测定不同浓度下黄芩苷的蛋白结合率,为临床设计合理的给药方案提供了参考.黄芩苷与蛋白在高度结合(80%以上)时,或者当病理状态或其它伍用药物的交互作用影响结合率时,可使游离药物浓度增高,此时蛋白结合率的测定,是必须的临床检验项目.
参考文献:
[1]毛凤斐,朱家璧,屠锡德,等. 黄芩苷在人体内吸收的研究. 南京药学院学报,1983,21(1):61~66
[2] 徐叔云,卞如濂,陈修主编.药理学实验方法.北京:人民卫生出版社,1982.441~445
收稿日期:1999-07-09
, 百拇医药