����ݷ�ϸ�����TNT�ζ��ԵĹ�ϵ
���ߣ���ΰ ��Ԫѫ ��Ⱥ �■ ������ ���� ��Ѹ ������
��λ����ΰ ��Ԫѫ ��Ⱥ �■(����ҽ�ƴ�ѧ�Ͷ����������ң�100083)�������� ����(����ʡƽ��ɽú̼����ѧУ)����Ѹ ������(����ʡ�Ͷ�����ְҵ��������)
�ؼ��ʣ�*****���ݷ���ϸ�����ζ��ԣ�������������
��������ѧ��־000211 ��ժҪ�� Ŀ�� ̽�ִ������Kupfferϸ�����ܻ��TNT�ζ��ԵĹ�ϵ�����ܻ��ơ����� ����Kupfferϸ�����ܻ�Ĵ���ģ�ͣ��۲�TNT��VA+TNT���ϴ�������Ѫ����ALT��AST�������Ѫ����SOD��CAT��GSH-Px���Եı仯����� TNT��Ѫ����ALT��AST�������Ե��ڶ����飬��VA+TNT�������Ը��ڶ��������ӦTNT�顣TNT������Ѫ����SOD��CAT��GSH-Px���������ͷdz��������ڶ�����(P<0.05��P<0.01)��VA+TNT��ijЩø���������ͷdz��������ڶ��������Ӧ��TNT��(P<0.05��P<0.01)��TNT�ɼ�ǿ��Kupfferϸ�����ܻ����ĸζ��ԡ����� �������Kupfferϸ����VA��ɼ�ǿTNT�ζ��ԣ��Ʋ����������������йء�
, ��Ĵҽҩ
The relationship between functional activation of Kupffer cells in rat liver and TNT-induced hepatotoxicity
CUI Jing-Wei,CHANG Yuan-Xun,GUO Qun,(Department.of Occupational Health,Beijing Medical University,Beijing 100083,China.)
��Abstract�� Objective To explore the relationship between the functional activation of Kupffer cells in rat livers and TNT-induced hepatotoxicity in order to define possible mechanism of TNT-induced liver injury.Methods The model of the functional activation of rat Kupffer cells was observed during the acute exposure of TNT.Results The activities of ALT and AST in sera of TNT-treated rats were more lower than those of controls,while activities of ALT and AST in sera of VA+TNT-treated rats rose significantly.The activation of SOD,CAT and GSH-Px rose significantly in sera and liver of TNT and VA+TNT-treated rats.The changes could be seen more clearly under the condition of VA+TNT treatment.The functional activation of Kupffer cells in liver of VA+TNT-treated rats could enhance TNT-induced hepatoxicity.Conclusion Kupffer cells activated by VA,can intensify TNT-induced hepatotoxicity,which is presumed to be related with generation of reative oxygen.
, ��Ĵҽҩ
��Key words�� Trinitrotoluene; Kupffer cell; Hepatotoxicity; Reactive oxygen; Rats
��֪TNT��Ҫ�ڸ���ͨ��������ԭ�շ�������(O��(-)/(*) 2)����[1��2]������TNTΪ����Ӧ���������ݷ�(Kupffer)ϸ����λ�ڸ�Ѫ��ڵľ���ϸ������ѪҺֱ�ӽӴ��������ѪҺ�к��ɷּ�������ԭ������Ӧ��ȶ��ֹ���[3��4]��������ʵ�������ijЩ��ѧ�ﴦ�������Kupffcrϸ�����ֿ��ټ��ۣ�ϸ�����ܱ�������ͷų��������ͻ��Ե��ȶ��ֽ���[5��7]�����о���ͼ����֪��Kupfferϸ�����ά����A��������۲�TNT�����ԵĹ�ϵ��
1 �����뷽��
TNT�Ǻ���ƽ��ɽúҵ(����)��˾ij�������ṩ�����û�����ʵ���Ҳⶨ����Ϊ99.9 %��
, ��Ĵҽҩ
1.1 ����ģ���Ʊ�
1.1.1 ʵ�鶯�P���� ѡ�ý�������Wistar����28ֻ������170��200 g�������Ϊ4�飬ÿ��7ֻ��(1)�����飻(2)ά����A������(VA��)��(3)���Ȼ�̼������(CCl4��)��(4)VA��CCl4���ϴ�����(VA+CCl4��)��������ÿ�վ��ڸ���1.5 ml/100 g�����������Ϊ10 %�ı��������������Ϊ7 %������-20������7 d��VA���VA+CCl4��ÿ�վ��ڸ���250 000 IU/kg����VA(���ڱ�����������-20)������7 d��VA+CCl4���CCl4����VA�������8�죬����ǻע��(ip)0.15 ml/kg����CCl4(����������)��
1.1.2 �۲�ָ���뷽�� ����������24 h��ÿ�������ͷ����5ֻ����ȡѪ��ⶨ������ת��ø(ALT)����(��)������ת��ø(AST)�Ļ��ԡ�
, ��Ĵҽҩ
1.2 TNT����Ⱦ��ʵ��
1.2.1 TNT��ͬ��������Ⱦ�� ѡ�ý�������Wistar����100ֻ������170��200 g�������Ϊ10�飬ÿ��10ֻ���ֱ�Ϊ�����飻VA�飻TNT250��500��1 000��2 000 mg/kg�飻VA+TNT250��500��1 000��2 000 mg/kg�顣VA���VA+TNT��ÿ�վ��ڸ���VA250 000 IU/kg����������7 d����8����鰴��ͬ�������ڸ���TNT(�����ڵ��ۻ���Һ)��Ⱦ����24 h�������
1.2.2 TNT��ͬʱ�伱��Ⱦ�� ѡ�ý�������Wistar����90ֻ������170��200 g�������Ϊ3�顣�ֱ�Ϊ������(10ֻ)��TNT1 000 mg/kg��(40ֻ)��VA+TNT1 000 mg/kg��(40ֻ)��VA+TNT��ÿ�վ��ڸ���VA250 000 IU/kg����������7 d���ڵ�8�쾭�ڸ���1 000 mg/kgTNT(�����ڵ��ۻ���Һ)���ֱ���Ⱦ�����12��24��36��48 h�������
, ��Ĵҽҩ
1.2.3 �۲�ָ�꼰���� ÿ�������ͷ����5ֻ�����ﴦ����Ѹ��ȡ����������ಢ�Ʊ��Σ����Ƚ���Ѫ�壬�ֱ�ⶨ�κ����Ƚ��г��������绯ø(SOD)��������ø(CAT)���Ƚ��й����Ĺ�������ø(GSH-Px)�Ļ��Լ��������Լ�Ѫ����ALT��AST��SOD��CAT�Ļ��ԡ�
2 ���
2.1 ����ģ���Ʊ�
��1 CCl4�Դ���Ѫ��ALT��AST����(U/L)��Ӱ��(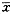 ��s) ���
��s) ���
ALT����
AST����
VA��
, ��Ĵҽҩ
113.61��24.05
159.06��23.76
CCl4��
140.38��42.10
179.14��42.28
VA+CCl4��
275.51��24.53* *
451.34��35.83* *
������
95.91��12.24
, ��Ĵҽҩ
135.14��15.73
������顢VA���CCl4��Ƚϣ�* *P<0.01
�ɱ�1�ɼ�VA���CCl4�����Ѫ��ALT��AST���Ծ����ڶ����飬�������������ԡ�VA+CCl4�����Ѫ��ALT��AST���Ծ����������ڶ����顢VA���CCl4��(P<0.01)��
2.2 VA�Լ�ǿTNT�ζ��Ե�Ӱ��
2.2.1 Ѫ��AST��ALT����
�ɱ�2�ɼ�����VA+TNT���������У�Ѫ��ALT�����������ڶ��������Ӧ������TNT��(P<0.05��P<0.01)����250 mg/kg���⣬Ѫ��AST���Ծ����������ڶ��������Ӧ������TNT������(P<0.01)��
, ��Ĵҽҩ
��2 ���ϴ���24 h����Ѫ��ALT��AST����(U/L)�ı仯(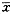 ��s)
��s)
������
VA��
TNT��(mg/kg)
VA+TNT��(mg/kg)
250
500
1 000
2 000
250
500
, ��Ĵҽҩ
1 000
2 000
ALT
101.27
��5.92
108.08
��8.20
89.92
��10.20
92.68
��15.45
87.20
��17.34
, http://www.100md.com
78.75
��16.11
126.41
��17.90* # #
138.28
��8.94* * # #
173.90
��11.54* * # #
175.82
��8.59* * # #
AST
, ��Ĵҽҩ
135.14
��12.79
142.30
��16.54
132.17
��13.15
122.92
��11.84
129.75
��18.55
127.81
��15.87
, ��Ĵҽҩ 142.65
��8.41
151.73
��9.77* * # #
185.95
��9.80* * # #
205.50
��21.13* * # #
�������Ƚϣ�*P<0.05��* *P<0.01������ͬ����TNT������Ƚϣ�# #P<0.01��3 ��ͬʱ�����Ѫ��ALT��AST����(U/L)�ı仯(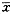 ��s)
��s)
, ��Ĵҽҩ
���
12 h
24 h
36 h
48 h
ALT
TNT��
102.14�� 6.56
93.41��13.76
88.35��14.48
90.27��11.20
VA+TNT��
, http://www.100md.com
105.81�� 8.02
167.96��16.63* * # #
165.87��12.35* * # #
169.02��10.66* * # #
������
102.32�� 6.00
112.54��12.58
AST
TNT��
132.19��10.53
, ��Ĵҽҩ
126.84�� 8.95
125.09��16.90
125.28��15.84
VA+TNT��
139.93��11.65
177.22��13.04* * # #
169.36��21.02* * # #
172.85��11.38* * # #
������
135.84��15.25
, ��Ĵҽҩ
119.98��18.45
�������Ƚϣ�* *P<0.01������ͬ����TNT��Ƚϣ�# #P<0.01 TNTȾ������Ϊ1 000mg/kg���ɱ�3�ɼ�����VA+TNT���ϴ���24 h���ʱ���Ѫ��ALT��AST���Ծ����������ڶ��������Ӧ��TNT��(P<0.01)��
2.3 ��ijЩ������ø���Ե�Ӱ��
2.3.1 TNT��ͬ����������SOD��CAT��GSH-Px�ı仯
�ɱ�4�ɼ���TNT���250 mg/kg���⣬��������������SOD�����������������ڶ�����(P<0.05��P<0.01)��VA+TNT�����SOD�����������������ڶ��������Ӧ������TNT��(P<0.05��P<0.01)��TNT���VA+TNT��1 000��2 000 mg/kg�����CAT���Ծ��������ڶ�����(P<0.05��P<0.01)��VA+TNT1 000 mg/kg�����CAT���Լ�����������Ӧ������TNT��(P<0.01)��TNT1 000 mg/kg ���VA+TNT�����������GSH-Px���Ծ��������������ڶ�����(P<0.05��P<0.01)����VA+TNT2 000 mg/kg���⣬������������������������Ӧ������TNT��(P<0.05��P<0.01)��
, http://www.100md.com
�ɱ�5�ɼ�����TNT250 mg/kg���⣬TNT�������������VA+TNT��������Ѫ��SOD���Ծ��������������ڶ�����(P<0.05��P<0.01)��VA+TNT 1 000��2 000 mg/kg��Ѫ��SOD�����������ڶ��������Ӧ����TNT��(P<0.05��P<0.01)��TNT 1 000��2 000 mg/kg�鼰��VA+TNT250 mg/kg����Ѫ��CAT�����������������ڶ����飻VA+TNT1 000 mg/kg��Ѫ��CAT��������������Ӧ������TNT��(P<0.05)��
2.3.2 TNT��ͬʱ�䴦����SOD��CAT��GSH-Px���Եı仯
TNTȾ������Ϊ1 000 mg/kg���ɱ�6�ɼ���TNT���VA+TNT���ڴ���24 h��ĸ���ʱ��㣬����SOD��CAT��GSH-Px�Ļ����������������ڶ�����(P<0.05��P<0.01)��VA+TNT���ڴ������24 h��36 h����SOD������������TNT��(P<0.05)��24 h��48 h����CAT������������������TNT��(P<0.05��P<0.01)��24 h����GSH-Px������������TNT��(P<0.05)��
, ��Ĵҽҩ
��4 �������SODa��CATb��GSH-Pxc���Եı仯(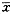 ��s)
��s)
������
TNT��(mg/kg)
VA+TNT��(mg/kg)
250
500
1 000
2 000
250
500
, ��Ĵҽҩ
1 000
2 000
SOD
360.64
��67.50
405.58
��78.95
452.95
��71.44*
485.61
��76.61* *
446.50
, http://www.100md.com
��63.41* *
489.04
��86.72* * # #
499.25
��86.30* * #
509.48
��83.14* * #
448.00
��60.08* *
CAT
43.31
, ��Ĵҽҩ
��5.50
42.89
��6.42
44.62
��4.25
51.44
��3.46*
54.99
��4.85* *
43.76
��2.12
46.02
, ��Ĵҽҩ
��3.81
58.14
��4.44* * #
56.34
��6.35* *
GSH-Px
����
847.61
��23.47
834.11
��22.88
855.91
, ��Ĵҽҩ
��32.73
899.58
��18.59* *
883.63
��47.40
877.51
��14.69* # #
899.16
��24.96* * #
990.88
��36.73* # #
, ��Ĵҽҩ
925.77
��29.91* *
a:U/mg���ף� b��mmol H2O2/30 min-1*mg-1�� c:U/g��
�������Ƚϣ�*P<0.05��* *P<0.01������ͬ����TNT������Ƚϣ�#P<0.05��# #P<0.01��5 ����Ѫ��SODa��CATb���Եı仯(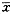 ��s)
��s)
������
TNT��(mg/kg)
, ��Ĵҽҩ
VA+TNT��(mg/kg)
250
500
1 000
2 000
250
500
1 000
2 000
SOD
98.39
��16.53
105.89
, ��Ĵҽҩ
��25.72
121.81
��28.41*
127.41
��24.23*
145.74
��24.26* *
117.43
��26.78*
127.77
��25.08* *
, http://www.100md.com
136.97
��14.52* * #
159.59
��18.96* * #
CAT
2.75
��0.72
2.66
��0.88
2.84
��0.68
3.19
, http://www.100md.com
��0.62*
3.76
��0.82*
2.93
��0.41
3.03
��0.70*
3.76
��0.76* * #
3.85
��0.52*
, ��Ĵҽҩ
a:U/mg�� b��mmol H2O2/30 min-1*mg-1
�������Ƚϣ�*P<0.05��* *P<0.01������ͬ����TNT������Ƚϣ�#P<0.05 ��6 ��ͬʱ���������SODa��CATb��GSH-Pcx�Ļ��Եı仯(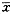 ��s)
��s)
���
12 h
24 h
36 h
, ��Ĵҽҩ
48 h
SOD
TNT��
361.83��38.61
411.90��41.34*
409.20��59.95*
395.59��44.46*
VA+TNT��
369.30��19.11
453.11��31.08* * #
, ��Ĵҽҩ 432.85��42.56* * #
410.23��33.63*
������
355.96��44.65
369.58��38.77
CAT
TNT��
44.24��5.35
50.49��5.52*
53.76��8.44*
59.22��4.13* *
, ��Ĵҽҩ
VA+TNT��
47.18��4.22
58.89��5.09* # #
58.59��3.18* *
62.40��4.89* * #
������
41.95��5.64
43.58��8.65
GSH-Px
TNT��
840.08��28.36
, http://www.100md.com
897.58��19.19* *
871.21��28.25*
860.66��16.04*
VA+TNT��
829.24��21.25
961.61��44.39* * #
900.53��23.76* *
950.73��55.46*
������
834.12��16.63
, ��Ĵҽҩ
835.43��17.56
a:U/mg���ף� b��mmol H2O2/30 min-1*mg-1�� c:U/g�� �������Ƚϣ�*P<0.05��* *P<0.01������ͬ����TNT��Ƚϣ�#P<0.05��# #P<0.01
��7 ��ͬʱ������Ѫ����SODa��CATb���Եı仯(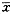 ��s)
��s)
���
12 h
24 h
, ��Ĵҽҩ
36 h
48 h
SOD
TNT��
107.27��16.02
124.42��38.14*
119.75��21.20*
126.81��37.55*
VA+TNT��
103.65��12.59
139.76��29.77* * #
, http://www.100md.com
133.39��21.96* #
131.45��25.59* *
������
110.49��21.43
94.36��11.85
CAT
TNT��
3.01��0.56
3.85��0.77* *
3.85��0.97*
3.78��0.50* *
, ��Ĵҽҩ
VA+TNT��
3.19��0.53
4.25��0.83* * #
3.96��0.61*
3.95��0.70* *
������
2.64��0.38
2.91��0.42
a:U/mg���ף� b:mmol H2O2/30min-1\5mg-1 �������Ƚϣ�*P<0.05��* *P<0.01������ͬ����TNT��Ƚϣ�#P<0.05
, ��Ĵҽҩ
TNTȾ������Ϊ1 000 mg/kg���ɱ�7�ɼ���TNT���VA+TNT���ڴ���24 h��ĸ���ʱ��㣬Ѫ��SOD��CAT�Ļ����������������ڶ�����(P<0.05��P<0.01)��VA+TNT���ڴ�����24 h��36 hѪ��SOD������������TNT��(P<0.05)��24 hѪ��CAT������������TNT��(P<0.05)�����Ƚ���SOD��CAT�����������ȽϾ����������ƣ��������������ԡ�
3 ����
�ɱ�1�ɼ�����������֪��kupfferϸ�����VA��������7 d���پ���ǻע��CCl4(0.15 ml/kg)������Ѫ��ALT��AST���Լ��������ڶ����顢VA���CCl4��(P<0.01)������VA������kupfferϸ�����ܱ���ɼ�ǿCCl4�Դ���ĸζ��ԣ��ɴ˿ɼ�������ģ��ʵ���Ʊ��dzɹ��ġ�
��ȥ�о�֤ʵ��TNT���ڴ�����������������ͨ��������ԭ����� ��H2O2[1��2]����2�ͱ�3�����������ͬ�����Ͳ�ͬʱ��VA+TNT���ϴ�����Ѫ��ALT��AST���Ծ����Ը��ڶ��������Ӧ����TNT��(P<0.05��P<0.01)��������VAǰ������ɼ�ǿTNT�ζ��ԡ�Ȼ��������VA��Ѫ��ALT��AST���Խӽ�������ˮƽ������VAδ��ʾ���и���ԡ��ɱ�4�ͱ�5�ɼ�������ͬ����TNT������TNT���VA+TNT�����SOD��CAT��GSH-Px��Ѫ��SOD��CAT���Ծ������ڶ����飻VA+TNT���ijЩø��������������������Ӧ��TNT�顣�ɱ�6�ͱ�7�������������ͬʱ��TNT������TNT���VA+TNT�����SOD��CAT��GSH-Px��Ѫ��SOD��CAT�����ڴ���24 h��ĸ���ʱ�����������������ڶ����飻VA+TNT���ijЩø������������������TNT�飬�ڴ������24 h��Ϊ���ԡ�������VAǰ����ʹ��Kupfferϸ�����ܱ�������ͷŻ�������ʹ��SOD��CAT��GSH-Px�������ߡ�����SOD��CAT��������������Ӧ����TNT��ȽϾ����������ƣ��������������ԡ�����TNTͨ����ԭ�����Kupfferϸ�����ܱ���ͷŻ����������������˹�ϵ����
��H2O2[1��2]����2�ͱ�3�����������ͬ�����Ͳ�ͬʱ��VA+TNT���ϴ�����Ѫ��ALT��AST���Ծ����Ը��ڶ��������Ӧ����TNT��(P<0.05��P<0.01)��������VAǰ������ɼ�ǿTNT�ζ��ԡ�Ȼ��������VA��Ѫ��ALT��AST���Խӽ�������ˮƽ������VAδ��ʾ���и���ԡ��ɱ�4�ͱ�5�ɼ�������ͬ����TNT������TNT���VA+TNT�����SOD��CAT��GSH-Px��Ѫ��SOD��CAT���Ծ������ڶ����飻VA+TNT���ijЩø��������������������Ӧ��TNT�顣�ɱ�6�ͱ�7�������������ͬʱ��TNT������TNT���VA+TNT�����SOD��CAT��GSH-Px��Ѫ��SOD��CAT�����ڴ���24 h��ĸ���ʱ�����������������ڶ����飻VA+TNT���ijЩø������������������TNT�飬�ڴ������24 h��Ϊ���ԡ�������VAǰ����ʹ��Kupfferϸ�����ܱ�������ͷŻ�������ʹ��SOD��CAT��GSH-Px�������ߡ�����SOD��CAT��������������Ӧ����TNT��ȽϾ����������ƣ��������������ԡ�����TNTͨ����ԭ�����Kupfferϸ�����ܱ���ͷŻ����������������˹�ϵ����
, ��Ĵҽҩ
��֪SOD����Ҫ�����ǽ� ת��ΪH2O2��CAT�ֽ��ϸ���ڹ������ɵ�H2O2(8��9)����VAǰ������Ĵ�������Ѫ����SOD��CAT��GSH-Px���Բ����������ڶ����飬������������Ӧ��TNT�飬��ʾ��ϸ���ڻ����������ɳ���ͨ��TNT�Ļ�ԭ������⣬��������Kupfferϸ���Ļ�ͷ��йء�
ת��ΪH2O2��CAT�ֽ��ϸ���ڹ������ɵ�H2O2(8��9)����VAǰ������Ĵ�������Ѫ����SOD��CAT��GSH-Px���Բ����������ڶ����飬������������Ӧ��TNT�飬��ʾ��ϸ���ڻ����������ɳ���ͨ��TNT�Ļ�ԭ������⣬��������Kupfferϸ���Ļ�ͷ��йء�
���о��������������Kupfferϸ����VA��ɼ�ǿTNT�ĸζ��ԣ�����ΪѪ��ALT��AST�������ߣ�ͬʱ��ʹ�ø���SOD��CAT��GSH-Px��Ѫ��SOD��CAT�������ߡ��Ʋ�VAǰ�������ǿTNT�ζ��ԣ����ֹ�����kupfferϸ������ͷŻ������йء�Ȼ�������о������ų�TNT����ͨ����ԭ����ɻ�������
�����
, ��Ĵҽҩ
[1] ��Ȫ�ۡ���ΰ.*****�ڴ����ԡ����ࡢ������غ��Ļ�ԭ�.��������ѧ��־��1987��1��37-39.
[2] �����¡���Ȫ�ۡ�����ɽ.*****�ڴ�����������������廹ԭ�.��������ѧ��־��1988��2��87-90.
[3] Wisse E.An ultrastructural characterization of the endothelial cell in the rat liver sinusoid under normal and various experimental conditions,as a contribution to the distinction between endothelial and Kupffer cells.J Ultrastruct Res.1972,38:528-535.
[4] Wake K,Decker K.Cell biology and kinetics of Kupffer cells in the liver.Int Rev Cytol��1989,118:173-179.
, ��Ĵҽҩ
[5] Laskin DL,Pilaro AM.Potential role of activated macrophages in acetaminophen hepatotoxicity:Isolation and characterization of activated macrophages from rat liver.Toxicol Appl Pharmacol��1986,98:204-215.
[6] Rubin R,Farber JL.Mechanisms of the killing of cultured hepatocytes by hydrogen peroxide.Arch Biochem Biophys��1984,228:450-459.
[7] Shieatori Y,Taklkawa H.Superoxide anion generating capacity and lysosomal enzyme activities of Kupffer cells in galactosamine-induced hepatitis.Gastroenterol Jpn,1986,21:135-144.
, http://www.100md.com
[8] Halliwell B,Gutteridge JMC.Oxygen toxicity,oxygen radicals,transition metals and disease.Biochem J,1984,219:1-14.
[9] Roney PL,Holian A.Possible mechanism of chrysotile asbestos-stimulated superoxide anion production in guinea pig alveolar macrophages.Toxicol Appl Pharmacol,1989,100:132-144.
(�ո����ڣ�1998-10-28), ��Ĵҽҩ
��λ����ΰ ��Ԫѫ ��Ⱥ �■(����ҽ�ƴ�ѧ�Ͷ����������ң�100083)�������� ����(����ʡƽ��ɽú̼����ѧУ)����Ѹ ������(����ʡ�Ͷ�����ְҵ��������)
�ؼ��ʣ�*****���ݷ���ϸ�����ζ��ԣ�������������
��������ѧ��־000211 ��ժҪ�� Ŀ�� ̽�ִ������Kupfferϸ�����ܻ��TNT�ζ��ԵĹ�ϵ�����ܻ��ơ����� ����Kupfferϸ�����ܻ�Ĵ���ģ�ͣ��۲�TNT��VA+TNT���ϴ�������Ѫ����ALT��AST�������Ѫ����SOD��CAT��GSH-Px���Եı仯����� TNT��Ѫ����ALT��AST�������Ե��ڶ����飬��VA+TNT�������Ը��ڶ��������ӦTNT�顣TNT������Ѫ����SOD��CAT��GSH-Px���������ͷdz��������ڶ�����(P<0.05��P<0.01)��VA+TNT��ijЩø���������ͷdz��������ڶ��������Ӧ��TNT��(P<0.05��P<0.01)��TNT�ɼ�ǿ��Kupfferϸ�����ܻ����ĸζ��ԡ����� �������Kupfferϸ����VA��ɼ�ǿTNT�ζ��ԣ��Ʋ����������������йء�
, ��Ĵҽҩ
The relationship between functional activation of Kupffer cells in rat liver and TNT-induced hepatotoxicity
CUI Jing-Wei,CHANG Yuan-Xun,GUO Qun,(Department.of Occupational Health,Beijing Medical University,Beijing 100083,China.)
��Abstract�� Objective To explore the relationship between the functional activation of Kupffer cells in rat livers and TNT-induced hepatotoxicity in order to define possible mechanism of TNT-induced liver injury.Methods The model of the functional activation of rat Kupffer cells was observed during the acute exposure of TNT.Results The activities of ALT and AST in sera of TNT-treated rats were more lower than those of controls,while activities of ALT and AST in sera of VA+TNT-treated rats rose significantly.The activation of SOD,CAT and GSH-Px rose significantly in sera and liver of TNT and VA+TNT-treated rats.The changes could be seen more clearly under the condition of VA+TNT treatment.The functional activation of Kupffer cells in liver of VA+TNT-treated rats could enhance TNT-induced hepatoxicity.Conclusion Kupffer cells activated by VA,can intensify TNT-induced hepatotoxicity,which is presumed to be related with generation of reative oxygen.
, ��Ĵҽҩ
��Key words�� Trinitrotoluene; Kupffer cell; Hepatotoxicity; Reactive oxygen; Rats
��֪TNT��Ҫ�ڸ���ͨ��������ԭ�շ�������(O��(-)/(*) 2)����[1��2]������TNTΪ����Ӧ���������ݷ�(Kupffer)ϸ����λ�ڸ�Ѫ��ڵľ���ϸ������ѪҺֱ�ӽӴ��������ѪҺ�к��ɷּ�������ԭ������Ӧ��ȶ��ֹ���[3��4]��������ʵ�������ijЩ��ѧ�ﴦ�������Kupffcrϸ�����ֿ��ټ��ۣ�ϸ�����ܱ�������ͷų��������ͻ��Ե��ȶ��ֽ���[5��7]�����о���ͼ����֪��Kupfferϸ�����ά����A��������۲�TNT�����ԵĹ�ϵ��
1 �����뷽��
TNT�Ǻ���ƽ��ɽúҵ(����)��˾ij�������ṩ�����û�����ʵ���Ҳⶨ����Ϊ99.9 %��
, ��Ĵҽҩ
1.1 ����ģ���Ʊ�
1.1.1 ʵ�鶯�P���� ѡ�ý�������Wistar����28ֻ������170��200 g�������Ϊ4�飬ÿ��7ֻ��(1)�����飻(2)ά����A������(VA��)��(3)���Ȼ�̼������(CCl4��)��(4)VA��CCl4���ϴ�����(VA+CCl4��)��������ÿ�վ��ڸ���1.5 ml/100 g�����������Ϊ10 %�ı��������������Ϊ7 %������-20������7 d��VA���VA+CCl4��ÿ�վ��ڸ���250 000 IU/kg����VA(���ڱ�����������-20)������7 d��VA+CCl4���CCl4����VA�������8�죬����ǻע��(ip)0.15 ml/kg����CCl4(����������)��
1.1.2 �۲�ָ���뷽�� ����������24 h��ÿ�������ͷ����5ֻ����ȡѪ��ⶨ������ת��ø(ALT)����(��)������ת��ø(AST)�Ļ��ԡ�
, ��Ĵҽҩ
1.2 TNT����Ⱦ��ʵ��
1.2.1 TNT��ͬ��������Ⱦ�� ѡ�ý�������Wistar����100ֻ������170��200 g�������Ϊ10�飬ÿ��10ֻ���ֱ�Ϊ�����飻VA�飻TNT250��500��1 000��2 000 mg/kg�飻VA+TNT250��500��1 000��2 000 mg/kg�顣VA���VA+TNT��ÿ�վ��ڸ���VA250 000 IU/kg����������7 d����8����鰴��ͬ�������ڸ���TNT(�����ڵ��ۻ���Һ)��Ⱦ����24 h�������
1.2.2 TNT��ͬʱ�伱��Ⱦ�� ѡ�ý�������Wistar����90ֻ������170��200 g�������Ϊ3�顣�ֱ�Ϊ������(10ֻ)��TNT1 000 mg/kg��(40ֻ)��VA+TNT1 000 mg/kg��(40ֻ)��VA+TNT��ÿ�վ��ڸ���VA250 000 IU/kg����������7 d���ڵ�8�쾭�ڸ���1 000 mg/kgTNT(�����ڵ��ۻ���Һ)���ֱ���Ⱦ�����12��24��36��48 h�������
, ��Ĵҽҩ
1.2.3 �۲�ָ�꼰���� ÿ�������ͷ����5ֻ�����ﴦ����Ѹ��ȡ����������ಢ�Ʊ��Σ����Ƚ���Ѫ�壬�ֱ�ⶨ�κ����Ƚ��г��������绯ø(SOD)��������ø(CAT)���Ƚ��й����Ĺ�������ø(GSH-Px)�Ļ��Լ��������Լ�Ѫ����ALT��AST��SOD��CAT�Ļ��ԡ�
2 ���
2.1 ����ģ���Ʊ�
��1 CCl4�Դ���Ѫ��ALT��AST����(U/L)��Ӱ��(
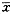 ��s) ���
��s) ���ALT����
AST����
VA��
, ��Ĵҽҩ
113.61��24.05
159.06��23.76
CCl4��
140.38��42.10
179.14��42.28
VA+CCl4��
275.51��24.53* *
451.34��35.83* *
������
95.91��12.24
, ��Ĵҽҩ
135.14��15.73
������顢VA���CCl4��Ƚϣ�* *P<0.01
�ɱ�1�ɼ�VA���CCl4�����Ѫ��ALT��AST���Ծ����ڶ����飬�������������ԡ�VA+CCl4�����Ѫ��ALT��AST���Ծ����������ڶ����顢VA���CCl4��(P<0.01)��
2.2 VA�Լ�ǿTNT�ζ��Ե�Ӱ��
2.2.1 Ѫ��AST��ALT����
�ɱ�2�ɼ�����VA+TNT���������У�Ѫ��ALT�����������ڶ��������Ӧ������TNT��(P<0.05��P<0.01)����250 mg/kg���⣬Ѫ��AST���Ծ����������ڶ��������Ӧ������TNT������(P<0.01)��
, ��Ĵҽҩ
��2 ���ϴ���24 h����Ѫ��ALT��AST����(U/L)�ı仯(
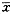 ��s)
��s)������
VA��
TNT��(mg/kg)
VA+TNT��(mg/kg)
250
500
1 000
2 000
250
500
, ��Ĵҽҩ
1 000
2 000
ALT
101.27
��5.92
108.08
��8.20
89.92
��10.20
92.68
��15.45
87.20
��17.34
, http://www.100md.com
78.75
��16.11
126.41
��17.90* # #
138.28
��8.94* * # #
173.90
��11.54* * # #
175.82
��8.59* * # #
AST
, ��Ĵҽҩ
135.14
��12.79
142.30
��16.54
132.17
��13.15
122.92
��11.84
129.75
��18.55
127.81
��15.87
, ��Ĵҽҩ 142.65
��8.41
151.73
��9.77* * # #
185.95
��9.80* * # #
205.50
��21.13* * # #
�������Ƚϣ�*P<0.05��* *P<0.01������ͬ����TNT������Ƚϣ�# #P<0.01��3 ��ͬʱ�����Ѫ��ALT��AST����(U/L)�ı仯(
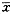 ��s)
��s), ��Ĵҽҩ
���
12 h
24 h
36 h
48 h
ALT
TNT��
102.14�� 6.56
93.41��13.76
88.35��14.48
90.27��11.20
VA+TNT��
, http://www.100md.com
105.81�� 8.02
167.96��16.63* * # #
165.87��12.35* * # #
169.02��10.66* * # #
������
102.32�� 6.00
112.54��12.58
AST
TNT��
132.19��10.53
, ��Ĵҽҩ
126.84�� 8.95
125.09��16.90
125.28��15.84
VA+TNT��
139.93��11.65
177.22��13.04* * # #
169.36��21.02* * # #
172.85��11.38* * # #
������
135.84��15.25
, ��Ĵҽҩ
119.98��18.45
�������Ƚϣ�* *P<0.01������ͬ����TNT��Ƚϣ�# #P<0.01 TNTȾ������Ϊ1 000mg/kg���ɱ�3�ɼ�����VA+TNT���ϴ���24 h���ʱ���Ѫ��ALT��AST���Ծ����������ڶ��������Ӧ��TNT��(P<0.01)��
2.3 ��ijЩ������ø���Ե�Ӱ��
2.3.1 TNT��ͬ����������SOD��CAT��GSH-Px�ı仯
�ɱ�4�ɼ���TNT���250 mg/kg���⣬��������������SOD�����������������ڶ�����(P<0.05��P<0.01)��VA+TNT�����SOD�����������������ڶ��������Ӧ������TNT��(P<0.05��P<0.01)��TNT���VA+TNT��1 000��2 000 mg/kg�����CAT���Ծ��������ڶ�����(P<0.05��P<0.01)��VA+TNT1 000 mg/kg�����CAT���Լ�����������Ӧ������TNT��(P<0.01)��TNT1 000 mg/kg ���VA+TNT�����������GSH-Px���Ծ��������������ڶ�����(P<0.05��P<0.01)����VA+TNT2 000 mg/kg���⣬������������������������Ӧ������TNT��(P<0.05��P<0.01)��
, http://www.100md.com
�ɱ�5�ɼ�����TNT250 mg/kg���⣬TNT�������������VA+TNT��������Ѫ��SOD���Ծ��������������ڶ�����(P<0.05��P<0.01)��VA+TNT 1 000��2 000 mg/kg��Ѫ��SOD�����������ڶ��������Ӧ����TNT��(P<0.05��P<0.01)��TNT 1 000��2 000 mg/kg�鼰��VA+TNT250 mg/kg����Ѫ��CAT�����������������ڶ����飻VA+TNT1 000 mg/kg��Ѫ��CAT��������������Ӧ������TNT��(P<0.05)��
2.3.2 TNT��ͬʱ�䴦����SOD��CAT��GSH-Px���Եı仯
TNTȾ������Ϊ1 000 mg/kg���ɱ�6�ɼ���TNT���VA+TNT���ڴ���24 h��ĸ���ʱ��㣬����SOD��CAT��GSH-Px�Ļ����������������ڶ�����(P<0.05��P<0.01)��VA+TNT���ڴ������24 h��36 h����SOD������������TNT��(P<0.05)��24 h��48 h����CAT������������������TNT��(P<0.05��P<0.01)��24 h����GSH-Px������������TNT��(P<0.05)��
, ��Ĵҽҩ
��4 �������SODa��CATb��GSH-Pxc���Եı仯(
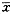 ��s)
��s)������
TNT��(mg/kg)
VA+TNT��(mg/kg)
250
500
1 000
2 000
250
500
, ��Ĵҽҩ
1 000
2 000
SOD
360.64
��67.50
405.58
��78.95
452.95
��71.44*
485.61
��76.61* *
446.50
, http://www.100md.com
��63.41* *
489.04
��86.72* * # #
499.25
��86.30* * #
509.48
��83.14* * #
448.00
��60.08* *
CAT
43.31
, ��Ĵҽҩ
��5.50
42.89
��6.42
44.62
��4.25
51.44
��3.46*
54.99
��4.85* *
43.76
��2.12
46.02
, ��Ĵҽҩ
��3.81
58.14
��4.44* * #
56.34
��6.35* *
GSH-Px
����
847.61
��23.47
834.11
��22.88
855.91
, ��Ĵҽҩ
��32.73
899.58
��18.59* *
883.63
��47.40
877.51
��14.69* # #
899.16
��24.96* * #
990.88
��36.73* # #
, ��Ĵҽҩ
925.77
��29.91* *
a:U/mg���ף� b��mmol H2O2/30 min-1*mg-1�� c:U/g��
�������Ƚϣ�*P<0.05��* *P<0.01������ͬ����TNT������Ƚϣ�#P<0.05��# #P<0.01��5 ����Ѫ��SODa��CATb���Եı仯(
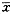 ��s)
��s)������
TNT��(mg/kg)
, ��Ĵҽҩ
VA+TNT��(mg/kg)
250
500
1 000
2 000
250
500
1 000
2 000
SOD
98.39
��16.53
105.89
, ��Ĵҽҩ
��25.72
121.81
��28.41*
127.41
��24.23*
145.74
��24.26* *
117.43
��26.78*
127.77
��25.08* *
, http://www.100md.com
136.97
��14.52* * #
159.59
��18.96* * #
CAT
2.75
��0.72
2.66
��0.88
2.84
��0.68
3.19
, http://www.100md.com
��0.62*
3.76
��0.82*
2.93
��0.41
3.03
��0.70*
3.76
��0.76* * #
3.85
��0.52*
, ��Ĵҽҩ
a:U/mg�� b��mmol H2O2/30 min-1*mg-1
�������Ƚϣ�*P<0.05��* *P<0.01������ͬ����TNT������Ƚϣ�#P<0.05 ��6 ��ͬʱ���������SODa��CATb��GSH-Pcx�Ļ��Եı仯(
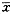 ��s)
��s)���
12 h
24 h
36 h
, ��Ĵҽҩ
48 h
SOD
TNT��
361.83��38.61
411.90��41.34*
409.20��59.95*
395.59��44.46*
VA+TNT��
369.30��19.11
453.11��31.08* * #
, ��Ĵҽҩ 432.85��42.56* * #
410.23��33.63*
������
355.96��44.65
369.58��38.77
CAT
TNT��
44.24��5.35
50.49��5.52*
53.76��8.44*
59.22��4.13* *
, ��Ĵҽҩ
VA+TNT��
47.18��4.22
58.89��5.09* # #
58.59��3.18* *
62.40��4.89* * #
������
41.95��5.64
43.58��8.65
GSH-Px
TNT��
840.08��28.36
, http://www.100md.com
897.58��19.19* *
871.21��28.25*
860.66��16.04*
VA+TNT��
829.24��21.25
961.61��44.39* * #
900.53��23.76* *
950.73��55.46*
������
834.12��16.63
, ��Ĵҽҩ
835.43��17.56
a:U/mg���ף� b��mmol H2O2/30 min-1*mg-1�� c:U/g�� �������Ƚϣ�*P<0.05��* *P<0.01������ͬ����TNT��Ƚϣ�#P<0.05��# #P<0.01
��7 ��ͬʱ������Ѫ����SODa��CATb���Եı仯(
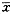 ��s)
��s)���
12 h
24 h
, ��Ĵҽҩ
36 h
48 h
SOD
TNT��
107.27��16.02
124.42��38.14*
119.75��21.20*
126.81��37.55*
VA+TNT��
103.65��12.59
139.76��29.77* * #
, http://www.100md.com
133.39��21.96* #
131.45��25.59* *
������
110.49��21.43
94.36��11.85
CAT
TNT��
3.01��0.56
3.85��0.77* *
3.85��0.97*
3.78��0.50* *
, ��Ĵҽҩ
VA+TNT��
3.19��0.53
4.25��0.83* * #
3.96��0.61*
3.95��0.70* *
������
2.64��0.38
2.91��0.42
a:U/mg���ף� b:mmol H2O2/30min-1\5mg-1 �������Ƚϣ�*P<0.05��* *P<0.01������ͬ����TNT��Ƚϣ�#P<0.05
, ��Ĵҽҩ
TNTȾ������Ϊ1 000 mg/kg���ɱ�7�ɼ���TNT���VA+TNT���ڴ���24 h��ĸ���ʱ��㣬Ѫ��SOD��CAT�Ļ����������������ڶ�����(P<0.05��P<0.01)��VA+TNT���ڴ�����24 h��36 hѪ��SOD������������TNT��(P<0.05)��24 hѪ��CAT������������TNT��(P<0.05)�����Ƚ���SOD��CAT�����������ȽϾ����������ƣ��������������ԡ�
3 ����
�ɱ�1�ɼ�����������֪��kupfferϸ�����VA��������7 d���پ���ǻע��CCl4(0.15 ml/kg)������Ѫ��ALT��AST���Լ��������ڶ����顢VA���CCl4��(P<0.01)������VA������kupfferϸ�����ܱ���ɼ�ǿCCl4�Դ���ĸζ��ԣ��ɴ˿ɼ�������ģ��ʵ���Ʊ��dzɹ��ġ�
��ȥ�о�֤ʵ��TNT���ڴ�����������������ͨ��������ԭ�����
 ��H2O2[1��2]����2�ͱ�3�����������ͬ�����Ͳ�ͬʱ��VA+TNT���ϴ�����Ѫ��ALT��AST���Ծ����Ը��ڶ��������Ӧ����TNT��(P<0.05��P<0.01)��������VAǰ������ɼ�ǿTNT�ζ��ԡ�Ȼ��������VA��Ѫ��ALT��AST���Խӽ�������ˮƽ������VAδ��ʾ���и���ԡ��ɱ�4�ͱ�5�ɼ�������ͬ����TNT������TNT���VA+TNT�����SOD��CAT��GSH-Px��Ѫ��SOD��CAT���Ծ������ڶ����飻VA+TNT���ijЩø��������������������Ӧ��TNT�顣�ɱ�6�ͱ�7�������������ͬʱ��TNT������TNT���VA+TNT�����SOD��CAT��GSH-Px��Ѫ��SOD��CAT�����ڴ���24 h��ĸ���ʱ�����������������ڶ����飻VA+TNT���ijЩø������������������TNT�飬�ڴ������24 h��Ϊ���ԡ�������VAǰ����ʹ��Kupfferϸ�����ܱ�������ͷŻ�������ʹ��SOD��CAT��GSH-Px�������ߡ�����SOD��CAT��������������Ӧ����TNT��ȽϾ����������ƣ��������������ԡ�����TNTͨ����ԭ�����Kupfferϸ�����ܱ���ͷŻ����������������˹�ϵ����
��H2O2[1��2]����2�ͱ�3�����������ͬ�����Ͳ�ͬʱ��VA+TNT���ϴ�����Ѫ��ALT��AST���Ծ����Ը��ڶ��������Ӧ����TNT��(P<0.05��P<0.01)��������VAǰ������ɼ�ǿTNT�ζ��ԡ�Ȼ��������VA��Ѫ��ALT��AST���Խӽ�������ˮƽ������VAδ��ʾ���и���ԡ��ɱ�4�ͱ�5�ɼ�������ͬ����TNT������TNT���VA+TNT�����SOD��CAT��GSH-Px��Ѫ��SOD��CAT���Ծ������ڶ����飻VA+TNT���ijЩø��������������������Ӧ��TNT�顣�ɱ�6�ͱ�7�������������ͬʱ��TNT������TNT���VA+TNT�����SOD��CAT��GSH-Px��Ѫ��SOD��CAT�����ڴ���24 h��ĸ���ʱ�����������������ڶ����飻VA+TNT���ijЩø������������������TNT�飬�ڴ������24 h��Ϊ���ԡ�������VAǰ����ʹ��Kupfferϸ�����ܱ�������ͷŻ�������ʹ��SOD��CAT��GSH-Px�������ߡ�����SOD��CAT��������������Ӧ����TNT��ȽϾ����������ƣ��������������ԡ�����TNTͨ����ԭ�����Kupfferϸ�����ܱ���ͷŻ����������������˹�ϵ����, ��Ĵҽҩ
��֪SOD����Ҫ�����ǽ�
 ת��ΪH2O2��CAT�ֽ��ϸ���ڹ������ɵ�H2O2(8��9)����VAǰ������Ĵ�������Ѫ����SOD��CAT��GSH-Px���Բ����������ڶ����飬������������Ӧ��TNT�飬��ʾ��ϸ���ڻ����������ɳ���ͨ��TNT�Ļ�ԭ������⣬��������Kupfferϸ���Ļ�ͷ��йء�
ת��ΪH2O2��CAT�ֽ��ϸ���ڹ������ɵ�H2O2(8��9)����VAǰ������Ĵ�������Ѫ����SOD��CAT��GSH-Px���Բ����������ڶ����飬������������Ӧ��TNT�飬��ʾ��ϸ���ڻ����������ɳ���ͨ��TNT�Ļ�ԭ������⣬��������Kupfferϸ���Ļ�ͷ��йء����о��������������Kupfferϸ����VA��ɼ�ǿTNT�ĸζ��ԣ�����ΪѪ��ALT��AST�������ߣ�ͬʱ��ʹ�ø���SOD��CAT��GSH-Px��Ѫ��SOD��CAT�������ߡ��Ʋ�VAǰ�������ǿTNT�ζ��ԣ����ֹ�����kupfferϸ������ͷŻ������йء�Ȼ�������о������ų�TNT����ͨ����ԭ����ɻ�������
�����
, ��Ĵҽҩ
[1] ��Ȫ�ۡ���ΰ.*****�ڴ����ԡ����ࡢ������غ��Ļ�ԭ�.��������ѧ��־��1987��1��37-39.
[2] �����¡���Ȫ�ۡ�����ɽ.*****�ڴ�����������������廹ԭ�.��������ѧ��־��1988��2��87-90.
[3] Wisse E.An ultrastructural characterization of the endothelial cell in the rat liver sinusoid under normal and various experimental conditions,as a contribution to the distinction between endothelial and Kupffer cells.J Ultrastruct Res.1972,38:528-535.
[4] Wake K,Decker K.Cell biology and kinetics of Kupffer cells in the liver.Int Rev Cytol��1989,118:173-179.
, ��Ĵҽҩ
[5] Laskin DL,Pilaro AM.Potential role of activated macrophages in acetaminophen hepatotoxicity:Isolation and characterization of activated macrophages from rat liver.Toxicol Appl Pharmacol��1986,98:204-215.
[6] Rubin R,Farber JL.Mechanisms of the killing of cultured hepatocytes by hydrogen peroxide.Arch Biochem Biophys��1984,228:450-459.
[7] Shieatori Y,Taklkawa H.Superoxide anion generating capacity and lysosomal enzyme activities of Kupffer cells in galactosamine-induced hepatitis.Gastroenterol Jpn,1986,21:135-144.
, http://www.100md.com
[8] Halliwell B,Gutteridge JMC.Oxygen toxicity,oxygen radicals,transition metals and disease.Biochem J,1984,219:1-14.
[9] Roney PL,Holian A.Possible mechanism of chrysotile asbestos-stimulated superoxide anion production in guinea pig alveolar macrophages.Toxicol Appl Pharmacol,1989,100:132-144.
(�ո����ڣ�1998-10-28), ��Ĵҽҩ