环磷酰胺与异环磷酰胺致肝毒性机制的比较
作者:施畅 廖明阳
单位:军事医学科学院毒物药物研究所,北京 100850
关键词:环磷酰胺;异环磷酰胺;巯基;P450;肝脏
卫生毒理学杂志000210 【摘要】 目的 为阐明环磷酰胺(CP)和异环磷酰胺(IFO)肝脏毒作用机制。方法 给大鼠腹腔注射CP或IFO 40 mg.kg-1.d-1连续5 d,观察停药后1、4、7、10 d血清生化指标、肝组织中丙二醛含量、巯基状态和细胞色素P450含量的变化。结果 两组动物血浆生化指标和肝组织丙二醛含量没有显著变化,而肝组织总巯基、非蛋白巯基、蛋白结合巯基和细胞色素P450含量下降,蛋白巯基的消耗与总巯基含量下降相关。但两药引起上述变化的程度不同。肝微粒体总P450含量的变化趋势与巯基相似,CP组细胞色素P450含量给药结束后1、4、7、10 d分别下降了19.2 %、26.8 %、61.1 %、15.2 %,IFO组细胞色素P450仅在1、7 d分别下降20.7 %和40.2 %。结论 CP引起肝脏巯基和细胞色素P450含量下降程度明显强于1FO,表明这两种药物的差异可能与其毒性不同有关。
, 百拇医药
A comparative study on the mechanism(s) of the hepatotoxicity induced by Cyclophasphamide and Ifosfamide in rats
SHI Chang,LIAO Ming-Yang
(Institute of Pharmacology and Toxicology,The Academy of Military Medical Sciences,Beijing 100850,China.)
【Abstract】 Objective The present study was undertaken to investigate the differences of the hepatotocixity induced by Cyclophosphamide(CP)and its isomeric analogue ifosfamide(IFO).Methods The contents of malondialdehyde(MDA),sulfhydryl groups and micriosomal cytochromes(Cyt-P450) of live tissue and biochemical indexes of serum in rats exposed at doses of 40 mg/kg CP and IFO for 5 days after treatment 1、4、7 and 10 hr.Results The biochemical indexes of serum and contents of MDA of liver tissue didn't change significantly in both treated goups,while total,nonprotien, protienbound sulfhydryl and cyt-P450 contents of liver tissue were declined the decreases of protenbound sulfhydryl were associated with total sufhydryl's depletion.However,the extents of these changes caused by both drugs were different.The changes of Cyt-P450 contents were similar to those of suifhydryl groups.The decreases of Cyp-P450 contents were 19.2%、26.8%、61.1%、15.2% on day 1、4、7 and 10 in group-treated with cp,respectively,while in group-treated with IFO it was 20.7% and 40.2% only on day 1 and 7.Conclusion The results indicated that the changes of sulflydryl and Cyt-P450 contents of live the induced by CP were difference from IFO.The difference of the hepatotoxicity between CP and IFO probably was caused by the metabolic difference of both drugs.
, 百拇医药
【Key words】 Cyclophosphamide; Ifosfamide; Sulfhydryl Group; Cytochrome-P450; Liver
环磷酰胺(Cyclophosphamide,CP)是40年代人工合成的氮芥类烷化剂,是细胞周期非特异性的广谱抗肿瘤药。异环磷酰胺(Ifosfamide,IFO)是磷酰胺类衍生物,60年代中期首次在德国合成,于80年代进入临床,与CP在结构上仅有一个氯乙基的位置不同。
研究表明,两者在体外均无活性,需进入体内经肝脏P450氧化裂环,生成有活性的中间代谢产物才能与DNA等生物大分子发生共价结合,因此肝脏是两者的代谢活化器官也是毒作用靶器官。动物实验证明CP致大鼠肝细胞脂质过氧化增强,肝组织中丙二醛(MDA)含量升高,谷胱甘肽耗竭,微粒体细胞色素P450下降。临床也观察到CP可引起部分患者肝功能损害,血清转氨酶升高,胆汗分泌异常,出现黄疸。而IFO对肝毒性动物实验则未见专门报道,临床观察肝损伤发生率为0 %~20 %[1]。本研究采用同等剂量,重复给药后不同时间取材检测两药对血浆多项生化指标、肝组织MDA、巯基状态和肝微粒体酶的影响,为阐明两药对肝脏的毒性和毒作用机制,比较两药对肝脏的毒性大小和特征,指导临床合理用药提供实验依据。
, 百拇医药
1 材料与方法
1.1 实验动物 雄性Wistar大鼠,180~220 g,由军事医学科学院实验动物中心提供。动物饲养昼夜循环为10/14 h,环境温度为25 ℃左右,自由饮食进水。
1.2 药物来源 CP由上海华联制药有限公司生产,批号:980106。IFO由连云港恒瑞制药有限公司生产,批号:9902092。
1.3 动物分组及给药途径 大鼠按体重由计算机随机分组,即CP40 mg.kg-1.d-1×5 d组、IFO40 mg.kg-1.d-1×5 d组、阳性对照(CCl4)组、正常对照组。每组均观察给药结束后1、4、7、10 d各项指标的变化,每个时间点3只动物。给药途径为腹腔注射,给药容量为5 ml/kg。CP、IFO用生理盐水溶解,给药时临时配制,CCl4以花生油为溶剂,剂量为1 600 mg.kg-1.d-1×1 d,观察24 h,即在检测前1天给药,正常对照组给予生理盐水。
, http://www.100md.com
1.4 检测指标及方法 血浆生化指标用7020全自动生化仪(日本,日立公司)检测。肝组织中MDA含量用硫代巴比妥酸法测定[2]。总巯基(TSH)、非蛋白巯基(NPSH)测定用DTNB法,蛋白巯基(PSH)含量=TSH-NPSH[3]。以钙沉淀法制备肝脏微粒体,用Lowry法测定微粒体蛋白含量,采用CO吹泡测450 nm与490 nm 处差示光谱,计算P450含量,以nmol/mg蛋白表示[4]。
1.5 统计处理 采用SAS软件包进行方差分析和Dunnett'st检验。
2 结果
2.1 CP与IFO对血浆生化指标的影响 大鼠分别经腹腔注射CP、IFO 40 mg.kg-1.d-1×5 d后,不同时间点测定血浆ALT、AST、ALP、G-GT、TBILI和LDH 6项生化指标。各项指标在各时间点未见明显变化,与正常对照组比较差异无显著性(表1)。提示两药没有引起细胞膜的直接损伤。
, 百拇医药
2.2 CP与IFO对肝组织MDA含量的影响 CP和IFO重复给药后大鼠肝组织MDA含量的影响见表2。从表中可以看出,两组动物不同时间点肝组织MDA未见明显变化,与正常对照组比较,差异无统计学意义。
表1 CP和IFO对大鼠血浆生化指标的影响 组别(mg/kg)
ALT
(U/L)
AST
(U/L)
ALP
(U/L)
G-GT
(U/L)
, 百拇医药
TBILI
(μmol/L)
LDH
(U/L)
CP 40
-
-
-
-
-
-
IFO 40
-
, 百拇医药
-
-
-
-
-
CCl4 1 600
+
+
-
-
+
+
正常对照
, 百拇医药 -
-
-
-
-
-
+表示阳性,-表示阴性表2 重复给药后不同时间肝组织MDA含量的变化( ±s) 组别(mg/kg)
±s) 组别(mg/kg)
MDA(μmol/g肝)
1 d
4 d
7 d
, 百拇医药
10 d
CP 40
0.508±0.062
0.564±0.150
0.595±0.096
0.423±0.069
IFO 40
0.717±0.065
0.558±0.040
0.514±0.072
0.425±0.005
CCl4 1 600
, 百拇医药
1.116±0.177* *
1.028±0.231* *
0.948±0.207* *
0.964±0.159* *
正常对照组
0.556±0.039
0.499±0.047
0.441±0.004
0.469±0.028
与正常对照组比较,* *P<0.012.3 CP与IFO对肝组织巯基含量的影响 大鼠分别经腹腔注射CP、IFO40 mg.kg-1.d-1×5 d后,肝组织TSH、NPSH、PSH的变化分别见图1、2和表3。
, http://www.100md.com
给药后,两组动物肝组织中TSH含量均随时间延长呈逐步下降趋势,但下降的程度不同。CP组停药后1 d TSH即出现明显下降,与正常对照组比较差异有非常显著性(P<0.01),第4天持续下降,第7天降到最低值,而IFO组停药后1 d TSH下降不明显,第4天才开始下降,与正常对照组比,差异有显著性(P<0.05),到第7天降至最低值(P<0.01)。两组在第10天TSH含量均有所恢复,但与正常对照组比较,差异仍有显著性(P<0.01)。
CP组致NPSH下降的明显,到第7天降至最低值时与正常对照组比较,差异有显著性(P<0.01),而IFO致NPSH下降趋势则较为缓和,第7天也降至最低值。第10天两组的NPSH含量均有一定恢复,与正常对照组比较差异,无显著性。表3 重复给药后不同时间肝组织PSH含量的变化( ±s) 组别(mg/kg)
±s) 组别(mg/kg)
PSH(μmol/g肝)
, http://www.100md.com
1 d
4 d
7 d
10 d
CP40
12.82±0.42*
13.31±0.85* *
14.69±0.74* *
15.35±1.28* *
IFO40
17.05±2.81
, 百拇医药
16.15±1.21
15.19±0.83* *
17.28±0.35*
CCl41600
14.84±0.38
14.06±1.29* *
13.54±0.39* *
14.02±1.09* *
正常对照组
17.94±1.52
, 百拇医药
18.21±1.02
19.27±1.18
19.27±0.16
与正常对照组比较,*P<0.05,* *P<0.01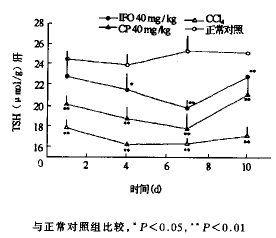
图1 重复给药后不同时间肝组织总巯基(TSH)变化
图2 重复给药后不同时间肝组织非蛋白巯基(NPSH)的变化
此外,两药对PSH的影响也较为明显,CP组在第1天就出现下降,第4、7、10天维持在一个较低的水平,P值均小于0.01。IFO组在药后第7天才出现显著下降(P<0.01),第10天略有恢复,但与正常对照组比较差异仍有统计学意义(P<0.05)。
, http://www.100md.com
2.4 CP与IFO对肝微粒体P450含量的影响 两药对P450含量的影响见图3。从图中可以看出,CP引起P450含量下降比IFO显著,给药结束后第1、4、7、10天CP组P450含量分别下降了19.2 %、26.8 %、61.1 %、15.2 %,而IFO组给药结束后1 d P450含量明显下降(20.7 %),4 d 后呈现恢复趋势,仅下降6.7 %,7 d 又下降40.2 %,到第10天则基本恢复正常。
图3 重复给药后不同时间肝组织P450含量变化
3 讨论
在中毒机制研究中,自由基和脂质过氧化理论是开展最早、研究最广泛和最成熟的理论之一,近年来,自由基对蛋白质的氧化损害也得到深入的研究。
文献报道,CP在经肝脏微粒体P450酶系代谢活化过程中消耗了P450,而其活性代谢产物Acroclein又直接抑制了P450同功酶及NADPH-细胞色素P450还原酶的活性[5],代谢活化过程大大增加了活性氧的含量,引发内质网膜系统脂质过氧化反应,胞内抗氧化防御体系通过非酶促反应清除自由基,GSH迅速耗竭[6]。我们研究发现大鼠小剂量重复腹腔注射CP或IFO后,肝组织P450含量、巯基状态发生明显改变,TSH、NPSH、PSH都有不同程度下降,其中PSH下降在TSH耗竭中起主要作用。可见两药致肝损伤作用机制有相同的一面,即P450酶系的抑制、自由基导致的氧化应激都有一定作用。由于蛋白质是自由基攻击的重要靶分子,其中蛋白质的巯基是外源性化学物或其活性代谢物攻击的最敏感的亲核靶基团,TSH的损伤可导致重要功能酶活性改变,影响细胞内稳态,而GSH的耗竭又使TSH对氧化攻击、混合二硫化物、共价化合形成更为易感,因而巯基状态的改变CP、IFO致氧化性细胞损害中起到至关重要的作用。
, http://www.100md.com
上述变化中,IFO对巯基和P450的影响明显弱于CP,这可能与两者的代谢途径、活化速度不尽相同有关。CP、IFO进入体内后除了氧化裂环生成活性代谢产物外,IFO有50 %以上在活化前发生脱氯乙基作用,而CP经此途径不足10 %,同时IFO活化速度慢于CP,血浆等效剂量IFO∶CP约为3.5~5∶1。此外药代学研究表明IFO连续给药可使其清除加快,作用不减而毒性减轻,这可能也与两药毒性差异有一定关系。
与文献报道不同的是,我们没有观察到血浆生化指标和肝组织MDA含量的变化,这不能否定过氧化反应在两药致肝损伤中的作用。Sies对氧化应激的定义为:促氧化与抗氧化之间的平衡失调而倾向于前者,导致可能的损害,即氧化应激的组织改变也可能是由于所应用的抗氧化防御体系和修复系统的指标改变引起的,不一定达到对组织和细胞的损害程度。文献报道CP致游离肝细胞GSH耗竭后才出现脂质过氧化反应,最后引起细胞毒作用,此作用可被抗氧化剂延迟[7],而巯基对抗CP引起的过氧化损伤作用也是明确的[8]。业已证实自由基介导的蛋白质破坏甚至比脂质过氧化发生得更早[9],因而自由基、氧化应激在两药的肝损伤中的作用是不容忽视的。
, 百拇医药
综上,我们认为IFO与CP对肝脏的毒作用机制有相同之处,即过氧化损伤在两者致肝损害中都起了一定作用,但IFO对肝脏的毒性明显弱于CP,因而在治疗某些肿瘤时,可以用IFO代替CP,以减轻毒性。鉴于二者对肝脏的毒作用机制都与自由基、过氧化反应有一定关系,临床用药时可考虑与抗氧化剂、巯基试剂合用,从而达到保护作用。
另外,肝脏细胞色素P450酶系在CP与IFO的代谢活化过程中起到十分重要的作用。P450酶系主要包括细胞色素P450混合功能氧化酶、NADPH-细胞色素P450还原酶、细胞色素b5、NADPH-细胞色素b5还原酶。本试验只检测了总的P450含量以初步探讨CP与IFO对P450酶系的影响。国外对CP引起P450抑制已有比较深入的研究,在不同品系的大鼠P450含量下降的程度不同、亚型不同,还有性别差异,与血浆T3、T4水平有一定关系,同时细胞色素b5、NADPH-细胞色素P450还原酶活性也有一定下降[10]。本研究发现IFO对P450酶系也有一定的抑制作用,但较CP弱,抑制规律也不如CP明显,因而IFO对P450酶系的影响有待深入研究。
, 百拇医药
参考文献
[1] Paschke R,Worst P.Hepatotoxicity with etoposide-ifosfamide combination therapy.Onkologic,1988,11:273-275.
[2] Ohkawa H,Nobuko Ohishi.Assay for Lipid Peroxides in Animal Tissues by Thiobarbituric acid reaction.Anal Biochem,1979,95:351-358.
[3] Sedlak J,Raymond H.Linosay.Estimation of total、protein-bound and nonprotein sulfhydryl groups in tissue with ellman's reagent.Anal Biochem,1968,25:192-205.
, 百拇医药
[4] Omura T,Sato R.The carbon monoxide-binding pigment of liver microsomes.J Biol Chem,1964,239:2370-2385.
[5] Mcclure MT,Stupans I.Investigation of the mechanism by which Cyclophosphamide alters P450 in male rats.Biochem Pharmacol,1992,43:2655-2658.
[6] Lear L,Nation RL,Stupans I.Effects of CP and adriamycin on rat hepatic microsomal glucuronidation and lipid peroxidation.Biochem Pharmacol,1992 ,44:747-753.
, http://www.100md.com
[7] Khan S,Ramwani JJ,O'Brien PJ.Hepatocyte toxicity of mechlorethamine and other alkylating anticancer drugs.Role of lipid peroxidation.Biochem Pharmacol,1992 43:1963-1967.
[8] Roberts JC,Francetic DJ,Zera RT.Chemoprotection against Cyclophosphamide-induced urotoxicity:comparision of nine thiol protective agents.Anticancer Res,1994,14:389-396.
[9] 张铣,刘毓谷,主编.毒理学.北京:北京医科大学中国协和医科大学联合出版社,1997.136-153.
[10] Kraner JC,Morgan ET,Poet TS.Suppression of rat hepatic microsomal cytochromes P450 by cyclophosphamide is correlated with plasma thyroid hormone levels and display differential strain sensitivity.J Pharmacol Exp Ther,1996,276:258-264.
(收稿日期:1999-08-05), 百拇医药
单位:军事医学科学院毒物药物研究所,北京 100850
关键词:环磷酰胺;异环磷酰胺;巯基;P450;肝脏
卫生毒理学杂志000210 【摘要】 目的 为阐明环磷酰胺(CP)和异环磷酰胺(IFO)肝脏毒作用机制。方法 给大鼠腹腔注射CP或IFO 40 mg.kg-1.d-1连续5 d,观察停药后1、4、7、10 d血清生化指标、肝组织中丙二醛含量、巯基状态和细胞色素P450含量的变化。结果 两组动物血浆生化指标和肝组织丙二醛含量没有显著变化,而肝组织总巯基、非蛋白巯基、蛋白结合巯基和细胞色素P450含量下降,蛋白巯基的消耗与总巯基含量下降相关。但两药引起上述变化的程度不同。肝微粒体总P450含量的变化趋势与巯基相似,CP组细胞色素P450含量给药结束后1、4、7、10 d分别下降了19.2 %、26.8 %、61.1 %、15.2 %,IFO组细胞色素P450仅在1、7 d分别下降20.7 %和40.2 %。结论 CP引起肝脏巯基和细胞色素P450含量下降程度明显强于1FO,表明这两种药物的差异可能与其毒性不同有关。
, 百拇医药
A comparative study on the mechanism(s) of the hepatotoxicity induced by Cyclophasphamide and Ifosfamide in rats
SHI Chang,LIAO Ming-Yang
(Institute of Pharmacology and Toxicology,The Academy of Military Medical Sciences,Beijing 100850,China.)
【Abstract】 Objective The present study was undertaken to investigate the differences of the hepatotocixity induced by Cyclophosphamide(CP)and its isomeric analogue ifosfamide(IFO).Methods The contents of malondialdehyde(MDA),sulfhydryl groups and micriosomal cytochromes(Cyt-P450) of live tissue and biochemical indexes of serum in rats exposed at doses of 40 mg/kg CP and IFO for 5 days after treatment 1、4、7 and 10 hr.Results The biochemical indexes of serum and contents of MDA of liver tissue didn't change significantly in both treated goups,while total,nonprotien, protienbound sulfhydryl and cyt-P450 contents of liver tissue were declined the decreases of protenbound sulfhydryl were associated with total sufhydryl's depletion.However,the extents of these changes caused by both drugs were different.The changes of Cyt-P450 contents were similar to those of suifhydryl groups.The decreases of Cyp-P450 contents were 19.2%、26.8%、61.1%、15.2% on day 1、4、7 and 10 in group-treated with cp,respectively,while in group-treated with IFO it was 20.7% and 40.2% only on day 1 and 7.Conclusion The results indicated that the changes of sulflydryl and Cyt-P450 contents of live the induced by CP were difference from IFO.The difference of the hepatotoxicity between CP and IFO probably was caused by the metabolic difference of both drugs.
, 百拇医药
【Key words】 Cyclophosphamide; Ifosfamide; Sulfhydryl Group; Cytochrome-P450; Liver
环磷酰胺(Cyclophosphamide,CP)是40年代人工合成的氮芥类烷化剂,是细胞周期非特异性的广谱抗肿瘤药。异环磷酰胺(Ifosfamide,IFO)是磷酰胺类衍生物,60年代中期首次在德国合成,于80年代进入临床,与CP在结构上仅有一个氯乙基的位置不同。
研究表明,两者在体外均无活性,需进入体内经肝脏P450氧化裂环,生成有活性的中间代谢产物才能与DNA等生物大分子发生共价结合,因此肝脏是两者的代谢活化器官也是毒作用靶器官。动物实验证明CP致大鼠肝细胞脂质过氧化增强,肝组织中丙二醛(MDA)含量升高,谷胱甘肽耗竭,微粒体细胞色素P450下降。临床也观察到CP可引起部分患者肝功能损害,血清转氨酶升高,胆汗分泌异常,出现黄疸。而IFO对肝毒性动物实验则未见专门报道,临床观察肝损伤发生率为0 %~20 %[1]。本研究采用同等剂量,重复给药后不同时间取材检测两药对血浆多项生化指标、肝组织MDA、巯基状态和肝微粒体酶的影响,为阐明两药对肝脏的毒性和毒作用机制,比较两药对肝脏的毒性大小和特征,指导临床合理用药提供实验依据。
, 百拇医药
1 材料与方法
1.1 实验动物 雄性Wistar大鼠,180~220 g,由军事医学科学院实验动物中心提供。动物饲养昼夜循环为10/14 h,环境温度为25 ℃左右,自由饮食进水。
1.2 药物来源 CP由上海华联制药有限公司生产,批号:980106。IFO由连云港恒瑞制药有限公司生产,批号:9902092。
1.3 动物分组及给药途径 大鼠按体重由计算机随机分组,即CP40 mg.kg-1.d-1×5 d组、IFO40 mg.kg-1.d-1×5 d组、阳性对照(CCl4)组、正常对照组。每组均观察给药结束后1、4、7、10 d各项指标的变化,每个时间点3只动物。给药途径为腹腔注射,给药容量为5 ml/kg。CP、IFO用生理盐水溶解,给药时临时配制,CCl4以花生油为溶剂,剂量为1 600 mg.kg-1.d-1×1 d,观察24 h,即在检测前1天给药,正常对照组给予生理盐水。
, http://www.100md.com
1.4 检测指标及方法 血浆生化指标用7020全自动生化仪(日本,日立公司)检测。肝组织中MDA含量用硫代巴比妥酸法测定[2]。总巯基(TSH)、非蛋白巯基(NPSH)测定用DTNB法,蛋白巯基(PSH)含量=TSH-NPSH[3]。以钙沉淀法制备肝脏微粒体,用Lowry法测定微粒体蛋白含量,采用CO吹泡测450 nm与490 nm 处差示光谱,计算P450含量,以nmol/mg蛋白表示[4]。
1.5 统计处理 采用SAS软件包进行方差分析和Dunnett'st检验。
2 结果
2.1 CP与IFO对血浆生化指标的影响 大鼠分别经腹腔注射CP、IFO 40 mg.kg-1.d-1×5 d后,不同时间点测定血浆ALT、AST、ALP、G-GT、TBILI和LDH 6项生化指标。各项指标在各时间点未见明显变化,与正常对照组比较差异无显著性(表1)。提示两药没有引起细胞膜的直接损伤。
, 百拇医药
2.2 CP与IFO对肝组织MDA含量的影响 CP和IFO重复给药后大鼠肝组织MDA含量的影响见表2。从表中可以看出,两组动物不同时间点肝组织MDA未见明显变化,与正常对照组比较,差异无统计学意义。
表1 CP和IFO对大鼠血浆生化指标的影响 组别(mg/kg)
ALT
(U/L)
AST
(U/L)
ALP
(U/L)
G-GT
(U/L)
, 百拇医药
TBILI
(μmol/L)
LDH
(U/L)
CP 40
-
-
-
-
-
-
IFO 40
-
, 百拇医药
-
-
-
-
-
CCl4 1 600
+
+
-
-
+
+
正常对照
, 百拇医药 -
-
-
-
-
-
+表示阳性,-表示阴性表2 重复给药后不同时间肝组织MDA含量的变化(
 ±s) 组别(mg/kg)
±s) 组别(mg/kg)MDA(μmol/g肝)
1 d
4 d
7 d
, 百拇医药
10 d
CP 40
0.508±0.062
0.564±0.150
0.595±0.096
0.423±0.069
IFO 40
0.717±0.065
0.558±0.040
0.514±0.072
0.425±0.005
CCl4 1 600
, 百拇医药
1.116±0.177* *
1.028±0.231* *
0.948±0.207* *
0.964±0.159* *
正常对照组
0.556±0.039
0.499±0.047
0.441±0.004
0.469±0.028
与正常对照组比较,* *P<0.012.3 CP与IFO对肝组织巯基含量的影响 大鼠分别经腹腔注射CP、IFO40 mg.kg-1.d-1×5 d后,肝组织TSH、NPSH、PSH的变化分别见图1、2和表3。
, http://www.100md.com
给药后,两组动物肝组织中TSH含量均随时间延长呈逐步下降趋势,但下降的程度不同。CP组停药后1 d TSH即出现明显下降,与正常对照组比较差异有非常显著性(P<0.01),第4天持续下降,第7天降到最低值,而IFO组停药后1 d TSH下降不明显,第4天才开始下降,与正常对照组比,差异有显著性(P<0.05),到第7天降至最低值(P<0.01)。两组在第10天TSH含量均有所恢复,但与正常对照组比较,差异仍有显著性(P<0.01)。
CP组致NPSH下降的明显,到第7天降至最低值时与正常对照组比较,差异有显著性(P<0.01),而IFO致NPSH下降趋势则较为缓和,第7天也降至最低值。第10天两组的NPSH含量均有一定恢复,与正常对照组比较差异,无显著性。表3 重复给药后不同时间肝组织PSH含量的变化(
 ±s) 组别(mg/kg)
±s) 组别(mg/kg)PSH(μmol/g肝)
, http://www.100md.com
1 d
4 d
7 d
10 d
CP40
12.82±0.42*
13.31±0.85* *
14.69±0.74* *
15.35±1.28* *
IFO40
17.05±2.81
, 百拇医药
16.15±1.21
15.19±0.83* *
17.28±0.35*
CCl41600
14.84±0.38
14.06±1.29* *
13.54±0.39* *
14.02±1.09* *
正常对照组
17.94±1.52
, 百拇医药
18.21±1.02
19.27±1.18
19.27±0.16
与正常对照组比较,*P<0.05,* *P<0.01

图1 重复给药后不同时间肝组织总巯基(TSH)变化

图2 重复给药后不同时间肝组织非蛋白巯基(NPSH)的变化
此外,两药对PSH的影响也较为明显,CP组在第1天就出现下降,第4、7、10天维持在一个较低的水平,P值均小于0.01。IFO组在药后第7天才出现显著下降(P<0.01),第10天略有恢复,但与正常对照组比较差异仍有统计学意义(P<0.05)。
, http://www.100md.com
2.4 CP与IFO对肝微粒体P450含量的影响 两药对P450含量的影响见图3。从图中可以看出,CP引起P450含量下降比IFO显著,给药结束后第1、4、7、10天CP组P450含量分别下降了19.2 %、26.8 %、61.1 %、15.2 %,而IFO组给药结束后1 d P450含量明显下降(20.7 %),4 d 后呈现恢复趋势,仅下降6.7 %,7 d 又下降40.2 %,到第10天则基本恢复正常。

图3 重复给药后不同时间肝组织P450含量变化
3 讨论
在中毒机制研究中,自由基和脂质过氧化理论是开展最早、研究最广泛和最成熟的理论之一,近年来,自由基对蛋白质的氧化损害也得到深入的研究。
文献报道,CP在经肝脏微粒体P450酶系代谢活化过程中消耗了P450,而其活性代谢产物Acroclein又直接抑制了P450同功酶及NADPH-细胞色素P450还原酶的活性[5],代谢活化过程大大增加了活性氧的含量,引发内质网膜系统脂质过氧化反应,胞内抗氧化防御体系通过非酶促反应清除自由基,GSH迅速耗竭[6]。我们研究发现大鼠小剂量重复腹腔注射CP或IFO后,肝组织P450含量、巯基状态发生明显改变,TSH、NPSH、PSH都有不同程度下降,其中PSH下降在TSH耗竭中起主要作用。可见两药致肝损伤作用机制有相同的一面,即P450酶系的抑制、自由基导致的氧化应激都有一定作用。由于蛋白质是自由基攻击的重要靶分子,其中蛋白质的巯基是外源性化学物或其活性代谢物攻击的最敏感的亲核靶基团,TSH的损伤可导致重要功能酶活性改变,影响细胞内稳态,而GSH的耗竭又使TSH对氧化攻击、混合二硫化物、共价化合形成更为易感,因而巯基状态的改变CP、IFO致氧化性细胞损害中起到至关重要的作用。
, http://www.100md.com
上述变化中,IFO对巯基和P450的影响明显弱于CP,这可能与两者的代谢途径、活化速度不尽相同有关。CP、IFO进入体内后除了氧化裂环生成活性代谢产物外,IFO有50 %以上在活化前发生脱氯乙基作用,而CP经此途径不足10 %,同时IFO活化速度慢于CP,血浆等效剂量IFO∶CP约为3.5~5∶1。此外药代学研究表明IFO连续给药可使其清除加快,作用不减而毒性减轻,这可能也与两药毒性差异有一定关系。
与文献报道不同的是,我们没有观察到血浆生化指标和肝组织MDA含量的变化,这不能否定过氧化反应在两药致肝损伤中的作用。Sies对氧化应激的定义为:促氧化与抗氧化之间的平衡失调而倾向于前者,导致可能的损害,即氧化应激的组织改变也可能是由于所应用的抗氧化防御体系和修复系统的指标改变引起的,不一定达到对组织和细胞的损害程度。文献报道CP致游离肝细胞GSH耗竭后才出现脂质过氧化反应,最后引起细胞毒作用,此作用可被抗氧化剂延迟[7],而巯基对抗CP引起的过氧化损伤作用也是明确的[8]。业已证实自由基介导的蛋白质破坏甚至比脂质过氧化发生得更早[9],因而自由基、氧化应激在两药的肝损伤中的作用是不容忽视的。
, 百拇医药
综上,我们认为IFO与CP对肝脏的毒作用机制有相同之处,即过氧化损伤在两者致肝损害中都起了一定作用,但IFO对肝脏的毒性明显弱于CP,因而在治疗某些肿瘤时,可以用IFO代替CP,以减轻毒性。鉴于二者对肝脏的毒作用机制都与自由基、过氧化反应有一定关系,临床用药时可考虑与抗氧化剂、巯基试剂合用,从而达到保护作用。
另外,肝脏细胞色素P450酶系在CP与IFO的代谢活化过程中起到十分重要的作用。P450酶系主要包括细胞色素P450混合功能氧化酶、NADPH-细胞色素P450还原酶、细胞色素b5、NADPH-细胞色素b5还原酶。本试验只检测了总的P450含量以初步探讨CP与IFO对P450酶系的影响。国外对CP引起P450抑制已有比较深入的研究,在不同品系的大鼠P450含量下降的程度不同、亚型不同,还有性别差异,与血浆T3、T4水平有一定关系,同时细胞色素b5、NADPH-细胞色素P450还原酶活性也有一定下降[10]。本研究发现IFO对P450酶系也有一定的抑制作用,但较CP弱,抑制规律也不如CP明显,因而IFO对P450酶系的影响有待深入研究。
, 百拇医药
参考文献
[1] Paschke R,Worst P.Hepatotoxicity with etoposide-ifosfamide combination therapy.Onkologic,1988,11:273-275.
[2] Ohkawa H,Nobuko Ohishi.Assay for Lipid Peroxides in Animal Tissues by Thiobarbituric acid reaction.Anal Biochem,1979,95:351-358.
[3] Sedlak J,Raymond H.Linosay.Estimation of total、protein-bound and nonprotein sulfhydryl groups in tissue with ellman's reagent.Anal Biochem,1968,25:192-205.
, 百拇医药
[4] Omura T,Sato R.The carbon monoxide-binding pigment of liver microsomes.J Biol Chem,1964,239:2370-2385.
[5] Mcclure MT,Stupans I.Investigation of the mechanism by which Cyclophosphamide alters P450 in male rats.Biochem Pharmacol,1992,43:2655-2658.
[6] Lear L,Nation RL,Stupans I.Effects of CP and adriamycin on rat hepatic microsomal glucuronidation and lipid peroxidation.Biochem Pharmacol,1992 ,44:747-753.
, http://www.100md.com
[7] Khan S,Ramwani JJ,O'Brien PJ.Hepatocyte toxicity of mechlorethamine and other alkylating anticancer drugs.Role of lipid peroxidation.Biochem Pharmacol,1992 43:1963-1967.
[8] Roberts JC,Francetic DJ,Zera RT.Chemoprotection against Cyclophosphamide-induced urotoxicity:comparision of nine thiol protective agents.Anticancer Res,1994,14:389-396.
[9] 张铣,刘毓谷,主编.毒理学.北京:北京医科大学中国协和医科大学联合出版社,1997.136-153.
[10] Kraner JC,Morgan ET,Poet TS.Suppression of rat hepatic microsomal cytochromes P450 by cyclophosphamide is correlated with plasma thyroid hormone levels and display differential strain sensitivity.J Pharmacol Exp Ther,1996,276:258-264.
(收稿日期:1999-08-05), 百拇医药