离子通道在卵母细胞中的表达及电生理学实验方法
作者:蒋学俊 李晓艳 Randall L.Rasmusson
单位:蒋学俊 李晓艳 Randall L.Rasmusson(Penn State College of Medicine,Department of Cellular and Molecular Physiology);李晓艳(湖北医科大学附属第一医院心内科,湖北武汉 430060)
关键词:
中国心脏起搏与心电生理杂志000222 中图分类号 Q813.1+1 R331.3+8 文献标识码 A
文章编号 1007—2659(2000)02—0134—03
Ⅱ 卵母细胞的电生理实验方法
, 百拇医药
卵母细胞是研究离子通道结构及其功能较为理想的表达系统。理论上卵母细胞的电生理记录方法与一般细胞基本相似,但仍有其特殊之处。常用方法主要包括双微电极电压钳制记录法、cut-open电压钳制记录法及macro-patch,giant-patch等记录法。每种方法的应用范围各有不同,根据实验要求的不同进行选择。几种方法中,cut-open的方法最为特殊,专用于卵母细胞的电生理记录。双微电极和macro-patch等技术不仅适用于卵母细胞,也适用于其他小细胞。本节将专门介绍cut-open实验方法,以介绍实验技术为主,有关电生理理论和放大器工作原理请读者参考其他有关文献。
cut-open电压钳制法是90年代初由Stefani等研究出来的一项实验方法,经过近十年的发展已基本成熟。该方法不仅信号噪音低,记录稳定,而且可控制细胞内和细胞外环境,因而被越来越多的实验室所采用。
1 cut-open电压钳制法基本原理
, 百拇医药
cut-open设计原理是基于将卵母细胞分成三个独立部分(图1)。最下层与细胞内相通,被钳制到零电位,中间层和最上层则通过各自独立的电路被钳制到相同的电位,电流通过最上层的记录电极输入到放大器(图2)。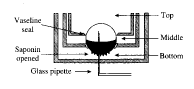
图1 cut-open设计模式图 卵母细胞被特制的细胞固定槽分成三个独立部分:上槽(T, top),中槽(M,middle)和底槽(B, bottom)。上槽和中槽底部各有一小圆孔,直径约为700 μm,四周涂以凡士林油脂使每部分之间绝缘。卵母细胞被固定于中间,但各有一小部分胞膜通过小孔暴露于上槽和底槽。各槽中的液体可通过各自的灌流装置进行液体灌流
cut-open的设计考虑到了细胞内及细胞外的灌流,上槽、中槽用于细胞外灌流,底槽用于细胞内灌流。细胞内的灌流是通过暴露于底槽的卵母细胞膜进行。方法有两种,一种是用皂角苷(saponin)增加此部分膜的通透性,使水分子和其他离子进入细胞内;另一种则是用底座上的微穿刺针直接穿刺于细胞内,用微泵调节流速进行细胞内灌流。两种方法均可有效控制细胞内成分。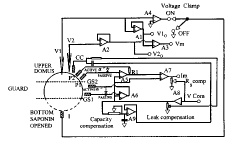
, http://www.100md.com
图2 cut-open 放大电路 卵母细胞被分成三个部分,通过各自独立的电路进行电压钳制,电流信号经V1输入到放大器
2 仪器设备
目前绝大多数实验室选用美国Dagan公司的放大器及相关设备。
2.1 放大器 美国Dagan公司生产的卵母细胞实验专用放大器CA-1B,除用于cut-open电压钳制法外,亦可用于双微电极电压钳制法。该放大器附有五个headstage,分别为V1,V2,Vi(仅用于双微电极电压钳制法),I,及bath guard。电流信号通过V1输入到放大器,其余的则用于电压钳制。
2.2 细胞固定槽 用于固定卵母细胞,基本型号为CC-1D(不带穿刺针头)或CCP-2D(带穿刺针头),在此基础上,可加选温度控制装置等其他附属设施。
, 百拇医药
2.3 六孔连接板(PL-6) 为六个斜槽,附有相应的Ag/AgCl电极。斜槽用于连接琼脂糖盐桥(AB,agar bridge)和Ag/AgCl电极。电极尾端与headstage相连。
有关放大器的技术参数及附属设备请进入http://www.dagan.com/ca-1b.html网站查询。
2.4 本实验较为精细,需有良好的稳定性和屏蔽性,应选用带屏蔽装置的气垫实验台。
2.5 示波器、数模转换器、计算机、信号采集和分析软件各一套。此部分设备和传统的膜片钳技术要求相似。
2.6 其他附属设施:显微镜一台,三维微操纵器两个。
3 准备工作
3.1 细胞固定槽结构见图3。固定槽分上槽、中槽和底槽。底槽附有固定穿刺针头。将固定槽固定于支架(Dagan, MS-104,PS-104)上,如果拟用微穿刺针进行细胞内灌流,则应事先调节针尖的位置使之位于小孔的正中,尖端稍低于固定槽的底部,以免折断针尖。
, 百拇医药
图3 卵母细胞固定槽的结构 固定槽由三部分组成,卵母细胞被固定于上槽和中槽之间,底槽的底部可固定穿刺针,针尖与中槽小孔的中心位于同一轴线上
3.2 并排固定六孔连接板于固定槽后方,加入1 mol/L NaCl,六个斜槽中分别置入Ag/AgCl电极, Ag/AgCl电极的尾端与headstage相连,分别为Bath Guard上的P1,P2,GS1,GS2和CC,另一电极尾端连接于headstage I。
3.3 实验需自行制备六个琼脂糖盐桥,因细胞固定槽的空间很小,每个盐桥的长度和形状应正好和需要连接的位置相匹配。具体连接方法参见图4。琼脂糖的浓度为1%~3%,液体成分依实验的不同而不同。为尽可能减小电阻,在盐桥中加入直径150 μm的铂金丝,注意不要让铂金丝直接接触液体。相对而言,P1和GS1的盐桥因无记录电流通过,不如其他盐桥重要。连接底槽和headstage I的盐桥一般横截面积更大,以尽可能减小电阻。
, http://www.100md.com
图4 cut-open方法中电极的设置 TC(top chamber)、MC(middle chamber)、BC(bottom chamber)分别表示固定槽的上、中、下三部分;AB(agar bridge)为琼脂糖盐桥;EH示Ag/AgCl电极;EP示六孔板中的孔,EH和AB的各一端位于其中,小孔中液体为1M NaCl;RP(recording pool)为细胞固定槽的上槽,除记录钳制电极ME(microelectrode)外,另有三个盐桥也位于其中,此三个盐桥分别连接于bath guard上的P1、P2、CC;GP(guard pool)为固定槽中槽,两个盐桥位于其中,分别与bath guard上的GS1和GS2相连; IP(current injection pool)为底槽,此处盐桥连接于headstage I
3.4 电极 记录电极尖端直径一般为2~5 μm, 电阻在1 MΩ以下,比较理想的电极阻抗为100~200 kΩ。电极内液大多情况下用3 mol/L KCl。与常规的膜片钳技术相似,电极内液需用0.22 μm滤器过滤。
, http://www.100md.com
4 卵母细胞的固定
4.1 小心移走上层槽,在中槽底部小孔四周均匀地涂抹一层凡士林油脂,厚度约为200-300 μm,注意不要堵塞小孔。
4.2 于底槽中加入细胞内液,此部分液体可与细胞内相通,因此成分与细胞内相似。在中槽加入细胞外液。此时如用两个盐桥分别与I 和 P1或P2相连,再将放大器上“TEST”置于“ON”的位置(给予20mV的电压),两部分液体相通,示波器上可观察到明显的电流曲线。
4.3 将卵母细胞小心置入中槽,使卵母细胞“坐”在小孔之上,并将着色部分向上,以便看清针尖的部位。此时观察示波器,电流较放置细胞前明显减小,轻压卵母细胞使之与小孔四周接触略为紧密,由于电阻增大,电流信号进一步减小。
4.4 用同样方法将凡士林油脂涂抹于上槽小孔底部周围,慢慢置于卵母细胞之上,用手指轻轻将上槽压在卵母细胞上,然后在上槽中加入细胞外液。
, http://www.100md.com
4.5 调整各盐桥至正确的位置(参见图4),此时再将放大器上的“TEST”置于“ON”,电流信号应接近于零。
5 细胞内灌流的两种方法
5.1 用吸管将含0.1%~0.3%皂角苷的细胞内液快速滴入固定槽的底层,同时在另一方向用负压抽吸。灌流时注意观察示波器上电流图形的变化。若细胞膜的通透性增加,则液体与细胞内相通连,示波器上即出现相应的电流的变化,如图5所示。图形一旦出现变化,立即用细胞内液灌流,洗去残存皂角苷以免皂角苷作用时间过长损伤细胞膜,造成漏流的增加。灌流时应控制好适当的液面,避免气泡进入底部,否则会引起电路断路。
5.2 另一方法是用微穿刺针头直接穿刺细胞,将原固定于固定槽底部的微穿刺针轻轻向上旋转,直至穿透细胞膜,示波器上出现相似的变化。然后在尾部接上微泵,以2 μl/min左右的速度灌流,并注意观察细胞体积应无明显变化。
, http://www.100md.com
图5 皂角苷处理细胞膜前后电流变化 左图 皂角苷处理前 右图 皂角苷处理后
6 细胞的钳制
至此实验的准备工作基本完成。在最后的电极钳制前,预先固定好细胞内外灌流和负压的装置。将拉制好的电极充以电极内液,固定于headstage V1上,用三维微操纵器将针尖移入上槽的液体中,调节放大器上的V1至零电位,测量电极电阻(理想的电极电阻在100~200 kΩ)。轻移电极使尖端逐渐移至上层小孔正中,小心刺入细胞,注意观察放大器上电位的变化,一旦进入细胞,膜电位立即变为负值,状态良好的细胞膜电位多在-30~-70 mV之间。将放大器上的钳制置于“ON”的位置,打开电容及电阻补偿,调节至适当的增益,即可记录通道电流。用同样方法将V2电极置入上槽液体,但我们一般将此处连接于P1的尾端,同样也可将电位钳制到零电位。
7 实验要点
, 百拇医药 本实验中,几个步骤是成功实现钳制的关键,应予注意。
7.1 卵母细胞三部分之间的绝缘十分重要。卵母细胞固定于固定槽中时,若加压偏小,各层之间绝缘不好,漏流过大;若加压偏大,细胞易于破裂。合适的压力是本实验的关键。
7.2 盐桥 电阻应尽可能小,不要忽视铂金丝,尤其是与I连接的盐桥,应特别注意。
7.3 用皂角苷打开细胞膜时,一旦图形出现变化,应尽可能快地洗去多余的皂角苷。
7.4 实验台的稳定至关重要,否则实验过程中尤其是细胞外灌流时极易导致钳制的失败。
8 小结
cut-open电压钳制法主要优点有:①高频响应及低噪音。可用于分析通道的激活(activation)和失活(deactivation)特性。与膜片钳技术相比,具有相似的时间分辨率,但记录到的通道电流较膜片钳技术大几十倍,可达20~30 μA。②稳定记录可达数小时。相对而言,本方法衰减现象不明显。③易于控制细胞内液体成分,可用于研究细胞内药物对通道功能的影响。也可在特殊环境下研究通道的功能,如研究细胞外高渗对通道功能的影响时,本方法可有效防止细胞的萎缩。
作者简介:蒋学俊(1967— ),男(汉族),湖北武汉人,博士后,现从事心血管的临床及基础研究。
2000-04-23收稿, http://www.100md.com
单位:蒋学俊 李晓艳 Randall L.Rasmusson(Penn State College of Medicine,Department of Cellular and Molecular Physiology);李晓艳(湖北医科大学附属第一医院心内科,湖北武汉 430060)
关键词:
中国心脏起搏与心电生理杂志000222 中图分类号 Q813.1+1 R331.3+8 文献标识码 A
文章编号 1007—2659(2000)02—0134—03
Ⅱ 卵母细胞的电生理实验方法
, 百拇医药
卵母细胞是研究离子通道结构及其功能较为理想的表达系统。理论上卵母细胞的电生理记录方法与一般细胞基本相似,但仍有其特殊之处。常用方法主要包括双微电极电压钳制记录法、cut-open电压钳制记录法及macro-patch,giant-patch等记录法。每种方法的应用范围各有不同,根据实验要求的不同进行选择。几种方法中,cut-open的方法最为特殊,专用于卵母细胞的电生理记录。双微电极和macro-patch等技术不仅适用于卵母细胞,也适用于其他小细胞。本节将专门介绍cut-open实验方法,以介绍实验技术为主,有关电生理理论和放大器工作原理请读者参考其他有关文献。
cut-open电压钳制法是90年代初由Stefani等研究出来的一项实验方法,经过近十年的发展已基本成熟。该方法不仅信号噪音低,记录稳定,而且可控制细胞内和细胞外环境,因而被越来越多的实验室所采用。
1 cut-open电压钳制法基本原理
, 百拇医药
cut-open设计原理是基于将卵母细胞分成三个独立部分(图1)。最下层与细胞内相通,被钳制到零电位,中间层和最上层则通过各自独立的电路被钳制到相同的电位,电流通过最上层的记录电极输入到放大器(图2)。

图1 cut-open设计模式图 卵母细胞被特制的细胞固定槽分成三个独立部分:上槽(T, top),中槽(M,middle)和底槽(B, bottom)。上槽和中槽底部各有一小圆孔,直径约为700 μm,四周涂以凡士林油脂使每部分之间绝缘。卵母细胞被固定于中间,但各有一小部分胞膜通过小孔暴露于上槽和底槽。各槽中的液体可通过各自的灌流装置进行液体灌流
cut-open的设计考虑到了细胞内及细胞外的灌流,上槽、中槽用于细胞外灌流,底槽用于细胞内灌流。细胞内的灌流是通过暴露于底槽的卵母细胞膜进行。方法有两种,一种是用皂角苷(saponin)增加此部分膜的通透性,使水分子和其他离子进入细胞内;另一种则是用底座上的微穿刺针直接穿刺于细胞内,用微泵调节流速进行细胞内灌流。两种方法均可有效控制细胞内成分。

, http://www.100md.com
图2 cut-open 放大电路 卵母细胞被分成三个部分,通过各自独立的电路进行电压钳制,电流信号经V1输入到放大器
2 仪器设备
目前绝大多数实验室选用美国Dagan公司的放大器及相关设备。
2.1 放大器 美国Dagan公司生产的卵母细胞实验专用放大器CA-1B,除用于cut-open电压钳制法外,亦可用于双微电极电压钳制法。该放大器附有五个headstage,分别为V1,V2,Vi(仅用于双微电极电压钳制法),I,及bath guard。电流信号通过V1输入到放大器,其余的则用于电压钳制。
2.2 细胞固定槽 用于固定卵母细胞,基本型号为CC-1D(不带穿刺针头)或CCP-2D(带穿刺针头),在此基础上,可加选温度控制装置等其他附属设施。
, 百拇医药
2.3 六孔连接板(PL-6) 为六个斜槽,附有相应的Ag/AgCl电极。斜槽用于连接琼脂糖盐桥(AB,agar bridge)和Ag/AgCl电极。电极尾端与headstage相连。
有关放大器的技术参数及附属设备请进入http://www.dagan.com/ca-1b.html网站查询。
2.4 本实验较为精细,需有良好的稳定性和屏蔽性,应选用带屏蔽装置的气垫实验台。
2.5 示波器、数模转换器、计算机、信号采集和分析软件各一套。此部分设备和传统的膜片钳技术要求相似。
2.6 其他附属设施:显微镜一台,三维微操纵器两个。
3 准备工作
3.1 细胞固定槽结构见图3。固定槽分上槽、中槽和底槽。底槽附有固定穿刺针头。将固定槽固定于支架(Dagan, MS-104,PS-104)上,如果拟用微穿刺针进行细胞内灌流,则应事先调节针尖的位置使之位于小孔的正中,尖端稍低于固定槽的底部,以免折断针尖。

, 百拇医药
图3 卵母细胞固定槽的结构 固定槽由三部分组成,卵母细胞被固定于上槽和中槽之间,底槽的底部可固定穿刺针,针尖与中槽小孔的中心位于同一轴线上
3.2 并排固定六孔连接板于固定槽后方,加入1 mol/L NaCl,六个斜槽中分别置入Ag/AgCl电极, Ag/AgCl电极的尾端与headstage相连,分别为Bath Guard上的P1,P2,GS1,GS2和CC,另一电极尾端连接于headstage I。
3.3 实验需自行制备六个琼脂糖盐桥,因细胞固定槽的空间很小,每个盐桥的长度和形状应正好和需要连接的位置相匹配。具体连接方法参见图4。琼脂糖的浓度为1%~3%,液体成分依实验的不同而不同。为尽可能减小电阻,在盐桥中加入直径150 μm的铂金丝,注意不要让铂金丝直接接触液体。相对而言,P1和GS1的盐桥因无记录电流通过,不如其他盐桥重要。连接底槽和headstage I的盐桥一般横截面积更大,以尽可能减小电阻。

, http://www.100md.com
图4 cut-open方法中电极的设置 TC(top chamber)、MC(middle chamber)、BC(bottom chamber)分别表示固定槽的上、中、下三部分;AB(agar bridge)为琼脂糖盐桥;EH示Ag/AgCl电极;EP示六孔板中的孔,EH和AB的各一端位于其中,小孔中液体为1M NaCl;RP(recording pool)为细胞固定槽的上槽,除记录钳制电极ME(microelectrode)外,另有三个盐桥也位于其中,此三个盐桥分别连接于bath guard上的P1、P2、CC;GP(guard pool)为固定槽中槽,两个盐桥位于其中,分别与bath guard上的GS1和GS2相连; IP(current injection pool)为底槽,此处盐桥连接于headstage I
3.4 电极 记录电极尖端直径一般为2~5 μm, 电阻在1 MΩ以下,比较理想的电极阻抗为100~200 kΩ。电极内液大多情况下用3 mol/L KCl。与常规的膜片钳技术相似,电极内液需用0.22 μm滤器过滤。
, http://www.100md.com
4 卵母细胞的固定
4.1 小心移走上层槽,在中槽底部小孔四周均匀地涂抹一层凡士林油脂,厚度约为200-300 μm,注意不要堵塞小孔。
4.2 于底槽中加入细胞内液,此部分液体可与细胞内相通,因此成分与细胞内相似。在中槽加入细胞外液。此时如用两个盐桥分别与I 和 P1或P2相连,再将放大器上“TEST”置于“ON”的位置(给予20mV的电压),两部分液体相通,示波器上可观察到明显的电流曲线。
4.3 将卵母细胞小心置入中槽,使卵母细胞“坐”在小孔之上,并将着色部分向上,以便看清针尖的部位。此时观察示波器,电流较放置细胞前明显减小,轻压卵母细胞使之与小孔四周接触略为紧密,由于电阻增大,电流信号进一步减小。
4.4 用同样方法将凡士林油脂涂抹于上槽小孔底部周围,慢慢置于卵母细胞之上,用手指轻轻将上槽压在卵母细胞上,然后在上槽中加入细胞外液。
, http://www.100md.com
4.5 调整各盐桥至正确的位置(参见图4),此时再将放大器上的“TEST”置于“ON”,电流信号应接近于零。
5 细胞内灌流的两种方法
5.1 用吸管将含0.1%~0.3%皂角苷的细胞内液快速滴入固定槽的底层,同时在另一方向用负压抽吸。灌流时注意观察示波器上电流图形的变化。若细胞膜的通透性增加,则液体与细胞内相通连,示波器上即出现相应的电流的变化,如图5所示。图形一旦出现变化,立即用细胞内液灌流,洗去残存皂角苷以免皂角苷作用时间过长损伤细胞膜,造成漏流的增加。灌流时应控制好适当的液面,避免气泡进入底部,否则会引起电路断路。
5.2 另一方法是用微穿刺针头直接穿刺细胞,将原固定于固定槽底部的微穿刺针轻轻向上旋转,直至穿透细胞膜,示波器上出现相似的变化。然后在尾部接上微泵,以2 μl/min左右的速度灌流,并注意观察细胞体积应无明显变化。

, http://www.100md.com
图5 皂角苷处理细胞膜前后电流变化 左图 皂角苷处理前 右图 皂角苷处理后
6 细胞的钳制
至此实验的准备工作基本完成。在最后的电极钳制前,预先固定好细胞内外灌流和负压的装置。将拉制好的电极充以电极内液,固定于headstage V1上,用三维微操纵器将针尖移入上槽的液体中,调节放大器上的V1至零电位,测量电极电阻(理想的电极电阻在100~200 kΩ)。轻移电极使尖端逐渐移至上层小孔正中,小心刺入细胞,注意观察放大器上电位的变化,一旦进入细胞,膜电位立即变为负值,状态良好的细胞膜电位多在-30~-70 mV之间。将放大器上的钳制置于“ON”的位置,打开电容及电阻补偿,调节至适当的增益,即可记录通道电流。用同样方法将V2电极置入上槽液体,但我们一般将此处连接于P1的尾端,同样也可将电位钳制到零电位。
7 实验要点
, 百拇医药 本实验中,几个步骤是成功实现钳制的关键,应予注意。
7.1 卵母细胞三部分之间的绝缘十分重要。卵母细胞固定于固定槽中时,若加压偏小,各层之间绝缘不好,漏流过大;若加压偏大,细胞易于破裂。合适的压力是本实验的关键。
7.2 盐桥 电阻应尽可能小,不要忽视铂金丝,尤其是与I连接的盐桥,应特别注意。
7.3 用皂角苷打开细胞膜时,一旦图形出现变化,应尽可能快地洗去多余的皂角苷。
7.4 实验台的稳定至关重要,否则实验过程中尤其是细胞外灌流时极易导致钳制的失败。
8 小结
cut-open电压钳制法主要优点有:①高频响应及低噪音。可用于分析通道的激活(activation)和失活(deactivation)特性。与膜片钳技术相比,具有相似的时间分辨率,但记录到的通道电流较膜片钳技术大几十倍,可达20~30 μA。②稳定记录可达数小时。相对而言,本方法衰减现象不明显。③易于控制细胞内液体成分,可用于研究细胞内药物对通道功能的影响。也可在特殊环境下研究通道的功能,如研究细胞外高渗对通道功能的影响时,本方法可有效防止细胞的萎缩。
作者简介:蒋学俊(1967— ),男(汉族),湖北武汉人,博士后,现从事心血管的临床及基础研究。
2000-04-23收稿, http://www.100md.com