α干扰素联合化疗治疗CML的分子水平疗效观察
作者:宋献民 夏放 袁有忠 闵碧荷
单位:宋献民(第二军医大学长海医学院血液内科,上海 200433);夏放(第二军医大学长海医学院血液内科,上海 200433);袁有忠(第二军医大学长海医学院血液内科,上海 200433);闵碧荷(第二军医大学长海医学院血液内科,上海 200433)
关键词:干扰素α;慢性粒细胞白血病;融合基因,bcr/abl
第二军医大学学报000312 【摘要】 目的:分析bcr/abl融合基因表达水平与α干扰素(IFNα)治疗慢性粒细胞白血病(CML)疗效及预后的关系。方法:应用半定量RT-PCR方法,分析6例α干扰素治疗的CML患者不同时期骨髓细胞bcr/abl融合基因表达水平。结果:5例患者bcr/abl融合基因表达水平减低,临床获得持久完全血液学缓解。结论:半定量RT-PCR有助于α干扰素治疗CML的疗效观察及预后判断。
, 百拇医药
【中图分类号】 R 733.72 【文献标识码】 A 【文章编号】 0258-879X(2000)03-0236-03
Therapeutical effects of interferon-α combining chemotherapy on CML at the molecular level
SONG Xian-Min XIA Fang YUAN You-Zhong MIN Bi-He
(Department of Hematology,Changhai Hospital, Second Military Medical University, Shanghai 200433, China)
【ABSTRACT】 Objective: To study the relation between the expression of bcr/abl gene and the effects of interferon-α in treatment of CML. Methods: By using semi-quantitative RT-PCR, bone marrow cells from 6 CML(chronic phase) patients were analyzed for the expression of fusion gene at pre-treatment and during intervals after treatment with interferon-α. Results:Five patients with decreasing levels of bcr/abl mRNA expression were in complete hematological remission. Conclusion: The semi-quantitative RT-PCR may be used to evaluate the prognosis of CML with interferon-α treatment.
, 百拇医药
【KEY WORDS】 interferon alpha; chronic myelogenous leukemia; fusion genes, bcr/abl▲
[Acad J Sec Mil Med Univ, 2000, 21(3): 236-238]
慢性粒细胞白血病(CML)是一种源于多能造血干细胞的骨髓增殖性疾病,在95%的患者中具有 特征性的Ph1染色体,即t(9,22)(q34,q11),分子水平的移位表现为bcr/abl融合基因形成。bcr/abl融合基因编码相对分子质量为21万的融合蛋白,其酪氨酸激酶活性明显增高,可刺激造血祖细胞的增殖,在CML的发病机制中可能起重要作用。单药或联合化疗不能持久地抑制Ph1染色体及阻止CML的急性变,而α干扰素对大约70%的患者有效,且可使部分患者获得持久完全的血液学及细胞遗传学缓解[1,2]。本实验采用半定量RT-PCR方法检测用α干扰素治疗的CML患者不同时期bcr/abl基因表达水平,以期评价治疗效果及判断预后。
, 百拇医药
1 材料和方法
1.1 病例与标本 6例CML慢性期患者诊断均符合血液病诊断标准;除例3经HA(H:三尖杉脂碱,杭州民生制药公司;A:阿糖胞苷,上海华联制药公司)化疗1疗程后,给予白消安(英国威康制药公司)和α-2a干扰素(上海罗氏制药公司)治疗外,余均给予羟基脲和α-2a干扰素治疗,干扰素剂量为3.0×106 U,隔日1次,持续用药;标本源于治疗前及治疗后不同时期骨髓;白血病细胞系K562细胞株。
1.2 引物设计与合成 根据文献[3]设计bcr/abl基因巢式PCR引物两对,序列分别如下:bcr/abl-A:5′-TGCAGATGCTGACCAACTCG-3′,bcr/abl-B: 5′ - GATTATAGCCTAAGACCCGGAGC - 3′,bcr/abl-C: 5′ - ACTCCAGACTGTCCACAGCAT TCC- 3′,bcr/abl-D:5′-AACGAGCGGCTTCACT CAGACC-3′,两轮PCR扩增产生157 bp的bcr/abl基因片段;内参照β-actin基因引物序列为β-1:5′-AACGGCTCCGGCATGTGCAA-3′,β-2:5′-CTT CTGACCCATGCCCACCA-3′ ,扩增产生108 bp的片段。上述引物由中科院上海细胞研究所合成。
, 百拇医药
1.3 RNA抽提与定量 按异硫氰酸胍-酚-氯仿一步法抽取细胞总RNA,其定量分析采用分光光度仪和溴乙啶凝胶染色法。
1.4 反转录-聚合酶链反应(RT-PCR)
1.4.1 反转录反应 所有试剂均由PE公司生产。20 μl体系内,包括2 μg细胞总RNA, 2.5 U/μl MMLV反转录酶,50 pmol随机引物, 500 μmol/L dNTPS,1×PCR缓冲液,5 mmol/L MgCl2。42℃反应30 min,99℃加热5 min,4℃保存。
1.4.2 聚合酶链反应 采用内参照巢式PCR方法[4,5]:首轮PCR反应体系含RT产物10 μl,β-actin引物各50 pmol,bcr/abl引物A,B各40 pmol ,dNTPS 200 μmol/L,Taq酶2 U;次轮反应体系含首轮产物2 μl,bcr/abl引物C,D各40 pmol,余同首轮。共进行33个循环。K562细胞作为阳性对照,空白管作为空白对照。
, 百拇医药
1.5 聚丙烯酰胺凝胶电泳-银染显色 5 μl PCR扩增产物,10%中性聚丙烯酰胺凝胶电泳,150 V,1 h;电泳完毕后凝胶经固定、银染、显影处理后,凉干。
1.6 光密度扫描 采用日本Sharp公司JX330扫描仪对凝胶进行扫描,Compaq.575计算机,Image-master.TM软件处理凝胶扫描值。
1.7 Ph1染色体检查 G染带分区技术。
2 结 果
采用半定量RT-PCR方法对6例α-2a干扰素治疗的CML慢性期患者bcr/abl融合基因表达进行检测,结果如表1及图1。从表1中可以看出,病例1,2,3,5,6 bcr/abl基因表达量呈下降趋势,血液学检查示完全缓解,而病例4 bcr/abl表达量基本无变化,血液学检查示部分缓解;从图1中可以看出,bcr/abl基因表达灰度逐渐减弱。
, 百拇医药
表1 α干扰素治疗前后不同时期bcr/abl基因表达情况
Tab 1 The expression of bcr/abl gene at pre-treatment and during intervals after treatment with interferon-α Case
Age/Sex
bcr-abl/β-actin ratio
Ph1 chromosome
Result
Pre-treatment
After treatment
, 百拇医药
Pre-treatment
After-treatment
1
64/M
2.68
2.96
1.55
0.97
96%
50%
CR
(4)
(11)
, 百拇医药
(15)
(4)
2
33/M
3.47
1.50
1.75
100%
50%
CR
(9)
(16)
(9)
, 百拇医药
3
45/M
2.71
3.01
2.10
90%
-
CR
(3)
(10)
4
43/F
2.65
, http://www.100md.com
2.79
2.64
100%
90%
PR
(3)
(6)
(3)
5
42/M
2.77
2.52
1.97
, 百拇医药
100%
-
CR
(5)
(14)
6
34/F
2.53
1.92
1.94
92%
50%
CR
, 百拇医药
(6)
(11)
(6)
CR:Complete remission; PR:Partial remission;The values in parentheses are months after treatment
3 讨 论
半定量RT-PCR方法较传统的Northern-blot方法和Ph1染色体方法敏感性高,不依赖分裂期细胞。RT-PCR是检测处于转录水平的靶基因,可反映体内残留白血病细胞动力学。国外文献认为bcr/abl基因表达水平持续增高,提示白血病细胞克隆的扩增,体内残留白血病细胞活性增强,有利于疾病进程的早期判断[6]。
Lion等[7]报道长期接受α-干扰素治疗并获血液学完全缓解的CML患者,bcr/abl基因表达水平较治疗前降低,而bcr/abl基因表达量增高的患者在平均半年内均发生慢粒急性变。另有报道,1例骨髓移植后患者bcr/abl表达量增高,其后很快复发[5]。本研究中例1,2,3,5,6 bcr/abl基因表达水平呈下降趋势,他们自α干扰素治疗后1年余均仍处于血液学完全缓解状态,提示其能获得较长期缓解,预后可能较佳;而患者4的bcr/abl基因表达水平无明显变化,骨髓形态学检查示未获血液学完全缓解,可能预示着治疗效果欠佳。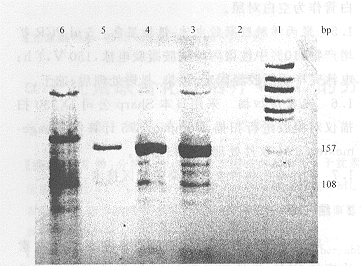
, 百拇医药
图1 2号病例骨髓细胞bcr/abl基因的表达
Fig 1 The expression of bcr/abl gene of bone marrow
cells from patient 2
Lane 1: Marker; Lane 2: Control; Lane 3: K562; Lane 4:
Pre-treatment; Lane 5,6: 9 and 16 months after treatment
本实验结果提示半定量RT-PCR方法检测bcr/abl融合基因表达水平有助于α干扰素治疗CML的疗效判断,明确的结果有待扩大样本量作深入研究。■
基金项目:国家自然科学基金资助项目(39970709)
, http://www.100md.com
作者简介:宋献民(1967-),男(汉族),硕士,主治医师
【参 考 文 献】
[1] Opalka B,Wandl UB,Becher R,et al. Minimal residual disease in patients with chronic myelogenous leukemia undergoing long-term treatment with recombinant interferon alpha-2b alone or in combination with interferon gamma[J].Blood, 1991,78(9):2188-2193.
[2] Dhingra K,Kurzrock R,Kantarjian H. Minimal residual disease in interferon-treated chronic myelogenous leukemia:results and pitfalls of analysis based on polymerase chain reaction[J]. Leukemia, 1992,6(8):754-760.
, 百拇医药
[3] Shtivelman E,Litshit B,Gale RB,et al.Fused transcripts of abl and bcr genes in chronic myelogenous leukemia[J]. Nature, 1985,315(6020):550-554.
[4] Maurer J,Thiel E. Rapid detection of chimeric bcr/abl mRNA in acute lymphoblastic and chronic myeloid leukemia by the polymerase chain reaction[J]. Blut, 1990,61(6):350-356.
[5] Lion T,Izraeli S,Henn T, et al. Monitoring of residual disease in chronic myelogenous leukemia by quantitative polymerase chain reaction[J]. Leukemia, 1992,6(6):495-499.
, 百拇医药
[6] Lion T,Henn T, Gaiger A,et al. Early detection of relapse after bone marrow transplantation in patients with chronic myelogenous leukemia[J].Lancet, 1993,341(8840):275-276.
[7] Lion T,Gaiger A,Henn E, et al. Use of quantitative polymerase chain reaction to monitor residual disease in chronic myelogenous leukemia during treatment with interferon[J]. Leukemia, 1995,9(8):1353-1360.
【收稿日期】 1999-10-11
【修回日期】 1999-12-31, 百拇医药
单位:宋献民(第二军医大学长海医学院血液内科,上海 200433);夏放(第二军医大学长海医学院血液内科,上海 200433);袁有忠(第二军医大学长海医学院血液内科,上海 200433);闵碧荷(第二军医大学长海医学院血液内科,上海 200433)
关键词:干扰素α;慢性粒细胞白血病;融合基因,bcr/abl
第二军医大学学报000312 【摘要】 目的:分析bcr/abl融合基因表达水平与α干扰素(IFNα)治疗慢性粒细胞白血病(CML)疗效及预后的关系。方法:应用半定量RT-PCR方法,分析6例α干扰素治疗的CML患者不同时期骨髓细胞bcr/abl融合基因表达水平。结果:5例患者bcr/abl融合基因表达水平减低,临床获得持久完全血液学缓解。结论:半定量RT-PCR有助于α干扰素治疗CML的疗效观察及预后判断。
, 百拇医药
【中图分类号】 R 733.72 【文献标识码】 A 【文章编号】 0258-879X(2000)03-0236-03
Therapeutical effects of interferon-α combining chemotherapy on CML at the molecular level
SONG Xian-Min XIA Fang YUAN You-Zhong MIN Bi-He
(Department of Hematology,Changhai Hospital, Second Military Medical University, Shanghai 200433, China)
【ABSTRACT】 Objective: To study the relation between the expression of bcr/abl gene and the effects of interferon-α in treatment of CML. Methods: By using semi-quantitative RT-PCR, bone marrow cells from 6 CML(chronic phase) patients were analyzed for the expression of fusion gene at pre-treatment and during intervals after treatment with interferon-α. Results:Five patients with decreasing levels of bcr/abl mRNA expression were in complete hematological remission. Conclusion: The semi-quantitative RT-PCR may be used to evaluate the prognosis of CML with interferon-α treatment.
, 百拇医药
【KEY WORDS】 interferon alpha; chronic myelogenous leukemia; fusion genes, bcr/abl▲
[Acad J Sec Mil Med Univ, 2000, 21(3): 236-238]
慢性粒细胞白血病(CML)是一种源于多能造血干细胞的骨髓增殖性疾病,在95%的患者中具有 特征性的Ph1染色体,即t(9,22)(q34,q11),分子水平的移位表现为bcr/abl融合基因形成。bcr/abl融合基因编码相对分子质量为21万的融合蛋白,其酪氨酸激酶活性明显增高,可刺激造血祖细胞的增殖,在CML的发病机制中可能起重要作用。单药或联合化疗不能持久地抑制Ph1染色体及阻止CML的急性变,而α干扰素对大约70%的患者有效,且可使部分患者获得持久完全的血液学及细胞遗传学缓解[1,2]。本实验采用半定量RT-PCR方法检测用α干扰素治疗的CML患者不同时期bcr/abl基因表达水平,以期评价治疗效果及判断预后。
, 百拇医药
1 材料和方法
1.1 病例与标本 6例CML慢性期患者诊断均符合血液病诊断标准;除例3经HA(H:三尖杉脂碱,杭州民生制药公司;A:阿糖胞苷,上海华联制药公司)化疗1疗程后,给予白消安(英国威康制药公司)和α-2a干扰素(上海罗氏制药公司)治疗外,余均给予羟基脲和α-2a干扰素治疗,干扰素剂量为3.0×106 U,隔日1次,持续用药;标本源于治疗前及治疗后不同时期骨髓;白血病细胞系K562细胞株。
1.2 引物设计与合成 根据文献[3]设计bcr/abl基因巢式PCR引物两对,序列分别如下:bcr/abl-A:5′-TGCAGATGCTGACCAACTCG-3′,bcr/abl-B: 5′ - GATTATAGCCTAAGACCCGGAGC - 3′,bcr/abl-C: 5′ - ACTCCAGACTGTCCACAGCAT TCC- 3′,bcr/abl-D:5′-AACGAGCGGCTTCACT CAGACC-3′,两轮PCR扩增产生157 bp的bcr/abl基因片段;内参照β-actin基因引物序列为β-1:5′-AACGGCTCCGGCATGTGCAA-3′,β-2:5′-CTT CTGACCCATGCCCACCA-3′ ,扩增产生108 bp的片段。上述引物由中科院上海细胞研究所合成。
, 百拇医药
1.3 RNA抽提与定量 按异硫氰酸胍-酚-氯仿一步法抽取细胞总RNA,其定量分析采用分光光度仪和溴乙啶凝胶染色法。
1.4 反转录-聚合酶链反应(RT-PCR)
1.4.1 反转录反应 所有试剂均由PE公司生产。20 μl体系内,包括2 μg细胞总RNA, 2.5 U/μl MMLV反转录酶,50 pmol随机引物, 500 μmol/L dNTPS,1×PCR缓冲液,5 mmol/L MgCl2。42℃反应30 min,99℃加热5 min,4℃保存。
1.4.2 聚合酶链反应 采用内参照巢式PCR方法[4,5]:首轮PCR反应体系含RT产物10 μl,β-actin引物各50 pmol,bcr/abl引物A,B各40 pmol ,dNTPS 200 μmol/L,Taq酶2 U;次轮反应体系含首轮产物2 μl,bcr/abl引物C,D各40 pmol,余同首轮。共进行33个循环。K562细胞作为阳性对照,空白管作为空白对照。
, 百拇医药
1.5 聚丙烯酰胺凝胶电泳-银染显色 5 μl PCR扩增产物,10%中性聚丙烯酰胺凝胶电泳,150 V,1 h;电泳完毕后凝胶经固定、银染、显影处理后,凉干。
1.6 光密度扫描 采用日本Sharp公司JX330扫描仪对凝胶进行扫描,Compaq.575计算机,Image-master.TM软件处理凝胶扫描值。
1.7 Ph1染色体检查 G染带分区技术。
2 结 果
采用半定量RT-PCR方法对6例α-2a干扰素治疗的CML慢性期患者bcr/abl融合基因表达进行检测,结果如表1及图1。从表1中可以看出,病例1,2,3,5,6 bcr/abl基因表达量呈下降趋势,血液学检查示完全缓解,而病例4 bcr/abl表达量基本无变化,血液学检查示部分缓解;从图1中可以看出,bcr/abl基因表达灰度逐渐减弱。
, 百拇医药
表1 α干扰素治疗前后不同时期bcr/abl基因表达情况
Tab 1 The expression of bcr/abl gene at pre-treatment and during intervals after treatment with interferon-α Case
Age/Sex
bcr-abl/β-actin ratio
Ph1 chromosome
Result
Pre-treatment
After treatment
, 百拇医药
Pre-treatment
After-treatment
1
64/M
2.68
2.96
1.55
0.97
96%
50%
CR
(4)
(11)
, 百拇医药
(15)
(4)
2
33/M
3.47
1.50
1.75
100%
50%
CR
(9)
(16)
(9)
, 百拇医药
3
45/M
2.71
3.01
2.10
90%
-
CR
(3)
(10)
4
43/F
2.65
, http://www.100md.com
2.79
2.64
100%
90%
PR
(3)
(6)
(3)
5
42/M
2.77
2.52
1.97
, 百拇医药
100%
-
CR
(5)
(14)
6
34/F
2.53
1.92
1.94
92%
50%
CR
, 百拇医药
(6)
(11)
(6)
CR:Complete remission; PR:Partial remission;The values in parentheses are months after treatment
3 讨 论
半定量RT-PCR方法较传统的Northern-blot方法和Ph1染色体方法敏感性高,不依赖分裂期细胞。RT-PCR是检测处于转录水平的靶基因,可反映体内残留白血病细胞动力学。国外文献认为bcr/abl基因表达水平持续增高,提示白血病细胞克隆的扩增,体内残留白血病细胞活性增强,有利于疾病进程的早期判断[6]。
Lion等[7]报道长期接受α-干扰素治疗并获血液学完全缓解的CML患者,bcr/abl基因表达水平较治疗前降低,而bcr/abl基因表达量增高的患者在平均半年内均发生慢粒急性变。另有报道,1例骨髓移植后患者bcr/abl表达量增高,其后很快复发[5]。本研究中例1,2,3,5,6 bcr/abl基因表达水平呈下降趋势,他们自α干扰素治疗后1年余均仍处于血液学完全缓解状态,提示其能获得较长期缓解,预后可能较佳;而患者4的bcr/abl基因表达水平无明显变化,骨髓形态学检查示未获血液学完全缓解,可能预示着治疗效果欠佳。

, 百拇医药
图1 2号病例骨髓细胞bcr/abl基因的表达
Fig 1 The expression of bcr/abl gene of bone marrow
cells from patient 2
Lane 1: Marker; Lane 2: Control; Lane 3: K562; Lane 4:
Pre-treatment; Lane 5,6: 9 and 16 months after treatment
本实验结果提示半定量RT-PCR方法检测bcr/abl融合基因表达水平有助于α干扰素治疗CML的疗效判断,明确的结果有待扩大样本量作深入研究。■
基金项目:国家自然科学基金资助项目(39970709)
, http://www.100md.com
作者简介:宋献民(1967-),男(汉族),硕士,主治医师
【参 考 文 献】
[1] Opalka B,Wandl UB,Becher R,et al. Minimal residual disease in patients with chronic myelogenous leukemia undergoing long-term treatment with recombinant interferon alpha-2b alone or in combination with interferon gamma[J].Blood, 1991,78(9):2188-2193.
[2] Dhingra K,Kurzrock R,Kantarjian H. Minimal residual disease in interferon-treated chronic myelogenous leukemia:results and pitfalls of analysis based on polymerase chain reaction[J]. Leukemia, 1992,6(8):754-760.
, 百拇医药
[3] Shtivelman E,Litshit B,Gale RB,et al.Fused transcripts of abl and bcr genes in chronic myelogenous leukemia[J]. Nature, 1985,315(6020):550-554.
[4] Maurer J,Thiel E. Rapid detection of chimeric bcr/abl mRNA in acute lymphoblastic and chronic myeloid leukemia by the polymerase chain reaction[J]. Blut, 1990,61(6):350-356.
[5] Lion T,Izraeli S,Henn T, et al. Monitoring of residual disease in chronic myelogenous leukemia by quantitative polymerase chain reaction[J]. Leukemia, 1992,6(6):495-499.
, 百拇医药
[6] Lion T,Henn T, Gaiger A,et al. Early detection of relapse after bone marrow transplantation in patients with chronic myelogenous leukemia[J].Lancet, 1993,341(8840):275-276.
[7] Lion T,Gaiger A,Henn E, et al. Use of quantitative polymerase chain reaction to monitor residual disease in chronic myelogenous leukemia during treatment with interferon[J]. Leukemia, 1995,9(8):1353-1360.
【收稿日期】 1999-10-11
【修回日期】 1999-12-31, 百拇医药