脂质体异体瘤苗对肿瘤的治疗效应研究
作者:甘岫云 王东 李增鹏 王远东 肖华亮 雍凌
单位:肖华亮(第三军医大学附属三院);甘岫云 王东 李增鹏 王远东(广州市肿瘤医院 广州 510095)雍凌(广州市肿瘤医院 广州 510095)
关键词:肿瘤;治疗;瘤苗;异体;脂质体
中国肿瘤生物治疗杂志000319 《中国图书资料分类法》分类号 R73-36
应用瘤苗诱导肿瘤宿主产生抗肿瘤免疫反应以治疗肿瘤的主动免疫治疗肿瘤是目前肿瘤生物治疗有效的方法之一,受到国内外的广泛重视[1,2]。我们已开展自体瘤苗治疗肿瘤的研究并已取得一定进展[3]。进一步提高瘤苗免疫治疗肿瘤的疗效,寻求制备高效、安全的异体瘤苗的途径极为重要。据文献报道脂质体(liposome)包裹瘤苗抗原性强,又可作异体瘤苗的载体,其诱导机体产生的抗体比单纯性瘤苗高100~400倍,且具有作用持久、毒副反应轻等优点[4,5]。为此本研究观察了脂质体异体瘤苗对肿瘤的抑制作用,以期为临床应用提供实验依据。
, 百拇医药
1 材料与方法
1.1 动物
BALB/c小鼠雌性,体重20~30 g,由第三军医大学动物所提供Ⅰ级动物,批号(048/1999)。
1.2 瘤源
小鼠乳腺癌细胞系(Scc891)(由第三军医大学动物所提供),作为瘤源和制备自体瘤苗用;人乳腺癌细胞取自人体手术标本,作为异体瘤苗用。Scc981细胞系用RPMI 1640培养基和小牛血清进行体外培养增殖,于对数生长期制成1×107瘤细胞悬液接种于4只BALB/c小鼠腋部皮下,成瘤后处死。取新鲜瘤组织块制成瘤细胞悬液再接种13只BALB/c小鼠腋部皮下成瘤后作为正式实验瘤源。
1.3 瘤细胞悬液制备
, 百拇医药
荷Scc891瘤BALB/c小鼠13只,引颈处死。在无菌条件下取出肿瘤组织,去除外膜与坏死组织。用Hank's液洗涤。按1 g瘤组织加4 ml生理盐水放入组织研磨器内研磨,经200目筛网过滤制成瘤细胞悬液。用台盼兰拒染法观察活瘤细胞数在95%以上,配成1×107活瘤细胞悬液备用[3]。
1.4 肿瘤抗原裂解物瘤苗的制备
参照Steele等[6]的TAA制备方法进行。步骤如下: ① 如上法制备的单细胞性肿瘤细胞悬液,在液氮中反复冻融3次,使瘤细胞碎裂; ② 加入2.5% (V/V)正丁醇PBS(pH7.4) 液重新悬浮,室温轻轻震荡5 min; ③ 4℃ 5 000 ×g离心10 min取上清液,4℃ 2 000 ×g离心20 min,取上清液; ④ 上清液经透析72 h (4℃, 100 V); ⑤ 最后标本经200 000 ×g超速离心1 h (4℃),取上清液即为制备的TAA备用; ⑥用Lowry's法检测上清液抗原蛋白含量浓度合格。
, http://www.100md.com
1.5 脂质体瘤苗的制备
脂质体(购自Simga公司),将1.5 ml脂质体+2 ml甲醇+5 ml氯仿摇匀成稀释液;再将2.6 ml脂质体稀释液+6 ml TAA PBS液,震荡20 min备用(经光镜与电镜观察合格)。
1.6 瘤苗抑制肿瘤实验分组
BALB/c小鼠30只,分为3组,每组10只。A组为对照组:同一时间在鼠右侧腋部皮下注射1×107瘤细胞悬液0.2 ml,第2天起左液部皮下注射PBS液0.2 ml,再隔5 d同样注射2次;B组为脂质体自体瘤苗治疗组(简称自体瘤组):与对照组相同在右腋部皮下注射相同量的瘤细胞悬液,第2天起每隔5 d左侧腋部皮下注射3次脂质体自体瘤苗0.2 ml;C组为脂质体异体瘤苗治疗组(简称异体瘤组):与对照组相同在右侧腋部皮下注射相同量瘤细胞悬液。第2天起与自体瘤组相同注射脂质体异体瘤苗0.2 ml 3 次。第16天处死动物进行解剖观察。
, 百拇医药
1.7 检查指标
① 肿瘤和瘤苗接种处进行大体观察,有肿瘤生长者将瘤块分离取下,称瘤体重量,并观察心、肺、肝、脾及肾等器官有无转移和异常,淋巴结是否肿大。所有组织均进行常规10%福尔马林液固定; ②常规石蜡埋切片,HE染色,进行组织学观察。
1.8 统计学分析
对3组肿瘤重量进行统计分析比较t检验(Spss80软件包)。
1.9 抑瘤率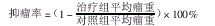
2 结果与讨论
经治疗后观察表明,在对照组,10只动物全部有肿瘤生长。肿瘤重量为0.5 g,0.7 g,1.3 g,1.0 g,1.7 g, 1.5 g, 0.9 g, 1.1 g, 0.8 g, 1.7 g,平均1.12±0.42 g。组织学观察:瘤组织为中度分化腺癌,呈不规则癌巢,间质少而疏松,均有不同程度的肿瘤中央性坏死。肿瘤周围有纤维组织包绕,并有少量多形核粒细胞、淋巴细胞、组织细胞浸润。脾脏中脾小体无明显增生。其他脏器未查见明显病变和肿瘤转移。淋巴结未查见肿大及转移。
, 百拇医药
在脂质体自体瘤苗治疗组,5只动物有肿瘤生长,另5只动物未见肿瘤生长,肿瘤重量分别为0.6 g,0.5 g, 1.0 g, 0.4 g, 0.5 g,平均0.30±0.35 g。组织学观察:肿瘤组织学类型与中央性坏死及外周情况与对照组无明显差异,脾脏小体较明显的增大和数量增多。其他脏器无明显病变。瘤苗区未查见肿瘤生长。
在脂质体异体瘤苗治疗组,有5只动物大体未见肿瘤生长,另5只肿瘤重量分别为1.3 g,0.7 g, 0.5 g, 0.7 g, 0.4 g,平均0.36±0.45 g。组织学观察:肿瘤组织学类型及坏死等病变与上组相似。脾脏的脾小体增大及数量增多。瘤苗注射区未查见肿瘤生长。3组动物均未查见淋巴结肿大。肝脏枯否氏细胞(Kupffer's cells)数量无明显差异。
表1 脂质体瘤苗治疗肿瘤效应结果 组别
动物数(只) ±SD
±SD
, http://www.100md.com
抑瘤率(%)
(1)对照组
10
1.12±0.42
(2)自体瘤组
10
0.30±0.35
73.22
(3)异体瘤组
10
0.36±0.45
67.86
, http://www.100md.com 注:分组统计学比较(1) vs (2) P<0.01; (1) vs (3) P<0.01; (2) vs(3) P>0.05
本实验结果表明,脂质体自体与异体瘤苗诱导的动物主动免疫治疗肿瘤是可行的,有非常明显的抑瘤效果(P<0.01),且无明显的毒副反应。为进一步临床应用提供了有价值的依据。同时应用脂质体异体瘤苗治疗动物肿瘤安全有效,扩大了瘤苗材料的来源,为更广泛地开展瘤苗治疗肿瘤创造有利条件。
本实验所用瘤苗的制备方法,优选了文献推荐的瘤细胞反复冻融灭活法。该法使瘤细胞破碎,同时加用超速离心将细胞核和较大的胞浆颗粒等成份除去,从而得到高浓度的细胞膜抗原,增强激发宿主的免疫效应,提高了对瘤细胞杀伤效果[5,6]。
本实验结果显示自体与异体脂质体瘤苗两组均有50%动物未见肿瘤生长。两组肿瘤重量与对照组相比较均有非常显著的差异(P<0.01),而两治疗组之间抑瘤效果无显著差异(P>0.05)。表明脂质体瘤苗具有非常显著的抑瘤效果,且无明显的毒副反应。在本实验之前作了单纯自体瘤苗与脂质体自体瘤苗对比动物实验,结果显示脂质体瘤苗较单纯瘤苗的抑瘤效果更明显(P<0.05)。以上实验结果进一步证明脂质体异体瘤苗具有高效、安全的抑瘤效应,为临床应用提供了依据。
, http://www.100md.com
本实验加用了脂质体包裹瘤苗治疗肿瘤的结果证明,不但脂质体可作为瘤苗的载体,且可明显增强瘤苗的抗原性诱导产生细胞免疫与体液免疫,提高主动免疫杀瘤效能。同时文献报告它能延缓抗原的释放致免疫功能持久。因此它是较为理想的增强免疫效应佐剂[5]。虽然目前国内外在探索基因工程瘤苗,但有许多困难有待解决。因而脂质体瘤苗仍是当前行之有效,易于开展的主动免疫治疗肿瘤的较好方法之一。
从肿瘤组织学观察脂质体治疗的肿瘤组织周围有较多的淋巴组织细胞浸润。治疗组肿瘤均显示片状坏死。50%动物未见肿瘤生长,且脾脏的脾小体较对照组有明显的增生。推想脂质体瘤苗首先激活辅助T淋巴细胞,再激发B淋巴细胞增生而产生较强的细胞与体液免疫。因此作者认为脂质体苗有增强宿主免疫抑瘤效应; 实验结果表明,脂质体瘤苗具有较强的诱导宿主的主动免疫效应抑制肿瘤生长,作用快而持久,使植入瘤细胞早期被抑制或杀灭。因此应用于肿瘤切除后防止肿瘤扩散转移和复发最为适宜; 实验结果表明脂质体异体瘤苗与脂质体自体瘤苗一样均有非常显著的抑瘤效果,且无明显毒副反应,因此克服了应用自体瘤苗材料来源的限制。为今后临床更广泛的应用异体瘤苗提供了很有用的资料。
, http://www.100md.com
本课题受广东省科委重点科研究攻关项目(962046-04)资助
参 考 文 献
1,袁 玫. 肿瘤的主动特异性免疫治疗研究进展. 中国肿瘤生物治疗杂志, 1995, 2(2): 56
2,曹雪涛. 肿瘤免疫治疗和基因治疗研究某些新进展. 中国肿瘤生物治疗杂志, 1997, 2(1): 79
3,甘岫云,张 一,高 虹. 瘤苗主动免疫疗法的实验研究. 中国人兽共患病杂志, 1996, 12(3): 30
4,Phillips NC. Clinical evaluation of liposomal tumor antigen vaccines in patients with stage-Ⅲ melanoma. Cancer Detect Prev, 1990, 14: 491
, 百拇医药
5,Phillips NC, Emili A. Enhanced antibody response to liposome associated protein antigens; preferential stimulation of IgGza/b production. Vaccine, 1992, 10: 1
6,Steele G. Specific active immunotherapy with butanolextracted, tumor-associated antigens incorporated into lipoeome. Surgery, 1984, 96(2): 352
(2000-03-09收稿; 2000-04-20修回), 百拇医药
单位:肖华亮(第三军医大学附属三院);甘岫云 王东 李增鹏 王远东(广州市肿瘤医院 广州 510095)雍凌(广州市肿瘤医院 广州 510095)
关键词:肿瘤;治疗;瘤苗;异体;脂质体
中国肿瘤生物治疗杂志000319 《中国图书资料分类法》分类号 R73-36
应用瘤苗诱导肿瘤宿主产生抗肿瘤免疫反应以治疗肿瘤的主动免疫治疗肿瘤是目前肿瘤生物治疗有效的方法之一,受到国内外的广泛重视[1,2]。我们已开展自体瘤苗治疗肿瘤的研究并已取得一定进展[3]。进一步提高瘤苗免疫治疗肿瘤的疗效,寻求制备高效、安全的异体瘤苗的途径极为重要。据文献报道脂质体(liposome)包裹瘤苗抗原性强,又可作异体瘤苗的载体,其诱导机体产生的抗体比单纯性瘤苗高100~400倍,且具有作用持久、毒副反应轻等优点[4,5]。为此本研究观察了脂质体异体瘤苗对肿瘤的抑制作用,以期为临床应用提供实验依据。
, 百拇医药
1 材料与方法
1.1 动物
BALB/c小鼠雌性,体重20~30 g,由第三军医大学动物所提供Ⅰ级动物,批号(048/1999)。
1.2 瘤源
小鼠乳腺癌细胞系(Scc891)(由第三军医大学动物所提供),作为瘤源和制备自体瘤苗用;人乳腺癌细胞取自人体手术标本,作为异体瘤苗用。Scc981细胞系用RPMI 1640培养基和小牛血清进行体外培养增殖,于对数生长期制成1×107瘤细胞悬液接种于4只BALB/c小鼠腋部皮下,成瘤后处死。取新鲜瘤组织块制成瘤细胞悬液再接种13只BALB/c小鼠腋部皮下成瘤后作为正式实验瘤源。
1.3 瘤细胞悬液制备
, 百拇医药
荷Scc891瘤BALB/c小鼠13只,引颈处死。在无菌条件下取出肿瘤组织,去除外膜与坏死组织。用Hank's液洗涤。按1 g瘤组织加4 ml生理盐水放入组织研磨器内研磨,经200目筛网过滤制成瘤细胞悬液。用台盼兰拒染法观察活瘤细胞数在95%以上,配成1×107活瘤细胞悬液备用[3]。
1.4 肿瘤抗原裂解物瘤苗的制备
参照Steele等[6]的TAA制备方法进行。步骤如下: ① 如上法制备的单细胞性肿瘤细胞悬液,在液氮中反复冻融3次,使瘤细胞碎裂; ② 加入2.5% (V/V)正丁醇PBS(pH7.4) 液重新悬浮,室温轻轻震荡5 min; ③ 4℃ 5 000 ×g离心10 min取上清液,4℃ 2 000 ×g离心20 min,取上清液; ④ 上清液经透析72 h (4℃, 100 V); ⑤ 最后标本经200 000 ×g超速离心1 h (4℃),取上清液即为制备的TAA备用; ⑥用Lowry's法检测上清液抗原蛋白含量浓度合格。
, http://www.100md.com
1.5 脂质体瘤苗的制备
脂质体(购自Simga公司),将1.5 ml脂质体+2 ml甲醇+5 ml氯仿摇匀成稀释液;再将2.6 ml脂质体稀释液+6 ml TAA PBS液,震荡20 min备用(经光镜与电镜观察合格)。
1.6 瘤苗抑制肿瘤实验分组
BALB/c小鼠30只,分为3组,每组10只。A组为对照组:同一时间在鼠右侧腋部皮下注射1×107瘤细胞悬液0.2 ml,第2天起左液部皮下注射PBS液0.2 ml,再隔5 d同样注射2次;B组为脂质体自体瘤苗治疗组(简称自体瘤组):与对照组相同在右腋部皮下注射相同量的瘤细胞悬液,第2天起每隔5 d左侧腋部皮下注射3次脂质体自体瘤苗0.2 ml;C组为脂质体异体瘤苗治疗组(简称异体瘤组):与对照组相同在右侧腋部皮下注射相同量瘤细胞悬液。第2天起与自体瘤组相同注射脂质体异体瘤苗0.2 ml 3 次。第16天处死动物进行解剖观察。
, 百拇医药
1.7 检查指标
① 肿瘤和瘤苗接种处进行大体观察,有肿瘤生长者将瘤块分离取下,称瘤体重量,并观察心、肺、肝、脾及肾等器官有无转移和异常,淋巴结是否肿大。所有组织均进行常规10%福尔马林液固定; ②常规石蜡埋切片,HE染色,进行组织学观察。
1.8 统计学分析
对3组肿瘤重量进行统计分析比较t检验(Spss80软件包)。
1.9 抑瘤率
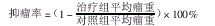
2 结果与讨论
经治疗后观察表明,在对照组,10只动物全部有肿瘤生长。肿瘤重量为0.5 g,0.7 g,1.3 g,1.0 g,1.7 g, 1.5 g, 0.9 g, 1.1 g, 0.8 g, 1.7 g,平均1.12±0.42 g。组织学观察:瘤组织为中度分化腺癌,呈不规则癌巢,间质少而疏松,均有不同程度的肿瘤中央性坏死。肿瘤周围有纤维组织包绕,并有少量多形核粒细胞、淋巴细胞、组织细胞浸润。脾脏中脾小体无明显增生。其他脏器未查见明显病变和肿瘤转移。淋巴结未查见肿大及转移。
, 百拇医药
在脂质体自体瘤苗治疗组,5只动物有肿瘤生长,另5只动物未见肿瘤生长,肿瘤重量分别为0.6 g,0.5 g, 1.0 g, 0.4 g, 0.5 g,平均0.30±0.35 g。组织学观察:肿瘤组织学类型与中央性坏死及外周情况与对照组无明显差异,脾脏小体较明显的增大和数量增多。其他脏器无明显病变。瘤苗区未查见肿瘤生长。
在脂质体异体瘤苗治疗组,有5只动物大体未见肿瘤生长,另5只肿瘤重量分别为1.3 g,0.7 g, 0.5 g, 0.7 g, 0.4 g,平均0.36±0.45 g。组织学观察:肿瘤组织学类型及坏死等病变与上组相似。脾脏的脾小体增大及数量增多。瘤苗注射区未查见肿瘤生长。3组动物均未查见淋巴结肿大。肝脏枯否氏细胞(Kupffer's cells)数量无明显差异。
表1 脂质体瘤苗治疗肿瘤效应结果 组别
动物数(只)
 ±SD
±SD, http://www.100md.com
抑瘤率(%)
(1)对照组
10
1.12±0.42
(2)自体瘤组
10
0.30±0.35
73.22
(3)异体瘤组
10
0.36±0.45
67.86
, http://www.100md.com 注:分组统计学比较(1) vs (2) P<0.01; (1) vs (3) P<0.01; (2) vs(3) P>0.05
本实验结果表明,脂质体自体与异体瘤苗诱导的动物主动免疫治疗肿瘤是可行的,有非常明显的抑瘤效果(P<0.01),且无明显的毒副反应。为进一步临床应用提供了有价值的依据。同时应用脂质体异体瘤苗治疗动物肿瘤安全有效,扩大了瘤苗材料的来源,为更广泛地开展瘤苗治疗肿瘤创造有利条件。
本实验所用瘤苗的制备方法,优选了文献推荐的瘤细胞反复冻融灭活法。该法使瘤细胞破碎,同时加用超速离心将细胞核和较大的胞浆颗粒等成份除去,从而得到高浓度的细胞膜抗原,增强激发宿主的免疫效应,提高了对瘤细胞杀伤效果[5,6]。
本实验结果显示自体与异体脂质体瘤苗两组均有50%动物未见肿瘤生长。两组肿瘤重量与对照组相比较均有非常显著的差异(P<0.01),而两治疗组之间抑瘤效果无显著差异(P>0.05)。表明脂质体瘤苗具有非常显著的抑瘤效果,且无明显的毒副反应。在本实验之前作了单纯自体瘤苗与脂质体自体瘤苗对比动物实验,结果显示脂质体瘤苗较单纯瘤苗的抑瘤效果更明显(P<0.05)。以上实验结果进一步证明脂质体异体瘤苗具有高效、安全的抑瘤效应,为临床应用提供了依据。
, http://www.100md.com
本实验加用了脂质体包裹瘤苗治疗肿瘤的结果证明,不但脂质体可作为瘤苗的载体,且可明显增强瘤苗的抗原性诱导产生细胞免疫与体液免疫,提高主动免疫杀瘤效能。同时文献报告它能延缓抗原的释放致免疫功能持久。因此它是较为理想的增强免疫效应佐剂[5]。虽然目前国内外在探索基因工程瘤苗,但有许多困难有待解决。因而脂质体瘤苗仍是当前行之有效,易于开展的主动免疫治疗肿瘤的较好方法之一。
从肿瘤组织学观察脂质体治疗的肿瘤组织周围有较多的淋巴组织细胞浸润。治疗组肿瘤均显示片状坏死。50%动物未见肿瘤生长,且脾脏的脾小体较对照组有明显的增生。推想脂质体瘤苗首先激活辅助T淋巴细胞,再激发B淋巴细胞增生而产生较强的细胞与体液免疫。因此作者认为脂质体苗有增强宿主免疫抑瘤效应; 实验结果表明,脂质体瘤苗具有较强的诱导宿主的主动免疫效应抑制肿瘤生长,作用快而持久,使植入瘤细胞早期被抑制或杀灭。因此应用于肿瘤切除后防止肿瘤扩散转移和复发最为适宜; 实验结果表明脂质体异体瘤苗与脂质体自体瘤苗一样均有非常显著的抑瘤效果,且无明显毒副反应,因此克服了应用自体瘤苗材料来源的限制。为今后临床更广泛的应用异体瘤苗提供了很有用的资料。
, http://www.100md.com
本课题受广东省科委重点科研究攻关项目(962046-04)资助
参 考 文 献
1,袁 玫. 肿瘤的主动特异性免疫治疗研究进展. 中国肿瘤生物治疗杂志, 1995, 2(2): 56
2,曹雪涛. 肿瘤免疫治疗和基因治疗研究某些新进展. 中国肿瘤生物治疗杂志, 1997, 2(1): 79
3,甘岫云,张 一,高 虹. 瘤苗主动免疫疗法的实验研究. 中国人兽共患病杂志, 1996, 12(3): 30
4,Phillips NC. Clinical evaluation of liposomal tumor antigen vaccines in patients with stage-Ⅲ melanoma. Cancer Detect Prev, 1990, 14: 491
, 百拇医药
5,Phillips NC, Emili A. Enhanced antibody response to liposome associated protein antigens; preferential stimulation of IgGza/b production. Vaccine, 1992, 10: 1
6,Steele G. Specific active immunotherapy with butanolextracted, tumor-associated antigens incorporated into lipoeome. Surgery, 1984, 96(2): 352
(2000-03-09收稿; 2000-04-20修回), 百拇医药