重组人干扰素-β制品的质量标准研究
作者:刘长暖 张翊 饶春明 林建伟 高凯 张明芳 王军志
单位:刘长暖 张翊 饶春明 林建伟 高凯 张明芳 王军志(中国药品生物制品检定所 北京 100050)
关键词:β-干扰素;质量标准;基因工程
中国肿瘤生物治疗杂志000314 摘 要 目的: 通过对重组IFN-β的质量研究和实验方法参数的选择,建立重组IFN-β的质量控制标准。方法: 通过采用细胞病变抑制法,以IFN-α国家标准品、WHO的IFN-β国际标准品作为参考品测定样品的含量,比较Lowry法、BCA法测定IFN-β的蛋白浓度,采用鲎试剂法检测内毒素含量,按照《中国生物制品规程》的有关要求进行其他项目的测定。结果: 结果表明可用IFN-α标准品和IFN-β标准品测定IFN-β的生物活性,用Lowry法测定的蛋白浓度与实际值基本一致,鲎试剂法可用于制品细菌内毒素含量的测定。国内生产的重组IFN-β制品达到了国家有关规定的要求。结论: 建立了重组IFN-β的质量标准,并可以有效地控制制品的质量,为我国重组IFN-β的研制及临床研究打下基础。
, 百拇医药
《中国图书资料分类法》分类号
Quality Specification for Recombinant IFN-β
Liu Changnuan, Zhang Yi, Rao Chunming, Lin Jianwei, Gao Kai, Zhang Mingfang, Wang Junzhi
(National Institute for the Control of Pharmaceutical and Biological Products, Beijing 100050)
Abstract Objective: To investigate the quality and optimizing test methods and establish the quality specifications for recombinant IFN-β preparation. Methods: The bioactivity of IFN-β against national standard of IFN-α or international standard of IFN-β was assayed by the method of cell pathological effect. The Lowry's method and BCA for determination of protein content was compared. The bacterial endotoxin was detected by LAL assay. Other tests were carried out according to the National Requirements for Biological Products. Results: The bioactivity of IFN-β can be measured by CPE using both IFN-α or IFN-β as the standard. The accuracy of Lowry's method is suitable for protein content determination. LAL assay is useful for endotoxin titration. The quality of recombinant IFN-β preparation produced domestically can meet the related requirements. Conclusion: The specification for recombinant IFN-β preparation is established and can be used for the quality control of the product.
, 百拇医药
Key words Interferon-β; quality specification; recombinant
人β干扰素(IFN-β)除具有α干扰素所有的抗病毒感染、抗肿瘤作用外还有较强的免疫调节作用。其基因位于人第9号染色体上,与α干扰素(IFN-β)的基因连锁在一起,基因内部不含内含子。天然人β干扰素是一种由166个氨基酸组成的分子量为20 kD的糖蛋白,分子中有一个糖基化位点。体内主要由RNA病毒和天然或人工合成的双股RNA诱导成纤维细胞后分泌产生。虽然其与IFN-α只有20%的同源性,但其识别的受体与IFN-α相同并具有相似的生物学活性[1~3]。
天然的干扰素分子中含有3个半胱氨酸,分别在17,31和141位,第31 和141位的半胱氨酸之间形成的二硫键对干扰素的生物学活性非常重要。体外研究发现,第17位的半胱氨酸对干扰素的分子空间结构无明显作用,用其他的氨基酸如丝氨酸替代后,不但对其活性无影响,反而增加了稳定性及活性。基因工程重组的IFN-β多为17Ser-IFN-β,它是将17位的半光氨酸由丝氨酸取代后在大肠杆菌中表达的,它在体外能正确折叠形成具有高活性的重组17Ser-IFN-β[4],表观分子量为18 kD。
, 百拇医药
基因工程IFN-β目前已经FDA审批,用于治疗多发性硬化症(MS),该症是与免疫应答有关的神经系统疾病,IFN的治疗是基于它的免疫调节作用,其中包括IFN-β对IFN-γ合成的抑制作用,能显著降低该疾病的恶化率。许多肿瘤细胞表面均表达IFN-β受体,体外实验表明,IFN-β可直接抑制肿瘤细胞的生长,因此,IFN-β对某些肿瘤也有一定的治疗作用[5]。另外,IFN-β也可应用于某些病毒感染性疾病的治疗,如丙型肝炎等[6]。
由于IFN-β在治疗MS及病毒感染性疾病等方面的用途,目前国内已有多家研究机构及公司开展了IFN-β的研制工作。我们在对由大肠杆菌表达的重组人IFN-β的检定过程中,参照我国《人用重组DNA制品质量控制要点》的要求[7],研究国外同类制品的标准,结合本品的特点,在对该制品生物学活性测定、蛋白浓度测定、等电聚集检测、内毒素检测等方面的进行优化,建立了重组IFN-β的质量标准,并对国内首次生产的产品进行了质量检定,为国内开展IFN-β的临床研究打下基础。
, 百拇医药
1 材料与方法
1.1 主要试剂及细胞株
IFN-α国家标准品为本所制备;IFN-β国际标准品(85/536)来自WHO国际标准品实验室(NIBSC);Wish细胞经本室常规传代保存,VSV病毒为本室制备,保存于-70℃。
1.2 生物学活性测定
参照文献[8~10]方法进行。将生长24~48 h的Wish细胞(于含10%小牛血清的MEM培养基)配成细胞浓度约为3×105/ml的悬液,加到96孔细胞培养板上,100 μl/孔。同时设立标准品对照,体积与样品相同。在含5%CO2,37℃孵箱中培养4~6 h后,每孔加入4倍系列稀释的干扰素样品100 μl,样品稀释用含7%小牛血清的MEM培养液,37℃培养18~24 h。弃上清后用含3%小牛血清MEM培养基稀释的VSV病毒(100TCID50)攻击,然后于含5%CO2,37℃孵箱中培养24 h左右。弃掉培养板中的上清液,每孔加入40 μl的结晶紫液室温染色30 min,弃掉染液,用自来水冲洗残余的染液,用滤纸吸干后每孔加入100 μl的脱色液脱色,在Spectra MAX250型的自动酶标仪上于570 nm波长处测定每孔的吸收值(OD)。
, 百拇医药
分别以干扰素-α国家标准品和干扰素-β国际标准品的效价值在自动酶标仪上计算样品的效价值。
1.3 蛋白含量测定
分别采用紫外分光光度计法、BCA蛋白浓度测定法及Lowry法测定原液中的蛋白浓度。BCA蛋白浓度检测试剂盒购自Pierce Inc, Rockford, Illinois, USA。按试剂盒说明书操作。
1.4 等电聚焦
取干扰素原液0.5 ml,超滤装置浓缩后,按文献方法[10~11]进行等电聚焦电泳。
1.5 细菌内毒素含量测定
由于制品中含有SDS,因此将样品用无热原注射用水稀释,使所含的SDS量低于0.025%后,再按照《中国药典》(二部)的方法,并参照《中国生物制品规程》中白细胞介素-2制检规程的要求测定样品中细菌内毒素的含量[10,12]。
, 百拇医药
1.6 肽图测定
样品对超纯水透析过夜,冷冻干燥,加0.025 mol/L NH4HCO3(pH8.0)溶解,以1∶100加入胰蛋白酶,25℃处理16 h,放置4℃冰箱待用。样品的分离检测用色谱柱为Waters Symmetry C18柱,流动相A: 0.1%TFA,流动相B: 0.1%TFA乙腈,检测波长为214 nm,梯度洗脱程序为线性梯度:0~70 min,流动相B从0~70%。
1.7 其它检定项目
按照《中国生物制品规程》2000年版的要求和方法进行[10]。
2 结 果
2.1 生物学活性测定
, 百拇医药
IFN-α与IFN-β均通过细胞表面的共同受体发挥作用,国外目前对IFN-β的生物学活性检测多采用VSV攻击的Wish细胞病变法。由于目前国内尚无IFN-β国家标准品,因此我们采用IFN-α国家标准品及WHO的IFN-β国际标准品对国内生产的重组IFN-β进行了测定。
以往测定干扰素往往通过肉眼观察细胞病变法来确定实验结果,该方法往往会产生误差,我们通过研究建立了结晶紫染色法测定干扰素效价的方法[9],降低了人为因素的影响。图1是用国家标准品测定IFN-β效价的剂量反应曲线,实验结果表明,该方法具有较好的量效关系,标准品和待检品的剂量反应曲线具有较好的平行性,且重复性高。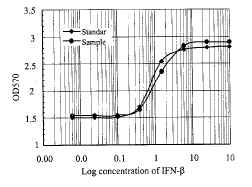
图1 重组IFN-β生物学活性测定的剂量反应曲线
Fig.1 The dose-response curve of interferon beta
, http://www.100md.com
我们分别用IFN-α国家标准品及WIO的IFN-β国际标准品对国内生产的IFN-β制品进行了测定,结果表明,采用上述二种标准品测定的结果无显著性差异(P<0.05),结果见表1。
表1 用国家标准品和国际标准品测定IFN-β的效价(IU)
Tab. 1 IFN-β bioactivity assay demarcate with national
IFN-α standard and intional IFN-β standard Sample
National IFN-α
standard
Internation IFN-β
, 百拇医药
standard
1
2.00×107
2.00×107
2
2.91×107
2.43×107
3
2.40×107
2.26×107
4
, http://www.100md.com
2.66×107
2.24×107
5
3.27×107
2.78×107
6
2.90×107
2.84×107
2.2 蛋白浓度测定
蛋白浓度的测定是原液检定过程中一项重要的指标,蛋白浓度的高低直接影响制品纯度的测定结果。目前我国多采用Lowry法检定,该方法采用牛血清白蛋白作为蛋白浓度标准品,但由于不同蛋白质的氨基酸组成上存在差异,会导致测定结果与实际蛋白浓度产生一定的偏差。因此我们在建立蛋白浓度测定方法时,有必要对该方法进行验证。我们用3种不同的方法对样品进行了比较测定,在分光光度法中根据IFN-β的氨基酸组成计算其旋光系数用于结果校正,IFN-β的A280为1.84/mg。3种不同方法测定的结果分别为A280:327 μg/ml、Lowry法:352 μg/ml、BCA法:543 μg/ml。表明Lowry法测定值与实际值比较相符,两组数据间无统计学差异(P>0.05),而采用BCA法测定时,蛋白浓度高于实际值(P<0.05),因此在测定蛋白浓度时宜采用Lowry法。
, 百拇医药
2.3 细菌内毒素测定
我们采用《中华人民共和国药典》规定的限度法对样品中细菌内毒素的含量进行了测定,内毒素含量低于10 EU/ml。结果表明,该方法可用于控制制品中内毒素的含量。
另外,我们还用定量法测定了样品中细菌内毒素的含量,利用鲎试剂与合成基质鲎三肽的显色反应来定量测定内毒素的量,结果表明,该方法的测定结果在一定范围内成直线关系(结果见图2),直线回归方程为y=0.0004x-0.0042,可定量测定样品中内毒素的含量。
2.4 肽图测定
在上述条件下,裂解后的重组IFN-β蛋白可以通过C18柱得到有效的分离,测定结果表明,重组IFN-β蛋白的胰酶裂解后的图谱与国外同类制品的图谱一致,提示具有相同的一级分子结构。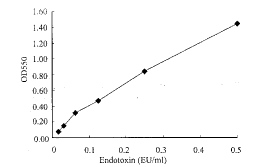
, http://www.100md.com
图2 内毒素检测标准曲线
Fig. 2 Standard curve of endotoxin by LAL assay
2.5 其它检定项目
按照《中国生物制品规程》的要求,我们对重组IFN-β制品进行了检定。包括原液的SDS-PAGE纯度分析及HPLC纯度分析、N端氨基酸序列分析、免疫印迹鉴别试验、光谱扫描分析、残留DNA及残余宿主菌体蛋白含量测定等。还对成品进行了水分含量测定、家兔热源试验、小鼠和豚鼠异常毒性试验等,均达到了《中国生物制品规程》的要求。氨基酸序列分析结果表明,大肠杆菌重组表达的IFN-β, 其N端比理论上少一个蛋氨酸,与天然IFN-β相同,这与蛋白表达过程中N端蛋氨酸的降解有关,与国外文献报道相一致,等电点为6.5~8.0。总的检定结果表明,我国生产的重组17Ser-IFN-β均达到了相关规定的要求。
, 百拇医药
3 讨 论
生物学活性测定是生物制品质量的关键质控指标,由于IFN-β具有广泛的生物学活性,因此其活性测定方法也各不相同。目前国内外大多数研究均采用VSV攻击的Wish细胞病变法测定的抗病毒活性来表示其生物学活性和有效成分的含量。因此,在本质量标准中我们也采用了抗病毒活性来表示IFN-β的含量。在国内目前尚无IFN-β标准品的情况下,利用IFN-α与IFN-β均通过细胞表面的共同受体发挥作用,两者均具有相同的抗病毒生物学活性的特点,使用IFN-α标准品来测定重组IFN-β的生物学活性[13]。本研究结果表明,应用IFN-α国家标准品与IFN-β国际标准品的测定结果无显著性差异,提示在缺乏IFN-β标准品时,也可采用IFN-α标准品来测定IFN-β制品的抗病毒活性。
本研究中,我们采用结晶紫染色法取代以往的肉眼观察细胞病变法来确定结果,该方法定量准确,量效关系明确,重复性较好。但在实验中必须掌握VSV攻击的量及作用时间,根据实验结果我们认为加入病毒后培养18~24 h检测结果为最佳。
, 百拇医药
蛋白浓度的测定结果直接影响制品比活性的高低。目前我国生物制品规程中规定的lowry法采用非同质的蛋白作为测定标准品,因此有可能由于不同蛋白质的氨基酸组成上的差异,即分子中含芳香族氨基酸的比例不同,导致测定的蛋白浓度与实际值产生一定的偏差。但本实验的结果表明,Lowry法测定的结果与实际值间的差别不显著(P<0.05)。文献报道[14],根据氨基酸组成,IFN-β的旋光系数为1.7。在建立蛋白浓度测定质控规程时,可根据A280测得的吸光度计算出蛋白浓度,然后对蛋白浓度测定方法进行验证。本研究结果表明,采用Lowry法测定蛋白浓度较BCA法更接近实际值,因此在重组IFN-β质控时,我们采用了Lowry法来测定制品的蛋白浓度。
由于IFN-β蛋白具有很强的疏水性,因此在制备过程及成品中均需加入一定量的SDS,以增加其稳定性。在测定内毒素含量时,高浓度的SDS会干扰定性观察,本研究中,我们根据限量测定的要求将样品进行一定的稀释,在SDS的含量低于0.025%时,SDS对观察结果不产生影响。另外我们还采用定量检测试剂盒来测定内毒素的含量,发现其能排除肉眼观察所带来的误差,可以准确测定成品中内毒素含量。
, 百拇医药
根据生物制品检定规程要求,结合本研究结果,经过修改完善的重组IFN-β质控标准,已达到国外同类产品的质量标准,这为我国重组IFN-β的研制及临床研究打下基础。
刘长暖,女38岁,助理研究员,主要从事重组IFN制品质量控制研究.
参 考 文 献
1,Arnason BG. Treatment of multiple sclerosis with interferon beta. Biomed Pharmacother, 1999, 53(8): 344
2,Alam JJ. Interferon-beta treatment of human disease. Curr Opin Biotechnol, 1995, 6(6): 688
3,Goodkin DE. Interferon beta-1b. Lancet, 1994, 334: 1057
, 百拇医药
4,The IFN beta Multiple Sclerosis Study Group. Interferon beta-1b is effective in relapsing-remitting multiple sclerosis. Ⅰ. clinical results of a multicenter, ramdomized, double-blind, placebo-controlled trial. Neurology, 1993, 43: 655
5,Scoponi C, Torresi U, Di Giuseppe M. Long-lasting complete remission of pulmonary metastases consequent to renal cell carcinoma obtained with interferon-beta therapy: Review of the literature and a case report. Tumori, 1995, 81(3): 201
, 百拇医药
6,Alam JJ, Fox IH. Use of natural interferon-beta in the treatment of acute hepatitis C. Hepatology, 1993, 17(4): 752
7,卫生部. 人用重组DNA制品质量控制要点, 1990
8,刘长暖, 刘 兰, 王军志, 等. 应用结晶紫染色法测定干扰素效价. 中国生物制品学杂志, 1999, 12(1): 36
9,Familletti PC, Rubinstein S, Pestka S. A convenient and rapid cytopathic effect inhibition assay for interferon. Meth Enzymol, 1981, 78: 387
10,卫生部生物制品标准化委员会. 中国生物制品规程. 北京: 化学工业出版社, 2000
, http://www.100md.com
11,郭尧君. 蛋白电泳实验技术. pp161-212. 北京:科学出版社, 1999. 2
12,国家药典委员会. 中华人民共和国药典. 北京: 化学工业出版社, 2000
13,Russell-Harde D, Wagner TC, Perez HD, et al. Formation of a uniquely stable type Ⅰ interferon receptor complex by interferon beta is dependent upon particular interactions between interferon beta and its receptor and independent of tyrosine phosphorylation. Biochem Biophys Res Commun, 1999, 255 (2): 539
14,Lin LS, Yamamoto R, Drummond RJ. Purification of recombinant human interferon beta expressed in Escherichia coli. Meth Enzymol, 1986, 119: 183
(2000-03-05收稿; 2000-04-20修回), 百拇医药
单位:刘长暖 张翊 饶春明 林建伟 高凯 张明芳 王军志(中国药品生物制品检定所 北京 100050)
关键词:β-干扰素;质量标准;基因工程
中国肿瘤生物治疗杂志000314 摘 要 目的: 通过对重组IFN-β的质量研究和实验方法参数的选择,建立重组IFN-β的质量控制标准。方法: 通过采用细胞病变抑制法,以IFN-α国家标准品、WHO的IFN-β国际标准品作为参考品测定样品的含量,比较Lowry法、BCA法测定IFN-β的蛋白浓度,采用鲎试剂法检测内毒素含量,按照《中国生物制品规程》的有关要求进行其他项目的测定。结果: 结果表明可用IFN-α标准品和IFN-β标准品测定IFN-β的生物活性,用Lowry法测定的蛋白浓度与实际值基本一致,鲎试剂法可用于制品细菌内毒素含量的测定。国内生产的重组IFN-β制品达到了国家有关规定的要求。结论: 建立了重组IFN-β的质量标准,并可以有效地控制制品的质量,为我国重组IFN-β的研制及临床研究打下基础。
, 百拇医药
《中国图书资料分类法》分类号
Quality Specification for Recombinant IFN-β
Liu Changnuan, Zhang Yi, Rao Chunming, Lin Jianwei, Gao Kai, Zhang Mingfang, Wang Junzhi
(National Institute for the Control of Pharmaceutical and Biological Products, Beijing 100050)
Abstract Objective: To investigate the quality and optimizing test methods and establish the quality specifications for recombinant IFN-β preparation. Methods: The bioactivity of IFN-β against national standard of IFN-α or international standard of IFN-β was assayed by the method of cell pathological effect. The Lowry's method and BCA for determination of protein content was compared. The bacterial endotoxin was detected by LAL assay. Other tests were carried out according to the National Requirements for Biological Products. Results: The bioactivity of IFN-β can be measured by CPE using both IFN-α or IFN-β as the standard. The accuracy of Lowry's method is suitable for protein content determination. LAL assay is useful for endotoxin titration. The quality of recombinant IFN-β preparation produced domestically can meet the related requirements. Conclusion: The specification for recombinant IFN-β preparation is established and can be used for the quality control of the product.
, 百拇医药
Key words Interferon-β; quality specification; recombinant
人β干扰素(IFN-β)除具有α干扰素所有的抗病毒感染、抗肿瘤作用外还有较强的免疫调节作用。其基因位于人第9号染色体上,与α干扰素(IFN-β)的基因连锁在一起,基因内部不含内含子。天然人β干扰素是一种由166个氨基酸组成的分子量为20 kD的糖蛋白,分子中有一个糖基化位点。体内主要由RNA病毒和天然或人工合成的双股RNA诱导成纤维细胞后分泌产生。虽然其与IFN-α只有20%的同源性,但其识别的受体与IFN-α相同并具有相似的生物学活性[1~3]。
天然的干扰素分子中含有3个半胱氨酸,分别在17,31和141位,第31 和141位的半胱氨酸之间形成的二硫键对干扰素的生物学活性非常重要。体外研究发现,第17位的半胱氨酸对干扰素的分子空间结构无明显作用,用其他的氨基酸如丝氨酸替代后,不但对其活性无影响,反而增加了稳定性及活性。基因工程重组的IFN-β多为17Ser-IFN-β,它是将17位的半光氨酸由丝氨酸取代后在大肠杆菌中表达的,它在体外能正确折叠形成具有高活性的重组17Ser-IFN-β[4],表观分子量为18 kD。
, 百拇医药
基因工程IFN-β目前已经FDA审批,用于治疗多发性硬化症(MS),该症是与免疫应答有关的神经系统疾病,IFN的治疗是基于它的免疫调节作用,其中包括IFN-β对IFN-γ合成的抑制作用,能显著降低该疾病的恶化率。许多肿瘤细胞表面均表达IFN-β受体,体外实验表明,IFN-β可直接抑制肿瘤细胞的生长,因此,IFN-β对某些肿瘤也有一定的治疗作用[5]。另外,IFN-β也可应用于某些病毒感染性疾病的治疗,如丙型肝炎等[6]。
由于IFN-β在治疗MS及病毒感染性疾病等方面的用途,目前国内已有多家研究机构及公司开展了IFN-β的研制工作。我们在对由大肠杆菌表达的重组人IFN-β的检定过程中,参照我国《人用重组DNA制品质量控制要点》的要求[7],研究国外同类制品的标准,结合本品的特点,在对该制品生物学活性测定、蛋白浓度测定、等电聚集检测、内毒素检测等方面的进行优化,建立了重组IFN-β的质量标准,并对国内首次生产的产品进行了质量检定,为国内开展IFN-β的临床研究打下基础。
, 百拇医药
1 材料与方法
1.1 主要试剂及细胞株
IFN-α国家标准品为本所制备;IFN-β国际标准品(85/536)来自WHO国际标准品实验室(NIBSC);Wish细胞经本室常规传代保存,VSV病毒为本室制备,保存于-70℃。
1.2 生物学活性测定
参照文献[8~10]方法进行。将生长24~48 h的Wish细胞(于含10%小牛血清的MEM培养基)配成细胞浓度约为3×105/ml的悬液,加到96孔细胞培养板上,100 μl/孔。同时设立标准品对照,体积与样品相同。在含5%CO2,37℃孵箱中培养4~6 h后,每孔加入4倍系列稀释的干扰素样品100 μl,样品稀释用含7%小牛血清的MEM培养液,37℃培养18~24 h。弃上清后用含3%小牛血清MEM培养基稀释的VSV病毒(100TCID50)攻击,然后于含5%CO2,37℃孵箱中培养24 h左右。弃掉培养板中的上清液,每孔加入40 μl的结晶紫液室温染色30 min,弃掉染液,用自来水冲洗残余的染液,用滤纸吸干后每孔加入100 μl的脱色液脱色,在Spectra MAX250型的自动酶标仪上于570 nm波长处测定每孔的吸收值(OD)。
, 百拇医药
分别以干扰素-α国家标准品和干扰素-β国际标准品的效价值在自动酶标仪上计算样品的效价值。
1.3 蛋白含量测定
分别采用紫外分光光度计法、BCA蛋白浓度测定法及Lowry法测定原液中的蛋白浓度。BCA蛋白浓度检测试剂盒购自Pierce Inc, Rockford, Illinois, USA。按试剂盒说明书操作。
1.4 等电聚焦
取干扰素原液0.5 ml,超滤装置浓缩后,按文献方法[10~11]进行等电聚焦电泳。
1.5 细菌内毒素含量测定
由于制品中含有SDS,因此将样品用无热原注射用水稀释,使所含的SDS量低于0.025%后,再按照《中国药典》(二部)的方法,并参照《中国生物制品规程》中白细胞介素-2制检规程的要求测定样品中细菌内毒素的含量[10,12]。
, 百拇医药
1.6 肽图测定
样品对超纯水透析过夜,冷冻干燥,加0.025 mol/L NH4HCO3(pH8.0)溶解,以1∶100加入胰蛋白酶,25℃处理16 h,放置4℃冰箱待用。样品的分离检测用色谱柱为Waters Symmetry C18柱,流动相A: 0.1%TFA,流动相B: 0.1%TFA乙腈,检测波长为214 nm,梯度洗脱程序为线性梯度:0~70 min,流动相B从0~70%。
1.7 其它检定项目
按照《中国生物制品规程》2000年版的要求和方法进行[10]。
2 结 果
2.1 生物学活性测定
, 百拇医药
IFN-α与IFN-β均通过细胞表面的共同受体发挥作用,国外目前对IFN-β的生物学活性检测多采用VSV攻击的Wish细胞病变法。由于目前国内尚无IFN-β国家标准品,因此我们采用IFN-α国家标准品及WHO的IFN-β国际标准品对国内生产的重组IFN-β进行了测定。
以往测定干扰素往往通过肉眼观察细胞病变法来确定实验结果,该方法往往会产生误差,我们通过研究建立了结晶紫染色法测定干扰素效价的方法[9],降低了人为因素的影响。图1是用国家标准品测定IFN-β效价的剂量反应曲线,实验结果表明,该方法具有较好的量效关系,标准品和待检品的剂量反应曲线具有较好的平行性,且重复性高。

图1 重组IFN-β生物学活性测定的剂量反应曲线
Fig.1 The dose-response curve of interferon beta
, http://www.100md.com
我们分别用IFN-α国家标准品及WIO的IFN-β国际标准品对国内生产的IFN-β制品进行了测定,结果表明,采用上述二种标准品测定的结果无显著性差异(P<0.05),结果见表1。
表1 用国家标准品和国际标准品测定IFN-β的效价(IU)
Tab. 1 IFN-β bioactivity assay demarcate with national
IFN-α standard and intional IFN-β standard Sample
National IFN-α
standard
Internation IFN-β
, 百拇医药
standard
1
2.00×107
2.00×107
2
2.91×107
2.43×107
3
2.40×107
2.26×107
4
, http://www.100md.com
2.66×107
2.24×107
5
3.27×107
2.78×107
6
2.90×107
2.84×107
2.2 蛋白浓度测定
蛋白浓度的测定是原液检定过程中一项重要的指标,蛋白浓度的高低直接影响制品纯度的测定结果。目前我国多采用Lowry法检定,该方法采用牛血清白蛋白作为蛋白浓度标准品,但由于不同蛋白质的氨基酸组成上存在差异,会导致测定结果与实际蛋白浓度产生一定的偏差。因此我们在建立蛋白浓度测定方法时,有必要对该方法进行验证。我们用3种不同的方法对样品进行了比较测定,在分光光度法中根据IFN-β的氨基酸组成计算其旋光系数用于结果校正,IFN-β的A280为1.84/mg。3种不同方法测定的结果分别为A280:327 μg/ml、Lowry法:352 μg/ml、BCA法:543 μg/ml。表明Lowry法测定值与实际值比较相符,两组数据间无统计学差异(P>0.05),而采用BCA法测定时,蛋白浓度高于实际值(P<0.05),因此在测定蛋白浓度时宜采用Lowry法。
, 百拇医药
2.3 细菌内毒素测定
我们采用《中华人民共和国药典》规定的限度法对样品中细菌内毒素的含量进行了测定,内毒素含量低于10 EU/ml。结果表明,该方法可用于控制制品中内毒素的含量。
另外,我们还用定量法测定了样品中细菌内毒素的含量,利用鲎试剂与合成基质鲎三肽的显色反应来定量测定内毒素的量,结果表明,该方法的测定结果在一定范围内成直线关系(结果见图2),直线回归方程为y=0.0004x-0.0042,可定量测定样品中内毒素的含量。
2.4 肽图测定
在上述条件下,裂解后的重组IFN-β蛋白可以通过C18柱得到有效的分离,测定结果表明,重组IFN-β蛋白的胰酶裂解后的图谱与国外同类制品的图谱一致,提示具有相同的一级分子结构。

, http://www.100md.com
图2 内毒素检测标准曲线
Fig. 2 Standard curve of endotoxin by LAL assay
2.5 其它检定项目
按照《中国生物制品规程》的要求,我们对重组IFN-β制品进行了检定。包括原液的SDS-PAGE纯度分析及HPLC纯度分析、N端氨基酸序列分析、免疫印迹鉴别试验、光谱扫描分析、残留DNA及残余宿主菌体蛋白含量测定等。还对成品进行了水分含量测定、家兔热源试验、小鼠和豚鼠异常毒性试验等,均达到了《中国生物制品规程》的要求。氨基酸序列分析结果表明,大肠杆菌重组表达的IFN-β, 其N端比理论上少一个蛋氨酸,与天然IFN-β相同,这与蛋白表达过程中N端蛋氨酸的降解有关,与国外文献报道相一致,等电点为6.5~8.0。总的检定结果表明,我国生产的重组17Ser-IFN-β均达到了相关规定的要求。
, 百拇医药
3 讨 论
生物学活性测定是生物制品质量的关键质控指标,由于IFN-β具有广泛的生物学活性,因此其活性测定方法也各不相同。目前国内外大多数研究均采用VSV攻击的Wish细胞病变法测定的抗病毒活性来表示其生物学活性和有效成分的含量。因此,在本质量标准中我们也采用了抗病毒活性来表示IFN-β的含量。在国内目前尚无IFN-β标准品的情况下,利用IFN-α与IFN-β均通过细胞表面的共同受体发挥作用,两者均具有相同的抗病毒生物学活性的特点,使用IFN-α标准品来测定重组IFN-β的生物学活性[13]。本研究结果表明,应用IFN-α国家标准品与IFN-β国际标准品的测定结果无显著性差异,提示在缺乏IFN-β标准品时,也可采用IFN-α标准品来测定IFN-β制品的抗病毒活性。
本研究中,我们采用结晶紫染色法取代以往的肉眼观察细胞病变法来确定结果,该方法定量准确,量效关系明确,重复性较好。但在实验中必须掌握VSV攻击的量及作用时间,根据实验结果我们认为加入病毒后培养18~24 h检测结果为最佳。
, 百拇医药
蛋白浓度的测定结果直接影响制品比活性的高低。目前我国生物制品规程中规定的lowry法采用非同质的蛋白作为测定标准品,因此有可能由于不同蛋白质的氨基酸组成上的差异,即分子中含芳香族氨基酸的比例不同,导致测定的蛋白浓度与实际值产生一定的偏差。但本实验的结果表明,Lowry法测定的结果与实际值间的差别不显著(P<0.05)。文献报道[14],根据氨基酸组成,IFN-β的旋光系数为1.7。在建立蛋白浓度测定质控规程时,可根据A280测得的吸光度计算出蛋白浓度,然后对蛋白浓度测定方法进行验证。本研究结果表明,采用Lowry法测定蛋白浓度较BCA法更接近实际值,因此在重组IFN-β质控时,我们采用了Lowry法来测定制品的蛋白浓度。
由于IFN-β蛋白具有很强的疏水性,因此在制备过程及成品中均需加入一定量的SDS,以增加其稳定性。在测定内毒素含量时,高浓度的SDS会干扰定性观察,本研究中,我们根据限量测定的要求将样品进行一定的稀释,在SDS的含量低于0.025%时,SDS对观察结果不产生影响。另外我们还采用定量检测试剂盒来测定内毒素的含量,发现其能排除肉眼观察所带来的误差,可以准确测定成品中内毒素含量。
, 百拇医药
根据生物制品检定规程要求,结合本研究结果,经过修改完善的重组IFN-β质控标准,已达到国外同类产品的质量标准,这为我国重组IFN-β的研制及临床研究打下基础。
刘长暖,女38岁,助理研究员,主要从事重组IFN制品质量控制研究.
参 考 文 献
1,Arnason BG. Treatment of multiple sclerosis with interferon beta. Biomed Pharmacother, 1999, 53(8): 344
2,Alam JJ. Interferon-beta treatment of human disease. Curr Opin Biotechnol, 1995, 6(6): 688
3,Goodkin DE. Interferon beta-1b. Lancet, 1994, 334: 1057
, 百拇医药
4,The IFN beta Multiple Sclerosis Study Group. Interferon beta-1b is effective in relapsing-remitting multiple sclerosis. Ⅰ. clinical results of a multicenter, ramdomized, double-blind, placebo-controlled trial. Neurology, 1993, 43: 655
5,Scoponi C, Torresi U, Di Giuseppe M. Long-lasting complete remission of pulmonary metastases consequent to renal cell carcinoma obtained with interferon-beta therapy: Review of the literature and a case report. Tumori, 1995, 81(3): 201
, 百拇医药
6,Alam JJ, Fox IH. Use of natural interferon-beta in the treatment of acute hepatitis C. Hepatology, 1993, 17(4): 752
7,卫生部. 人用重组DNA制品质量控制要点, 1990
8,刘长暖, 刘 兰, 王军志, 等. 应用结晶紫染色法测定干扰素效价. 中国生物制品学杂志, 1999, 12(1): 36
9,Familletti PC, Rubinstein S, Pestka S. A convenient and rapid cytopathic effect inhibition assay for interferon. Meth Enzymol, 1981, 78: 387
10,卫生部生物制品标准化委员会. 中国生物制品规程. 北京: 化学工业出版社, 2000
, http://www.100md.com
11,郭尧君. 蛋白电泳实验技术. pp161-212. 北京:科学出版社, 1999. 2
12,国家药典委员会. 中华人民共和国药典. 北京: 化学工业出版社, 2000
13,Russell-Harde D, Wagner TC, Perez HD, et al. Formation of a uniquely stable type Ⅰ interferon receptor complex by interferon beta is dependent upon particular interactions between interferon beta and its receptor and independent of tyrosine phosphorylation. Biochem Biophys Res Commun, 1999, 255 (2): 539
14,Lin LS, Yamamoto R, Drummond RJ. Purification of recombinant human interferon beta expressed in Escherichia coli. Meth Enzymol, 1986, 119: 183
(2000-03-05收稿; 2000-04-20修回), 百拇医药