银杏萜内酯的化学性质及合成
作者:张鹤鸣 王宁生
单位:广州中医药大学临床药理研究所,广州 510405
关键词:银杏萜内酯/化学;综述;指导性
广州中医药大学学报000325摘要:介绍了银杏萜内酯的化学结构特征及性质,化学合成的方法,细胞工程研究的最新进展,生物合成研究的途径及萜内酯前体的研究。认为细胞生物工程及生物合成将为提高银杏产物中萜内酯的产量,保护银杏资源提供有效途径。
中图分类号:R914.5 文献标识码:A
文章编号:1007-3213(2000)03-0266-05 银杏科植物银杏Ginkgo biboba L.又名公孙树、白果树,是最古老的中生代孑遗植物之一,属我国特产珍贵药用植物。银杏提取物(简称EGb)及其制剂中主要活性成分是银杏黄酮和银杏萜内酯,其中银杏萜内酯被认为是银杏叶中起关键作用的活性成分。银杏萜内酯目前共分离提取到6种:二萜类化合物银杏内酯A、B、C、M、J(GinkgolideA、B、C、M、J,以下简称GA、GB、GC、GM、GJ)和倍半萜化合物白果内酯(bilobalide,BB),它们都具有3个五元内酯环和一个罕见的特丁基等结构特征,迄今尚未发现存在于其他任何植物中。从20世纪60年代开始,国内外学者对银杏的药理和生理活性进行了广泛深入的研究,业已证实GA、GB、GC、GJ,均为血小板活化因子(platelet activating factor, PAF)拮抗剂。BB可用于治疗脱髓鞘脑、脊髓和神经疾病,可能与神经系统生理活性有关[1]。银杏萜内酯含量高低,对EGb及其制剂的内在质量起着关键的作用。由于萜内酯特殊的化学结构,化学与生物合成困难,分析难度大,故在现存文献中有关银杏黄酮的研究文献较多,而关于萜内酯的研究文献相对较少。随着对其有效成分认识的逐步深化,黄酮作为银杏中主要有效成分和质量指标的地位逐步下降,而作为银杏叶中主要活性成分的萜内酯的研究越来越受到重视。本文就国内外目前关于银杏萜内酯化学结构性质、合成的研究进展作一综述。
, 百拇医药
1 银杏萜内酯的化学结构及性质研究
最早进行银杏化学成分研究的是20世纪20年代日本学者Furakawa和中西香尔[2]。1932年Furukawa首次从银杏叶中分离到萜内酯化合物[3]。1967年Maruyama等从银杏的根皮中分离到了GA、GB、GC和GM,他们通过1H-NMR.MS及其他物理测试手段和化学反应,阐明了它们的化学结构[3],如图1。1969年Weinges从银杏叶中分离并鉴定了与二萜内酯结构相关的倍半萜化合物——白果内酯[4],如图2。1987年德国的Weinges小组又从银杏叶中分离到银杏内酯J[5]。 从图1可以看出银杏内酯具有独特的C20笼型结构。这类化合物都含有一个螺(4,4)壬烷(A环与B环),一个四氢呋喃环(D环)和3个γ-内酯环(C、E和F环),并有一个特丁基侧链。顺式稠合的五元环F、A、D、C以特定方式折叠,形成一个大小恰当的半球形腔,该腔能接受大多数离子(Fe2+、Ca2+等)或某些有机基团,腔的两个平行边被F环和C环的C11.C12内酯环所限定,四氢呋喃环占据“笼”的中心位置,这一富含电子的腔适于键合正离子或正极性基团,而叔丁基则使其键合具有良好的立体专一性。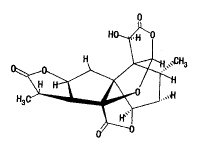
, 百拇医药
图1 银杏叶中萜类化合物分子结构示意图
图2 白果内酯的分子结构示意图
银杏内酯为强PFA拮抗剂,它们对PFA拮抗作用的IC50:GA、GB、GC和GJ分别为7.4×10-7、2.5×10-7、7.1×10-6和5.4×10-5 mol/L。可以看出GA和GB对PFA拮抗作用最强,尤其是GB。白果内酯对PFA拮抗性较弱,但对神经系统有保护作用[6]。银杏内酯抗PAF的活性与D环、羟基位置有关,如C1和C3的2个羟基基团的存在,表明银杏内酯B是最有效的PAF拮抗剂。相反C7上具有羟基基团的内酯C、M、J活性很小。银杏内酯对PFA的拮抗具有一定的专一特异性。银杏内酯基本骨架虽属非极性萜类,但因结构中有多个羟基取代,极性得到加强,不溶于石油醚和苯,易溶于醋酸乙酯、丙酮及低级醇类,略溶于水,这些化合物于酸性或中性溶液中稳定,遇强碱则内酯环打开而溶解,由于银杏内酯的刚性骨架固定了羰基间的距离,因此开环化合物经酸化后再环化能得到原来化合物,而白果内酯开环后再环合则得不到白果内酯本身,若加碱溶解制作针剂,则针剂中不存在白果内酯。
, http://www.100md.com
2 银杏萜内酯的化学合成研究
银杏萜内酯在银杏中含量很低,一般含量在0.25%以下,且受地域、季节的影响很大。提取分离手续复杂,有学者对银杏萜内酯的合成途径进行了研究。
1986年Weinges进行白果内酯的半合成研究,并用13C-NMR对各步反应产物加以认定[7]。1993年Crimmins等研究了白果内酯的全合成途径并获得了成功[8]。
1988年Corey以包含26步反应的复杂而微妙的合成路线,第一次完成GB的全合成[9]。其后又采用三内酯(trilactone)和GB两条途径合成了GA[10]。1989年他们又合成了具有高度抗PAF活性而结构简单的GB同系物,并通过对3个类似GB的化合物的研究发现其中主要的活性部分似是C4~C12间的醚桥和C4~C6间的内酯桥,这可能拟似PAF结构中占举足轻重的乙酰基;认为在银杏内酯类的简单同系物中,很有可能再发现抗PAF活性更强的化合物[11]。1992年Corey在研究GA、GB和GC的全合成途径反化学和生物学活性的基础上,通过对银杏内酯的特殊的羟基及其趋向的研究,阐明了这3种内酯化合物分子内和分子间羟基的反应所存在的差异,并将其应用于内酯的分离技术中。此外还通过向分子结构中引入稳定的3H标记(non labile lritium marker)研究从GC转变成GB的途径[12]。但银杏萜内酯的分子立体结构复杂,化学合成途径的技术难度大。
, 百拇医药
3 银杏萜内酯的生物合成研究
3.1 细胞工程研究 近年来国内外生物、生化学者开展了细胞工程及生物合成途径的研究。1991年Carrier等首次肯定了银杏组织培养物中银杏内酯的存在[13]。1993年Huh等报道银杏内酯(GA+GB+GC)在愈伤组织和悬浮细胞中含量分别为0.0026%和0.0047%,而茎尖和内胚起源的根等器官的培养物中银杏内酯含量较高,分别为0.08%和0.03%[14]。1995年Jeon等在用银杏叶诱导的愈伤组织和细胞悬浮培养中检测到了GB,并发现有MS培养基时GB含量最高,而Schenk-Hildebrandt培养基对细胞生长有利[15]。1996年郑玉果在国内首次进行了利用组织培养法生产银杏萜内酯的研究。所 筛选的高产细胞株中GA+GB含量为0.0062%,达到了当时国外报道的最高水平[16]。Laurain 等在1997年用野生型发根农杆菌Agrobacterium rhizogenes A4菌株感染银杏合子胚诱导发根,建立了悬浮细胞培养系,同时用银杏胚囊(雌配子体)作外植体诱导,建立了悬浮培养系,用HPLC测定了GA、GB、GC、GJ和BB的含量。“转化”培养物中次生代谢物含量为0.065%,其中GB为0.0083%;在胚囊起源细胞悬浮培养物含量为0.87%,其中GB为0.16%;“转化”培养物中含有更多的BB,而GA、GB、GC在胚囊起源的培养物中含量更高[17]。1997年孙天恩等利用发根农杆菌的Ri质粒转化银杏叶细胞,得到银杏叶转化发根。初步分析表明,银杏萜内酯的含量为0.04%~0.1%,其GA∶GB∶GC∶BB为8∶11∶1∶22,银杏黄酮的含量为0.06%~1%,并申请了发明专利(专利申请号97109254.4)[18]。1997年Cartayrade等用[14C]CO2、[U-14C]glucose饲喂3月龄的银杏幼苗,研究了GA、GB、GC和BB合成转移与积累的部位,示踪结果显示:催化产生银杏二萜类化合物终产物的所有酶促步骤均在根中,而非叶中;根 同时是银杏内酯与白果内酯合成及积累的部位,而叶只是贮藏部位;银杏二萜类在根与叶之间以源—池方式(source-sink manner)转移[19]。1998年戴均贵在对不同培养基(MS、B5、DCR、P6)、激素(2,4_D、NAA、6_BA)、氮源(NO3、NH4+)和碳源(蔗糖、葡萄糖、果糖)对银杏愈伤组织生长及银杏内酯B形成的影响研究中发现:MS、DCR和P63种培养基对愈伤组织Gb3的生长及GB形成的效果都较好,它们之间不存在显著性差异,而B5培养基的效果较差。2,4-D浓度的增加有利于愈伤组织的生长,当浓度为2.0 mg/L时GB的含量最高;NAA浓度为0.5 mg/L时愈伤组织的生长指数及GB的含量均达到最高;6-BA不利于愈伤组织生长及GB的形成。总氮量保持60mmol不变情况下,NH+4与NO-3之比为1∶2时,GB的产量最高;NO-3有利于GB的形成,当NO-3为60 mmol时GB的含量达到0.018 3%。在蔗糖、葡萄糖和果糖3种碳源中,蔗糖效最佳,且浓度为4%时,愈伤组织生长指数达到3.66,GB的含量达到0.022 3%[20]。1999年陈云龙对银杏幼叶、种胚愈伤组织按文献方法进行诱导,MS固体培养基中含1.0 mg/L NNA、0.1mg/L KT、30g/L蔗糖,调pH至6.0,培养温度(25±1)℃,每周继代1次,续代2代后,用HPLC测得银杏幼叶愈伤组织、种胚愈伤组织中GA的含量分别为0.048、0.012 mg/g[21]。
, 百拇医药
3.2 生物合成研究
关于银杏萜内酯的生物合成途径,早在1971年Nakanishik等用[2-C14]MVA饲喂银杏幼苗,证明了银杏萜内酯经由异戊烯基焦磷酸(IPP)聚合生成香叶基焦磷酸(GGPP)而生成,符合异戊烯法则(Ruzicka, 1953)[22]。Lichtenthaler等证明,银杏中通过几乎完全被胞质和质体隔离的两个彼此不同的生源途径生成IPP,但胞浆和质体中IPP的来源和去路不同:[胞浆途径]→MVA→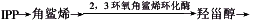 谷甾醇;[质体途径]→IPP→FPP→GGPP→→→银杏内酯和白果内酯。根据上述合成途径,可以设计2,3-环氧角鲨烯环化酶的抑制剂以阻断甾醇生成支路,使由醋酸途径生成的IPP在胞浆大量积累而进入质体,参与银杏内酯和白果内酯生成途径而增加其产量。同时也可用化学合成的2,3-环氧角鲨烯作为2,3-环氧角鲨烯环化酶的竞争性抑制剂实现上述目标。
谷甾醇;[质体途径]→IPP→FPP→GGPP→→→银杏内酯和白果内酯。根据上述合成途径,可以设计2,3-环氧角鲨烯环化酶的抑制剂以阻断甾醇生成支路,使由醋酸途径生成的IPP在胞浆大量积累而进入质体,参与银杏内酯和白果内酯生成途径而增加其产量。同时也可用化学合成的2,3-环氧角鲨烯作为2,3-环氧角鲨烯环化酶的竞争性抑制剂实现上述目标。
, http://www.100md.com
关于倍半萜、二萜生物合成前体的研究,Neau等用tetcyclacis和clotrimazole作细胞色素P-450氧化酶的抑制剂,用[14C]示踪证明了银杏内酶和白果内酯的烃类前体是脱氢松香烷(dehydroabitane)[23]。见图3。
由此可知,银杏内酯、白果内酯和其烃类前体在结构上相差悬殊,由该前体到终产
图3 银杏内酯和白果内酯的生物合成途径
A:Sandaraco-Pimarenyl cation;B:脱氢松香烷;C:银杏内酯;D:白果内酯
4 结语
银杏萜内酯是银杏叶中主要活性成分,是一类特异有效的PFA拮抗剂。近年来,国内外学者对萜内酯研究十分活跃,萜内酯在保护中枢神经系统、抗缺血损伤、抗过敏、抗异体移植排斥反应方面具有重要的药理作用。但由于萜内酯迄今尚未发现存在于其他任何植物中,且在银杏叶和根皮中含量极低,仅为万分之几,甚至百万分之几,茎皮及根皮内部组织中则更低,因此银杏萜内酯的药用资源受到限制。近10多年来国内外学者在对银杏萜内酯的化学结构及性质进行深入研究的同时,对其化学元素合成进行了研究,但由于合成工艺复杂,成本相当高,目前仍仅限于实验室研究。细胞生物工程及生物合成途径的研究则取得令人瞩目的成绩,向人们展示了诱人的前景,但目前尚未进入工业化大生产。因此,银杏叶仍是提取银杏萜内酯化合物的主要来源。相信随着人们对银杏研究的进一步深入,银杏萜内酯资源的开发和应用,将会成为下一步研究的热点。
, http://www.100md.com
作者简介:张鹤鸣(1962-),男,医学博士
参考文献:
[1] Kriegstein J. Neuroprotective properties of Ginkgo biloba constituents demonstrated in vivo and vitro [J].Rev Bras Neurol Agosto,1994,30,1 (Suppl):7
[2] 齐之尧,李家玉.银杏叶的药用价值[J].世界林业研究,1994,7(3):92
[3] Maruyama M,Terahara A,Nakanishi K.The Ginkgolides isolation and characterization of the various groups[J].Tetrahedron Lett,1967 (4):299
, http://www.100md.com
[4] Weinges Von Klaus,Bhr Wolfgang. Bilobalid A,ein neues Sespuiterpen mit tert-Butyl-Gruppe aus den Blttern von Ginkgo biloba[J].Leibigs Ann Chem,1969,1724:214
[5] Weinges K, Hepp M, Jaggy H.Chemistry of Ginkgolides Ⅱ:Isolation and structural elucidation of a new ginkgolide [J].Liegbigs Amm Chem,1987(6):521
[6] Steinke B,Muller B,Wanger H.Biological standard of Ginkgo biloba L[J].Planta Medica,1993,59:155
, http://www.100md.com
[7] Weinges K ,Hepp M,Huber-Patz U, et al.10-acety1-1-methoxycarbony1-2,3,14,15,16-pentanorginkgolid A,ein Zwischenprodukt zur Herstellung von Bilobalid [J].Liebigs Ann Chem ,1986:1057
[8] Crimmins M T.Synthetic studies of the ginkgolides:total synthesis of bilobalide [J].J Am Chem Soc,1993,115(8):3146
[9] Corey E J,Kang M C,Desai M,et al. Total synthesis of (±) ginkgolides B[J].J Am Chem,1988,110(2):649
, 百拇医药
[10] Corey E J,Gavai A .Total synthesis of ginkgolides [J].Atetrahedron Lett,1988,29(26):3205
[11] 史玉俊.具有高度抗 PAF 活性而结构较简单的银杏萜内酯 B 同系物[J].国外医药*植物药分册,1990,5(4):176
[12] Corey E J,Reo K,Ghosh A.Intramolecular and intermolecular hydroxy reactivity differences in ginkgolides A,B and C and their chemical applications[J].Tetrahedron Lett,1992,33(46):6955
[13] Carrier D J,Chauret N,Mancini M,et al.Detection of ginkgolide A in Ginkgo biloba cell cultures[J]. Plant Cell Rep,1991,10:256
, http://www.100md.com
[14] Huh H E,John Staba.Ontogenic aspects of ginkgolide production in Ginkgo biloba [J].Planta Med,1993,59:232
[15] Jeon M H,Sung S H,Huh H,et al.Ginkgolide B production in cultured cells derived from Ginkgo biloba L.leaves [J].Plant Cell Rep,1995,14:501
[16] 郑玉果,于荣敏,姚新生,等.银杏愈伤组织培养及银杏内酯测定的研究[J].沈阳药科大学学报,1999,16(1):10
[17] Laurain D ,Guiller J T,Chenieux J C,et al.Production of ginkgolide and bilobalide in transformed and gametophyte derived cell cultures of Ginkgo biloba [J]. Phytochemistry,1997,46(1):127
, 百拇医药
[18] 孙天恩,李根保.银杏发根克隆及其培养技术研究进展[J].中草药,1989,29 (增刊):25
[19] Cartayrade A, Neau E,Sohier C,et al. Ginkgolide and bilobalide biosynthesis in Ginkgo biloba. I: Sites of synthesis ,translocation and accumulation of ginkgolides and bilobalide [J]. Plant Physiol Biochem,1997,35(11)859
[20] 戴均贵,朱蔚华,吴蕴祺,等.不同培养基、激素、碳源和氮源对银杏愈伤组织生长及银杏内酯 B 形成的影响[J].中草药,1998,29 (增刊):63
[21] 陈云龙,徐程,徐礼根,等.HPLC 测定银杏愈伤组织内酯 A 的研究[J].中草药,1999,30(6):45
, 百拇医药
[22] Nakanishi K. Structure of bilobalide a rare tert-buty1 containing sesquiterpenoid related to the C20-ginkgolides [J].J Am Chem soc,1971,93(14):3544
[23] Neau E, Cartayrade A,Balz J P,et al.Ginkgolide and bilobalide biosynthesis in Ginkgo biloba.Ⅱ:Identification of a possible intermediate compound by using inhibitors of cytochrome P-450-dependent oxygenases[J].Plant Physiol Biochem,1997,35(11):869
收稿日期:2000-04-07, 百拇医药
单位:广州中医药大学临床药理研究所,广州 510405
关键词:银杏萜内酯/化学;综述;指导性
广州中医药大学学报000325摘要:介绍了银杏萜内酯的化学结构特征及性质,化学合成的方法,细胞工程研究的最新进展,生物合成研究的途径及萜内酯前体的研究。认为细胞生物工程及生物合成将为提高银杏产物中萜内酯的产量,保护银杏资源提供有效途径。
中图分类号:R914.5 文献标识码:A
文章编号:1007-3213(2000)03-0266-05 银杏科植物银杏Ginkgo biboba L.又名公孙树、白果树,是最古老的中生代孑遗植物之一,属我国特产珍贵药用植物。银杏提取物(简称EGb)及其制剂中主要活性成分是银杏黄酮和银杏萜内酯,其中银杏萜内酯被认为是银杏叶中起关键作用的活性成分。银杏萜内酯目前共分离提取到6种:二萜类化合物银杏内酯A、B、C、M、J(GinkgolideA、B、C、M、J,以下简称GA、GB、GC、GM、GJ)和倍半萜化合物白果内酯(bilobalide,BB),它们都具有3个五元内酯环和一个罕见的特丁基等结构特征,迄今尚未发现存在于其他任何植物中。从20世纪60年代开始,国内外学者对银杏的药理和生理活性进行了广泛深入的研究,业已证实GA、GB、GC、GJ,均为血小板活化因子(platelet activating factor, PAF)拮抗剂。BB可用于治疗脱髓鞘脑、脊髓和神经疾病,可能与神经系统生理活性有关[1]。银杏萜内酯含量高低,对EGb及其制剂的内在质量起着关键的作用。由于萜内酯特殊的化学结构,化学与生物合成困难,分析难度大,故在现存文献中有关银杏黄酮的研究文献较多,而关于萜内酯的研究文献相对较少。随着对其有效成分认识的逐步深化,黄酮作为银杏中主要有效成分和质量指标的地位逐步下降,而作为银杏叶中主要活性成分的萜内酯的研究越来越受到重视。本文就国内外目前关于银杏萜内酯化学结构性质、合成的研究进展作一综述。
, 百拇医药
1 银杏萜内酯的化学结构及性质研究
最早进行银杏化学成分研究的是20世纪20年代日本学者Furakawa和中西香尔[2]。1932年Furukawa首次从银杏叶中分离到萜内酯化合物[3]。1967年Maruyama等从银杏的根皮中分离到了GA、GB、GC和GM,他们通过1H-NMR.MS及其他物理测试手段和化学反应,阐明了它们的化学结构[3],如图1。1969年Weinges从银杏叶中分离并鉴定了与二萜内酯结构相关的倍半萜化合物——白果内酯[4],如图2。1987年德国的Weinges小组又从银杏叶中分离到银杏内酯J[5]。 从图1可以看出银杏内酯具有独特的C20笼型结构。这类化合物都含有一个螺(4,4)壬烷(A环与B环),一个四氢呋喃环(D环)和3个γ-内酯环(C、E和F环),并有一个特丁基侧链。顺式稠合的五元环F、A、D、C以特定方式折叠,形成一个大小恰当的半球形腔,该腔能接受大多数离子(Fe2+、Ca2+等)或某些有机基团,腔的两个平行边被F环和C环的C11.C12内酯环所限定,四氢呋喃环占据“笼”的中心位置,这一富含电子的腔适于键合正离子或正极性基团,而叔丁基则使其键合具有良好的立体专一性。

, 百拇医药
图1 银杏叶中萜类化合物分子结构示意图

图2 白果内酯的分子结构示意图
银杏内酯为强PFA拮抗剂,它们对PFA拮抗作用的IC50:GA、GB、GC和GJ分别为7.4×10-7、2.5×10-7、7.1×10-6和5.4×10-5 mol/L。可以看出GA和GB对PFA拮抗作用最强,尤其是GB。白果内酯对PFA拮抗性较弱,但对神经系统有保护作用[6]。银杏内酯抗PAF的活性与D环、羟基位置有关,如C1和C3的2个羟基基团的存在,表明银杏内酯B是最有效的PAF拮抗剂。相反C7上具有羟基基团的内酯C、M、J活性很小。银杏内酯对PFA的拮抗具有一定的专一特异性。银杏内酯基本骨架虽属非极性萜类,但因结构中有多个羟基取代,极性得到加强,不溶于石油醚和苯,易溶于醋酸乙酯、丙酮及低级醇类,略溶于水,这些化合物于酸性或中性溶液中稳定,遇强碱则内酯环打开而溶解,由于银杏内酯的刚性骨架固定了羰基间的距离,因此开环化合物经酸化后再环化能得到原来化合物,而白果内酯开环后再环合则得不到白果内酯本身,若加碱溶解制作针剂,则针剂中不存在白果内酯。
, http://www.100md.com
2 银杏萜内酯的化学合成研究
银杏萜内酯在银杏中含量很低,一般含量在0.25%以下,且受地域、季节的影响很大。提取分离手续复杂,有学者对银杏萜内酯的合成途径进行了研究。
1986年Weinges进行白果内酯的半合成研究,并用13C-NMR对各步反应产物加以认定[7]。1993年Crimmins等研究了白果内酯的全合成途径并获得了成功[8]。
1988年Corey以包含26步反应的复杂而微妙的合成路线,第一次完成GB的全合成[9]。其后又采用三内酯(trilactone)和GB两条途径合成了GA[10]。1989年他们又合成了具有高度抗PAF活性而结构简单的GB同系物,并通过对3个类似GB的化合物的研究发现其中主要的活性部分似是C4~C12间的醚桥和C4~C6间的内酯桥,这可能拟似PAF结构中占举足轻重的乙酰基;认为在银杏内酯类的简单同系物中,很有可能再发现抗PAF活性更强的化合物[11]。1992年Corey在研究GA、GB和GC的全合成途径反化学和生物学活性的基础上,通过对银杏内酯的特殊的羟基及其趋向的研究,阐明了这3种内酯化合物分子内和分子间羟基的反应所存在的差异,并将其应用于内酯的分离技术中。此外还通过向分子结构中引入稳定的3H标记(non labile lritium marker)研究从GC转变成GB的途径[12]。但银杏萜内酯的分子立体结构复杂,化学合成途径的技术难度大。
, 百拇医药
3 银杏萜内酯的生物合成研究
3.1 细胞工程研究 近年来国内外生物、生化学者开展了细胞工程及生物合成途径的研究。1991年Carrier等首次肯定了银杏组织培养物中银杏内酯的存在[13]。1993年Huh等报道银杏内酯(GA+GB+GC)在愈伤组织和悬浮细胞中含量分别为0.0026%和0.0047%,而茎尖和内胚起源的根等器官的培养物中银杏内酯含量较高,分别为0.08%和0.03%[14]。1995年Jeon等在用银杏叶诱导的愈伤组织和细胞悬浮培养中检测到了GB,并发现有MS培养基时GB含量最高,而Schenk-Hildebrandt培养基对细胞生长有利[15]。1996年郑玉果在国内首次进行了利用组织培养法生产银杏萜内酯的研究。所 筛选的高产细胞株中GA+GB含量为0.0062%,达到了当时国外报道的最高水平[16]。Laurain 等在1997年用野生型发根农杆菌Agrobacterium rhizogenes A4菌株感染银杏合子胚诱导发根,建立了悬浮细胞培养系,同时用银杏胚囊(雌配子体)作外植体诱导,建立了悬浮培养系,用HPLC测定了GA、GB、GC、GJ和BB的含量。“转化”培养物中次生代谢物含量为0.065%,其中GB为0.0083%;在胚囊起源细胞悬浮培养物含量为0.87%,其中GB为0.16%;“转化”培养物中含有更多的BB,而GA、GB、GC在胚囊起源的培养物中含量更高[17]。1997年孙天恩等利用发根农杆菌的Ri质粒转化银杏叶细胞,得到银杏叶转化发根。初步分析表明,银杏萜内酯的含量为0.04%~0.1%,其GA∶GB∶GC∶BB为8∶11∶1∶22,银杏黄酮的含量为0.06%~1%,并申请了发明专利(专利申请号97109254.4)[18]。1997年Cartayrade等用[14C]CO2、[U-14C]glucose饲喂3月龄的银杏幼苗,研究了GA、GB、GC和BB合成转移与积累的部位,示踪结果显示:催化产生银杏二萜类化合物终产物的所有酶促步骤均在根中,而非叶中;根 同时是银杏内酯与白果内酯合成及积累的部位,而叶只是贮藏部位;银杏二萜类在根与叶之间以源—池方式(source-sink manner)转移[19]。1998年戴均贵在对不同培养基(MS、B5、DCR、P6)、激素(2,4_D、NAA、6_BA)、氮源(NO3、NH4+)和碳源(蔗糖、葡萄糖、果糖)对银杏愈伤组织生长及银杏内酯B形成的影响研究中发现:MS、DCR和P63种培养基对愈伤组织Gb3的生长及GB形成的效果都较好,它们之间不存在显著性差异,而B5培养基的效果较差。2,4-D浓度的增加有利于愈伤组织的生长,当浓度为2.0 mg/L时GB的含量最高;NAA浓度为0.5 mg/L时愈伤组织的生长指数及GB的含量均达到最高;6-BA不利于愈伤组织生长及GB的形成。总氮量保持60mmol不变情况下,NH+4与NO-3之比为1∶2时,GB的产量最高;NO-3有利于GB的形成,当NO-3为60 mmol时GB的含量达到0.018 3%。在蔗糖、葡萄糖和果糖3种碳源中,蔗糖效最佳,且浓度为4%时,愈伤组织生长指数达到3.66,GB的含量达到0.022 3%[20]。1999年陈云龙对银杏幼叶、种胚愈伤组织按文献方法进行诱导,MS固体培养基中含1.0 mg/L NNA、0.1mg/L KT、30g/L蔗糖,调pH至6.0,培养温度(25±1)℃,每周继代1次,续代2代后,用HPLC测得银杏幼叶愈伤组织、种胚愈伤组织中GA的含量分别为0.048、0.012 mg/g[21]。
, 百拇医药
3.2 生物合成研究
关于银杏萜内酯的生物合成途径,早在1971年Nakanishik等用[2-C14]MVA饲喂银杏幼苗,证明了银杏萜内酯经由异戊烯基焦磷酸(IPP)聚合生成香叶基焦磷酸(GGPP)而生成,符合异戊烯法则(Ruzicka, 1953)[22]。Lichtenthaler等证明,银杏中通过几乎完全被胞质和质体隔离的两个彼此不同的生源途径生成IPP,但胞浆和质体中IPP的来源和去路不同:[胞浆途径]→MVA→
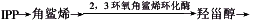 谷甾醇;[质体途径]→IPP→FPP→GGPP→→→银杏内酯和白果内酯。根据上述合成途径,可以设计2,3-环氧角鲨烯环化酶的抑制剂以阻断甾醇生成支路,使由醋酸途径生成的IPP在胞浆大量积累而进入质体,参与银杏内酯和白果内酯生成途径而增加其产量。同时也可用化学合成的2,3-环氧角鲨烯作为2,3-环氧角鲨烯环化酶的竞争性抑制剂实现上述目标。
谷甾醇;[质体途径]→IPP→FPP→GGPP→→→银杏内酯和白果内酯。根据上述合成途径,可以设计2,3-环氧角鲨烯环化酶的抑制剂以阻断甾醇生成支路,使由醋酸途径生成的IPP在胞浆大量积累而进入质体,参与银杏内酯和白果内酯生成途径而增加其产量。同时也可用化学合成的2,3-环氧角鲨烯作为2,3-环氧角鲨烯环化酶的竞争性抑制剂实现上述目标。, http://www.100md.com
关于倍半萜、二萜生物合成前体的研究,Neau等用tetcyclacis和clotrimazole作细胞色素P-450氧化酶的抑制剂,用[14C]示踪证明了银杏内酶和白果内酯的烃类前体是脱氢松香烷(dehydroabitane)[23]。见图3。
由此可知,银杏内酯、白果内酯和其烃类前体在结构上相差悬殊,由该前体到终产

图3 银杏内酯和白果内酯的生物合成途径
A:Sandaraco-Pimarenyl cation;B:脱氢松香烷;C:银杏内酯;D:白果内酯
4 结语
银杏萜内酯是银杏叶中主要活性成分,是一类特异有效的PFA拮抗剂。近年来,国内外学者对萜内酯研究十分活跃,萜内酯在保护中枢神经系统、抗缺血损伤、抗过敏、抗异体移植排斥反应方面具有重要的药理作用。但由于萜内酯迄今尚未发现存在于其他任何植物中,且在银杏叶和根皮中含量极低,仅为万分之几,甚至百万分之几,茎皮及根皮内部组织中则更低,因此银杏萜内酯的药用资源受到限制。近10多年来国内外学者在对银杏萜内酯的化学结构及性质进行深入研究的同时,对其化学元素合成进行了研究,但由于合成工艺复杂,成本相当高,目前仍仅限于实验室研究。细胞生物工程及生物合成途径的研究则取得令人瞩目的成绩,向人们展示了诱人的前景,但目前尚未进入工业化大生产。因此,银杏叶仍是提取银杏萜内酯化合物的主要来源。相信随着人们对银杏研究的进一步深入,银杏萜内酯资源的开发和应用,将会成为下一步研究的热点。
, http://www.100md.com
作者简介:张鹤鸣(1962-),男,医学博士
参考文献:
[1] Kriegstein J. Neuroprotective properties of Ginkgo biloba constituents demonstrated in vivo and vitro [J].Rev Bras Neurol Agosto,1994,30,1 (Suppl):7
[2] 齐之尧,李家玉.银杏叶的药用价值[J].世界林业研究,1994,7(3):92
[3] Maruyama M,Terahara A,Nakanishi K.The Ginkgolides isolation and characterization of the various groups[J].Tetrahedron Lett,1967 (4):299
, http://www.100md.com
[4] Weinges Von Klaus,Bhr Wolfgang. Bilobalid A,ein neues Sespuiterpen mit tert-Butyl-Gruppe aus den Blttern von Ginkgo biloba[J].Leibigs Ann Chem,1969,1724:214
[5] Weinges K, Hepp M, Jaggy H.Chemistry of Ginkgolides Ⅱ:Isolation and structural elucidation of a new ginkgolide [J].Liegbigs Amm Chem,1987(6):521
[6] Steinke B,Muller B,Wanger H.Biological standard of Ginkgo biloba L[J].Planta Medica,1993,59:155
, http://www.100md.com
[7] Weinges K ,Hepp M,Huber-Patz U, et al.10-acety1-1-methoxycarbony1-2,3,14,15,16-pentanorginkgolid A,ein Zwischenprodukt zur Herstellung von Bilobalid [J].Liebigs Ann Chem ,1986:1057
[8] Crimmins M T.Synthetic studies of the ginkgolides:total synthesis of bilobalide [J].J Am Chem Soc,1993,115(8):3146
[9] Corey E J,Kang M C,Desai M,et al. Total synthesis of (±) ginkgolides B[J].J Am Chem,1988,110(2):649
, 百拇医药
[10] Corey E J,Gavai A .Total synthesis of ginkgolides [J].Atetrahedron Lett,1988,29(26):3205
[11] 史玉俊.具有高度抗 PAF 活性而结构较简单的银杏萜内酯 B 同系物[J].国外医药*植物药分册,1990,5(4):176
[12] Corey E J,Reo K,Ghosh A.Intramolecular and intermolecular hydroxy reactivity differences in ginkgolides A,B and C and their chemical applications[J].Tetrahedron Lett,1992,33(46):6955
[13] Carrier D J,Chauret N,Mancini M,et al.Detection of ginkgolide A in Ginkgo biloba cell cultures[J]. Plant Cell Rep,1991,10:256
, http://www.100md.com
[14] Huh H E,John Staba.Ontogenic aspects of ginkgolide production in Ginkgo biloba [J].Planta Med,1993,59:232
[15] Jeon M H,Sung S H,Huh H,et al.Ginkgolide B production in cultured cells derived from Ginkgo biloba L.leaves [J].Plant Cell Rep,1995,14:501
[16] 郑玉果,于荣敏,姚新生,等.银杏愈伤组织培养及银杏内酯测定的研究[J].沈阳药科大学学报,1999,16(1):10
[17] Laurain D ,Guiller J T,Chenieux J C,et al.Production of ginkgolide and bilobalide in transformed and gametophyte derived cell cultures of Ginkgo biloba [J]. Phytochemistry,1997,46(1):127
, 百拇医药
[18] 孙天恩,李根保.银杏发根克隆及其培养技术研究进展[J].中草药,1989,29 (增刊):25
[19] Cartayrade A, Neau E,Sohier C,et al. Ginkgolide and bilobalide biosynthesis in Ginkgo biloba. I: Sites of synthesis ,translocation and accumulation of ginkgolides and bilobalide [J]. Plant Physiol Biochem,1997,35(11)859
[20] 戴均贵,朱蔚华,吴蕴祺,等.不同培养基、激素、碳源和氮源对银杏愈伤组织生长及银杏内酯 B 形成的影响[J].中草药,1998,29 (增刊):63
[21] 陈云龙,徐程,徐礼根,等.HPLC 测定银杏愈伤组织内酯 A 的研究[J].中草药,1999,30(6):45
, 百拇医药
[22] Nakanishi K. Structure of bilobalide a rare tert-buty1 containing sesquiterpenoid related to the C20-ginkgolides [J].J Am Chem soc,1971,93(14):3544
[23] Neau E, Cartayrade A,Balz J P,et al.Ginkgolide and bilobalide biosynthesis in Ginkgo biloba.Ⅱ:Identification of a possible intermediate compound by using inhibitors of cytochrome P-450-dependent oxygenases[J].Plant Physiol Biochem,1997,35(11):869
收稿日期:2000-04-07, 百拇医药