实验性脑缺血再灌流后不同时程热休克蛋白基因表达的变化
作者:孙运娟 孙运芝 王纪佐
单位:(孙运娟300021 天津医科大学第二医院神经内科);王纪佐(300021 天津医科大学第二医院神经内科);孙运芝(莒南县人民医院)
关键词:HSP70;脑缺血;基因表达▲
脑与神经疾病杂志000303
摘 要 为探讨脑缺血再灌流后热休克蛋白(HSP70)基因表达的变化, 采用原位杂交和免疫组化方法检测了脑缺血2h再灌流后不同时程应激蛋白-热休克蛋白(hsp70)mRNA和蛋白表达的变化。 结果显示再灌流后早期即可见hsp70mRNA的蛋白表达增加, 以18~24h阳性染色最强, HSP70阳性细胞主要分布于缺血周围半暗带区, 提示HSP70蛋白表达增加可抵御缺血性脑损伤, 对神经元具有保护作用。
The temporal-spatial expression of HSP70 following middle cerebral artery occlusion in rat.
, http://www.100md.com
Sun Yunjuan Sun yunzhi Wang Jizuo
(department of neurology, the Second Teaching Hospital affiliated to Tianjin Medical University)
Abstract Purpose: To clarify the temporal-spatial expression of HSP70 following transient focal ischemic-reperfusion injury in rat.Methods: The ischemic-reperfusion model was produced by 2-hour of right MCA occlusion in male Wistar rat. The expressions of hsp70 mRNA and protein were examined by in situ hybridyzation and immonohistchemistry respectively. Results: Expression of hsp70 mRNA and protein were enhanced following reperfusion within 48h. Strong singals for hsp 70 mRNA appeared in the dorsal and lateral cortex and striatum-regions and further into preoptic area and alteral hypothalamus. While HSP70 protein immunoreactivity mainty existed in peripheral area of focal ischemic core. Conclusion: Our results suggest that hsp70 mRNA is a marker of neuronal injury and the increase in HSP70 protein may confer resistance to ischemic cerebral injury.
, http://www.100md.com
Key words HSP70 cerebral ischemia gene expression
缺血性脑血管病是常见的神经系统疾病死亡原因之一,具有较高的发病率和患病率,是目前重点防治的一种疾病。因此研究脑缺血再灌流后基因表达变化对了解脑损伤和神经保护机制具有重要的意义[1,3]。虽然以往对短暂性局灶性脑缺血后HSP70表达进行了一些研究,但多采用全脑缺血模型或较短时间(90min以内)局灶性脑缺血模型,而且HSP70表达在脑缺血中的作用尚不完全清楚。因此,本研究应用标准化的局灶性脑缺血(MCAo)模型,分析了脑缺血2h再灌流不同时程hsp70mRNA转录和翻译的变化,以进一步探讨脑缺血再灌流后脑损伤和神经保护机制。
材料与方法
1.局灶性脑缺血模型制备
健康雄性Wistar大鼠45只,体重270~300g,随机分为假手术组和再灌流2h、6h、18h、24h和48h组。根据Nagasawa[1]提出的大脑中动脉(MCA)线栓法并加以改进制作局灶性脑缺血再灌流模型。以大鼠清醒后出现对侧上肢为重的瘫痪及同侧Horner征为模型成功的判断标准。再灌流达到规定时间后,深度麻醉,对部分大鼠迅速开胸暴露心脏,经升主动脉插管,先用100ml肝素生理盐水快速冲洗,随后以4%多聚甲醛磷酸缓冲液(4℃,pH7.4)灌注约1h,然后迅速取脑,浸入上述固定液中24h,再以福尔马林固定,常规制成石蜡切片;部分大鼠快速断头取脑,OCT包埋,置液氮中短暂保存,制作冰冻切片。
, http://www.100md.com
2.免疫组化检测HSP70蛋白
石蜡切片常规脱蜡至水;以新鲜配制的3%H2O2浸泡10min,蒸馏水洗3次;微波抗原修复,蒸馏水洗3次;滴加正常山羊血清,室温下15min,甩去多余液体,不洗;滴加鼠抗HSP70单克隆抗体(浓度1∶100,SantaCruzCo.美国Cat#SC~24),将标本片置湿盒内,4℃过夜(18~20h);次日晨取出,置室温下复温30min,0.01MPBS洗5min×3次;将切片浸入生物素化羊抗鼠IgG中,室温孵育60min,0.01MPBS洗5min×3次;滴加SABC复合物,室温60min,0.01MPBS洗5min×4次;DAB显色5~10min,镜下监视,显色满意后以蒸馏水终止反应,苏木素轻度复染。脱水、透明、封片。阳性染色为胞浆或胞核棕黄色颗粒。阴性对照以PBS或正常山羊血清代替一抗。
3.原位杂交检测hsp70mRNA
, 百拇医药
①探针的制备[4]:包括感受态细菌的制备、细菌转化、扩增;质粒的少量提取、酶切鉴定及质粒大量提取(碱裂解法)、纯化和酶切;然后回收hsp70cNDA片段(聚乙二醇法)并纯化。
②探针标记:操作方法严格按说明书进行(cDNA地高辛标记及检测试剂盒为BoehringerMannheuim公司产品)。然后检测探针标记的产量。
③原位杂交及检测[4]:将冰冻组织切片(12μm厚)预处理后,42℃预杂交2h,每片加50μl杂交液(探针浓度1ng/ml),上盖乙醇处理的Parafilm膜,置于湿盒内42℃杂交18~20h。杂交后充分洗涤,滴加抗地高辛抗体(1∶5000)室温下孵育2h,以BCIP/NBT法显色,亲水性封片剂封片,显微镜下观察。阳性反应为胞核或胞浆紫兰色颗粒。
4.图像分析技术
, 百拇医药
将免疫组化和原位杂交切片染色结果输入图像分析仪,测定阳性染色细胞的光密度并进行统计分析。
5.统计方法
计量资料以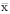 ±s表示,组间比较采用单因素方差分析,以P<0.05作为显著性检验的标准。
±s表示,组间比较采用单因素方差分析,以P<0.05作为显著性检验的标准。
结 果
1.大鼠MCAo后神经功能改变
在缺血前所有大鼠神经功能检查均正常,而MCAo后2h检查时均显示明显的神经功能缺损,表现为向左侧转圈,倾倒及Horner's征,提尾时可见左前肢内收、屈曲。假手术组神经功能正常。
2.HSP70蛋白表达变化
, 百拇医药
在假手术组和正常侧大脑半球无阳性免疫反应细胞,脑缺血再灌流后2~6h可见少量阳性免疫反应细胞,再灌流18h后阳性染色明显增强(P<0.05),以再灌流后1d免疫反应最强,阳性免疫反应细胞主要位于缺血灶的周围,阳性细胞主要为神经元,并可见少量的胶质细胞和毛细血管内皮细胞,缺血中心仅少量阳性染色细胞,主要为血管内皮细胞。HSP70蛋白阳性颗粒主要位于胞浆,也可见少量细胞核染色。
3.hsp70mRNA表达变化
在假手术组和正常侧大脑半球无阳性杂交信号,再灌流后2h在缺血侧背外侧皮层及纹状体外侧部可见少量阳性信号,再灌流6h后上述部位杂交信号明显增强(P<0.05),并扩散至视前区及下丘脑外侧,以再灌流后1d时杂交信号最强,并在背侧海马出现不同程度的阳性染色。再灌流2d时杂交信号明显减弱。
讨 论
大脑中动脉(MCA)是临床上ICVD的易患部位,在脑梗塞患者中,大脑中动脉主干分布区梗塞占82.2%,其中70%有明显的栓子来源,所以对大脑中动脉主干闭塞(MCAo)的研究在脑血管病的研究中占有极其重要的地位[5]。本研究采用线栓法制作局灶性脑缺血模型,在一定程度上模拟了人类大脑中动脉主干栓塞的临床表现和病理变化。因而对研究脑缺血再灌流损害的机制及评价药物的疗效具有重要的意义,并可为临床卒中病人的治疗学提供重要的理论依据。
, 百拇医药
热休克蛋白是一类在进化上高度保守,广泛存在于原核和真核细胞内的因高温、病原体及其它有害因素的刺激而产生的蛋白质。其中HSP70是最保守和最主要的一类,在大多数生物中含量最高,是目前分析的主要伴侣蛋白之一,能够介导细胞内蛋白质的正确装配,保证新合成的蛋白质分子的正常构型,防止在多聚体形成以前,蛋白亚单位出现异常折叠或解聚,陪伴蛋白分子在细胞内转运、跨膜,参与蛋白质的折叠、伸展和多聚复合体的组装,在线粒体及内质网部位等不同的区域内发挥作用;同时还可促进某些变性蛋白的降解和清除、重新激活某些酶的活性,参与调节细胞K+、Na+-ATP酶活性等功能[6,7]。
关于hsp70mRNA转录调控机制,一般认为与热休克转录因子(heatshocktranscriptionfactor,HSTF)激活有关,在非应激状态下,HSF以无活性的单聚多肽形式存在于胞浆内,部分与HSP70结合成复合物。在应激状态下,由于细胞损伤后异常蛋白的增加,HSP与异常蛋白结合,致使游离的HSTF增多,HSTF单体发生同型三聚体构型改变,而获得了DNA结合活性,由胞浆转移到细胞核内,后者与HSP基因启动子TATA盒上游处的HSP元件(heatshockelement,HSE)特异性的结合,从而保证HSP基因的高效转录,进而引起HSP70蛋白合成增加,以清除细胞内的异常蛋白质[6,7]。另外研究分析HSP70的突变可引起HSP的异常高表达,表明野生型HSP70是作为一个负调节物来调节HSP表达。
, 百拇医药
应激状态下如脑缺血,受损细胞内的变性蛋白可诱导HSP70表达,增加神经元对缺血缺氧的耐受能力,以维护细胞的功能和生存。本研究结果显示在假手术组及正常侧大脑半球无hsp70mRNA及蛋白表达,再灌流后2h即可见少量hsp70mRNA及蛋白表达,随再灌流时间的延长,阳性染色进一步增强,hsp70mRNA上调分布范围较广泛,而HSP70蛋白表达以半暗带区为主,后者可能由于缺血中心蛋白合成受抑制有关。提示HSP70蛋白表达增加可抵御缺血性脑损伤,提高细胞的应激能力,hsp70mRNA表达增加可反映神经损伤的程度,本结果与以往国外报道基本一致[8~10]。Lee[8]等在局灶性脑缺血的研究中发现脑缺血80min再灌流4h无HSP70蛋白表达,再灌流后1、3dHSP70蛋白表达位于梗塞周围的半暗带区,非缺血侧及正常神经元无表达。States[9]等应用免疫组化和TUNEL进行双染,发现在HSP70免疫反应阳性神经元内无DNA片段。以上结果提示HSP70免疫反应阳性神经元为可逆性损伤。在局灶性脑缺血2h再灌流模型的研究中发现再灌流后1、2天hsp70mRNA表达增加,且与缺血早期(缺血2h)脑血流减少的程度及后期(3d)组织病理改变呈高度相关,提示hsp70mRNA表达是细胞损伤的标志,并认为在MCAo2h缺血模型中hsp70mRNA表达可作为分子指纹(molecularfinger-print),即根据hsp70mRNA表达的情况指导临近切片其它基因mRNA杂交信号的分析[10]。在短暂性全脑缺血模型的研究中[11,12],HSP70主要在海马区结构完整的可逆性损伤的神经元内表达增加。因此可以认为HSP70表达增加可保护神经元避免继发性损害。
, 百拇医药
总之,短暂缺血再灌流后神经元内的自我保护功能是否受损或能否修复则可能是脑损伤的关键因素,尤其是基因介导的对神经元有保护作用的蛋白质表达可能是存活神经元是否存活的最后通路。许多研究已经证实,细胞内蛋白合成水平是神经元能否存活的指征,也是评价神经保护药物疗效的重要指标。
参 考 文 献
1,Nagasawa, H, Kogure, K, et al. Correlation between cerebral histologic changes in a new model of middle cerebral artery occlusion. Stroke, 1989,20∶1037~1043.
2,Alexis NE, Dietrich WD, Green EJ, et al. Nonocclusive common cariotid artery thrombosis resuits in reversible senseromoter and cognitive behavioral deficits. Stroke 1995,26∶2338~2346.
, http://www.100md.com
3,Belayev. L, et al. Middle cerebral artery occlusion in the rat by intraluminal suture. Stroke 1996,27(9)∶1616~1623.
4,姜泊等主编. 分子生物学常用实验方法. 北京: 人民卫生出版社, 1996.2.
5,Tsuchidate R. et al. Regional cerebral blood flow during and after 2 hour middie cerebral artery occlusion in the rat. J Cere Blood Flow Metab, 1997,17∶1066~1073.
6,Bukau B, Horwich Q. The Hsp70 and Hsp60 Chaperone machines. Cell, 1998,92∶351~366.
, 百拇医药
7,Voisine C, et al. The protein import motor of mitochondria: unfolding and rtapping of preproteins are distinct and separable functions of matrix Hsp 70. Cell, 1999,97∶565~574.
8,Lee TS, Kato H, Chen ST et al. Expression of nerve growth factor and trk A after transient focal cerebral ischemia in rats. Stroke, 1998,29∶1687~1697.
9,States B.A. Honkaniemi J, Weristein P.R. et al. DNA pragmentation and HSP protein induction in hippocampus and cortex occurs in separate neurons following permanent middle cerebral artery occusions. J. Cereb Blood Flow metab. 1996,16∶1165~1175.
, http://www.100md.com
10,Schmidt KR, Zhao W Truettner J. et al. Pixel-based image analysis of HSP70, GADD45 and MAP2 mRNA expression after focal cerebral ischemia: hemodynamic and histological correlates. Brain Res Mol Brain Res. 1998,10, 63(1)∶79~97.
11,Katayama T, Imaizumi K, Tsuda M. et al. Expression of an ADP-ribosylation factor like gene, ARF4L, is induced after transient forebrain ischemia in the gerbil. Brain Res Mol Brain Res. 1998,56(1~2)∶66~75.
12,Tomimoto H, Takemoto O, Akiguchi I, et al. Immunoelectron microscopic study of c-Fos, c-Jun and heat shock protein after transient cerebral ischemia in gerbils. Acta Neuropathol Berl. 1999,97(1)∶22~30.
(2000-01-26 收稿), 百拇医药
单位:(孙运娟300021 天津医科大学第二医院神经内科);王纪佐(300021 天津医科大学第二医院神经内科);孙运芝(莒南县人民医院)
关键词:HSP70;脑缺血;基因表达▲
脑与神经疾病杂志000303
摘 要 为探讨脑缺血再灌流后热休克蛋白(HSP70)基因表达的变化, 采用原位杂交和免疫组化方法检测了脑缺血2h再灌流后不同时程应激蛋白-热休克蛋白(hsp70)mRNA和蛋白表达的变化。 结果显示再灌流后早期即可见hsp70mRNA的蛋白表达增加, 以18~24h阳性染色最强, HSP70阳性细胞主要分布于缺血周围半暗带区, 提示HSP70蛋白表达增加可抵御缺血性脑损伤, 对神经元具有保护作用。
The temporal-spatial expression of HSP70 following middle cerebral artery occlusion in rat.
, http://www.100md.com
Sun Yunjuan Sun yunzhi Wang Jizuo
(department of neurology, the Second Teaching Hospital affiliated to Tianjin Medical University)
Abstract Purpose: To clarify the temporal-spatial expression of HSP70 following transient focal ischemic-reperfusion injury in rat.Methods: The ischemic-reperfusion model was produced by 2-hour of right MCA occlusion in male Wistar rat. The expressions of hsp70 mRNA and protein were examined by in situ hybridyzation and immonohistchemistry respectively. Results: Expression of hsp70 mRNA and protein were enhanced following reperfusion within 48h. Strong singals for hsp 70 mRNA appeared in the dorsal and lateral cortex and striatum-regions and further into preoptic area and alteral hypothalamus. While HSP70 protein immunoreactivity mainty existed in peripheral area of focal ischemic core. Conclusion: Our results suggest that hsp70 mRNA is a marker of neuronal injury and the increase in HSP70 protein may confer resistance to ischemic cerebral injury.
, http://www.100md.com
Key words HSP70 cerebral ischemia gene expression
缺血性脑血管病是常见的神经系统疾病死亡原因之一,具有较高的发病率和患病率,是目前重点防治的一种疾病。因此研究脑缺血再灌流后基因表达变化对了解脑损伤和神经保护机制具有重要的意义[1,3]。虽然以往对短暂性局灶性脑缺血后HSP70表达进行了一些研究,但多采用全脑缺血模型或较短时间(90min以内)局灶性脑缺血模型,而且HSP70表达在脑缺血中的作用尚不完全清楚。因此,本研究应用标准化的局灶性脑缺血(MCAo)模型,分析了脑缺血2h再灌流不同时程hsp70mRNA转录和翻译的变化,以进一步探讨脑缺血再灌流后脑损伤和神经保护机制。
材料与方法
1.局灶性脑缺血模型制备
健康雄性Wistar大鼠45只,体重270~300g,随机分为假手术组和再灌流2h、6h、18h、24h和48h组。根据Nagasawa[1]提出的大脑中动脉(MCA)线栓法并加以改进制作局灶性脑缺血再灌流模型。以大鼠清醒后出现对侧上肢为重的瘫痪及同侧Horner征为模型成功的判断标准。再灌流达到规定时间后,深度麻醉,对部分大鼠迅速开胸暴露心脏,经升主动脉插管,先用100ml肝素生理盐水快速冲洗,随后以4%多聚甲醛磷酸缓冲液(4℃,pH7.4)灌注约1h,然后迅速取脑,浸入上述固定液中24h,再以福尔马林固定,常规制成石蜡切片;部分大鼠快速断头取脑,OCT包埋,置液氮中短暂保存,制作冰冻切片。
, http://www.100md.com
2.免疫组化检测HSP70蛋白
石蜡切片常规脱蜡至水;以新鲜配制的3%H2O2浸泡10min,蒸馏水洗3次;微波抗原修复,蒸馏水洗3次;滴加正常山羊血清,室温下15min,甩去多余液体,不洗;滴加鼠抗HSP70单克隆抗体(浓度1∶100,SantaCruzCo.美国Cat#SC~24),将标本片置湿盒内,4℃过夜(18~20h);次日晨取出,置室温下复温30min,0.01MPBS洗5min×3次;将切片浸入生物素化羊抗鼠IgG中,室温孵育60min,0.01MPBS洗5min×3次;滴加SABC复合物,室温60min,0.01MPBS洗5min×4次;DAB显色5~10min,镜下监视,显色满意后以蒸馏水终止反应,苏木素轻度复染。脱水、透明、封片。阳性染色为胞浆或胞核棕黄色颗粒。阴性对照以PBS或正常山羊血清代替一抗。
3.原位杂交检测hsp70mRNA
, 百拇医药
①探针的制备[4]:包括感受态细菌的制备、细菌转化、扩增;质粒的少量提取、酶切鉴定及质粒大量提取(碱裂解法)、纯化和酶切;然后回收hsp70cNDA片段(聚乙二醇法)并纯化。
②探针标记:操作方法严格按说明书进行(cDNA地高辛标记及检测试剂盒为BoehringerMannheuim公司产品)。然后检测探针标记的产量。
③原位杂交及检测[4]:将冰冻组织切片(12μm厚)预处理后,42℃预杂交2h,每片加50μl杂交液(探针浓度1ng/ml),上盖乙醇处理的Parafilm膜,置于湿盒内42℃杂交18~20h。杂交后充分洗涤,滴加抗地高辛抗体(1∶5000)室温下孵育2h,以BCIP/NBT法显色,亲水性封片剂封片,显微镜下观察。阳性反应为胞核或胞浆紫兰色颗粒。
4.图像分析技术
, 百拇医药
将免疫组化和原位杂交切片染色结果输入图像分析仪,测定阳性染色细胞的光密度并进行统计分析。
5.统计方法
计量资料以
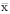 ±s表示,组间比较采用单因素方差分析,以P<0.05作为显著性检验的标准。
±s表示,组间比较采用单因素方差分析,以P<0.05作为显著性检验的标准。结 果
1.大鼠MCAo后神经功能改变
在缺血前所有大鼠神经功能检查均正常,而MCAo后2h检查时均显示明显的神经功能缺损,表现为向左侧转圈,倾倒及Horner's征,提尾时可见左前肢内收、屈曲。假手术组神经功能正常。
2.HSP70蛋白表达变化
, 百拇医药
在假手术组和正常侧大脑半球无阳性免疫反应细胞,脑缺血再灌流后2~6h可见少量阳性免疫反应细胞,再灌流18h后阳性染色明显增强(P<0.05),以再灌流后1d免疫反应最强,阳性免疫反应细胞主要位于缺血灶的周围,阳性细胞主要为神经元,并可见少量的胶质细胞和毛细血管内皮细胞,缺血中心仅少量阳性染色细胞,主要为血管内皮细胞。HSP70蛋白阳性颗粒主要位于胞浆,也可见少量细胞核染色。
3.hsp70mRNA表达变化
在假手术组和正常侧大脑半球无阳性杂交信号,再灌流后2h在缺血侧背外侧皮层及纹状体外侧部可见少量阳性信号,再灌流6h后上述部位杂交信号明显增强(P<0.05),并扩散至视前区及下丘脑外侧,以再灌流后1d时杂交信号最强,并在背侧海马出现不同程度的阳性染色。再灌流2d时杂交信号明显减弱。
讨 论
大脑中动脉(MCA)是临床上ICVD的易患部位,在脑梗塞患者中,大脑中动脉主干分布区梗塞占82.2%,其中70%有明显的栓子来源,所以对大脑中动脉主干闭塞(MCAo)的研究在脑血管病的研究中占有极其重要的地位[5]。本研究采用线栓法制作局灶性脑缺血模型,在一定程度上模拟了人类大脑中动脉主干栓塞的临床表现和病理变化。因而对研究脑缺血再灌流损害的机制及评价药物的疗效具有重要的意义,并可为临床卒中病人的治疗学提供重要的理论依据。
, 百拇医药
热休克蛋白是一类在进化上高度保守,广泛存在于原核和真核细胞内的因高温、病原体及其它有害因素的刺激而产生的蛋白质。其中HSP70是最保守和最主要的一类,在大多数生物中含量最高,是目前分析的主要伴侣蛋白之一,能够介导细胞内蛋白质的正确装配,保证新合成的蛋白质分子的正常构型,防止在多聚体形成以前,蛋白亚单位出现异常折叠或解聚,陪伴蛋白分子在细胞内转运、跨膜,参与蛋白质的折叠、伸展和多聚复合体的组装,在线粒体及内质网部位等不同的区域内发挥作用;同时还可促进某些变性蛋白的降解和清除、重新激活某些酶的活性,参与调节细胞K+、Na+-ATP酶活性等功能[6,7]。
关于hsp70mRNA转录调控机制,一般认为与热休克转录因子(heatshocktranscriptionfactor,HSTF)激活有关,在非应激状态下,HSF以无活性的单聚多肽形式存在于胞浆内,部分与HSP70结合成复合物。在应激状态下,由于细胞损伤后异常蛋白的增加,HSP与异常蛋白结合,致使游离的HSTF增多,HSTF单体发生同型三聚体构型改变,而获得了DNA结合活性,由胞浆转移到细胞核内,后者与HSP基因启动子TATA盒上游处的HSP元件(heatshockelement,HSE)特异性的结合,从而保证HSP基因的高效转录,进而引起HSP70蛋白合成增加,以清除细胞内的异常蛋白质[6,7]。另外研究分析HSP70的突变可引起HSP的异常高表达,表明野生型HSP70是作为一个负调节物来调节HSP表达。
, 百拇医药
应激状态下如脑缺血,受损细胞内的变性蛋白可诱导HSP70表达,增加神经元对缺血缺氧的耐受能力,以维护细胞的功能和生存。本研究结果显示在假手术组及正常侧大脑半球无hsp70mRNA及蛋白表达,再灌流后2h即可见少量hsp70mRNA及蛋白表达,随再灌流时间的延长,阳性染色进一步增强,hsp70mRNA上调分布范围较广泛,而HSP70蛋白表达以半暗带区为主,后者可能由于缺血中心蛋白合成受抑制有关。提示HSP70蛋白表达增加可抵御缺血性脑损伤,提高细胞的应激能力,hsp70mRNA表达增加可反映神经损伤的程度,本结果与以往国外报道基本一致[8~10]。Lee[8]等在局灶性脑缺血的研究中发现脑缺血80min再灌流4h无HSP70蛋白表达,再灌流后1、3dHSP70蛋白表达位于梗塞周围的半暗带区,非缺血侧及正常神经元无表达。States[9]等应用免疫组化和TUNEL进行双染,发现在HSP70免疫反应阳性神经元内无DNA片段。以上结果提示HSP70免疫反应阳性神经元为可逆性损伤。在局灶性脑缺血2h再灌流模型的研究中发现再灌流后1、2天hsp70mRNA表达增加,且与缺血早期(缺血2h)脑血流减少的程度及后期(3d)组织病理改变呈高度相关,提示hsp70mRNA表达是细胞损伤的标志,并认为在MCAo2h缺血模型中hsp70mRNA表达可作为分子指纹(molecularfinger-print),即根据hsp70mRNA表达的情况指导临近切片其它基因mRNA杂交信号的分析[10]。在短暂性全脑缺血模型的研究中[11,12],HSP70主要在海马区结构完整的可逆性损伤的神经元内表达增加。因此可以认为HSP70表达增加可保护神经元避免继发性损害。
, 百拇医药
总之,短暂缺血再灌流后神经元内的自我保护功能是否受损或能否修复则可能是脑损伤的关键因素,尤其是基因介导的对神经元有保护作用的蛋白质表达可能是存活神经元是否存活的最后通路。许多研究已经证实,细胞内蛋白合成水平是神经元能否存活的指征,也是评价神经保护药物疗效的重要指标。
参 考 文 献
1,Nagasawa, H, Kogure, K, et al. Correlation between cerebral histologic changes in a new model of middle cerebral artery occlusion. Stroke, 1989,20∶1037~1043.
2,Alexis NE, Dietrich WD, Green EJ, et al. Nonocclusive common cariotid artery thrombosis resuits in reversible senseromoter and cognitive behavioral deficits. Stroke 1995,26∶2338~2346.
, http://www.100md.com
3,Belayev. L, et al. Middle cerebral artery occlusion in the rat by intraluminal suture. Stroke 1996,27(9)∶1616~1623.
4,姜泊等主编. 分子生物学常用实验方法. 北京: 人民卫生出版社, 1996.2.
5,Tsuchidate R. et al. Regional cerebral blood flow during and after 2 hour middie cerebral artery occlusion in the rat. J Cere Blood Flow Metab, 1997,17∶1066~1073.
6,Bukau B, Horwich Q. The Hsp70 and Hsp60 Chaperone machines. Cell, 1998,92∶351~366.
, 百拇医药
7,Voisine C, et al. The protein import motor of mitochondria: unfolding and rtapping of preproteins are distinct and separable functions of matrix Hsp 70. Cell, 1999,97∶565~574.
8,Lee TS, Kato H, Chen ST et al. Expression of nerve growth factor and trk A after transient focal cerebral ischemia in rats. Stroke, 1998,29∶1687~1697.
9,States B.A. Honkaniemi J, Weristein P.R. et al. DNA pragmentation and HSP protein induction in hippocampus and cortex occurs in separate neurons following permanent middle cerebral artery occusions. J. Cereb Blood Flow metab. 1996,16∶1165~1175.
, http://www.100md.com
10,Schmidt KR, Zhao W Truettner J. et al. Pixel-based image analysis of HSP70, GADD45 and MAP2 mRNA expression after focal cerebral ischemia: hemodynamic and histological correlates. Brain Res Mol Brain Res. 1998,10, 63(1)∶79~97.
11,Katayama T, Imaizumi K, Tsuda M. et al. Expression of an ADP-ribosylation factor like gene, ARF4L, is induced after transient forebrain ischemia in the gerbil. Brain Res Mol Brain Res. 1998,56(1~2)∶66~75.
12,Tomimoto H, Takemoto O, Akiguchi I, et al. Immunoelectron microscopic study of c-Fos, c-Jun and heat shock protein after transient cerebral ischemia in gerbils. Acta Neuropathol Berl. 1999,97(1)∶22~30.
(2000-01-26 收稿), 百拇医药