细菌内同源重组法高效制备含CD、TK融合自杀基因重组体腺病毒
作者:魏道严 糜军 陈诗书
单位:魏道严 糜军 陈诗书(上海第二医科大学人类基因治疗研究中心,上海200025)
关键词:肿瘤;基因治疗;腺病毒载体;细菌
癌症000502
【摘要】目的:采用细菌内同源重组法高效制备含CD、TK融合自杀基因重组体腺病毒。方法:CD、TK融合基因CDglyTK自载体pWZLneoCDglyTK中切出,亚克隆至腺病毒穿梭质粒中,形成转移质粒pAdtrackCMV-CDglyTK,将之PmeI酶切线性化后与腺病毒基因组质粒pAdeasy-1共转化BJ5183菌,抽提重组体腺病毒基因组质粒DNA,PacI酶切后转染293细胞包装成腺病毒颗粒,采用PCR方法对重组体腺病毒进行鉴定,利用报告GFP基因对病毒滴度和感染效率进行测定,Western Blot检测感染腺病毒的肿瘤细胞中有无目的基因的表达。结果:由pAdTrack-CMV-CDglyTK和pAdeasy-1共转化BJ5183菌16~20h后,可获得30%左右的阳性重组体细菌克隆,由重组体克隆质粒DNA转染293细胞包装产生的重组体腺病毒,经PCR检测表明已含有目的基因,且无复制能力腺病毒的存在。纯化所得腺病毒滴度约为8×1012pfu/L,当MOI=100时,腺病毒感染HepG1细胞的效率>75%,Western Blot证实在感染重组体腺病毒的细胞中有相应基因产物的表达。结论:细菌内同源重组法是一种高效、简便、快捷的重组体腺病毒载体制备方法。所制备的Ad-CDglyTK在体外能有效表达相应的基因产物,为今后的深入研究奠定了基础。
, http://www.100md.com
中图分类号:R735.5文献标识码:A文章编号:1000-467X(2000)05-0399-05
High efficient generation of recombinant adenovirus containing CD、TK fusion gene by using a method of homologous recombination in bacteria
WEI Dao-yan, MI Jun, CHEN Shi-shu
(Research Center for Human Gene Therapy, Shanghai Second Medical University, Shanghai 200025, P.R.China)
【 Abstract】 Objective: To generate recombinant adenovirus (Ad) by using a novel and high efficient method of homologous recombination in bacteria with CDglyTK as target gene. Methods: CDglyTK gene was liberated from plasmid of pWZLneoCDglyTK and subcloned into shuttle plasmid and formed transfer plasmid of pAdTrackCMV-CDglyTK. Then it was linealized with PmeI and cotransformed into BJ5183 bacterial cells with adenovirus genomic DNA plasmid of pAdeasy-1. The identified recombinant adenovirus plasmid DNA was digested with PacI and transfected to 293 cells to package recombinant adenovirus particles. The PCR technique was used to detect target gene and replication-competent Ad (RCA) contamination. The titre and its infection rate of the recombinant Ad were measured with the aid of GFP expression. Western Blot technique was used to analyze the target gene expression in infected tumor cells. Results: There were over 30% positive recombinant bacterial clones after co-transformation of BJ5183 bacterial cells with pAdTrack-CMV-CDglyTK and pAdeasy-1. Recombinant adenovirus particles were produced after 293 cells transfected with recombinant Ad genomic plasmid DNA digested with PacI, then they were further amplified in 293 cells. PCR test indicated that the recombinant Ad contained the insert of CDglyTK gene and there was no contamination of RCA in high-titer viral stocks. The titre of purified Ad was 8× 1012 pfu/L, and more than 75% HepG1 cells were infected with Ad-CDglyTK adenoviruses when MOI reached 100. Meanwhile, protein product of CDglyTK gene was detected in the infected tumor cells. Conclusion: The method of homologous recombination in bacteria is a conve-nient and high efficient method to prepare recombinant Adenovirus, and the prepared adenoviruses can effectively madiate target gene expression in infected tumor cells, thus paves a sound foundation for further study.
, http://www.100md.com
Key words: Neoplasms;Cancer gene therapy; Adenovirus vector; Bacteria
恶性肿瘤的基因治疗是近年来的研究热点,高效基因转移载体和合适目的基因的选择是影响疗效的关键因素。由于重组腺病毒载体介导基因转移效率高,感染细胞谱广、病毒滴度高、易于浓缩和贮存等特点而成为肿瘤基因治疗临床试验的常用载体,当以invivo为基因转移途径,腺病毒载体则为病毒性载体中的首选[1]。但现行常用的细胞内同源重组腺病毒载体制备方法存在着成功率低、工作量大、实验周期长等缺陷,给研究工作带来了很大的不便。在目前众多的临床肿瘤基因治疗研究方案中,自杀基因是选用较多的一类目的基因。由于肿瘤病因复杂、类型繁多,加之肿瘤又存在明显的异质性,单一基因治疗效果较差,多基因联合治疗是今后研究的方向[2]。为此,本研究利用一种新型、高效的细菌内重源重组腺病毒制备方法,构建出同时含大肠杆菌胞嘧啶脱氨酶(cytosine deaminase,CD)基因和I型单纯疱疹病毒胸苷激酶(thymidine kinase,TK)基因的融合自杀基因重组腺病毒载体Ad-CDglyTK,其能在感染的肿瘤细胞中表达出相应的蛋白产物,从而为今后的深入研究奠定了基础。
, http://www.100md.com
1材料与方法
1.1材料
293细胞引自ATCC,HepG1肝癌细胞株为本室传代培养。BJ5183菌株、穿梭质粒pAdtrack-CMV、腺病毒基因组质粒pAdeasy-1由JohnHopkins肿瘤研究中心的Tong-chuanHe博士惠赠(质粒结构见图1)。含CD、TK融合基因的逆转录病毒载体pWZLneoCDglyTK由Henry Fork Health System的Rogulski博士惠赠。兔抗CD的多克隆抗体由Heidelberg大学Hacck博士惠赠惠赠,羊抗兔IgG-AP购自华美生物工程公司。LipofectAMINE,小牛血清、Opti-MEM、MEM及DMEM培养基为Gibco公司产品。
图1 pAdTrack-CMV和pAdeasy-1质粒结构示意图
, http://www.100md.com
1.2方法
1.2.1细胞培养:293细胞用含10%小牛血清的MEM培养基在37℃,5%的CO2培养,HepG1细胞用10%的DMEM培养基培养。
1.2.2细菌感受态的制备、质粒提取、纯化、酶切、连接及细菌转化等参见Sambrook等[3]方法。
1.2.3重组体腺病毒载体的构建:构建流程(见图2)。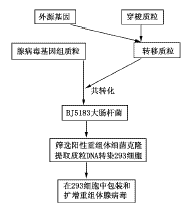
图2重组腺病毒载体构建流程示意图
1.2.3.1转移质粒的构建:目的基因CDglyTK自pWZLneoCDglyTK质粒中经EcoRI和BamHI部分酶切后,回收2.5kb的片段,亚克隆至pcDNA3质粒中,pcDNA3-CDglyTK质粒经XbaI+KpnI酶切,回收2.5kb的目的基因片段,插入至经同样酶切的穿梭质粒pAdtrack-CMV中,构建成转移质粒pAdtrack-CMV-CDglyTK,经酶切鉴定正确后,抽提质粒DNA备用。
, 百拇医药
1.2.3.2重组体腺病毒质粒载体的构建及鉴定:取0.5~1.0μgpAdTrackCMV-CDglyTKDNA,PmeI酶切后与0.1μg的pAdeasy-1质粒混匀,加至感受态菌BJ5183中,行电穿孔法质粒细菌转化。小量抽提转化克隆菌质粒DNA,根据琼脂糖电泳电泳质粒大小,选择可疑重组体腺病毒质粒DNA,经PacI、XbaI+KpnI酶切鉴定正确后,抽提重组体腺病毒质粒pAdeasy-CDglyTKDNA备用。
1.2.3.3重组体腺病毒的包装、扩增和纯化:重组体腺病毒质粒DNA经PacI酶切后采用LipofecTAMINE介导转染293细胞。于转染后不同时间在荧光显微镜下观察GFP表达状况,了解腺病毒包装过程。待有较明显的病毒克隆斑或蚀斑形成后,将293细胞自培养瓶内刮下,-70℃/+37℃反复冻融3次裂解细胞,离心取含病毒的上清,重新感染293细胞大量扩增病毒。病毒的纯化参照Hitt[4]等的方法。
1.2.4PCR对重组体腺病毒Ad-CDglyTK的鉴定:自高滴度病毒贮存液中提取腺病毒基组DNA作为模板,分别用可扩增目的基因CDglyTK和扩增腺病毒E1区的二对引物进行PCR反应,对腺病毒进行鉴定。扩增CDglyTK基因的引物:
, http://www.100md.com
上游引物:5'-GCGCGTTAAAGAGATGCTGGAG-3'
下游引物:5'-ATGGCGGTCGAAGATGAGGGTGA-3'
扩增E1区的引物:
上游引物:5'-TCGATCTTACCTTGCCACGC
下游引物:5'-GAGTCACAGCTATCCGTAGAC
1.2.5重组体腺病毒滴度及感染效率的测定:将浓缩后的病毒贮存液作不同比例的稀释,取400μl稀释液加至293细胞培养瓶中,放置37℃吸附30分钟,换新鲜培养基继续培养18~24h,于荧光显微镜下计数GFP阳性细胞数,按下列公式计算病毒滴度:
, http://www.100md.com
病毒感染效率测定:HepG1细胞按2×105细胞/孔接种于6孔板中,用0.1、1、10、100m.o.i(multiplicityofinfection)的腺病毒感染,48小时后在荧光显微镜下计数GFP阳性细胞百分率。
1.2.6重组体腺病毒的体外表达:对数生长期HepG1肿瘤细胞,用Ad-CDglyTK感染(m.o.i为50),72h后提取细胞蛋白,WesternBlot检测分析CDglyTK基因表达(方法参见文献[3])。
2结果
2.1转移质粒的构建
目的基因CDglyTK自载体pWZLnerCDglyTK中切下,经过一次亚克隆,被插入pAdtrackCMV中,形成转移质粒pAdtrackCMV-CDglyTK,经酶切鉴定正确(见图3)。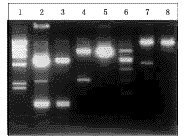
, 百拇医药
图3构建质粒载体的限制性内切酶解图谱
1.λ-HindIIIDNAMarker.
2.pWZLneoCDglyTK(EcoRI/partialBamHI).
3.pcDNA3CDglyTK(EcoRI/BamHI).
4.pAdTrackCMV-CDglyTK(XbaI/KpnI).
5.pAdTrackCMV(XbaI).
6.pAdeasy-CDglyTK(XbaI/KpnI).
7pAdeasy-CDglyTK(PacI).
8.pAdeasy-1(PacI)
, 百拇医药
2.2重组体腺病毒质粒载体构建及鉴定
转移质粒和pAdeasy-1共转化BJ5183细菌后,含有重组质粒的细菌可在含卡那霉素的培养基中生长形成克隆。挑取转化克隆,小量抽提质粒DNA,直接琼脂糖电泳,根据质粒大小作第一轮初筛;用PacI酶切,重组体质粒可出现一大于20kb的大片段和4.5kb的特征性小带而得以鉴定,再用XbaI+KpnI酶切可见一大小与插入的目的基因相对应的约2.5kb的条带(见图3)。
2.3重组体腺病毒的包装过程
线性化的pAdeasy-CDglyTKDNA经Lipofe-ctAMINE介导转染293细胞48小时后,在荧光显微镜下可见约10%左右的293细胞有GFP的表达。至转染后5~10天左右,大多数细胞的GFP荧光逐渐消失,而在有些局部的荧光斑点数增多,荧光增强,表明包装病毒的形成和扩增,而此时在普通的相差显微镜下难以判断病毒的包装是否形成。随后荧光斑点扩大,并形成明显的蚀斑,293细胞出现固缩、脱落、裂介等明显的病理现象(见图4)。

, 百拇医药
图4线性化pAdeasy-CDglyTKDNA转染293细胞后病毒包装过程
A:转染后第6天,见局部病毒克隆斑形成。B:转染后第10天,病毒克隆斑逐渐扩大,克隆斑中央293细胞因病变固缩,脱落,形成蚀斑。C:转染后第15天,局部细胞已全部固缩、脱落。
2.4重组体腺病毒的鉴定
PCR反应结果显示,用扩增CDglyTK引物进行的PCR反应,出现预期大小的合适条带(图5),表明CDglyTK基因已克隆入重组体腺病毒基因组中;而以扩增腺病毒E1区的引物未能扩增出相应的条带,以含E1区的JM17质粒DNA为模板则扩增出相应的条带,表明用此法制备的重组病毒浓缩贮存液中无具复制能力的腺病毒污染。
图5PCR鉴定重组腺病毒产物电泳图
, http://www.100md.com
A:扩增目的基因的引物:1.阴性对照,2.重组腺病毒基因组DNA,3.123DNA分子量标记。B:扩增E1区序列引物:1.重组腺病毒基因组DNA,2.pJM17DNA,3.123DNA分子量标记。
2.5重组体腺病毒滴度及感染效率的测定
根据GFP计数法测得的腺病毒滴度为8×1012pfu/L。采用不同MOI感染HepG1细胞,当MOI为1时,仅少数细胞有荧光;当MOI为100时,约75%以上的细胞GFP表达阳性(图6)。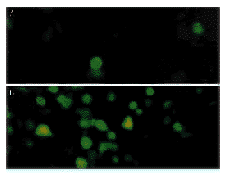
图6重组体腺病毒体外感染效率
A.当MOI为1时,仅少数细胞表达GFP。
B.当MOI为100时,约大于75%细胞表达GFP。×100
, http://www.100md.com
2.6重组体腺病毒介导基因体外表达
WesternBlot分析发现,在分子量约88KD处有特异性蛋白条带,(见图7),其大小与CDglyTK基因产物的相吻合[5],证明重组体腺病毒能有效介导目的基因在肿瘤细胞内的表达。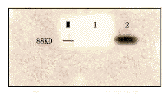
图7WesternBlot检测结果
M:蛋白质分子量标志;1:对照样品;2:实验组样品
3 讨论
CD/5-FC、TK/GCV自杀基因治疗系统是经研究证实效果较为确切的两种自杀基因,其中TK/GCV用于脑胶质瘤的治疗已进入临床Ⅲ期研究阶段。然而,随着研究的深入人们发现,不同类型的肿瘤对两种自杀基因治疗系统的敏感性不同,如胃肠系统的肿瘤CD/5-FC基因治疗系统较为敏感,而脑胶质瘤等则对TK/GCV自杀基因治疗系统敏感[5,6],由此限制了单一自杀基因治疗系统临床适用范围。其次,在单用CD/5-FC或TK/GCV自杀基因治疗系统治疗后复发的肿瘤细胞群体中,发现有相当数量的细胞对相应前药产生了抗性[7]。Uckert等[8]将两种自杀基因联合,既克服单一自杀基因的上述缺陷,又由于两者之间存在明显的协同效应,疗效得到了进一步提高,唯需同时构建两种基因转移载体是其不足。为此,本研究中我们选择具有双功能的CD、TK融合基因作为目的基因[5],再用腺病毒介导基因转移,可能是一种较为简便、有效的途径。
, 百拇医药
传统的细胞内同源重组腺病毒载体制备方法是由Bett[9]等建立。其是先将目的基因亚克隆至穿梭质粒中构建成转移质粒,再与腺病毒基因组质粒共转染293细胞,两质粒借所带的部分同源序列在293细胞内发生同源重组而形成重组体,并进一步包装成重组腺病毒颗粒。然而该方法涉及的步骤及环节较多,成功率较低、工作量大,实验周期长。其主要原因有:(1)细胞内质粒共转染效率较低,同源重组效率更低。而该种制备方法要求两种质粒的共转染及同源重组必须同时发生在293细胞内,才有可能形成重组体并包装成病毒。(2)包装形成的重组体病毒克隆须经过多轮筛选、鉴定和纯化,费时费力。(3)293细胞既是发生同源重组的场所,又是病毒包装的场所,293细胞的状态对实验能否成功影响很大。该种方法通常要求293细胞的培养传代次数不超过45代,从而给实验增加了难度;重复引进传代次数较低的293细胞既费时,代价也相当昂贵。随后Miyaks等[10]建立了COS-TPC制备方法,其基本原理与Bett的方法相似,只是在腺病毒基因组DNA5’末端共价结合末端蛋白复合物,通过提高转染效率使得同源重组率有了一定的提高,但方法学上并无根本性突破。本文采用新型的细菌内同源重组法[11]来制备重组腺病毒载体。由构建流程图(图1)可见,本法与细胞内同源重组法的根本不同之处在于,两种质粒共转染和同源重组在均在细菌内完成,继用经筛选鉴定的重组体克隆质粒DNA转染293细胞,包装和扩增病毒。其突出优点是:(1)成功率高。目前质粒转化细菌技术成熟、效率高,且细菌繁殖快,同源重组能力强,因而从根本克服细胞内同源重组率低的缺陷。(2)方法简便、快捷、实验周期短。重组体腺病毒载体制备的关键环节是同源重组和对重组体进行的筛选、鉴定。细菌内同源重组法的这一过程在细菌内完成。由于从质粒转化细菌到转化重组克隆的出现仅需12~20h;对细菌内质粒DNA的抽提、酶切鉴定远较对细胞内DNA的类似操作方便、容易。用经鉴定正确的重组体腺病毒质粒DNA转染293细胞,包装产生的腺病毒可省却细胞内同源重组法对包装出的病毒必须进行的多轮费时、费力的筛选鉴定。此外,由于在腺病毒骨架中含有的GFP报告基因,非常便于我们监测病毒包装成功与否、检测病毒滴度及感染效率等。如在重组体质粒转染293后的5~7天便可知道病毒是否被成功包装;病毒滴度的测定也仅需24h,这些均大大缩短了实验周期。(3)对293细胞的传代次数要求不太严格,如我们曾用传代次数约50余代的293细胞也包装出重组体腺病毒。经对纯化的重组体腺病毒进行的分析鉴定表明,重组体腺病毒基因组中已含有目的基因;重组体腺病毒能有效感染肿瘤细胞,并表达相应的蛋白产物,说明重组体病毒制备是成功的(其体内、外抗肿瘤作用另文报告)。因此,细菌内同源重组法是一种快速、高效、简便、可行的重组体腺病毒载体制备方法,值得进一步推广应用。
, 百拇医药
基金项目:国家“863”高技术计划基金(863-102-452)和国家自然科学基金(3970440)资助
[参考文献]
1,陈诗书.基因治疗研究进展[J].胃肠病学杂志,1999,4(1):36~40.
2,Paillard F. Cancer cells under the fire of combined therapies [J]. Hum Gene Ther, 1998,9: 1259~ 1260.
3,Sambrook J, Fritsch EF, Maniatis T. Molecular cloning [M]. 2nd ed. New York: Cold Spring Harbor Laboratory Press,1989:852~ 898.
, http://www.100md.com
4,Hitt M, Bett A, Prevec L, et al. Construction and propagation of human adenovirus vectors: In Cell Biology: A Laboratory Handbook [M]. Academic Press, 1998: 550~ 512.
5,Rogulski KR, Kim JH, Kim SH, et al. Glioma cell transduced with Echerichia coli CD/HSV-1 TK fusion gene exhibit enhanced metabolic suicide and radiosensitivity [J]. Hum Gene Ther, 1997, 8: 73~ 85.
6,Trinh QT, Austin EA, Murray DM, et al. Enzyme/prodrug gene therapy: comparison of cytosine deaminase/5-flurocytosone versus thymidine kinase/ganciclovir enzyme/prodrug systems in a human colorectal carcinoma cell line [J]. Cancer Res, 1995, 55: 4808~ 4812.
, 百拇医药
7,Cool V,Pirotte B, Gerard C, et al. Curative potential of herpes simplex virus thymidine kinase gene transfer in rats with 9L gliosarcoma [J]. Hum Gene Ther, 1996, 7: 627~ 635.
8,Uckert W, Kammertons T, Haack K, et al. Double suicide gene (cytosine deaminase and herpes simplex virus thymidine kinase) but not single gene transfer allows reliable elimination of tumor cells in vivo [J]. Hum Gene Ther, 1998, 9:855~865.
9,Bett AJ, Haddara W, Prevec L, et al. An efficient and flexible system for construction of adenovirus vectors with insertions or deletions in early regions 1 and 3 [J]. Proc Natl Acad Sci USA, 1994, 91: 8802~8806.
, 百拇医药
10,Miyake S, Makimura M, Kanegae Y, et al. Efficient generation of recombinant adenoviruses using adenovirus DNA-terminal protein complex and a cosmid bearing the full-length virus genome [J]. Proc Natl Acad Sci USA, 1996,93: 1320~ 1324.
11,He TC, Zhou S, Costa LT, et al. A simplified system for generating recombinant adenovirus [J]. Proc Natl Acad Sci USA, 1998, 95: 2509~ 2514.
收稿日期:2000-02-17;修回日期:2000-03-06, 百拇医药
单位:魏道严 糜军 陈诗书(上海第二医科大学人类基因治疗研究中心,上海200025)
关键词:肿瘤;基因治疗;腺病毒载体;细菌
癌症000502
【摘要】目的:采用细菌内同源重组法高效制备含CD、TK融合自杀基因重组体腺病毒。方法:CD、TK融合基因CDglyTK自载体pWZLneoCDglyTK中切出,亚克隆至腺病毒穿梭质粒中,形成转移质粒pAdtrackCMV-CDglyTK,将之PmeI酶切线性化后与腺病毒基因组质粒pAdeasy-1共转化BJ5183菌,抽提重组体腺病毒基因组质粒DNA,PacI酶切后转染293细胞包装成腺病毒颗粒,采用PCR方法对重组体腺病毒进行鉴定,利用报告GFP基因对病毒滴度和感染效率进行测定,Western Blot检测感染腺病毒的肿瘤细胞中有无目的基因的表达。结果:由pAdTrack-CMV-CDglyTK和pAdeasy-1共转化BJ5183菌16~20h后,可获得30%左右的阳性重组体细菌克隆,由重组体克隆质粒DNA转染293细胞包装产生的重组体腺病毒,经PCR检测表明已含有目的基因,且无复制能力腺病毒的存在。纯化所得腺病毒滴度约为8×1012pfu/L,当MOI=100时,腺病毒感染HepG1细胞的效率>75%,Western Blot证实在感染重组体腺病毒的细胞中有相应基因产物的表达。结论:细菌内同源重组法是一种高效、简便、快捷的重组体腺病毒载体制备方法。所制备的Ad-CDglyTK在体外能有效表达相应的基因产物,为今后的深入研究奠定了基础。
, http://www.100md.com
中图分类号:R735.5文献标识码:A文章编号:1000-467X(2000)05-0399-05
High efficient generation of recombinant adenovirus containing CD、TK fusion gene by using a method of homologous recombination in bacteria
WEI Dao-yan, MI Jun, CHEN Shi-shu
(Research Center for Human Gene Therapy, Shanghai Second Medical University, Shanghai 200025, P.R.China)
【 Abstract】 Objective: To generate recombinant adenovirus (Ad) by using a novel and high efficient method of homologous recombination in bacteria with CDglyTK as target gene. Methods: CDglyTK gene was liberated from plasmid of pWZLneoCDglyTK and subcloned into shuttle plasmid and formed transfer plasmid of pAdTrackCMV-CDglyTK. Then it was linealized with PmeI and cotransformed into BJ5183 bacterial cells with adenovirus genomic DNA plasmid of pAdeasy-1. The identified recombinant adenovirus plasmid DNA was digested with PacI and transfected to 293 cells to package recombinant adenovirus particles. The PCR technique was used to detect target gene and replication-competent Ad (RCA) contamination. The titre and its infection rate of the recombinant Ad were measured with the aid of GFP expression. Western Blot technique was used to analyze the target gene expression in infected tumor cells. Results: There were over 30% positive recombinant bacterial clones after co-transformation of BJ5183 bacterial cells with pAdTrack-CMV-CDglyTK and pAdeasy-1. Recombinant adenovirus particles were produced after 293 cells transfected with recombinant Ad genomic plasmid DNA digested with PacI, then they were further amplified in 293 cells. PCR test indicated that the recombinant Ad contained the insert of CDglyTK gene and there was no contamination of RCA in high-titer viral stocks. The titre of purified Ad was 8× 1012 pfu/L, and more than 75% HepG1 cells were infected with Ad-CDglyTK adenoviruses when MOI reached 100. Meanwhile, protein product of CDglyTK gene was detected in the infected tumor cells. Conclusion: The method of homologous recombination in bacteria is a conve-nient and high efficient method to prepare recombinant Adenovirus, and the prepared adenoviruses can effectively madiate target gene expression in infected tumor cells, thus paves a sound foundation for further study.
, http://www.100md.com
Key words: Neoplasms;Cancer gene therapy; Adenovirus vector; Bacteria
恶性肿瘤的基因治疗是近年来的研究热点,高效基因转移载体和合适目的基因的选择是影响疗效的关键因素。由于重组腺病毒载体介导基因转移效率高,感染细胞谱广、病毒滴度高、易于浓缩和贮存等特点而成为肿瘤基因治疗临床试验的常用载体,当以invivo为基因转移途径,腺病毒载体则为病毒性载体中的首选[1]。但现行常用的细胞内同源重组腺病毒载体制备方法存在着成功率低、工作量大、实验周期长等缺陷,给研究工作带来了很大的不便。在目前众多的临床肿瘤基因治疗研究方案中,自杀基因是选用较多的一类目的基因。由于肿瘤病因复杂、类型繁多,加之肿瘤又存在明显的异质性,单一基因治疗效果较差,多基因联合治疗是今后研究的方向[2]。为此,本研究利用一种新型、高效的细菌内重源重组腺病毒制备方法,构建出同时含大肠杆菌胞嘧啶脱氨酶(cytosine deaminase,CD)基因和I型单纯疱疹病毒胸苷激酶(thymidine kinase,TK)基因的融合自杀基因重组腺病毒载体Ad-CDglyTK,其能在感染的肿瘤细胞中表达出相应的蛋白产物,从而为今后的深入研究奠定了基础。
, http://www.100md.com
1材料与方法
1.1材料
293细胞引自ATCC,HepG1肝癌细胞株为本室传代培养。BJ5183菌株、穿梭质粒pAdtrack-CMV、腺病毒基因组质粒pAdeasy-1由JohnHopkins肿瘤研究中心的Tong-chuanHe博士惠赠(质粒结构见图1)。含CD、TK融合基因的逆转录病毒载体pWZLneoCDglyTK由Henry Fork Health System的Rogulski博士惠赠。兔抗CD的多克隆抗体由Heidelberg大学Hacck博士惠赠惠赠,羊抗兔IgG-AP购自华美生物工程公司。LipofectAMINE,小牛血清、Opti-MEM、MEM及DMEM培养基为Gibco公司产品。

图1 pAdTrack-CMV和pAdeasy-1质粒结构示意图
, http://www.100md.com
1.2方法
1.2.1细胞培养:293细胞用含10%小牛血清的MEM培养基在37℃,5%的CO2培养,HepG1细胞用10%的DMEM培养基培养。
1.2.2细菌感受态的制备、质粒提取、纯化、酶切、连接及细菌转化等参见Sambrook等[3]方法。
1.2.3重组体腺病毒载体的构建:构建流程(见图2)。

图2重组腺病毒载体构建流程示意图
1.2.3.1转移质粒的构建:目的基因CDglyTK自pWZLneoCDglyTK质粒中经EcoRI和BamHI部分酶切后,回收2.5kb的片段,亚克隆至pcDNA3质粒中,pcDNA3-CDglyTK质粒经XbaI+KpnI酶切,回收2.5kb的目的基因片段,插入至经同样酶切的穿梭质粒pAdtrack-CMV中,构建成转移质粒pAdtrack-CMV-CDglyTK,经酶切鉴定正确后,抽提质粒DNA备用。
, 百拇医药
1.2.3.2重组体腺病毒质粒载体的构建及鉴定:取0.5~1.0μgpAdTrackCMV-CDglyTKDNA,PmeI酶切后与0.1μg的pAdeasy-1质粒混匀,加至感受态菌BJ5183中,行电穿孔法质粒细菌转化。小量抽提转化克隆菌质粒DNA,根据琼脂糖电泳电泳质粒大小,选择可疑重组体腺病毒质粒DNA,经PacI、XbaI+KpnI酶切鉴定正确后,抽提重组体腺病毒质粒pAdeasy-CDglyTKDNA备用。
1.2.3.3重组体腺病毒的包装、扩增和纯化:重组体腺病毒质粒DNA经PacI酶切后采用LipofecTAMINE介导转染293细胞。于转染后不同时间在荧光显微镜下观察GFP表达状况,了解腺病毒包装过程。待有较明显的病毒克隆斑或蚀斑形成后,将293细胞自培养瓶内刮下,-70℃/+37℃反复冻融3次裂解细胞,离心取含病毒的上清,重新感染293细胞大量扩增病毒。病毒的纯化参照Hitt[4]等的方法。
1.2.4PCR对重组体腺病毒Ad-CDglyTK的鉴定:自高滴度病毒贮存液中提取腺病毒基组DNA作为模板,分别用可扩增目的基因CDglyTK和扩增腺病毒E1区的二对引物进行PCR反应,对腺病毒进行鉴定。扩增CDglyTK基因的引物:
, http://www.100md.com
上游引物:5'-GCGCGTTAAAGAGATGCTGGAG-3'
下游引物:5'-ATGGCGGTCGAAGATGAGGGTGA-3'
扩增E1区的引物:
上游引物:5'-TCGATCTTACCTTGCCACGC
下游引物:5'-GAGTCACAGCTATCCGTAGAC
1.2.5重组体腺病毒滴度及感染效率的测定:将浓缩后的病毒贮存液作不同比例的稀释,取400μl稀释液加至293细胞培养瓶中,放置37℃吸附30分钟,换新鲜培养基继续培养18~24h,于荧光显微镜下计数GFP阳性细胞数,按下列公式计算病毒滴度:

, http://www.100md.com
病毒感染效率测定:HepG1细胞按2×105细胞/孔接种于6孔板中,用0.1、1、10、100m.o.i(multiplicityofinfection)的腺病毒感染,48小时后在荧光显微镜下计数GFP阳性细胞百分率。
1.2.6重组体腺病毒的体外表达:对数生长期HepG1肿瘤细胞,用Ad-CDglyTK感染(m.o.i为50),72h后提取细胞蛋白,WesternBlot检测分析CDglyTK基因表达(方法参见文献[3])。
2结果
2.1转移质粒的构建
目的基因CDglyTK自载体pWZLnerCDglyTK中切下,经过一次亚克隆,被插入pAdtrackCMV中,形成转移质粒pAdtrackCMV-CDglyTK,经酶切鉴定正确(见图3)。

, 百拇医药
图3构建质粒载体的限制性内切酶解图谱
1.λ-HindIIIDNAMarker.
2.pWZLneoCDglyTK(EcoRI/partialBamHI).
3.pcDNA3CDglyTK(EcoRI/BamHI).
4.pAdTrackCMV-CDglyTK(XbaI/KpnI).
5.pAdTrackCMV(XbaI).
6.pAdeasy-CDglyTK(XbaI/KpnI).
7pAdeasy-CDglyTK(PacI).
8.pAdeasy-1(PacI)
, 百拇医药
2.2重组体腺病毒质粒载体构建及鉴定
转移质粒和pAdeasy-1共转化BJ5183细菌后,含有重组质粒的细菌可在含卡那霉素的培养基中生长形成克隆。挑取转化克隆,小量抽提质粒DNA,直接琼脂糖电泳,根据质粒大小作第一轮初筛;用PacI酶切,重组体质粒可出现一大于20kb的大片段和4.5kb的特征性小带而得以鉴定,再用XbaI+KpnI酶切可见一大小与插入的目的基因相对应的约2.5kb的条带(见图3)。
2.3重组体腺病毒的包装过程
线性化的pAdeasy-CDglyTKDNA经Lipofe-ctAMINE介导转染293细胞48小时后,在荧光显微镜下可见约10%左右的293细胞有GFP的表达。至转染后5~10天左右,大多数细胞的GFP荧光逐渐消失,而在有些局部的荧光斑点数增多,荧光增强,表明包装病毒的形成和扩增,而此时在普通的相差显微镜下难以判断病毒的包装是否形成。随后荧光斑点扩大,并形成明显的蚀斑,293细胞出现固缩、脱落、裂介等明显的病理现象(见图4)。



, 百拇医药
图4线性化pAdeasy-CDglyTKDNA转染293细胞后病毒包装过程
A:转染后第6天,见局部病毒克隆斑形成。B:转染后第10天,病毒克隆斑逐渐扩大,克隆斑中央293细胞因病变固缩,脱落,形成蚀斑。C:转染后第15天,局部细胞已全部固缩、脱落。
2.4重组体腺病毒的鉴定
PCR反应结果显示,用扩增CDglyTK引物进行的PCR反应,出现预期大小的合适条带(图5),表明CDglyTK基因已克隆入重组体腺病毒基因组中;而以扩增腺病毒E1区的引物未能扩增出相应的条带,以含E1区的JM17质粒DNA为模板则扩增出相应的条带,表明用此法制备的重组病毒浓缩贮存液中无具复制能力的腺病毒污染。

图5PCR鉴定重组腺病毒产物电泳图
, http://www.100md.com
A:扩增目的基因的引物:1.阴性对照,2.重组腺病毒基因组DNA,3.123DNA分子量标记。B:扩增E1区序列引物:1.重组腺病毒基因组DNA,2.pJM17DNA,3.123DNA分子量标记。
2.5重组体腺病毒滴度及感染效率的测定
根据GFP计数法测得的腺病毒滴度为8×1012pfu/L。采用不同MOI感染HepG1细胞,当MOI为1时,仅少数细胞有荧光;当MOI为100时,约75%以上的细胞GFP表达阳性(图6)。

图6重组体腺病毒体外感染效率
A.当MOI为1时,仅少数细胞表达GFP。
B.当MOI为100时,约大于75%细胞表达GFP。×100
, http://www.100md.com
2.6重组体腺病毒介导基因体外表达
WesternBlot分析发现,在分子量约88KD处有特异性蛋白条带,(见图7),其大小与CDglyTK基因产物的相吻合[5],证明重组体腺病毒能有效介导目的基因在肿瘤细胞内的表达。

图7WesternBlot检测结果
M:蛋白质分子量标志;1:对照样品;2:实验组样品
3 讨论
CD/5-FC、TK/GCV自杀基因治疗系统是经研究证实效果较为确切的两种自杀基因,其中TK/GCV用于脑胶质瘤的治疗已进入临床Ⅲ期研究阶段。然而,随着研究的深入人们发现,不同类型的肿瘤对两种自杀基因治疗系统的敏感性不同,如胃肠系统的肿瘤CD/5-FC基因治疗系统较为敏感,而脑胶质瘤等则对TK/GCV自杀基因治疗系统敏感[5,6],由此限制了单一自杀基因治疗系统临床适用范围。其次,在单用CD/5-FC或TK/GCV自杀基因治疗系统治疗后复发的肿瘤细胞群体中,发现有相当数量的细胞对相应前药产生了抗性[7]。Uckert等[8]将两种自杀基因联合,既克服单一自杀基因的上述缺陷,又由于两者之间存在明显的协同效应,疗效得到了进一步提高,唯需同时构建两种基因转移载体是其不足。为此,本研究中我们选择具有双功能的CD、TK融合基因作为目的基因[5],再用腺病毒介导基因转移,可能是一种较为简便、有效的途径。
, 百拇医药
传统的细胞内同源重组腺病毒载体制备方法是由Bett[9]等建立。其是先将目的基因亚克隆至穿梭质粒中构建成转移质粒,再与腺病毒基因组质粒共转染293细胞,两质粒借所带的部分同源序列在293细胞内发生同源重组而形成重组体,并进一步包装成重组腺病毒颗粒。然而该方法涉及的步骤及环节较多,成功率较低、工作量大,实验周期长。其主要原因有:(1)细胞内质粒共转染效率较低,同源重组效率更低。而该种制备方法要求两种质粒的共转染及同源重组必须同时发生在293细胞内,才有可能形成重组体并包装成病毒。(2)包装形成的重组体病毒克隆须经过多轮筛选、鉴定和纯化,费时费力。(3)293细胞既是发生同源重组的场所,又是病毒包装的场所,293细胞的状态对实验能否成功影响很大。该种方法通常要求293细胞的培养传代次数不超过45代,从而给实验增加了难度;重复引进传代次数较低的293细胞既费时,代价也相当昂贵。随后Miyaks等[10]建立了COS-TPC制备方法,其基本原理与Bett的方法相似,只是在腺病毒基因组DNA5’末端共价结合末端蛋白复合物,通过提高转染效率使得同源重组率有了一定的提高,但方法学上并无根本性突破。本文采用新型的细菌内同源重组法[11]来制备重组腺病毒载体。由构建流程图(图1)可见,本法与细胞内同源重组法的根本不同之处在于,两种质粒共转染和同源重组在均在细菌内完成,继用经筛选鉴定的重组体克隆质粒DNA转染293细胞,包装和扩增病毒。其突出优点是:(1)成功率高。目前质粒转化细菌技术成熟、效率高,且细菌繁殖快,同源重组能力强,因而从根本克服细胞内同源重组率低的缺陷。(2)方法简便、快捷、实验周期短。重组体腺病毒载体制备的关键环节是同源重组和对重组体进行的筛选、鉴定。细菌内同源重组法的这一过程在细菌内完成。由于从质粒转化细菌到转化重组克隆的出现仅需12~20h;对细菌内质粒DNA的抽提、酶切鉴定远较对细胞内DNA的类似操作方便、容易。用经鉴定正确的重组体腺病毒质粒DNA转染293细胞,包装产生的腺病毒可省却细胞内同源重组法对包装出的病毒必须进行的多轮费时、费力的筛选鉴定。此外,由于在腺病毒骨架中含有的GFP报告基因,非常便于我们监测病毒包装成功与否、检测病毒滴度及感染效率等。如在重组体质粒转染293后的5~7天便可知道病毒是否被成功包装;病毒滴度的测定也仅需24h,这些均大大缩短了实验周期。(3)对293细胞的传代次数要求不太严格,如我们曾用传代次数约50余代的293细胞也包装出重组体腺病毒。经对纯化的重组体腺病毒进行的分析鉴定表明,重组体腺病毒基因组中已含有目的基因;重组体腺病毒能有效感染肿瘤细胞,并表达相应的蛋白产物,说明重组体病毒制备是成功的(其体内、外抗肿瘤作用另文报告)。因此,细菌内同源重组法是一种快速、高效、简便、可行的重组体腺病毒载体制备方法,值得进一步推广应用。
, 百拇医药
基金项目:国家“863”高技术计划基金(863-102-452)和国家自然科学基金(3970440)资助
[参考文献]
1,陈诗书.基因治疗研究进展[J].胃肠病学杂志,1999,4(1):36~40.
2,Paillard F. Cancer cells under the fire of combined therapies [J]. Hum Gene Ther, 1998,9: 1259~ 1260.
3,Sambrook J, Fritsch EF, Maniatis T. Molecular cloning [M]. 2nd ed. New York: Cold Spring Harbor Laboratory Press,1989:852~ 898.
, http://www.100md.com
4,Hitt M, Bett A, Prevec L, et al. Construction and propagation of human adenovirus vectors: In Cell Biology: A Laboratory Handbook [M]. Academic Press, 1998: 550~ 512.
5,Rogulski KR, Kim JH, Kim SH, et al. Glioma cell transduced with Echerichia coli CD/HSV-1 TK fusion gene exhibit enhanced metabolic suicide and radiosensitivity [J]. Hum Gene Ther, 1997, 8: 73~ 85.
6,Trinh QT, Austin EA, Murray DM, et al. Enzyme/prodrug gene therapy: comparison of cytosine deaminase/5-flurocytosone versus thymidine kinase/ganciclovir enzyme/prodrug systems in a human colorectal carcinoma cell line [J]. Cancer Res, 1995, 55: 4808~ 4812.
, 百拇医药
7,Cool V,Pirotte B, Gerard C, et al. Curative potential of herpes simplex virus thymidine kinase gene transfer in rats with 9L gliosarcoma [J]. Hum Gene Ther, 1996, 7: 627~ 635.
8,Uckert W, Kammertons T, Haack K, et al. Double suicide gene (cytosine deaminase and herpes simplex virus thymidine kinase) but not single gene transfer allows reliable elimination of tumor cells in vivo [J]. Hum Gene Ther, 1998, 9:855~865.
9,Bett AJ, Haddara W, Prevec L, et al. An efficient and flexible system for construction of adenovirus vectors with insertions or deletions in early regions 1 and 3 [J]. Proc Natl Acad Sci USA, 1994, 91: 8802~8806.
, 百拇医药
10,Miyake S, Makimura M, Kanegae Y, et al. Efficient generation of recombinant adenoviruses using adenovirus DNA-terminal protein complex and a cosmid bearing the full-length virus genome [J]. Proc Natl Acad Sci USA, 1996,93: 1320~ 1324.
11,He TC, Zhou S, Costa LT, et al. A simplified system for generating recombinant adenovirus [J]. Proc Natl Acad Sci USA, 1998, 95: 2509~ 2514.
收稿日期:2000-02-17;修回日期:2000-03-06, 百拇医药