������Ѫϸ������Flt3����ı��P���Flt3����ķ�Ӧ���о�
���ߣ���־�� ��ӱ ʩ�� ��ӱ ������ ��ΰ�� ��ѧ��
��λ����־�� ��ӱ ʩ�� ��ӱ ��ѧ��(����ҽѧԺ���\���о��������о��ң����� ���� 215007)����־�� ������(����ҽѧԺ����Ժ������ ���� 215004)����ΰ��(�Ϻ�������ѧ����ϵ���Ϻ� 200433)
�ؼ��ʣ�Flt3���壻������Flt3����(rhFL)��������Ѫϸ������ֳ����������
��֢000505
��ժҪ��Ŀ�ģ��о�������Ѫϸ������Flt3����ı��TNF���͵�������(DXM)��Flt3�����������ü�������Flt3����(rhFL)�Զ�����Ѫϸ����ֳ��Ӱ�졣����������ʽϸ���Dzⶨ18�����������Ķ�����Ѫϸ����ϸ������Flt3���壬��MTT���ⶨrhFL�Զ�����Ѫϸ����ֳ��Ӱ�졣�����5��ϸ���������Flt3���塣B�ܰ���ϸ����Raji��Daudi����Թ�����ϸ����8266�����ˮƽFlt3���壻��ϵ��Ѫ��ϸ����HL-60�Ͷ�Թ�����ϸ����XG-6�����ˮƽ��Flt3���塣��10-6mol/LDXM����24h������ϸ��Flt3������オ�ͣ���20ng/mlTNF������24h��Raji��8266ϸ��Flt3������オ�ͣ�HL-60��XG-6ϸ��Flt3����������ߣ�Daudiϸ��Flt3������ﲻ��Ӱ�졣rhFL��10��100ng/mlŨ��ʱ���̼�Raji��HL-60ϸ������ֳ(P<0.05)�����Ծ�������Ķ�����Ѫϸ�������̼����á����ۣ�����������Ѫϸ��������Flt3���壻rhFLҲ���������ϸ������ֳ���������ɽ���Flt3����ı���п������ڷ�ֹ��FL�Բ��ֶ�����Ѫϸ���Ĵ̼����ã�ʹFL��Ӧ�ø�Ϊ��ȫ��
, http://www.100md.com
��ͼ����ţ�R733���ױ�ʶ�룺A���±�ţ�1000-467X(2000)05-0412-04
Flt3 receptor expression on the surface of malignant hematopoietic cells and responses to Flt3 ligand stimulation
XU Zhi-xiang��XU Ying��ZHANG Xue-guang��et al.
(Department of Immunology�� Biotechnology Research Institute��Suzhou Medical College�� Suzhou 215007�� P.R.China)
XU Zhi-xiang
, ��Ĵҽҩ
(The Second Affiliated Hospital�� Suzhou Medical College�� Suzhou 215004�� P.R.China)
��Abstract�� Objectives�� To investigate the Flt3 receptor expression on the surface of malignant hematopoietic cells�� the effect of TNF�� and dexamethasone (DXM) on its expression and the responses of those cells to recombinant human Flt3 ligand (rhFL). Methods�� Eighteen malignant hematopoietic cell lines were determined for the Flt3 receptor expression by flow cytometric analysis. The effect of rhFL on the proliferation of malignant hematopoietic cells in vitro was examined using MTT assay. Results�� The expressions of Flt3 receptor on the surface of Raji�� Daudi�� HL-60�� 8266�� and XG-6 cells were detected by flow cytometric analysis. Following incubation with 20 ng/ml TNF�� for 24 h�� the number of Flt3 receptor positive cells were decreased in Raji and 8266�� increased in HL-60 and XG-6�� and no difference in Daudi cells. After incubation with 10- 6 mol/L DXM for 24 h�� the number of Flt3 receptor positive cells decreased in all the 5 Flt3 receptor positive cell lines. rhFL stimulated the proliferation of HL-60 and Raji cells. Conclusions�� For most of the malignant hematopoietic cells�� there was neither the expression of Flt3 receptor nor the response to rhFL. DXM may be useful to reduce the effect of FL on the proliferation of some Flt3 receptor positive malignant hematopoietic cells in vitro and in vivo.
, http://www.100md.com
Key words�� Flt3 receptor; Recombinant human Flt3 ligand(rhFL); Malignant hematopoietic cell lines; Proliferation; Dexamethasone(DXM)
�������Ѫ���̸��ӣ��ܶ��������������ӵĵ��ء���Щ��Ѫ�������ӻ�ϸ�����ӵĵ���ʧ�⣬�ɵ���ijһϸ��ϵ�Ĺ�����ֳ���������ְ�Ѫ���ı䡣����Щϸ�������У�ϸ�������Ұ��ἤø�����(class��receptor-typetyrosinekinases��RTK-��)������������Ѫ���̣�������������Ѫ����������Ҫ����[1]��Flt3����(fms-liketyrosinekinasereceptor��FR)��Lyman����1993�귢�ֵ�һ��RTK-��[2]��Flt3�ڳ��˹��衢���ټ�̥�����١������и߱��Flt3����(Flt3ligand��FL)��һ�־��дٽ�������Ѫ���ܵ�ϸ�����ӣ�FL��FR��ϣ��ɴ̼�������Ѫ��ϸ��/��ϸ����ֳ���ٽ���Ѫ��FL�пɴ̼���ͻ״ϸ��(dendriticcell��DC)����Ȼɱ��ϸ��(naturalkillercell)�������ͷֻ����յ����ǵij��죬�Ӷ���������������[3��5]��
, ��Ĵҽҩ
��һ���棬FL����������¶���Ѫǰ��ϸ�����д̼���ֳ���ã�����Ѫϵͳ���ֶ���������Դ����Ѫǰ��ϸ����FL�������̼����ã��˹�ϵ��FL�ܷ����ڸ������Ѫ��������˥��ʱ�����ƣ����ϵ��FL�ܷ����ڴ���ߵĿ������������ơ����о�ּ��̽��FR������Ѫϵͳ���ֶ�������ϸ����ϸ������ı��TNF�����������ɶԴ�Ⱥϸ������FR��Ӱ�죬�Լ�������FL(rhFL)������Դ�Ⱥϸ���Ĵ̼����ã�����ΪFL���ٴ��е�Ӧ���ṩ�����о����ϡ�
1���Ϻͷ���
1.1ϸ�����Ӽ�ϸ����
rhFL�������ڱ��Ͻ�ĸ�б�����������롢������������SCF��IL-3��IL-4��GM-CSF��M-CSF��TNF������Immunogen��˾��Daudi��Raji��Jurkat��HL-60��U937��KG1-����U266��TF1��Baf��8266��Wehiϸ��ϵ����ATCC(����)��B9ϸ��ϵ��L.Arden��ʿ����(Amsterdam);B9-11��XG-1��XG-6��XG-7ϸ��ϵ��B.Klein��ʿ����(Montpellier)��HSB2��JJhanandSupT1ϸ��ϵ���Ͼ�ҽ�ƴ�ѧҦ���������͡�����ϸ������֧ԭ���⣬��֧ԭ����Ⱦ���������汣�档
, http://www.100md.com
1.2ϸ������
�ú���10%̥ţѪ���RPMI1640����������������ϸ��(37�棬5%CO2)��Bafϸ������ʱ��������1.5%��Wehi���壬��Ϊ��ϸ����������IL-3����Դ��TF-1��XG-1(XG-6��XG-7)��B9(B9-11)ϸ������ʱ���ֱ����10ng/mlGM-CSF��1ng/mlIL-6��0.5ng/mlIL-11��Ϊ�о�TNF���͵������ɶ�ϸ������FR��Ӱ�죬�ڲⶨFR����ǰ24h���������м���20ng/mlTNF����10-6mol/L��������(DXM)��
1.3��Ѫϵͳ��������ϸ����ϸ������Flt3�������ʽϸ���Ƿ���
�ռ����ڶ��������ڵ�����ϸ������PBSϴ��3�飬��������ȡ5��105ϸ������96�װ��У����뿹Flt3�����Ե�IgG1����SF1.340(����Immunotech��˾)��4�����30min����PBSϴ��δ��ϵĵ���������FITCӫ���ǵ�����IgG��4�����ڰ���30min��ϴ��3�����EPICS��ʽϸ����(CoulterElectronic)���Flt3���
, http://www.100md.com
1.4rhFL����Ѫϵͳ��������ϸ����ϸ������ֳ�����о�
�����ҽ����ij��淽�����У��������£�ȡ���������ڵļ��ϸ������ϴ��3�κ�����96�װ��У�ÿ��5000ϸ�������ں���10%̥ţѪ��RPMI1640�������У����벻ͬŨ��(0��100ng/ml)��rhFL��Bafϸ������ʱ������1.5%Wehi���壬��Ϊ��ϸ����������IL-3����Դ��TF1��XG-1(XG-7)��B9-11(B9)ϸ������ʱ���ֱ����10ng/mlGM-CSF��1ng/mlIL-6��0.5ng/mlIL-11������72h����MTT���ⶨϸ������ֳ����[6]��
2ʵ����
2.1��Ѫϵͳ��������ϸ����ϸ������Flt3����ı���
�������18���Ѫ�����ܰ�������Թ�����ϸ��ϵϸ���������Flt3��������������5����Flt3����ı����5��Flt3����������Ե�ϸ�����У�Flt3����ı���ˮƽ��һ�¡�Raji��Daudi��8266���������ʽϸߣ���HL-60��XG-6����Flt3���������ʽϵ�(��1��ͼ1)��
, ��Ĵҽҩ
2.2TNF���͵������ɶ���Ѫϵͳ��������ϸ����ϸ��Flt3��������Ӱ��
��20ng/mlTNF������24h��Raji��8266ϸ������Flt3���������ϸ�������ͣ���HL-60��XG-6ϸ����Flt3��������ϸ�������ߣ�Daudiϸ������Flt3���岻��Ӱ�졣��10-6mol/LDXM����24h��ϸ������Flt3���彵��(��1��ͼ1).
2.3rhFL����Ѫϵͳ��������ϸ����ϸ��������
rhFL��10��100ng/mlŨ��ʱ���̼�Raji��HL-60ϸ������ֳ(P<0.05) �� �� Jurkat��KG-1����8266��U266��U937��Daudi��Baf��B9��B9-11��TF1��XG-1��XG-6��XG-7��HSB2��JJhan��SupT1�ȶ��ְ�Ѫ��ϸ��ϵ���ܰ���ϸ��ϵ����Թ�����ϸ��ϵϸ���̼���ֳ����������(ͼ2)��
, ��Ĵҽҩ
��1��Ѫϵͳ��������ϸ����ϸ������Flt3
����ı��� ϸ��ϵ
ϸ������(ԭʼ��������)
����Flt3��ϸ��(���Զ���)(%)
����Flt3��ϸ��(%)
TNF���̼�����Flt3��ϸ��(%)
DXM���ú����Flt3��ϸ��(%)
Raji
lymphoid(Btype)
2.1
36.2
, ��Ĵҽҩ
30.8
14.7
Daudi
lymphoblastoid(Btype)
2.7
13.4
12.6
6.7
SUP-T1
lymphoid(Ttype)
0.7
0.4
, ��Ĵҽҩ
0.9
0.58
JJhan
lymphoid(Ttype)
1.4
1.3
1.8
1.2
HSB2
lymphoid(Ttype)
0.8
1.2
1.7
, ��Ĵҽҩ
1.2
Jurkat
lymphoid(ALLT)
0.8
0.7
0.5
1.2
HL-60
myeloid(AMLM2)
1.1
4.1
10.5
4.9
, ��Ĵҽҩ
KG-1��
myeloid(AML)
1.6
1.8
1.5
1.2
TF-1
Erythroid(AMLM6)
1.8
2.5
3.0
2.8
U937
, http://www.100md.com
monocytic(Histiocyticlymph)
1.7
3.8
1.9
1.9
8266
myeloma
0.7
45.5
34.2
22.8
U-266
, ��Ĵҽҩ myeloma
2.0
3.8
6.6
2.2
XG-1
myeloma
1.8
1.7
1.5
1.5
XG-6
myeloma
, ��Ĵҽҩ
2.5
6.3
12.6
4.3
XG-7
myeloma
1.9
3.0
4.1
4.0
B9
Murinelymphoid(Btype)
1.8
, ��Ĵҽҩ
1.4
1.9
1.2
B9-11
Murinelymphoid(Btype)
2.2
1.9
2.0
2.0
Baf
MurineProB-cell
1.1
, http://www.100md.com 1.2
1.3
1.2
3����
��Ѫ�����ܶ������Ժ��Ե������ӵĵ��ڣ���ά�ֻ������Ѫ������һ�����ƽ���״̬������Ѫ�������ӻ�ϸ�����ӵ���ʧ�⣬�ɵ���ijһϸ��ϵ�Ĺ�����ֳ���������ְ�Ѫ���ı䡣FL��һ����Ҫ�����Ե������ӣ�����Ѫ��/��ϸ�������Flt3�����ϣ��ٽ���Ѫ��/��ϸ����ֳ�����������������Ĵٽ���Ѫ���á�FL�ɴ̼���ͻ״ϸ��(dendriticcell��DC)����Ȼɱ��ϸ��(naturalkillercell)�������ͷֻ����յ����ǵij��죬�Ӷ����п���������[4��5��7]����ˣ�FL������Ҫ���о���DZ�ڵ��ٴ�Ӧ�ü�ֵ��
Ȼ������Ѫϵͳ���ֶ���������Դ����Ѫǰ��ϸ������Щϸ����������Flt3������FL�������̼����ã����ϵ��FL�ܷ����ڸ������Ѫ��������˥��ʱ�����ƣ����ϵ��FL�ܷ����ڴ���ߵĿ������������ơ����о����֣�B�ܰ���ϸ����Raji��Daudi����Թ�����ϸ����8266�����ˮƽFlt3���壻��ϵ��Ѫ��ϸ����HL-60�Ͷ�Թ�����ϸ����XG-6�����ˮƽ��Flt3���塣rhFL��Raji��HL-60ϸ���д̼���ֳ���ã����Ծ����������Ѫϵͳ����ϸ������Jurkat��KG-1����8266��U266��U937��Daudi��Baf��B9��B9-11��TF1��XG-1��XG-6��XG-7��HSB2��JJhan��SupT1��ϸ����������ֳ���������ã�˵��rhFL�����ھ����������Ѫϵͳ�������ߣ������������������Ѫϸ������ֳ������B�ܰ������ߺͼ�����ϵ��Ѫ�����ߣ�ʹ��ʱ������߶���ϸ������Flt3����ı��
, ��Ĵҽҩ
ͼ1Rajiϸ������Flt3�������ʽϸ���Ƿ���
ϸ���������ԵĿ�flt3���嵥��SF1.340Ⱦɫ���(ͼ�������º��岿��)�����Զ����þ�����ͬ�����͵��ؿ�����б��(ͼ���������пղ���)��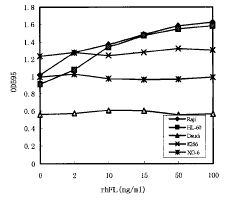
ͼ2rhFL��Flt3�������Զ�����Ѫϸ��ϵϸ����������
�����ǵ�ʵ����֣��������ɿ�����ϸ������Flt3����ı����TNF���Ը���ϸ��ϵϸ������Flt3��������ò���һ�¡��ý����ʾ������ϸ��Flt3�������Ե�ѪҺ�����߱���ʹ��FL������Ѫ����FL��������������ʱ�����õ������ɣ��п��ܷ�ֹ��FL����������ϸ���Ĵ̼����ã�ʹFL��Ӧ�ø�Ϊ��ȫ��������ָ�����������õ�ϸ����Ϊϸ��ϵϸ����Ҫ�����˽�FL����Ѫϵͳ����������Ӱ�죬�����һ���о�rhFL����������ϸ��������ЧӦ�Լ�̽��rhFL�����ڶԶ�������ϸ�������á�
, ��Ĵҽҩ
������Ŀ��������Ϊ�����ƹ�ί������Ŀ(Y5573162)����ԭ���ܻ���(IAEA)������Ŀ(CRP/9/025)
[�����]
[1] Ullrich A�� Schlessinger J. Signal transduction by receptors with tyrosine kinase activity [J]. Cell�� 1990�� 61�� 203�� 212.
[2] Rosnet O�� Schiff C�� Pebusque MJ�� et al. Human FLT3/FLK2 gene�� cDNA cloning and expression in hematopoietic cells [J]. Blood�� 1993�� 82(4)�� 1110�� 1119.
[3] Lyman SD�� James L�� Johnson L�� et al. Cloning of the human homologue of the murine Flt3 ligand�� a growth factor for early hematopoietic progenitor cells [J]. Blood�� 1994�� 83(10)�� 2795�� 2801.
, http://www.100md.com
[4] Lynch DH�� Andreasen A�� Maraskovsky E�� et al. Flt3 ligand induces tumor regression and antitumor immune responses in vivo [J]. Nat Med�� 1997�� 3(2)�� 625�� 631.
[5] Peron JM�� Esche C�� Subbotin VM�� et al. FLT3-ligand administration inhibits liver metastases�� role of NK cells [J]. J Immunol�� 1998�� 161(11)�� 6164�� 6170.
[6] Carmichael J�� DeGraff WG�� Gazdar AF�� et al. Evaluation of a tetrazolium-based semiautomated colorimetric assay�� Assessment of chemosensitivity testing [J]. Cancer Res�� 1987�� 47(4)�� 936�� 943.
[7] Sakabe H�� Kimura T�� Zeng Z�� et al. Haematopoietic action of Flt3 ligand on cord blood-derived CD34-positive cells expressing different levels of Flt3 or c-kit tyrosine kinase receptor�� comparison with stem cell factor [J]. Eur J Haematol�� 1998�� 60(5)�� 297�� 306.
�ո����ڣ�1999-11-11�������ڣ�1999-12-13, ��Ĵҽҩ
��λ����־�� ��ӱ ʩ�� ��ӱ ��ѧ��(����ҽѧԺ���\���о��������о��ң����� ���� 215007)����־�� ������(����ҽѧԺ����Ժ������ ���� 215004)����ΰ��(�Ϻ�������ѧ����ϵ���Ϻ� 200433)
�ؼ��ʣ�Flt3���壻������Flt3����(rhFL)��������Ѫϸ������ֳ����������
��֢000505
��ժҪ��Ŀ�ģ��о�������Ѫϸ������Flt3����ı��TNF���͵�������(DXM)��Flt3�����������ü�������Flt3����(rhFL)�Զ�����Ѫϸ����ֳ��Ӱ�졣����������ʽϸ���Dzⶨ18�����������Ķ�����Ѫϸ����ϸ������Flt3���壬��MTT���ⶨrhFL�Զ�����Ѫϸ����ֳ��Ӱ�졣�����5��ϸ���������Flt3���塣B�ܰ���ϸ����Raji��Daudi����Թ�����ϸ����8266�����ˮƽFlt3���壻��ϵ��Ѫ��ϸ����HL-60�Ͷ�Թ�����ϸ����XG-6�����ˮƽ��Flt3���塣��10-6mol/LDXM����24h������ϸ��Flt3������オ�ͣ���20ng/mlTNF������24h��Raji��8266ϸ��Flt3������オ�ͣ�HL-60��XG-6ϸ��Flt3����������ߣ�Daudiϸ��Flt3������ﲻ��Ӱ�졣rhFL��10��100ng/mlŨ��ʱ���̼�Raji��HL-60ϸ������ֳ(P<0.05)�����Ծ�������Ķ�����Ѫϸ�������̼����á����ۣ�����������Ѫϸ��������Flt3���壻rhFLҲ���������ϸ������ֳ���������ɽ���Flt3����ı���п������ڷ�ֹ��FL�Բ��ֶ�����Ѫϸ���Ĵ̼����ã�ʹFL��Ӧ�ø�Ϊ��ȫ��
, http://www.100md.com
��ͼ����ţ�R733���ױ�ʶ�룺A���±�ţ�1000-467X(2000)05-0412-04
Flt3 receptor expression on the surface of malignant hematopoietic cells and responses to Flt3 ligand stimulation
XU Zhi-xiang��XU Ying��ZHANG Xue-guang��et al.
(Department of Immunology�� Biotechnology Research Institute��Suzhou Medical College�� Suzhou 215007�� P.R.China)
XU Zhi-xiang
, ��Ĵҽҩ
(The Second Affiliated Hospital�� Suzhou Medical College�� Suzhou 215004�� P.R.China)
��Abstract�� Objectives�� To investigate the Flt3 receptor expression on the surface of malignant hematopoietic cells�� the effect of TNF�� and dexamethasone (DXM) on its expression and the responses of those cells to recombinant human Flt3 ligand (rhFL). Methods�� Eighteen malignant hematopoietic cell lines were determined for the Flt3 receptor expression by flow cytometric analysis. The effect of rhFL on the proliferation of malignant hematopoietic cells in vitro was examined using MTT assay. Results�� The expressions of Flt3 receptor on the surface of Raji�� Daudi�� HL-60�� 8266�� and XG-6 cells were detected by flow cytometric analysis. Following incubation with 20 ng/ml TNF�� for 24 h�� the number of Flt3 receptor positive cells were decreased in Raji and 8266�� increased in HL-60 and XG-6�� and no difference in Daudi cells. After incubation with 10- 6 mol/L DXM for 24 h�� the number of Flt3 receptor positive cells decreased in all the 5 Flt3 receptor positive cell lines. rhFL stimulated the proliferation of HL-60 and Raji cells. Conclusions�� For most of the malignant hematopoietic cells�� there was neither the expression of Flt3 receptor nor the response to rhFL. DXM may be useful to reduce the effect of FL on the proliferation of some Flt3 receptor positive malignant hematopoietic cells in vitro and in vivo.
, http://www.100md.com
Key words�� Flt3 receptor; Recombinant human Flt3 ligand(rhFL); Malignant hematopoietic cell lines; Proliferation; Dexamethasone(DXM)
�������Ѫ���̸��ӣ��ܶ��������������ӵĵ��ء���Щ��Ѫ�������ӻ�ϸ�����ӵĵ���ʧ�⣬�ɵ���ijһϸ��ϵ�Ĺ�����ֳ���������ְ�Ѫ���ı䡣����Щϸ�������У�ϸ�������Ұ��ἤø�����(class��receptor-typetyrosinekinases��RTK-��)������������Ѫ���̣�������������Ѫ����������Ҫ����[1]��Flt3����(fms-liketyrosinekinasereceptor��FR)��Lyman����1993�귢�ֵ�һ��RTK-��[2]��Flt3�ڳ��˹��衢���ټ�̥�����١������и߱��Flt3����(Flt3ligand��FL)��һ�־��дٽ�������Ѫ���ܵ�ϸ�����ӣ�FL��FR��ϣ��ɴ̼�������Ѫ��ϸ��/��ϸ����ֳ���ٽ���Ѫ��FL�пɴ̼���ͻ״ϸ��(dendriticcell��DC)����Ȼɱ��ϸ��(naturalkillercell)�������ͷֻ����յ����ǵij��죬�Ӷ���������������[3��5]��
, ��Ĵҽҩ
��һ���棬FL����������¶���Ѫǰ��ϸ�����д̼���ֳ���ã�����Ѫϵͳ���ֶ���������Դ����Ѫǰ��ϸ����FL�������̼����ã��˹�ϵ��FL�ܷ����ڸ������Ѫ��������˥��ʱ�����ƣ����ϵ��FL�ܷ����ڴ���ߵĿ������������ơ����о�ּ��̽��FR������Ѫϵͳ���ֶ�������ϸ����ϸ������ı��TNF�����������ɶԴ�Ⱥϸ������FR��Ӱ�죬�Լ�������FL(rhFL)������Դ�Ⱥϸ���Ĵ̼����ã�����ΪFL���ٴ��е�Ӧ���ṩ�����о����ϡ�
1���Ϻͷ���
1.1ϸ�����Ӽ�ϸ����
rhFL�������ڱ��Ͻ�ĸ�б�����������롢������������SCF��IL-3��IL-4��GM-CSF��M-CSF��TNF������Immunogen��˾��Daudi��Raji��Jurkat��HL-60��U937��KG1-����U266��TF1��Baf��8266��Wehiϸ��ϵ����ATCC(����)��B9ϸ��ϵ��L.Arden��ʿ����(Amsterdam);B9-11��XG-1��XG-6��XG-7ϸ��ϵ��B.Klein��ʿ����(Montpellier)��HSB2��JJhanandSupT1ϸ��ϵ���Ͼ�ҽ�ƴ�ѧҦ���������͡�����ϸ������֧ԭ���⣬��֧ԭ����Ⱦ���������汣�档
, http://www.100md.com
1.2ϸ������
�ú���10%̥ţѪ���RPMI1640����������������ϸ��(37�棬5%CO2)��Bafϸ������ʱ��������1.5%��Wehi���壬��Ϊ��ϸ����������IL-3����Դ��TF-1��XG-1(XG-6��XG-7)��B9(B9-11)ϸ������ʱ���ֱ����10ng/mlGM-CSF��1ng/mlIL-6��0.5ng/mlIL-11��Ϊ�о�TNF���͵������ɶ�ϸ������FR��Ӱ�죬�ڲⶨFR����ǰ24h���������м���20ng/mlTNF����10-6mol/L��������(DXM)��
1.3��Ѫϵͳ��������ϸ����ϸ������Flt3�������ʽϸ���Ƿ���
�ռ����ڶ��������ڵ�����ϸ������PBSϴ��3�飬��������ȡ5��105ϸ������96�װ��У����뿹Flt3�����Ե�IgG1����SF1.340(����Immunotech��˾)��4�����30min����PBSϴ��δ��ϵĵ���������FITCӫ���ǵ�����IgG��4�����ڰ���30min��ϴ��3�����EPICS��ʽϸ����(CoulterElectronic)���Flt3���
, http://www.100md.com
1.4rhFL����Ѫϵͳ��������ϸ����ϸ������ֳ�����о�
�����ҽ����ij��淽�����У��������£�ȡ���������ڵļ��ϸ������ϴ��3�κ�����96�װ��У�ÿ��5000ϸ�������ں���10%̥ţѪ��RPMI1640�������У����벻ͬŨ��(0��100ng/ml)��rhFL��Bafϸ������ʱ������1.5%Wehi���壬��Ϊ��ϸ����������IL-3����Դ��TF1��XG-1(XG-7)��B9-11(B9)ϸ������ʱ���ֱ����10ng/mlGM-CSF��1ng/mlIL-6��0.5ng/mlIL-11������72h����MTT���ⶨϸ������ֳ����[6]��
2ʵ����
2.1��Ѫϵͳ��������ϸ����ϸ������Flt3����ı���
�������18���Ѫ�����ܰ�������Թ�����ϸ��ϵϸ���������Flt3��������������5����Flt3����ı����5��Flt3����������Ե�ϸ�����У�Flt3����ı���ˮƽ��һ�¡�Raji��Daudi��8266���������ʽϸߣ���HL-60��XG-6����Flt3���������ʽϵ�(��1��ͼ1)��
, ��Ĵҽҩ
2.2TNF���͵������ɶ���Ѫϵͳ��������ϸ����ϸ��Flt3��������Ӱ��
��20ng/mlTNF������24h��Raji��8266ϸ������Flt3���������ϸ�������ͣ���HL-60��XG-6ϸ����Flt3��������ϸ�������ߣ�Daudiϸ������Flt3���岻��Ӱ�졣��10-6mol/LDXM����24h��ϸ������Flt3���彵��(��1��ͼ1).
2.3rhFL����Ѫϵͳ��������ϸ����ϸ��������
rhFL��10��100ng/mlŨ��ʱ���̼�Raji��HL-60ϸ������ֳ(P<0.05) �� �� Jurkat��KG-1����8266��U266��U937��Daudi��Baf��B9��B9-11��TF1��XG-1��XG-6��XG-7��HSB2��JJhan��SupT1�ȶ��ְ�Ѫ��ϸ��ϵ���ܰ���ϸ��ϵ����Թ�����ϸ��ϵϸ���̼���ֳ����������(ͼ2)��
, ��Ĵҽҩ
��1��Ѫϵͳ��������ϸ����ϸ������Flt3
����ı��� ϸ��ϵ
ϸ������(ԭʼ��������)
����Flt3��ϸ��(���Զ���)(%)
����Flt3��ϸ��(%)
TNF���̼�����Flt3��ϸ��(%)
DXM���ú����Flt3��ϸ��(%)
Raji
lymphoid(Btype)
2.1
36.2
, ��Ĵҽҩ
30.8
14.7
Daudi
lymphoblastoid(Btype)
2.7
13.4
12.6
6.7
SUP-T1
lymphoid(Ttype)
0.7
0.4
, ��Ĵҽҩ
0.9
0.58
JJhan
lymphoid(Ttype)
1.4
1.3
1.8
1.2
HSB2
lymphoid(Ttype)
0.8
1.2
1.7
, ��Ĵҽҩ
1.2
Jurkat
lymphoid(ALLT)
0.8
0.7
0.5
1.2
HL-60
myeloid(AMLM2)
1.1
4.1
10.5
4.9
, ��Ĵҽҩ
KG-1��
myeloid(AML)
1.6
1.8
1.5
1.2
TF-1
Erythroid(AMLM6)
1.8
2.5
3.0
2.8
U937
, http://www.100md.com
monocytic(Histiocyticlymph)
1.7
3.8
1.9
1.9
8266
myeloma
0.7
45.5
34.2
22.8
U-266
, ��Ĵҽҩ myeloma
2.0
3.8
6.6
2.2
XG-1
myeloma
1.8
1.7
1.5
1.5
XG-6
myeloma
, ��Ĵҽҩ
2.5
6.3
12.6
4.3
XG-7
myeloma
1.9
3.0
4.1
4.0
B9
Murinelymphoid(Btype)
1.8
, ��Ĵҽҩ
1.4
1.9
1.2
B9-11
Murinelymphoid(Btype)
2.2
1.9
2.0
2.0
Baf
MurineProB-cell
1.1
, http://www.100md.com 1.2
1.3
1.2
3����
��Ѫ�����ܶ������Ժ��Ե������ӵĵ��ڣ���ά�ֻ������Ѫ������һ�����ƽ���״̬������Ѫ�������ӻ�ϸ�����ӵ���ʧ�⣬�ɵ���ijһϸ��ϵ�Ĺ�����ֳ���������ְ�Ѫ���ı䡣FL��һ����Ҫ�����Ե������ӣ�����Ѫ��/��ϸ�������Flt3�����ϣ��ٽ���Ѫ��/��ϸ����ֳ�����������������Ĵٽ���Ѫ���á�FL�ɴ̼���ͻ״ϸ��(dendriticcell��DC)����Ȼɱ��ϸ��(naturalkillercell)�������ͷֻ����յ����ǵij��죬�Ӷ����п���������[4��5��7]����ˣ�FL������Ҫ���о���DZ�ڵ��ٴ�Ӧ�ü�ֵ��
Ȼ������Ѫϵͳ���ֶ���������Դ����Ѫǰ��ϸ������Щϸ����������Flt3������FL�������̼����ã����ϵ��FL�ܷ����ڸ������Ѫ��������˥��ʱ�����ƣ����ϵ��FL�ܷ����ڴ���ߵĿ������������ơ����о����֣�B�ܰ���ϸ����Raji��Daudi����Թ�����ϸ����8266�����ˮƽFlt3���壻��ϵ��Ѫ��ϸ����HL-60�Ͷ�Թ�����ϸ����XG-6�����ˮƽ��Flt3���塣rhFL��Raji��HL-60ϸ���д̼���ֳ���ã����Ծ����������Ѫϵͳ����ϸ������Jurkat��KG-1����8266��U266��U937��Daudi��Baf��B9��B9-11��TF1��XG-1��XG-6��XG-7��HSB2��JJhan��SupT1��ϸ����������ֳ���������ã�˵��rhFL�����ھ����������Ѫϵͳ�������ߣ������������������Ѫϸ������ֳ������B�ܰ������ߺͼ�����ϵ��Ѫ�����ߣ�ʹ��ʱ������߶���ϸ������Flt3����ı��

, ��Ĵҽҩ
ͼ1Rajiϸ������Flt3�������ʽϸ���Ƿ���
ϸ���������ԵĿ�flt3���嵥��SF1.340Ⱦɫ���(ͼ�������º��岿��)�����Զ����þ�����ͬ�����͵��ؿ�����б��(ͼ���������пղ���)��

ͼ2rhFL��Flt3�������Զ�����Ѫϸ��ϵϸ����������
�����ǵ�ʵ����֣��������ɿ�����ϸ������Flt3����ı����TNF���Ը���ϸ��ϵϸ������Flt3��������ò���һ�¡��ý����ʾ������ϸ��Flt3�������Ե�ѪҺ�����߱���ʹ��FL������Ѫ����FL��������������ʱ�����õ������ɣ��п��ܷ�ֹ��FL����������ϸ���Ĵ̼����ã�ʹFL��Ӧ�ø�Ϊ��ȫ��������ָ�����������õ�ϸ����Ϊϸ��ϵϸ����Ҫ�����˽�FL����Ѫϵͳ����������Ӱ�죬�����һ���о�rhFL����������ϸ��������ЧӦ�Լ�̽��rhFL�����ڶԶ�������ϸ�������á�
, ��Ĵҽҩ
������Ŀ��������Ϊ�����ƹ�ί������Ŀ(Y5573162)����ԭ���ܻ���(IAEA)������Ŀ(CRP/9/025)
[�����]
[1] Ullrich A�� Schlessinger J. Signal transduction by receptors with tyrosine kinase activity [J]. Cell�� 1990�� 61�� 203�� 212.
[2] Rosnet O�� Schiff C�� Pebusque MJ�� et al. Human FLT3/FLK2 gene�� cDNA cloning and expression in hematopoietic cells [J]. Blood�� 1993�� 82(4)�� 1110�� 1119.
[3] Lyman SD�� James L�� Johnson L�� et al. Cloning of the human homologue of the murine Flt3 ligand�� a growth factor for early hematopoietic progenitor cells [J]. Blood�� 1994�� 83(10)�� 2795�� 2801.
, http://www.100md.com
[4] Lynch DH�� Andreasen A�� Maraskovsky E�� et al. Flt3 ligand induces tumor regression and antitumor immune responses in vivo [J]. Nat Med�� 1997�� 3(2)�� 625�� 631.
[5] Peron JM�� Esche C�� Subbotin VM�� et al. FLT3-ligand administration inhibits liver metastases�� role of NK cells [J]. J Immunol�� 1998�� 161(11)�� 6164�� 6170.
[6] Carmichael J�� DeGraff WG�� Gazdar AF�� et al. Evaluation of a tetrazolium-based semiautomated colorimetric assay�� Assessment of chemosensitivity testing [J]. Cancer Res�� 1987�� 47(4)�� 936�� 943.
[7] Sakabe H�� Kimura T�� Zeng Z�� et al. Haematopoietic action of Flt3 ligand on cord blood-derived CD34-positive cells expressing different levels of Flt3 or c-kit tyrosine kinase receptor�� comparison with stem cell factor [J]. Eur J Haematol�� 1998�� 60(5)�� 297�� 306.
�ո����ڣ�1999-11-11�������ڣ�1999-12-13, ��Ĵҽҩ