细胞外Ba2+对双基因内向整流钾通道的阻断作用
作者:谢安 臧益民 朱妙章
单位:谢安(第四军医大学基础部生理学教研室,陕西 西安 710033);臧益民(第四军医大学基础部生理学教研室,陕西 西安 710033);朱妙章(第四军医大学基础部生理学教研室,陕西 西安 710033)
关键词:钡;内向整流钾通道;电压钳;爪蟾卵母细胞
心脏杂志000501摘 要: 目的:研究Ba2+对非洲爪蟾卵母细胞表达的双 基因内向整流钾通道(IRK1-T )的阻断作用。方法:采用双微电极电压钳(TEV)法。结果:细胞外Ba2+浓度分别为1,3,10 和100 μmol/L,K+浓度为90 mmol/L,可见Ba2+的阻断作用对IRK1-T的瞬间电流( 施加电压后1 ms)具有 浓度依赖性、时间依赖性和电压依赖性;快速开通道阻断剂Ba2+对IRK1-T 的通道开 关特性几乎无影响作用,IRK1-T对之不通透。三级指数拟合表明:细胞外Ba2+低浓 度(1和3 μmol/L)时,Ba2+与K+相互竞争同一结合位点,随着Ba2+浓度的增 加,时间常数不增加但拟 合的权数却浓度依赖性增加,所以失活过程随Ba2+浓度的增加越来越快;细胞外Ba 2+高浓度 (10和100 μmol/L)时,时间常数随Ba2+浓度的增加而减少,拟合的权数却浓度依赖 性减少, 失活过程也越来越快,说明Ba2+作用位点由通道的表面部位进入通道更深的地方。[ HTH 结论:Ba2+对IRK1-T的阻断存在两种不同的机制。
, 百拇医药
中图分类号:Q424 文献标识码:A
文章编号:1005-3271(2000)05- 0345-04
The blocking effects of extracellular Ba2+ on the inward rectifier potassi um tandem channel
XIE An ZANG Yi-min ZHU Miao-zhang
(Department of Physiology, Basic Science Institute, Fourth Military Medical University, Xi'an Shaanxi 710032, China)
Abstract: AIM: The blocking effects of extracellular Ba2+ o n the inward rectifi er potassium tandem channel (IRK1-T) expressed in the Xenopus oocytes was studi e d. METHODS: Two-microelectrode voltage clamp (TEV) method was used. RESULTS: Ba2+ can concentration-, time- and volt age dependently block IRK1-T instanta neous currents ( 1ms after voltage applied ) when external Ba2+ concentrat ion is 1,3,10 or 100 μmol/L with 90 mmol/L potassium. Fast open channel blocker Ba 2+ almost has no effect on the open/close property of IRK1-T. IRK1-T can not per meate Ba2+. Three exponential fitting results indicate that Ba2+and K+ compete the same bi nding site in IRK1-T when external Ba2+ concentration (1 or 3 μmol/L) is lower. Time constants do not increase but the weights of the fittings concentration de pendently enhance as the external Ba2+ concentration augments. So the inac tivati on becomes faster and faster as the external Ba2+ concentration increases. Time constants decrease and the weights of the fittings concentration dependently enh ance as the external Ba2+ concentration augments when external Ba2+ concentratio n (10 or 100 μmol/L) is higher. So the inactivation becomes faster and faster. It is showed that Ba2+ can go deeper in IRK1-T from the surface of the ch annel a s external Ba2+ concentration increases. CONCLUSION: Two diffe rent mechanisms for external Ba2+ blocking exist.
, 百拇医药
Key words: barium; open channel blocker; inward rectifier potassium chan nel; tandem
Ba2+是双基因内向整流钾通道(IRK1-T)的开通道阻断剂[1] 。研究Ba2+对IRK1-T的阻 断作用不仅对于二价阳离子阻断IRK1-T的分子机制的研究有重要意义,而且对于了解IRK1 -T 的通道结构和功能也有很大帮助。以往的研究由于技术水平的限制,对通道瞬间电流的分析 不够准确(施加电压后10 ms)[1],因而采用的数据分析方法也不够准确[2] 。作者使用高质量电流曲线对Ba2+的阻断作用做了重新评价,以其得出较准确的分析 结论。
1 材料和方法
大鼠巨噬细胞系的 IRK cDNA是加利福尼亚大学Jan博士赠与的。mRNA的线性化由Xh o I酶完成,转录过程使用mCAPTM mRNA capping试剂盒(Stratagene Inc,La,Jolla,CA) ,由T3 聚合酶转录。mRNA的检测用凝胶电泳;其浓度测量用光谱仪,并于-80℃贮存。使用第Ⅴ和 Ⅵ期的非州爪蟾卵母细胞;在无钙的Barth液中使用胶原酶I(SIGMA,10 mg/10 ml) 处理1.5 h , 温度20℃, 用钠升注射器(Drummond Scientific) 将mRNA(浓度:1.85 ng/nl,注射30 ng )注入细胞内;在正常带有抗菌素的Barth液中孵育24 h后使用。
, 百拇医药
全细胞电流记录使用双微电极电压钳(TEV)法,放大器为CA-1(Dagan Corp).用两 个有 3M KCl的微电极刺入细胞中,一个(尖端电阻0.2~0.3 MΩ)做为电流注射电极,另一个(尖端 电阻约0.5 MΩ)做为电压记录电极,两个电极尖端的形态漏斗状,并且镀上Sylgard。第三 个 电极置于与细胞1 mm左右的距离用于感受细胞膜外的钳制电压。为了测量串联电阻,一个微 电极置于细胞上前方约5 μm处,串联电阻约0.2 KΩ,在需要的时候使用串联电阻补偿。使 用 一接地的金属板置于微电极之间以减少电容耦合干扰。另一个电流电极用于进行电容补偿, 旋转三个时间常数和三个相位延迟可以很好地进行电容补偿。漏电流在分析数据时再除去。
对照浴液中含有(mmol/L):90 KCl, 5 HEPES,3MgCl2和0.2 Niflumic acid(用于阻 断内源性Cl-电流),pH7.4。再将1,3,10和100 μmol/L的BaCl2加入对照浴液中。 换浴液时连续灌流速率约2.5~3 ml/min。指令电压由486计算机与Digi Data 1200 (A xon Instruments)产生。电流滤波频率为2 kHz,采样频率为10 kHz,数据的获取由pCLAMP6 (Axon)完成。 实验时室内温度为23~25℃。
, 百拇医药
数据分析采用pCLAMP6, Excel 97与Origin完成。阳离子剂量依赖性阻断数据用下式拟 合:
I/I0=(I/I0-U)/{1+([X]/Kd)}+U (1)
其中I/I0为阻断剂浓度为[X]时电流残留分数,Kd为平衡解离常数,U是在饱和的[ X]时电流不可阻断的分数。使用Hill方程做拟合
I/I0=Kdn/(Kdn+[X]n),其中n为Hill系数 (2)
对Ba2+、Mg2+和Mn2+阻断动力学分析是先采用三级指数函数的拟合
, 百拇医药
I=A1e-(t-k)/τ1+A2e-(t-k)/τ2+A3e-(t-k)/τ3 (3)
其中τ为时间常数,A为指数函数的权,K为进行拟合的起始时间。然后进行下式拟合
1/τ=K(0)e-δzFV/RT , K(0)=1/τ(0) (4)
其中δ为电场距离分数,z为阻断剂的离子价,F,R和T为三个常用的热力学常数。
数据由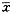 ±s表示,每组数据例数为3~4例。
±s表示,每组数据例数为3~4例。
2 结果
, 百拇医药
Ba2+对IRK1-T瞬间内向电流有浓度依赖性阻断作用,细胞外Ba2+ 浓度越大 ,电流越小(图1A,B);这种阻断也同时具有电压依赖性,膜电位越大,阻断越明显。 Ba2+可加快IRK1-T的失活过程。这时反转电位没有变化,因而IRK1-T对Ba2+ 不通透(图1A,B)。Ba2+对IRK1-T 的通道开关特性几乎没有影响,规一化的电导几乎不受Ba2+的影响(图1C)。可见Ba 2+是一快 速的开通道阻断剂。使用指数拟合分析表明(图1D,E):细胞外Ba2+低浓度(1和3 μm ol/L) 时,随着Ba2+浓度的增加,时间常数不增加但拟合的权数却浓度依赖性增加,失活过 程随Ba2+ 浓度的增加越来越快,表示Ba2+与K+相互竞争同一结合位点;细胞外Ba2+高 浓度(10和100 μmol/L)时,时间常数随Ba2+浓度的增加而减少,拟合的权数却浓度依赖性减少,失 活过程 也越来越快,说明Ba2+作用位点由通道的表面部位进入通道更深的地方。细胞外Ba 2+浓度 增加时,平衡解离常数明显降低,说明Ba2+与IRK1-T的结合程度增加,也说明Ba 2+对IRK1- T的阻断作用还有浓度依赖性(图2A,B)。但细胞外K+浓度为90 mmol/L时,Hill系数为1 .01±0.34,可以看出只有一个Ba2+进入通道进行阻断。
, 百拇医药
3 讨论
内向整流钾通道(IRK1)广泛存在于骨骼肌细胞、心肌细胞、神经细胞、胶质细胞、 血细胞和内皮细胞等,可维持细胞的静息电位和控制细胞的兴奋性,例如IRK1参与了心肌复极 化,还可延长心室肌细胞动作电位时程,对心律失常的产生和防治有很大影响。对IRK1的各 个基因进行功能研究现通常采用基因变异方法,由于基因变异可导致IRK1的通透性改变,所 以纯粹用变异基因表达的四聚体通道通常记录不到电流。解决这个问题的方法通常有两种: 一是采用变异基因与野生型基因等比例混合,然后注入细胞[3] ;二是采用双 基因表达 的二聚体通道,双基因中一是野生型基因,另一基因可以做成变异基因,然后对变异基因进 行功能研究。后一种方法的关键在于两个野生型基因连接后表达的二聚体通道应与四个野生 型基因表达的四聚体通道不仅通道特性完全相同,而且通道阻断剂的作用也要完全相同 [9] 。作者就后一点做了详细研究。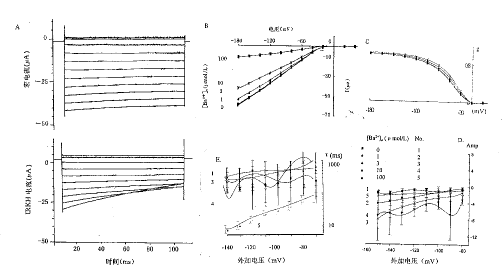
, http://www.100md.com
图 1 Ba2+对IRK1-T 有浓度依赖性阻断作用
A:上图为未加Ba2+时的宏电流。下图为Ba2+浓度为10 μmol/L时的IRK1-T电 流。电压波宽为110 ms,幅度从+40 mV至-180 mV,增量为-20 mV,保持电压为-30 mV。B: 瞬间I-V曲线(施加电压后1 ms时)。数据为A中电流,Ba2+浓度分别为1,3 ,10和 100 μmol/L。C:规一化的IRK1-T电导。D:指数函数拟合的阻断的指数函数的权, 见公 式(3)。E:指数函数拟合的阻断的时间常数, 见公式(3)。细胞外Ba2+浓度100 μmol/L时,电场距离分数δ为0.49。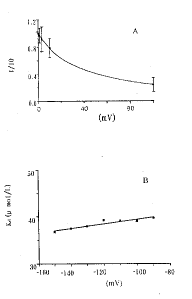
图2 Ba2+对IRK1-T平衡解离常数的作用
, 百拇医药
A:浓度依赖性Ba2+阻断。曲线为公式(1)的拟合曲线,细胞外K+浓度为90 mmol/L 时 ,Hill系数为1.01±0.34。膜电压-140 mV。B:电压依赖性平衡解离常数,由A中数据得 出。
Ba2+一直被认为是IRK1-T的快速开通道阻断剂,细胞外Ba2+可以电压 和时间依赖性地高 效地阻断IRK1-T。但以往所取得的通道电流仅在电压施加数ms后才能避开电容电流的影响 , 进而进行瞬间电流的分析,这样分析的准确性很差,例如以往报道Na+和Cs+也是IRK1- T的开 通道阻断剂[1],用本文的记录方法却得出相反的结论:Na+和Cs+(施加电压 后1 ms)可增 加通道的内向电流,不是IRK1-T的开通道阻断剂,作者较精确地证明Ba2+是IRK1-T 的快速开 通道阻断剂,但其瞬间电流的抑制作用却大大下降;而且以往对通道电流进行的拟合也采用 的是单指数函数的拟合,对于Ba2+对瞬间内向电流的抑制作用不能很好地拟合[ 1,2]。通过减 小电流电极尖端阻抗,用Sylgard涂电极尖端等多方改进,作者得到了施加电压后1 ms的高 质量电流曲线,并用三级指数函数对电流曲线进行了完美的拟合,分析的准确性大大提高 ,可得出下述众多以往未报道过的结果。
, http://www.100md.com
通过分析证实了Ba2+对IRK1-T的快速开通道阻断是Ba2+浓度、时间 和电压依赖性的 ,IRK1-T对Ba2+不通透,Ba2+对IRK1-T的通道开关特性也无影响。实验结果 表明Ba2+对IRK1 -T的阻断作用可通过两种不同的机制。一种机制是Ba2+与K+竞争性结合同一个位 点,因为Ba2+ 浓度较低时,阻断的时间常数不随Ba2+浓度的增加而增减;由于阻断大小与Ba2+ 浓度相关 ,不会通过表面电荷机制进行IRK1-T阻断[4,5]。另一种机制是IRK1-T的多离 子阻断[6,7] ,Ba2+随着浓度的增加,其结合位点也越来越深入通道,说明Ba2+在IRK1-T 有一系列的结合 位点,因为Ba2+浓度较高时,阻断的时间常数随Ba2+浓度的增加而减少。Hill 方程的拟合可 以看出,细胞外K+为90 mmol/L, Hill系数在1左右,表明只有一个Ba2+进入通道进 行阻断, 不因Ba2+浓度增加而变化[8]。细胞外Ba2+浓度为100 μmol/L时,电 场距离分数 不超过0.5,这说明Ba2+对IRK1-T的阻断位点在选择性滤过器的细胞膜外侧[9 ]。
, 百拇医药
本文结论表明:两个野生型基因连接后表达的二聚体通道IRK1-T与四个野生型基因表达的 四 聚体通道IRK1不仅通道特性完全相同,而且通道阻断剂 Ba2+的作用也几乎完全相同 [10] 。这样一来IRK1-T完全可以用来做成变异基因,然后对变异基因进行功能研究。
致谢:感谢日本国立生理学研究所冈田泰伸教授提供资助并提供实验场所,老木成 念教授对 本文工作的悉心指导,三轮晃子小姐,Ravshan ZS和名古屋大学的鱼助信之副教授在分子生 物学技术上的帮助。加利福尼亚大学的Jan博士提供IRK1-T克隆。
基金项目: 国家自然科学基金(No.39840022)
参考文献:
[1] Kubo Y,Timothy J,Jan YN,et al. Primary structure and functional expression of a mouse inward rectifier potassium channel[J]. Nature,199 3,362(11):127.
, http://www.100md.com
[2] Ravshan ZS,Tominaga T,Miwa A,et al. A conserved arginine residue in t he preregion of an inward rectifier K channel (IRK1-T) as an external barrier for cationic blockers[J]. J Gen Physiol,1997,110:665.
[3] Oiki S,Yamamoto T, Okada Y. Apparent stability constants and purity of Ca-chelating agents evaluated using Ca-selective electrodes by the double-log optimization method[J]. Cell Calcium, 1994,15(3):209.
[4] Block BM,Stacey WC. Jones SW. Surface charge and lanthanum block of calciu m current in bullfrog sympathetic neurons[J]. Biophys J,1997,74 (86):2278.
, 百拇医药
[5] Mackinnon R. Latorre R,Miller C. Role of surface electrostatics in the ope ration of a high conductance Ca2+ activated K+ channel[J]. Biochemis try,1989,28(20):8092.
[6] Hille B. Ionic channels of excitable membranes[M]. ed2. MA Sunderland: S inauer,1992.350~361.
[7] Doyle DA,Cabra JM,Richard A,et al. The structure of the potassium chan nel: molecular Basis of K+ conduction and selectivity[J]. Science,1 998,2 80(3):69.
, 百拇医药
[8] Collins A,Chuang H,Jan YN,et al. Scanning mutagenesis of the putative transmembrane segment of Kir2.1, an inward rectifier potassium channel[J]. Proc Natl Acad Sci USA,1997,94(10):5456.
[9] Lee JK, John SA, Weiss JN. Novel gating mechanism of polyamine block in th e strong inward rectifier K channel Kir2.1[J]. J Gen Physiol,1999,113(4) :555.
[10]谢 安,臧益民. 细胞外Ba2+对内向整流钾通道(IRK1)的阻断作用[J]. 生 理学报, 2000,52(1):1
收稿 1999-09-23
修回 2000-02-14, 百拇医药
单位:谢安(第四军医大学基础部生理学教研室,陕西 西安 710033);臧益民(第四军医大学基础部生理学教研室,陕西 西安 710033);朱妙章(第四军医大学基础部生理学教研室,陕西 西安 710033)
关键词:钡;内向整流钾通道;电压钳;爪蟾卵母细胞
心脏杂志000501摘 要: 目的:研究Ba2+对非洲爪蟾卵母细胞表达的双 基因内向整流钾通道(IRK1-T )的阻断作用。方法:采用双微电极电压钳(TEV)法。结果:细胞外Ba2+浓度分别为1,3,10 和100 μmol/L,K+浓度为90 mmol/L,可见Ba2+的阻断作用对IRK1-T的瞬间电流( 施加电压后1 ms)具有 浓度依赖性、时间依赖性和电压依赖性;快速开通道阻断剂Ba2+对IRK1-T 的通道开 关特性几乎无影响作用,IRK1-T对之不通透。三级指数拟合表明:细胞外Ba2+低浓 度(1和3 μmol/L)时,Ba2+与K+相互竞争同一结合位点,随着Ba2+浓度的增 加,时间常数不增加但拟 合的权数却浓度依赖性增加,所以失活过程随Ba2+浓度的增加越来越快;细胞外Ba 2+高浓度 (10和100 μmol/L)时,时间常数随Ba2+浓度的增加而减少,拟合的权数却浓度依赖 性减少, 失活过程也越来越快,说明Ba2+作用位点由通道的表面部位进入通道更深的地方。[ HTH 结论:Ba2+对IRK1-T的阻断存在两种不同的机制。
, 百拇医药
中图分类号:Q424 文献标识码:A
文章编号:1005-3271(2000)05- 0345-04
The blocking effects of extracellular Ba2+ on the inward rectifier potassi um tandem channel
XIE An ZANG Yi-min ZHU Miao-zhang
(Department of Physiology, Basic Science Institute, Fourth Military Medical University, Xi'an Shaanxi 710032, China)
Abstract: AIM: The blocking effects of extracellular Ba2+ o n the inward rectifi er potassium tandem channel (IRK1-T) expressed in the Xenopus oocytes was studi e d. METHODS: Two-microelectrode voltage clamp (TEV) method was used. RESULTS: Ba2+ can concentration-, time- and volt age dependently block IRK1-T instanta neous currents ( 1ms after voltage applied ) when external Ba2+ concentrat ion is 1,3,10 or 100 μmol/L with 90 mmol/L potassium. Fast open channel blocker Ba 2+ almost has no effect on the open/close property of IRK1-T. IRK1-T can not per meate Ba2+. Three exponential fitting results indicate that Ba2+and K+ compete the same bi nding site in IRK1-T when external Ba2+ concentration (1 or 3 μmol/L) is lower. Time constants do not increase but the weights of the fittings concentration de pendently enhance as the external Ba2+ concentration augments. So the inac tivati on becomes faster and faster as the external Ba2+ concentration increases. Time constants decrease and the weights of the fittings concentration dependently enh ance as the external Ba2+ concentration augments when external Ba2+ concentratio n (10 or 100 μmol/L) is higher. So the inactivation becomes faster and faster. It is showed that Ba2+ can go deeper in IRK1-T from the surface of the ch annel a s external Ba2+ concentration increases. CONCLUSION: Two diffe rent mechanisms for external Ba2+ blocking exist.
, 百拇医药
Key words: barium; open channel blocker; inward rectifier potassium chan nel; tandem
Ba2+是双基因内向整流钾通道(IRK1-T)的开通道阻断剂[1] 。研究Ba2+对IRK1-T的阻 断作用不仅对于二价阳离子阻断IRK1-T的分子机制的研究有重要意义,而且对于了解IRK1 -T 的通道结构和功能也有很大帮助。以往的研究由于技术水平的限制,对通道瞬间电流的分析 不够准确(施加电压后10 ms)[1],因而采用的数据分析方法也不够准确[2] 。作者使用高质量电流曲线对Ba2+的阻断作用做了重新评价,以其得出较准确的分析 结论。
1 材料和方法
大鼠巨噬细胞系的 IRK cDNA是加利福尼亚大学Jan博士赠与的。mRNA的线性化由Xh o I酶完成,转录过程使用mCAPTM mRNA capping试剂盒(Stratagene Inc,La,Jolla,CA) ,由T3 聚合酶转录。mRNA的检测用凝胶电泳;其浓度测量用光谱仪,并于-80℃贮存。使用第Ⅴ和 Ⅵ期的非州爪蟾卵母细胞;在无钙的Barth液中使用胶原酶I(SIGMA,10 mg/10 ml) 处理1.5 h , 温度20℃, 用钠升注射器(Drummond Scientific) 将mRNA(浓度:1.85 ng/nl,注射30 ng )注入细胞内;在正常带有抗菌素的Barth液中孵育24 h后使用。
, 百拇医药
全细胞电流记录使用双微电极电压钳(TEV)法,放大器为CA-1(Dagan Corp).用两 个有 3M KCl的微电极刺入细胞中,一个(尖端电阻0.2~0.3 MΩ)做为电流注射电极,另一个(尖端 电阻约0.5 MΩ)做为电压记录电极,两个电极尖端的形态漏斗状,并且镀上Sylgard。第三 个 电极置于与细胞1 mm左右的距离用于感受细胞膜外的钳制电压。为了测量串联电阻,一个微 电极置于细胞上前方约5 μm处,串联电阻约0.2 KΩ,在需要的时候使用串联电阻补偿。使 用 一接地的金属板置于微电极之间以减少电容耦合干扰。另一个电流电极用于进行电容补偿, 旋转三个时间常数和三个相位延迟可以很好地进行电容补偿。漏电流在分析数据时再除去。
对照浴液中含有(mmol/L):90 KCl, 5 HEPES,3MgCl2和0.2 Niflumic acid(用于阻 断内源性Cl-电流),pH7.4。再将1,3,10和100 μmol/L的BaCl2加入对照浴液中。 换浴液时连续灌流速率约2.5~3 ml/min。指令电压由486计算机与Digi Data 1200 (A xon Instruments)产生。电流滤波频率为2 kHz,采样频率为10 kHz,数据的获取由pCLAMP6 (Axon)完成。 实验时室内温度为23~25℃。
, 百拇医药
数据分析采用pCLAMP6, Excel 97与Origin完成。阳离子剂量依赖性阻断数据用下式拟 合:
I/I0=(I/I0-U)/{1+([X]/Kd)}+U (1)
其中I/I0为阻断剂浓度为[X]时电流残留分数,Kd为平衡解离常数,U是在饱和的[ X]时电流不可阻断的分数。使用Hill方程做拟合
I/I0=Kdn/(Kdn+[X]n),其中n为Hill系数 (2)
对Ba2+、Mg2+和Mn2+阻断动力学分析是先采用三级指数函数的拟合
, 百拇医药
I=A1e-(t-k)/τ1+A2e-(t-k)/τ2+A3e-(t-k)/τ3 (3)
其中τ为时间常数,A为指数函数的权,K为进行拟合的起始时间。然后进行下式拟合
1/τ=K(0)e-δzFV/RT , K(0)=1/τ(0) (4)
其中δ为电场距离分数,z为阻断剂的离子价,F,R和T为三个常用的热力学常数。
数据由
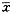 ±s表示,每组数据例数为3~4例。
±s表示,每组数据例数为3~4例。2 结果
, 百拇医药
Ba2+对IRK1-T瞬间内向电流有浓度依赖性阻断作用,细胞外Ba2+ 浓度越大 ,电流越小(图1A,B);这种阻断也同时具有电压依赖性,膜电位越大,阻断越明显。 Ba2+可加快IRK1-T的失活过程。这时反转电位没有变化,因而IRK1-T对Ba2+ 不通透(图1A,B)。Ba2+对IRK1-T 的通道开关特性几乎没有影响,规一化的电导几乎不受Ba2+的影响(图1C)。可见Ba 2+是一快 速的开通道阻断剂。使用指数拟合分析表明(图1D,E):细胞外Ba2+低浓度(1和3 μm ol/L) 时,随着Ba2+浓度的增加,时间常数不增加但拟合的权数却浓度依赖性增加,失活过 程随Ba2+ 浓度的增加越来越快,表示Ba2+与K+相互竞争同一结合位点;细胞外Ba2+高 浓度(10和100 μmol/L)时,时间常数随Ba2+浓度的增加而减少,拟合的权数却浓度依赖性减少,失 活过程 也越来越快,说明Ba2+作用位点由通道的表面部位进入通道更深的地方。细胞外Ba 2+浓度 增加时,平衡解离常数明显降低,说明Ba2+与IRK1-T的结合程度增加,也说明Ba 2+对IRK1- T的阻断作用还有浓度依赖性(图2A,B)。但细胞外K+浓度为90 mmol/L时,Hill系数为1 .01±0.34,可以看出只有一个Ba2+进入通道进行阻断。
, 百拇医药
3 讨论
内向整流钾通道(IRK1)广泛存在于骨骼肌细胞、心肌细胞、神经细胞、胶质细胞、 血细胞和内皮细胞等,可维持细胞的静息电位和控制细胞的兴奋性,例如IRK1参与了心肌复极 化,还可延长心室肌细胞动作电位时程,对心律失常的产生和防治有很大影响。对IRK1的各 个基因进行功能研究现通常采用基因变异方法,由于基因变异可导致IRK1的通透性改变,所 以纯粹用变异基因表达的四聚体通道通常记录不到电流。解决这个问题的方法通常有两种: 一是采用变异基因与野生型基因等比例混合,然后注入细胞[3] ;二是采用双 基因表达 的二聚体通道,双基因中一是野生型基因,另一基因可以做成变异基因,然后对变异基因进 行功能研究。后一种方法的关键在于两个野生型基因连接后表达的二聚体通道应与四个野生 型基因表达的四聚体通道不仅通道特性完全相同,而且通道阻断剂的作用也要完全相同 [9] 。作者就后一点做了详细研究。

, http://www.100md.com
图 1 Ba2+对IRK1-T 有浓度依赖性阻断作用
A:上图为未加Ba2+时的宏电流。下图为Ba2+浓度为10 μmol/L时的IRK1-T电 流。电压波宽为110 ms,幅度从+40 mV至-180 mV,增量为-20 mV,保持电压为-30 mV。B: 瞬间I-V曲线(施加电压后1 ms时)。数据为A中电流,Ba2+浓度分别为1,3 ,10和 100 μmol/L。C:规一化的IRK1-T电导。D:指数函数拟合的阻断的指数函数的权, 见公 式(3)。E:指数函数拟合的阻断的时间常数, 见公式(3)。细胞外Ba2+浓度100 μmol/L时,电场距离分数δ为0.49。

图2 Ba2+对IRK1-T平衡解离常数的作用
, 百拇医药
A:浓度依赖性Ba2+阻断。曲线为公式(1)的拟合曲线,细胞外K+浓度为90 mmol/L 时 ,Hill系数为1.01±0.34。膜电压-140 mV。B:电压依赖性平衡解离常数,由A中数据得 出。
Ba2+一直被认为是IRK1-T的快速开通道阻断剂,细胞外Ba2+可以电压 和时间依赖性地高 效地阻断IRK1-T。但以往所取得的通道电流仅在电压施加数ms后才能避开电容电流的影响 , 进而进行瞬间电流的分析,这样分析的准确性很差,例如以往报道Na+和Cs+也是IRK1- T的开 通道阻断剂[1],用本文的记录方法却得出相反的结论:Na+和Cs+(施加电压 后1 ms)可增 加通道的内向电流,不是IRK1-T的开通道阻断剂,作者较精确地证明Ba2+是IRK1-T 的快速开 通道阻断剂,但其瞬间电流的抑制作用却大大下降;而且以往对通道电流进行的拟合也采用 的是单指数函数的拟合,对于Ba2+对瞬间内向电流的抑制作用不能很好地拟合[ 1,2]。通过减 小电流电极尖端阻抗,用Sylgard涂电极尖端等多方改进,作者得到了施加电压后1 ms的高 质量电流曲线,并用三级指数函数对电流曲线进行了完美的拟合,分析的准确性大大提高 ,可得出下述众多以往未报道过的结果。
, http://www.100md.com
通过分析证实了Ba2+对IRK1-T的快速开通道阻断是Ba2+浓度、时间 和电压依赖性的 ,IRK1-T对Ba2+不通透,Ba2+对IRK1-T的通道开关特性也无影响。实验结果 表明Ba2+对IRK1 -T的阻断作用可通过两种不同的机制。一种机制是Ba2+与K+竞争性结合同一个位 点,因为Ba2+ 浓度较低时,阻断的时间常数不随Ba2+浓度的增加而增减;由于阻断大小与Ba2+ 浓度相关 ,不会通过表面电荷机制进行IRK1-T阻断[4,5]。另一种机制是IRK1-T的多离 子阻断[6,7] ,Ba2+随着浓度的增加,其结合位点也越来越深入通道,说明Ba2+在IRK1-T 有一系列的结合 位点,因为Ba2+浓度较高时,阻断的时间常数随Ba2+浓度的增加而减少。Hill 方程的拟合可 以看出,细胞外K+为90 mmol/L, Hill系数在1左右,表明只有一个Ba2+进入通道进 行阻断, 不因Ba2+浓度增加而变化[8]。细胞外Ba2+浓度为100 μmol/L时,电 场距离分数 不超过0.5,这说明Ba2+对IRK1-T的阻断位点在选择性滤过器的细胞膜外侧[9 ]。
, 百拇医药
本文结论表明:两个野生型基因连接后表达的二聚体通道IRK1-T与四个野生型基因表达的 四 聚体通道IRK1不仅通道特性完全相同,而且通道阻断剂 Ba2+的作用也几乎完全相同 [10] 。这样一来IRK1-T完全可以用来做成变异基因,然后对变异基因进行功能研究。
致谢:感谢日本国立生理学研究所冈田泰伸教授提供资助并提供实验场所,老木成 念教授对 本文工作的悉心指导,三轮晃子小姐,Ravshan ZS和名古屋大学的鱼助信之副教授在分子生 物学技术上的帮助。加利福尼亚大学的Jan博士提供IRK1-T克隆。
基金项目: 国家自然科学基金(No.39840022)
参考文献:
[1] Kubo Y,Timothy J,Jan YN,et al. Primary structure and functional expression of a mouse inward rectifier potassium channel[J]. Nature,199 3,362(11):127.
, http://www.100md.com
[2] Ravshan ZS,Tominaga T,Miwa A,et al. A conserved arginine residue in t he preregion of an inward rectifier K channel (IRK1-T) as an external barrier for cationic blockers[J]. J Gen Physiol,1997,110:665.
[3] Oiki S,Yamamoto T, Okada Y. Apparent stability constants and purity of Ca-chelating agents evaluated using Ca-selective electrodes by the double-log optimization method[J]. Cell Calcium, 1994,15(3):209.
[4] Block BM,Stacey WC. Jones SW. Surface charge and lanthanum block of calciu m current in bullfrog sympathetic neurons[J]. Biophys J,1997,74 (86):2278.
, 百拇医药
[5] Mackinnon R. Latorre R,Miller C. Role of surface electrostatics in the ope ration of a high conductance Ca2+ activated K+ channel[J]. Biochemis try,1989,28(20):8092.
[6] Hille B. Ionic channels of excitable membranes[M]. ed2. MA Sunderland: S inauer,1992.350~361.
[7] Doyle DA,Cabra JM,Richard A,et al. The structure of the potassium chan nel: molecular Basis of K+ conduction and selectivity[J]. Science,1 998,2 80(3):69.
, 百拇医药
[8] Collins A,Chuang H,Jan YN,et al. Scanning mutagenesis of the putative transmembrane segment of Kir2.1, an inward rectifier potassium channel[J]. Proc Natl Acad Sci USA,1997,94(10):5456.
[9] Lee JK, John SA, Weiss JN. Novel gating mechanism of polyamine block in th e strong inward rectifier K channel Kir2.1[J]. J Gen Physiol,1999,113(4) :555.
[10]谢 安,臧益民. 细胞外Ba2+对内向整流钾通道(IRK1)的阻断作用[J]. 生 理学报, 2000,52(1):1
收稿 1999-09-23
修回 2000-02-14, 百拇医药