人肝脏再生增强因子cDNA的克隆、表达及纯化
作者:陈世敏 蔡在龙 毛积芳
单位:陈世敏(第二军医大学基础医学部生物化学与分子生物学教研室, 上海 200433);蔡在龙(第二军医大学基础医学部生物化学与分子生物学教研室, 上海 200433);毛积芳(第二军医大学基础医学部生物化学与分子生物学教研室, 上海 200433)
关键词:肝再生;基因表达;纯化
第二军医大学学报000610 【摘要】 目的:克隆人肝脏再生增强因子(hALR) cDNA,构建重组表达载体并对其诱导表达、纯化。方法:提取胎儿肝组织总RNA,利用RT-PCR技术扩增出hALR cDNA,克隆于载体pGEM-T,酶切鉴定后亚克隆至表达载体pGEX-4T-3,测序证实序列正确并转化大肠杆菌BL21(DE3),IPTG诱导表达融合蛋白GST-hALR,表达产物通过谷胱甘肽 Sepharose 4B亲和层析纯化后进行Thrombin酶切。结果和结论:构建成融合蛋白GST-hALR的重组表达质粒,hALR在大肠杆菌高效表达,重组蛋白主要以可溶形式存在于胞质中,融合蛋白的分离纯化简单易行。
, 百拇医药
【中图分类号】 R 392.1 【文献标识码】 A
【文章编号】 0258-879X(2000)06-0534-03
Cloning,expression and purification of the human augmenter of liver regeneration (hALR) cDNA
CHEN Shi-Min,CAI Zai-Long,MAO Ji-Fang
(Department of Biochemistry & Molecular Biology, Department of Basic Medicine, Second Military Medical University, Shanghai 200433, China)
, http://www.100md.com
【ABSTRACT】 Objective: To clone human augmenter of liver regeneration (hALR) cDNA, construct the recombinant expression vector, express and purify its product. Methods: The hALR cDNA was obtained by using RT-PCR method with total RNA extracted from the fetal hepatic tissue. Then it was cloned into the pGEM-T vector, and subcloned into expression vector pGEX-4T-3.After proved to be correct by sequencing, recombinant expression plasmid pGEX-4T-3(hALR) was transformed into E.coli BL21(DE3). The fusion protein GST-hALR was produced by IPTG induction, isolated by affinity chromatography glutathione Sepharose 4B and cleaved by Thrombin. Results and Conclusion: Recombinant expression plasmid pGEX-4T-3(hALR) is constructed. The hALR is highly expressed in E.coli. The fusion protein in the plasma is resoluble. The procedure of purification and cleavage of fusion protein is easy and simple.
, http://www.100md.com
【KEY WORDS】 liver regeneration; gene expression; purification
人肝脏再生增强因子(hALR)是新近克隆到的一种热稳定性小分子促肝细胞增殖因子,其cDNA全长约1.4 kb,位于人第16条染色体上[1]。基因序列同源性分析发现hALR为酵母scERV1基因结构和功能上的同系物[2,3],scERV1基因是在线粒体生物起源和细胞周期调控中担负重要作用的双功能基因。ALR基因几乎在所有细胞和组织中都有低丰度表达,但在精子发生和损伤肝脏的再生过程中则出现高丰度表达[4]。1994年,Hagiya等[5,6]首先从含肝脏刺激物的胞液中分离纯化并克隆到了大鼠ALR cDNA,并通过犬的Eck瘘模型即门腔静脉吻合分流术证实了ALR的促肝细胞增殖作用。在此基础上,我们对hALR cDNA进行了克隆、表达及纯化,试图得到具有生物活性的hALR,为临床治疗严重肝病提供有效的药物。
, http://www.100md.com
1 材料和方法
1.1 质粒、宿主菌、胎肝 质粒pGEM-T, pGEX-4T-3,大肠杆菌DH5α, BL21(DE3)购自Promega公司;流产胎肝由长海医院妇产科提供。
1.2 试剂及试剂盒 100 bp DNA Ladder,TRIZOL试剂,逆转录试剂盒购自Gibco BRL公司; pGEM-T Vector System 购自Promega公司; GST Gene Fusion System购自Pharmacia Biotech公司。
1.3 引物序列 P1: 5′ G GGA TCC ATG CGG ACG CAG CAG AAG CGG GAC AC 3′;P2: 5′ GGA ATT CTA GTC ACA GGA GCC ATC CTT CCA GCC GTC G 3′。引物P1,P2分别包括BamHⅠ, EcoRⅠ识别位点(划线部分)。
, http://www.100md.com
1.4 总RNA的提取 取正常胎肝100 mg,用TRIZOL试剂抽提总RNA,甲醛变性琼脂糖凝胶电泳检查RNA的完整性,紫外分光光度法分析RNA的纯度及RNA含量。
1.5 逆转录反应、PCR扩增 2 μg总RNA和0.5 μg Oligo(dT)12~18溶于12 μl焦碳酸二乙酯处理的水中,70℃温育10 min后置于冰浴,加入10×PCR 缓冲液2 μl,25 mmol/L MgCl2 2 μl,10 mmol/L dNTP混合物1 μl,0.1 mol/L DTT 2 μl,短暂离心后42℃温育5 min。加入1 μl SuperScript RT(200 U),42℃温育50 min,70℃ 15 min 灭活酶活性,最后加入1 μl(2 U)RNase H,37℃ 20 min,以降解未逆转录的RNA。取上述制备的逆转录反应液2 μl,用本文设计的引物进行PCR扩增:94℃ 45 s, 56℃ 1 min, 72℃ 1 min,共35个循环。最后一次循环72℃ 延伸10 min。
, http://www.100md.com
1.6 PCR产物的克隆及重组转化子的鉴定 PCR产物经琼脂糖凝胶电泳、割胶、纯化,按pGEM-T Vector System试剂盒说明进行连接,连接液转化感受态大肠杆菌DH5α ,采用蓝白斑筛选,限制性内切酶分析鉴定重组转化子。
1.7 重组表达质粒的构建与筛选 鉴定过的重组转化子用EcoRⅠ,BamHⅠ双酶切,纯化后连接于用同样两种酶消化过的pGEX-4T-3表达载体中。重组质粒转化大肠杆菌BL21(DE3),在含有氨苄青霉素的LB培养基平板上筛选出阳性克隆。DNA测序由上海皓嘉公司完成。
1.8 融合蛋白的表达、纯化、电泳鉴定 含有重组质粒的大肠杆菌在含有氨苄青霉素的2-YT培养液中37℃振荡培养至D(600)=0.6~0.9,加入IPTG至终浓度0.2 mol/L诱导表达3 h。离心收集菌体后PBS悬浮超声破菌。1 000 r/min离心15 min,收集上清,进行纯化和蛋白酶消化。操作按GST Gene Fusion System说明进行。纯化的蛋白鉴定采用常规SDS-PAGE法鉴定。
, 百拇医药
2 结 果
2.1 RNA的完整性、纯度及定量 从胎肝提取的总RNA经甲醛变性琼脂糖凝胶电泳,可见明显的28 s,18 s和5 s条带,而且28 s的亮度大约是18 s的2倍,说明提取的总RNA基本没有降解,有较好的完整性。对RNA样品进行紫外分光光度分析得出D(260)/D(280)=0.157/0.075=2.1,说明RNA有较高的纯度,经紫外分光光度定量得出样品中RNA的含量为3 μg/μl。
2.2 PCR产物的大小鉴定 PCR产物进行琼脂糖凝胶电泳,可见片段大小约380 bp(图1),符合hALR cDNA可读框架的大小。
图 1 PCR产物琼脂糖凝胶电泳
Fig 1 Agarose gel electrophoresis of PCR products
, 百拇医药
A: 100 bp DNA ladder; B: PCR products
2.3 重组表达质粒的构建及目的序列的测定 构建融合蛋白GST-hALR的重组表达质粒如图2。表达质粒转化大肠杆菌BL21(DE3),测序证明序列正确,见图3。
2.4 融合蛋白表达、纯化及酶切电泳鉴定 SDS-PAGE分析显示(图4)重组菌在约4.1×104处出现一蛋白条带。融合蛋白前体谷胱甘肽S-转移酶约2.6×104,hALR约1.5×104。薄层扫描蛋白电泳结果表明,表达的融合蛋白占菌体蛋白总量的36.3%。
3 讨 论
ALR作为保肝因子最初是在部分肝切除后的再生肝脏以及初断乳的大鼠增生肝脏中分离、纯化和克隆得到的。Hagiya等[5]研究发现,基因重组产生的ALR与天然ALR具有相同的保肝效应。最初研究ALR的保肝效应是在已知ALR的物种非特异性的前提下,通过犬的Eck瘘模型进行的,即通过门腔静脉吻合分流术人为减少肝脏血液供应,并使左、右叶肝脏在相同的环境中独立行使功能。实验时一叶肝脏从外源泵入ALR,另一叶肝脏则作为内对照。结果发现,对照肝叶的肝细胞出现典型的Eck瘘损坏,而泵入ALR的肝叶其肝细胞具有正常的超微结构,而且能显著增强Eck瘘模型损伤后的细胞更新;加入抗ALR单克隆抗体能抵消此效应。目前,国内广泛应用从新生小牛肝、乳猪肝提取的促肝细胞增殖因子治疗重型病毒性肝炎,并取得较好疗效,但这些制剂受其来源、种源差异及其纯度的限制,应用推广受到较大的限定,而重组hALR则弥补了以上不足。因此,重组hALR的研究开发对于治疗肝炎、肝损伤、肝衰竭等肝脏疾病无疑将有着广阔的应用前景。我们采用GST Gene Fusion System表达hALR,其突出优点在于表达产率高,可溶形式存在的蛋白纯化步骤简单。融合蛋白中GST可与谷胱甘肽特异性结合,利用亲和层析法,表达产物经单位点酶切后再经凝胶过滤层析就可以得到纯化。另外,Adams 等[7]报道在胎鼠胰腺移植治疗糖尿病的研究中,ALR不仅能增加其移植的成功率,而且可减少用于成功的胎鼠胰腺移植所需的组织量。同时观察发现,在ALR存在的情况下,胎鼠胰腺移植受体的血糖水平转为正常后,不仅不出现过度补偿现象,而且能使其葡萄糖水平维持在正常大鼠的葡萄糖水平范围内。目前对ALR的理化性质及生物性能已有了一定的认识,但ALR的作用机制等仍有待于进一步研究。相信随着对ALR了解的逐步深入,必将能使ALR在临床疾病的治疗中发挥更大作用。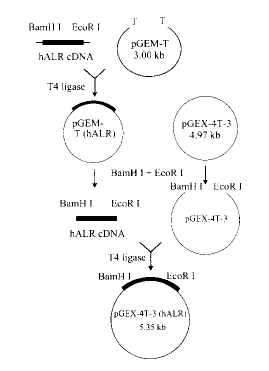
, 百拇医药
图 2 表达质粒pGEX-4T-3(hALR)的构建图
Fig 2 Schematic diagram of the construction
of the expression plasmid pGEX-4T-3(hALR)
图 3 人肝脏再生增强因子cDNA全序列
Fig 3 Sequence of human augmenter of
liver regeneration cDNA
, 百拇医药 图 4 表达蛋白的SDS-PAGE电泳
Fig 4 SDS-PAGE analysis of expressed protein
1: Molecular mass marker; 2: Purified fusion protein of hALR;3: Purified hALR cleavaged by Thrombin;4: Crude lysate of BL21(DE3) transformed by pGEX-4T-3;5: Crude lysate of BL21
(DE3) transformed by pGEX-4T-3(hALR)
【基金项目】国家自然科学基金资助项目(39600139)
【作者简介】陈世敏(1971~),女(汉族),硕士生
, 百拇医药
【参考文献】
[1] Giorda R, Hagiya M, Seki T, et al. Analysis of the structure and expression of the augmenter of liver regeneration(ALR) gene[J]. Mol Med, 1996, 2(1):97-108.
[2] Lisowsky T. Removal of an intron with unique 3′ branch site creates an amino terminal protein sequence directing the scERV1 gene product to mitochondria[J]. Yeast, 1996, 12(15):1501-1510.
[3] Stein G, Lisowsky T. Functional comparison of the yeast scERV1 and scERV2 genes[J]. Yeast, 1998, 14(3):171-180.
, 百拇医药
[4] Hofhaus G, Stein G, Polimeno L, et al. Highly divergent amino termini of the homologous human ALR and yeast scERV1 gene products define species specific differences in cellular localization[J]. Eur J Cell Biol, 1999, 78(5):349-356.
[5] Hagiya M, Francavilla A, Polimeno L, et al. Cloning and sequence analysis of the rat augmenter of liver regeneration(ALR) gene:expression of biologically active recombinant ALR and demonstration of tissue distribution[J]. Proc Natl Acad Sci USA, 1994, 91(17):8142-8146.
, http://www.100md.com
[6] Hagiya M, Francavilla A, Polimeno L, et al. Cloning and sequence analysis of the rat augmenter of liver regeneration(ALR) gene: expression of biologically active recombinant ALR and demonstration of tissue distribution[J]. Proc Natl Acad Sci USA, 1995, 92(12):3076.
[7] Adams GA, Maestri M, Squiers EC, et al. Augmenter of liver regeneration enhances the success rate of fetal pancreas transplantation in rodents[J]. Transplantation, 1998, 65(1): 32-36.
【收稿日期】2000-01-03
【修回日期】2000-04-10, http://www.100md.com
单位:陈世敏(第二军医大学基础医学部生物化学与分子生物学教研室, 上海 200433);蔡在龙(第二军医大学基础医学部生物化学与分子生物学教研室, 上海 200433);毛积芳(第二军医大学基础医学部生物化学与分子生物学教研室, 上海 200433)
关键词:肝再生;基因表达;纯化
第二军医大学学报000610 【摘要】 目的:克隆人肝脏再生增强因子(hALR) cDNA,构建重组表达载体并对其诱导表达、纯化。方法:提取胎儿肝组织总RNA,利用RT-PCR技术扩增出hALR cDNA,克隆于载体pGEM-T,酶切鉴定后亚克隆至表达载体pGEX-4T-3,测序证实序列正确并转化大肠杆菌BL21(DE3),IPTG诱导表达融合蛋白GST-hALR,表达产物通过谷胱甘肽 Sepharose 4B亲和层析纯化后进行Thrombin酶切。结果和结论:构建成融合蛋白GST-hALR的重组表达质粒,hALR在大肠杆菌高效表达,重组蛋白主要以可溶形式存在于胞质中,融合蛋白的分离纯化简单易行。
, 百拇医药
【中图分类号】 R 392.1 【文献标识码】 A
【文章编号】 0258-879X(2000)06-0534-03
Cloning,expression and purification of the human augmenter of liver regeneration (hALR) cDNA
CHEN Shi-Min,CAI Zai-Long,MAO Ji-Fang
(Department of Biochemistry & Molecular Biology, Department of Basic Medicine, Second Military Medical University, Shanghai 200433, China)
, http://www.100md.com
【ABSTRACT】 Objective: To clone human augmenter of liver regeneration (hALR) cDNA, construct the recombinant expression vector, express and purify its product. Methods: The hALR cDNA was obtained by using RT-PCR method with total RNA extracted from the fetal hepatic tissue. Then it was cloned into the pGEM-T vector, and subcloned into expression vector pGEX-4T-3.After proved to be correct by sequencing, recombinant expression plasmid pGEX-4T-3(hALR) was transformed into E.coli BL21(DE3). The fusion protein GST-hALR was produced by IPTG induction, isolated by affinity chromatography glutathione Sepharose 4B and cleaved by Thrombin. Results and Conclusion: Recombinant expression plasmid pGEX-4T-3(hALR) is constructed. The hALR is highly expressed in E.coli. The fusion protein in the plasma is resoluble. The procedure of purification and cleavage of fusion protein is easy and simple.
, http://www.100md.com
【KEY WORDS】 liver regeneration; gene expression; purification
人肝脏再生增强因子(hALR)是新近克隆到的一种热稳定性小分子促肝细胞增殖因子,其cDNA全长约1.4 kb,位于人第16条染色体上[1]。基因序列同源性分析发现hALR为酵母scERV1基因结构和功能上的同系物[2,3],scERV1基因是在线粒体生物起源和细胞周期调控中担负重要作用的双功能基因。ALR基因几乎在所有细胞和组织中都有低丰度表达,但在精子发生和损伤肝脏的再生过程中则出现高丰度表达[4]。1994年,Hagiya等[5,6]首先从含肝脏刺激物的胞液中分离纯化并克隆到了大鼠ALR cDNA,并通过犬的Eck瘘模型即门腔静脉吻合分流术证实了ALR的促肝细胞增殖作用。在此基础上,我们对hALR cDNA进行了克隆、表达及纯化,试图得到具有生物活性的hALR,为临床治疗严重肝病提供有效的药物。
, http://www.100md.com
1 材料和方法
1.1 质粒、宿主菌、胎肝 质粒pGEM-T, pGEX-4T-3,大肠杆菌DH5α, BL21(DE3)购自Promega公司;流产胎肝由长海医院妇产科提供。
1.2 试剂及试剂盒 100 bp DNA Ladder,TRIZOL试剂,逆转录试剂盒购自Gibco BRL公司; pGEM-T Vector System 购自Promega公司; GST Gene Fusion System购自Pharmacia Biotech公司。
1.3 引物序列 P1: 5′ G GGA TCC ATG CGG ACG CAG CAG AAG CGG GAC AC 3′;P2: 5′ GGA ATT CTA GTC ACA GGA GCC ATC CTT CCA GCC GTC G 3′。引物P1,P2分别包括BamHⅠ, EcoRⅠ识别位点(划线部分)。
, http://www.100md.com
1.4 总RNA的提取 取正常胎肝100 mg,用TRIZOL试剂抽提总RNA,甲醛变性琼脂糖凝胶电泳检查RNA的完整性,紫外分光光度法分析RNA的纯度及RNA含量。
1.5 逆转录反应、PCR扩增 2 μg总RNA和0.5 μg Oligo(dT)12~18溶于12 μl焦碳酸二乙酯处理的水中,70℃温育10 min后置于冰浴,加入10×PCR 缓冲液2 μl,25 mmol/L MgCl2 2 μl,10 mmol/L dNTP混合物1 μl,0.1 mol/L DTT 2 μl,短暂离心后42℃温育5 min。加入1 μl SuperScript RT(200 U),42℃温育50 min,70℃ 15 min 灭活酶活性,最后加入1 μl(2 U)RNase H,37℃ 20 min,以降解未逆转录的RNA。取上述制备的逆转录反应液2 μl,用本文设计的引物进行PCR扩增:94℃ 45 s, 56℃ 1 min, 72℃ 1 min,共35个循环。最后一次循环72℃ 延伸10 min。
, http://www.100md.com
1.6 PCR产物的克隆及重组转化子的鉴定 PCR产物经琼脂糖凝胶电泳、割胶、纯化,按pGEM-T Vector System试剂盒说明进行连接,连接液转化感受态大肠杆菌DH5α ,采用蓝白斑筛选,限制性内切酶分析鉴定重组转化子。
1.7 重组表达质粒的构建与筛选 鉴定过的重组转化子用EcoRⅠ,BamHⅠ双酶切,纯化后连接于用同样两种酶消化过的pGEX-4T-3表达载体中。重组质粒转化大肠杆菌BL21(DE3),在含有氨苄青霉素的LB培养基平板上筛选出阳性克隆。DNA测序由上海皓嘉公司完成。
1.8 融合蛋白的表达、纯化、电泳鉴定 含有重组质粒的大肠杆菌在含有氨苄青霉素的2-YT培养液中37℃振荡培养至D(600)=0.6~0.9,加入IPTG至终浓度0.2 mol/L诱导表达3 h。离心收集菌体后PBS悬浮超声破菌。1 000 r/min离心15 min,收集上清,进行纯化和蛋白酶消化。操作按GST Gene Fusion System说明进行。纯化的蛋白鉴定采用常规SDS-PAGE法鉴定。
, 百拇医药
2 结 果
2.1 RNA的完整性、纯度及定量 从胎肝提取的总RNA经甲醛变性琼脂糖凝胶电泳,可见明显的28 s,18 s和5 s条带,而且28 s的亮度大约是18 s的2倍,说明提取的总RNA基本没有降解,有较好的完整性。对RNA样品进行紫外分光光度分析得出D(260)/D(280)=0.157/0.075=2.1,说明RNA有较高的纯度,经紫外分光光度定量得出样品中RNA的含量为3 μg/μl。
2.2 PCR产物的大小鉴定 PCR产物进行琼脂糖凝胶电泳,可见片段大小约380 bp(图1),符合hALR cDNA可读框架的大小。

图 1 PCR产物琼脂糖凝胶电泳
Fig 1 Agarose gel electrophoresis of PCR products
, 百拇医药
A: 100 bp DNA ladder; B: PCR products
2.3 重组表达质粒的构建及目的序列的测定 构建融合蛋白GST-hALR的重组表达质粒如图2。表达质粒转化大肠杆菌BL21(DE3),测序证明序列正确,见图3。
2.4 融合蛋白表达、纯化及酶切电泳鉴定 SDS-PAGE分析显示(图4)重组菌在约4.1×104处出现一蛋白条带。融合蛋白前体谷胱甘肽S-转移酶约2.6×104,hALR约1.5×104。薄层扫描蛋白电泳结果表明,表达的融合蛋白占菌体蛋白总量的36.3%。
3 讨 论
ALR作为保肝因子最初是在部分肝切除后的再生肝脏以及初断乳的大鼠增生肝脏中分离、纯化和克隆得到的。Hagiya等[5]研究发现,基因重组产生的ALR与天然ALR具有相同的保肝效应。最初研究ALR的保肝效应是在已知ALR的物种非特异性的前提下,通过犬的Eck瘘模型进行的,即通过门腔静脉吻合分流术人为减少肝脏血液供应,并使左、右叶肝脏在相同的环境中独立行使功能。实验时一叶肝脏从外源泵入ALR,另一叶肝脏则作为内对照。结果发现,对照肝叶的肝细胞出现典型的Eck瘘损坏,而泵入ALR的肝叶其肝细胞具有正常的超微结构,而且能显著增强Eck瘘模型损伤后的细胞更新;加入抗ALR单克隆抗体能抵消此效应。目前,国内广泛应用从新生小牛肝、乳猪肝提取的促肝细胞增殖因子治疗重型病毒性肝炎,并取得较好疗效,但这些制剂受其来源、种源差异及其纯度的限制,应用推广受到较大的限定,而重组hALR则弥补了以上不足。因此,重组hALR的研究开发对于治疗肝炎、肝损伤、肝衰竭等肝脏疾病无疑将有着广阔的应用前景。我们采用GST Gene Fusion System表达hALR,其突出优点在于表达产率高,可溶形式存在的蛋白纯化步骤简单。融合蛋白中GST可与谷胱甘肽特异性结合,利用亲和层析法,表达产物经单位点酶切后再经凝胶过滤层析就可以得到纯化。另外,Adams 等[7]报道在胎鼠胰腺移植治疗糖尿病的研究中,ALR不仅能增加其移植的成功率,而且可减少用于成功的胎鼠胰腺移植所需的组织量。同时观察发现,在ALR存在的情况下,胎鼠胰腺移植受体的血糖水平转为正常后,不仅不出现过度补偿现象,而且能使其葡萄糖水平维持在正常大鼠的葡萄糖水平范围内。目前对ALR的理化性质及生物性能已有了一定的认识,但ALR的作用机制等仍有待于进一步研究。相信随着对ALR了解的逐步深入,必将能使ALR在临床疾病的治疗中发挥更大作用。

, 百拇医药
图 2 表达质粒pGEX-4T-3(hALR)的构建图
Fig 2 Schematic diagram of the construction
of the expression plasmid pGEX-4T-3(hALR)

图 3 人肝脏再生增强因子cDNA全序列
Fig 3 Sequence of human augmenter of
liver regeneration cDNA

, 百拇医药 图 4 表达蛋白的SDS-PAGE电泳
Fig 4 SDS-PAGE analysis of expressed protein
1: Molecular mass marker; 2: Purified fusion protein of hALR;3: Purified hALR cleavaged by Thrombin;4: Crude lysate of BL21(DE3) transformed by pGEX-4T-3;5: Crude lysate of BL21
(DE3) transformed by pGEX-4T-3(hALR)
【基金项目】国家自然科学基金资助项目(39600139)
【作者简介】陈世敏(1971~),女(汉族),硕士生
, 百拇医药
【参考文献】
[1] Giorda R, Hagiya M, Seki T, et al. Analysis of the structure and expression of the augmenter of liver regeneration(ALR) gene[J]. Mol Med, 1996, 2(1):97-108.
[2] Lisowsky T. Removal of an intron with unique 3′ branch site creates an amino terminal protein sequence directing the scERV1 gene product to mitochondria[J]. Yeast, 1996, 12(15):1501-1510.
[3] Stein G, Lisowsky T. Functional comparison of the yeast scERV1 and scERV2 genes[J]. Yeast, 1998, 14(3):171-180.
, 百拇医药
[4] Hofhaus G, Stein G, Polimeno L, et al. Highly divergent amino termini of the homologous human ALR and yeast scERV1 gene products define species specific differences in cellular localization[J]. Eur J Cell Biol, 1999, 78(5):349-356.
[5] Hagiya M, Francavilla A, Polimeno L, et al. Cloning and sequence analysis of the rat augmenter of liver regeneration(ALR) gene:expression of biologically active recombinant ALR and demonstration of tissue distribution[J]. Proc Natl Acad Sci USA, 1994, 91(17):8142-8146.
, http://www.100md.com
[6] Hagiya M, Francavilla A, Polimeno L, et al. Cloning and sequence analysis of the rat augmenter of liver regeneration(ALR) gene: expression of biologically active recombinant ALR and demonstration of tissue distribution[J]. Proc Natl Acad Sci USA, 1995, 92(12):3076.
[7] Adams GA, Maestri M, Squiers EC, et al. Augmenter of liver regeneration enhances the success rate of fetal pancreas transplantation in rodents[J]. Transplantation, 1998, 65(1): 32-36.
【收稿日期】2000-01-03
【修回日期】2000-04-10, http://www.100md.com