树立药品质量全程管理意识 强化医院药剂监督管理——北京市医院药剂管理的理论与实践
作者:张伟 杨小雷 连桂馨
单位:北京市卫生局
关键词:
首都医药000605 药品质量的全程管理是指运用科学合理的管理规范对药品研制、生产、检验、供应、使用及再评价诸环节实施全过程的质量控制,以保证药品的安全性和有效性。其过程用流程图来表示,即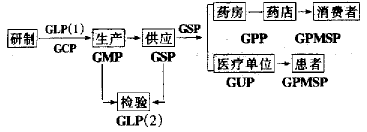
以上GLP(1)为药品非临床研究质量管理规范,GLP(2)为药品检验实验室质量管理规范,GCP为药品临床试验质量管理规范,GMP为药品生产质量管理规范,GSP为药品供应质量管理规范,GPP为药品调配质量管理规范,GUP为药品使用质量管理规范,GPMSP为药品上市后的监视质量管理规范。
就药品使用环节的质量监控而言,即医院药剂的监督管理,主要涉及两个方面:一是医院制剂(包括制剂的配制、灌装或分装、消毒、包装、检验等步骤);二是医院药品(包括药品的采购、贮存、供应、调配、使用诸环节)。
, 百拇医药
近年来,北京市卫生局在药品监督管理的实践中,积极贯彻药品质量全程管理的思想,在对药品研制、生产、供应等进行监督管理的同时,不断强化对医院药剂全过程的监督管理,具体开展了以下几项工作:
一、标本兼治,扶优汰劣,大力整顿医院制剂并取得成效
医院制剂是医院制剂室依照国家制定的药品生产工艺操作规程配制成的符合质量标准的药物制剂,它是满足医院临床、科研和教学用药的一种补充。然而,多年来由于某些原因,医院制剂管理方面一直是一个薄弱环节。
整顿前的基本情况。北京市共有医院500多家,其中取得《制剂许可证》的单位有143个,这些单位配制各类医院制剂8000多个,其中标准制剂[即《中国医院制剂规范》(第二册)和北京市医疗单位制剂规程1984年版收载的品种]近6000个,非标准制剂有3000余种。医院制剂存在着品种繁多、处方混乱、质量良莠不齐和监督管理松懈等问题,其原因剖析如下:
, 百拇医药
(1)一些制剂品种,药厂拥有正式批准的生产文号,但由于利润低、成本高或其他原因长期不生产,而医院临床又特殊需要,故由医院制剂室自行配制,作为商品药空缺的补充。
(2)某些制剂产品稳定性差,有效期短,在流通和贮存过程中易变质,故临床需及时配制,这些品种由制剂室生产则显得方便可行。
(3)有的制剂品种用量大,规格多,如肾透析液分为几种药液,于透析前按比例稀释混合使用,要根据病人病情的特殊需要使用不同规格的透析液。可见这类制剂专门由制剂室配制才容易达到要求。
(4)目前新药的研制投资大,风险高,周期长。为了满足临床和科研的需求,医院根据多年的经验筛选出一些处方以自配制剂的形式投入使用。这些品种中也不乏一些低水平重复生产、安全性和有效性未经严格科学论证、质量控制没有标准和配制工艺粗制滥造的制剂。
(5)近年来医院的评级达标工作对制剂品种也有一定数量的要求,致使不少医院制剂室盲目投资,制剂品种东拼西凑。
, 百拇医药
(6)随着我国经济体制的转轨,市场经济也被引入到了医院。少数医院受经济利益的驱使,非法配制或加工一些本不属于医院制剂范畴的制剂,还有个别医院未经批准就使用外埠医院的制剂。
(7)医院制剂的审批和配制尚缺少政策性和技术性法规,使得监管部门无法可依,加之技术把关不严,也是造成医院制剂品种过多过滥的原因之一。
采取的整治措施和对策。
(1)从1995年2月开始对医院制剂品种进行全面清理整顿。
首先,制订了工作程序和审查技术标准,出台了《医疗单位委托加工制剂管理办法(试行)》和《医疗单位制剂包装印制内容的规定(试行)》。
对于标准制剂,由区县卫生局初审,报市卫生局药政处登记备案,经市药检所进行技术审查后,统一核发批准文号,并编纂了批准文号汇编,这意味着医院制剂的管理由过去的备案制开始变为审批制。
, 百拇医药
对于非标准制剂,由区县卫生局初审后报市卫生局,再由医药学专家委员会对处方合理性、配制工艺、安全性、有效性和质量可控性进行审查,再经市药检所对样品进行试验技术复核,合格后统一发给批准文号。
(2)从1998年6月开始规范新制剂的申报。
制订并公布了《北京市医疗单位制剂审批办法(试行)》,进一步严格了医院制剂的申报技术标准。根据不同类别的制剂,按照相应的技术要求进行审核,分别发给批准文号:(年号)京卫药制试字[医院代号]第XXX号或(年号)京卫药制字[医院代号]第XXX号或(年号)京卫药制研字[医院代号]第XXX号。
(3)在清理整顿的基础上加强医院制剂的抽验,促进其质量的提高。
1999年3~4月,市卫生局对已获得制剂批准文号的10家医院的58个品种和59个批次的医院制剂进行了抽验,合格率93.2%,不合格率6.8%(不合格4件),另有7个品种的标签不符合规定。上述抽验结果在适当的场合予以公布,对医院制剂质量的提高起到了一定的警示作用和促进作用。
, 百拇医药
(4)在制剂整顿的基础上,着手编纂新版《医疗单位制剂规范》,进一步提高了质量控制要求。
(5)对医院制剂室实行许可证年检制度,要求覆盖率达100%。对医院制剂室的改造,坚持软硬件高标准,要求符合GMP的原则和规定。强化医院药检制度,要求提高自配制剂的全检率。严格控制新制剂室的开办和规模,避免卫生资源的浪费。
(6)加强对医院的日常监督检查,严厉打击非法制售医院制剂的行为。一方面通过制剂整顿,规范了制剂管理,促进了制剂质量的提高;另一方面通过查处伪劣制剂,通报重大案件,震慑了不法分子,也维护了医院制剂的声誉。
(7)针对医院制剂的一些热点、难点问题,组织医院药剂管理人员开展讨论,统一思想认识,如:医院制剂的委托加工、院外调剂、制剂的发展前景以及制剂中心等问题。
整顿后的基本情况。全市共有制剂141个,截止目前,获得批准文号制剂约占2/3,涉及全市215家医疗单位。经过整顿,全市有1/4~1/3的制剂品种经医院药事管理委员会初审和/或市卫生局医药学专家委员会审核后被淘汰,此外,部分品种均做了较大幅度的修改,特别是在质量控制方面。
, 百拇医药
二、积极探索,勇于实践,加强医院的药品管理工作
强化监督管理,规范医院药品的采购渠道。(1)颁布了《北京市卫生局药品采购管理监督暂行规定》,对药品采购程序、原则、渠道等做了具体规定,并制订了罚责。
(2)在全国率先推行药品推销员资格认定制度。要求本市药品生产经营企业的推销员必须经法规培训和考核合格后取得资格证书,到医院从事推销活动应持证书,医院对药品推销员所在单位和资格证书要进行备案。
(3)要求医院采购对供货单位进行资格认定,是进口药的,对进口检验报告书和《进口药品注册证》进行备案并保存二年以上,提供单位须加盖红章,以对文件的合法性负责。
(4)在全市医药供应网点不健全的农村地区实行医药一体化管理模式,推行乡卫生院向村卫生室和个体医生集中供药制度,杜绝假劣药品流入农村市场,从而危害广大农民的健康和生命的现象。集中供药不得从事经营性活动。
, 百拇医药
抓好整章建制,规范医院的调剂工作。(1)组织专家制订中西药品的调剂规程,为规范调剂工作打好基础。
(2)结合年检工作,重点对医院药库开展专项检查,要求条件比照药品经营企业(批发)药品库房的验收标准,改善了医院药品贮存的条件。
(3)开展精麻药品管理的专项检查,堵塞特殊管理药品非法流入社会的漏洞。在全国率先实行麻醉医师处方权资格证书制度,要求使用麻醉药品的医务人员须参加统一组织的法规培训和用药知识教育,经考核合格后发给资格证书。一方面规范了精麻药品的管理,另一方面促进了精麻药品的推广和合理使用。
(4)下发进一步加强临床用药管理的通知,规范临床试验用药的管理。对新药的临床试验限定研究单位数量和试验例数,对科研用药要求按照医院制剂申报程序进行审批。
完善组织机构,坚持开展药品不良反应监察工作。为了加强领导,理顺体制,保证药品不良反应监察工作的顺利开展,经市编办批准,北京市药品不良反应监察中心由挂靠北京地坛医院改为北京市药品监督办公室,人、财、物由市卫生局负责保障。该项工作由过去的民间操作过渡为现在的政府行为。全国第一个关于药品不良反应的专业杂志已于1999年下半年正式创刊。
, http://www.100md.com
三、以监督为主,帮促结合,保障医院药剂工作的顺利发展
“以监督为中心,监、帮、促相结合”是社会主义药品监管工作的指导方针,也是北京市药品监管工作的重要特色。
1.在药品监督管理体制发生变革的阶段,适时举办医院院长、药剂科主任参加的医院药剂管理研讨班,学习宣传药品管理法规,研究政策,转变观念,使医院药剂工作不断适应新时期药品监督管理的要求。
2.加强事前管理,保证新建、改建的制剂室顺利通过验收标准。做好政策咨询、施工图纸审查和现场勘查,避免医院制剂室的建设走弯路,减少资金浪费。
3.组织医院药剂科主任进行GMP企业的观摩活动。一方面密切了企业与医院的联系,另一方面引导医院的采购活动向优质、高效的方向发展。
4.充分发挥学会的桥梁作用,加强政府监管部门与医院的沟通联系。
, 百拇医药
(1)在北京药学会举办的学术活动中定期通报药品质量信息,为医院加强质量监控服务。通过《北京药品监督管理信息》和《首都医药》杂志及时转载国家药品监督管理法规,发布药品质量公报和假劣药品查处情况,传播医药信息。
(2)调动各方面积极性,开展上市药品的质量考察活动。这是一项政府指导、学会组织、专家把关、医院参与、企业资助和舆论导向评价药品质量的社会性活动。根据专家委员会的讨论意见,确定了在药品内在质量、临床疗效、药品价格、不良反应等方面容易出现问题的10个品种,组织有关医院的药检部门对多厂家、多批号进行质量考察试验工作,以期筛选出优质高效、价格合理的产品。一方面为医院购药择优汰劣和临床用药科学合理提供了参考依据,另一方面为药品监督管理部门监测药品质量、评价药品质量提供了参考结果,另一方面为加强医院学术交流,促进药检水平的提高提供了良好机会。, http://www.100md.com
单位:北京市卫生局
关键词:
首都医药000605 药品质量的全程管理是指运用科学合理的管理规范对药品研制、生产、检验、供应、使用及再评价诸环节实施全过程的质量控制,以保证药品的安全性和有效性。其过程用流程图来表示,即

以上GLP(1)为药品非临床研究质量管理规范,GLP(2)为药品检验实验室质量管理规范,GCP为药品临床试验质量管理规范,GMP为药品生产质量管理规范,GSP为药品供应质量管理规范,GPP为药品调配质量管理规范,GUP为药品使用质量管理规范,GPMSP为药品上市后的监视质量管理规范。
就药品使用环节的质量监控而言,即医院药剂的监督管理,主要涉及两个方面:一是医院制剂(包括制剂的配制、灌装或分装、消毒、包装、检验等步骤);二是医院药品(包括药品的采购、贮存、供应、调配、使用诸环节)。
, 百拇医药
近年来,北京市卫生局在药品监督管理的实践中,积极贯彻药品质量全程管理的思想,在对药品研制、生产、供应等进行监督管理的同时,不断强化对医院药剂全过程的监督管理,具体开展了以下几项工作:
一、标本兼治,扶优汰劣,大力整顿医院制剂并取得成效
医院制剂是医院制剂室依照国家制定的药品生产工艺操作规程配制成的符合质量标准的药物制剂,它是满足医院临床、科研和教学用药的一种补充。然而,多年来由于某些原因,医院制剂管理方面一直是一个薄弱环节。
整顿前的基本情况。北京市共有医院500多家,其中取得《制剂许可证》的单位有143个,这些单位配制各类医院制剂8000多个,其中标准制剂[即《中国医院制剂规范》(第二册)和北京市医疗单位制剂规程1984年版收载的品种]近6000个,非标准制剂有3000余种。医院制剂存在着品种繁多、处方混乱、质量良莠不齐和监督管理松懈等问题,其原因剖析如下:
, 百拇医药
(1)一些制剂品种,药厂拥有正式批准的生产文号,但由于利润低、成本高或其他原因长期不生产,而医院临床又特殊需要,故由医院制剂室自行配制,作为商品药空缺的补充。
(2)某些制剂产品稳定性差,有效期短,在流通和贮存过程中易变质,故临床需及时配制,这些品种由制剂室生产则显得方便可行。
(3)有的制剂品种用量大,规格多,如肾透析液分为几种药液,于透析前按比例稀释混合使用,要根据病人病情的特殊需要使用不同规格的透析液。可见这类制剂专门由制剂室配制才容易达到要求。
(4)目前新药的研制投资大,风险高,周期长。为了满足临床和科研的需求,医院根据多年的经验筛选出一些处方以自配制剂的形式投入使用。这些品种中也不乏一些低水平重复生产、安全性和有效性未经严格科学论证、质量控制没有标准和配制工艺粗制滥造的制剂。
(5)近年来医院的评级达标工作对制剂品种也有一定数量的要求,致使不少医院制剂室盲目投资,制剂品种东拼西凑。
, 百拇医药
(6)随着我国经济体制的转轨,市场经济也被引入到了医院。少数医院受经济利益的驱使,非法配制或加工一些本不属于医院制剂范畴的制剂,还有个别医院未经批准就使用外埠医院的制剂。
(7)医院制剂的审批和配制尚缺少政策性和技术性法规,使得监管部门无法可依,加之技术把关不严,也是造成医院制剂品种过多过滥的原因之一。
采取的整治措施和对策。
(1)从1995年2月开始对医院制剂品种进行全面清理整顿。
首先,制订了工作程序和审查技术标准,出台了《医疗单位委托加工制剂管理办法(试行)》和《医疗单位制剂包装印制内容的规定(试行)》。
对于标准制剂,由区县卫生局初审,报市卫生局药政处登记备案,经市药检所进行技术审查后,统一核发批准文号,并编纂了批准文号汇编,这意味着医院制剂的管理由过去的备案制开始变为审批制。
, 百拇医药
对于非标准制剂,由区县卫生局初审后报市卫生局,再由医药学专家委员会对处方合理性、配制工艺、安全性、有效性和质量可控性进行审查,再经市药检所对样品进行试验技术复核,合格后统一发给批准文号。
(2)从1998年6月开始规范新制剂的申报。
制订并公布了《北京市医疗单位制剂审批办法(试行)》,进一步严格了医院制剂的申报技术标准。根据不同类别的制剂,按照相应的技术要求进行审核,分别发给批准文号:(年号)京卫药制试字[医院代号]第XXX号或(年号)京卫药制字[医院代号]第XXX号或(年号)京卫药制研字[医院代号]第XXX号。
(3)在清理整顿的基础上加强医院制剂的抽验,促进其质量的提高。
1999年3~4月,市卫生局对已获得制剂批准文号的10家医院的58个品种和59个批次的医院制剂进行了抽验,合格率93.2%,不合格率6.8%(不合格4件),另有7个品种的标签不符合规定。上述抽验结果在适当的场合予以公布,对医院制剂质量的提高起到了一定的警示作用和促进作用。
, 百拇医药
(4)在制剂整顿的基础上,着手编纂新版《医疗单位制剂规范》,进一步提高了质量控制要求。
(5)对医院制剂室实行许可证年检制度,要求覆盖率达100%。对医院制剂室的改造,坚持软硬件高标准,要求符合GMP的原则和规定。强化医院药检制度,要求提高自配制剂的全检率。严格控制新制剂室的开办和规模,避免卫生资源的浪费。
(6)加强对医院的日常监督检查,严厉打击非法制售医院制剂的行为。一方面通过制剂整顿,规范了制剂管理,促进了制剂质量的提高;另一方面通过查处伪劣制剂,通报重大案件,震慑了不法分子,也维护了医院制剂的声誉。
(7)针对医院制剂的一些热点、难点问题,组织医院药剂管理人员开展讨论,统一思想认识,如:医院制剂的委托加工、院外调剂、制剂的发展前景以及制剂中心等问题。
整顿后的基本情况。全市共有制剂141个,截止目前,获得批准文号制剂约占2/3,涉及全市215家医疗单位。经过整顿,全市有1/4~1/3的制剂品种经医院药事管理委员会初审和/或市卫生局医药学专家委员会审核后被淘汰,此外,部分品种均做了较大幅度的修改,特别是在质量控制方面。
, 百拇医药
二、积极探索,勇于实践,加强医院的药品管理工作
强化监督管理,规范医院药品的采购渠道。(1)颁布了《北京市卫生局药品采购管理监督暂行规定》,对药品采购程序、原则、渠道等做了具体规定,并制订了罚责。
(2)在全国率先推行药品推销员资格认定制度。要求本市药品生产经营企业的推销员必须经法规培训和考核合格后取得资格证书,到医院从事推销活动应持证书,医院对药品推销员所在单位和资格证书要进行备案。
(3)要求医院采购对供货单位进行资格认定,是进口药的,对进口检验报告书和《进口药品注册证》进行备案并保存二年以上,提供单位须加盖红章,以对文件的合法性负责。
(4)在全市医药供应网点不健全的农村地区实行医药一体化管理模式,推行乡卫生院向村卫生室和个体医生集中供药制度,杜绝假劣药品流入农村市场,从而危害广大农民的健康和生命的现象。集中供药不得从事经营性活动。
, 百拇医药
抓好整章建制,规范医院的调剂工作。(1)组织专家制订中西药品的调剂规程,为规范调剂工作打好基础。
(2)结合年检工作,重点对医院药库开展专项检查,要求条件比照药品经营企业(批发)药品库房的验收标准,改善了医院药品贮存的条件。
(3)开展精麻药品管理的专项检查,堵塞特殊管理药品非法流入社会的漏洞。在全国率先实行麻醉医师处方权资格证书制度,要求使用麻醉药品的医务人员须参加统一组织的法规培训和用药知识教育,经考核合格后发给资格证书。一方面规范了精麻药品的管理,另一方面促进了精麻药品的推广和合理使用。
(4)下发进一步加强临床用药管理的通知,规范临床试验用药的管理。对新药的临床试验限定研究单位数量和试验例数,对科研用药要求按照医院制剂申报程序进行审批。
完善组织机构,坚持开展药品不良反应监察工作。为了加强领导,理顺体制,保证药品不良反应监察工作的顺利开展,经市编办批准,北京市药品不良反应监察中心由挂靠北京地坛医院改为北京市药品监督办公室,人、财、物由市卫生局负责保障。该项工作由过去的民间操作过渡为现在的政府行为。全国第一个关于药品不良反应的专业杂志已于1999年下半年正式创刊。
, http://www.100md.com
三、以监督为主,帮促结合,保障医院药剂工作的顺利发展
“以监督为中心,监、帮、促相结合”是社会主义药品监管工作的指导方针,也是北京市药品监管工作的重要特色。
1.在药品监督管理体制发生变革的阶段,适时举办医院院长、药剂科主任参加的医院药剂管理研讨班,学习宣传药品管理法规,研究政策,转变观念,使医院药剂工作不断适应新时期药品监督管理的要求。
2.加强事前管理,保证新建、改建的制剂室顺利通过验收标准。做好政策咨询、施工图纸审查和现场勘查,避免医院制剂室的建设走弯路,减少资金浪费。
3.组织医院药剂科主任进行GMP企业的观摩活动。一方面密切了企业与医院的联系,另一方面引导医院的采购活动向优质、高效的方向发展。
4.充分发挥学会的桥梁作用,加强政府监管部门与医院的沟通联系。
, 百拇医药
(1)在北京药学会举办的学术活动中定期通报药品质量信息,为医院加强质量监控服务。通过《北京药品监督管理信息》和《首都医药》杂志及时转载国家药品监督管理法规,发布药品质量公报和假劣药品查处情况,传播医药信息。
(2)调动各方面积极性,开展上市药品的质量考察活动。这是一项政府指导、学会组织、专家把关、医院参与、企业资助和舆论导向评价药品质量的社会性活动。根据专家委员会的讨论意见,确定了在药品内在质量、临床疗效、药品价格、不良反应等方面容易出现问题的10个品种,组织有关医院的药检部门对多厂家、多批号进行质量考察试验工作,以期筛选出优质高效、价格合理的产品。一方面为医院购药择优汰劣和临床用药科学合理提供了参考依据,另一方面为药品监督管理部门监测药品质量、评价药品质量提供了参考结果,另一方面为加强医院学术交流,促进药检水平的提高提供了良好机会。, http://www.100md.com