基因修饰细胞移植治疗大鼠脊髓损伤的电生理评价
作者:余科炜 叶晓健 冯红 曲伸 李家顺 路长林
单位:余科炜(武警上海总队医院骨科,上海201103);叶晓健(第二军医大学长征医院骨科,上海200003);冯红(第二军医大学长海医院药学部);曲伸(长海医院内分泌科);李家顺(第二军医大学长征医院骨科,上海200003)
关键词:脊髓损伤;基因修饰;成肌细胞;移植;电生理;神经营养因子,脑源性
第二军医大学学报000707 [摘要] 目的:采用神经电生理检查方法,观察逆转录病毒载体介导脑源性神经营养因子(BDNF)基因修饰成肌细胞对损伤脊髓的治疗作用。方法:30只SD大鼠在T9水平制成脊髓横断损伤模型,并随机分为基因细胞组(A组)、成肌细胞组(B组)及损伤对照组(C组),每组10只大鼠。术后3个月,采用皮质体感诱发电位(CSEP)和运动诱发电位(MEP)等电生理检测技术,观察轴突是否有再生及其神经功能恢复程度。结果:(1)A组中3只大鼠损伤3个月后出现CSEP波,5只出现MEP波,B,C组动物未发现电生理信号恢复; (2)重新出现的CSEP或MEP信号均较损伤前波幅减低,潜伏期延长。结论:BDNF基因修饰细胞脊髓内移植能有效促进损伤的脊髓神经部分传导功能恢复。
, 百拇医药
[中图分类号] R 651.205 [文献标识码] A
[文章编号] 0258-879X(2000)07-0621-04
Neurophysiological study on intraspinal implantation of genetically modified myoblast treating SCI in rats
YE Xiao-Jian LI Jia-Shun
(Department of Orthopaedics, Changzheng Hospital, Second Military Medical University, Shanghai 200003, China)
YU Ke-Wei
, 百拇医药
(Department of Othorpaedics, Shanghai Municipal Corps Hospital, 201103)
FENG Hong
(Department of Pharmacology, Changhai Hospital, Second Military Medical university)
QU Shen
(Department of Endocrine, Changhai Hospital)
LU Chang-Lin
(Department of Neurobiology, Department of Basic Medicine)
, 百拇医药
[ABSTRACT] Objective: To observe the value of gene therapy on SCI in vivo by transferring brain-derived neurotrophic factor (BDNF) to rat myoblast with retroviral vector using electrophysiological examination. Methods: Transection of spinal cord at the level of T9 were produced in 30 adult SD rats which were randomly divided into 3 groups (n=10): BDNF gene modified myoblast implantation (Group A), myoblast implantation (Group B) and without cell implantation as control (Group C). Three months after operation, whether the axon regenerated and how the neural function restored was observed by using cerebral somatosensory evoked potential (CSEP) and motor evoked potential (MEP). Results: (1) Thtee months after injury, 3 rats in Group A had CSEP signals and 5 rats had MEP signals, while no electrophysiological response was found in Group B or Group C. (2) The amplitudes of the recovered CSEP or MEP signals decreased and their latencies increased, comparing with those before injury. Conclusion: Treatment with genetically engineered myoblasts producing BDNF can accelerate recovery of traumatic spinal cord injury in adult rats.
, 百拇医药
[KEY WORDS] spinal cord injuries; genetically modified; myoblast; implantation; electrophysiology; neurotrophic factor, brain-derived
中枢神经系统(CNS)损伤后再生修复的研究一直是神经科学领域的前沿课题之一。过去认为,CNS损伤后神经元或轴突不能再生。但现代观点认为哺乳动物CNS损伤后神经元/轴突仍有再生潜力,并能形成新的突触联系,只是由于CNS内部微环境不适合,致使绝大部分轴突的再生努力归于失败,即所谓“夭折性再生(abortive regeneration)”[1]。其中神经营养因子或诱导因子不足是最重要的限制因素之一。由于血-脑屏障的影响,给予外源性神经营养因子的疗效不佳。而采用神经营养因子基因修饰细胞移植已被公认为最新、最有前途的治疗方法之一。此外,有关CNS损伤后神经功能损伤及恢复程度的判定,迫切需要有一种客观、定量的检测方法。本研究将脑源性营养因子(BDNF)基因修饰的成肌细胞移植到损伤脊髓内,探讨基因治疗脊髓损伤(SCI)的可行性,并采用包括体感诱发电位(somatosensory evoked potential, SEP)和运动诱发电位(motor evoked potential, MEP)在内的电生理检测技术验证其有效性,为将来基因治疗脊髓损伤应用于人类提供实验依据。
, 百拇医药
1 材料和方法
1.1 脊髓损伤模型与分组 30只成年SD大鼠,体质量(210±40)g,雌雄不限,由第二军医大学实验动物中心提供。按Tuszynski等[2]法制备大鼠脊髓横断伤模型。损伤水平位于T9。随机分为BDNF基因修饰成肌细胞组(A组)、成肌细胞组(B组)及损伤对照组(C组),每组10只大鼠。
1.2 BDNF基因修饰成肌细胞和成肌细胞的脊髓内移植 首先制备BDNF基因修饰的大鼠成肌细胞[3]。应用细胞悬液定向注射法分别注射基因细胞与成肌细胞至大鼠脊髓损伤区(悬液中细胞密度为2×104/μl)。损伤对照组无细胞移植。
1.3 皮质体感诱发电位(CSEP)检查 所有动物术前及术后3个月行CSEP检查。先分离动物左后肢坐骨神经,将其置于双极钩状银丝电极上,周围以温石蜡油保护。经Nihon Kohden 电刺激仪(日本)给予直流方波电脉冲刺激,强度50 mA,波宽0.1 ms,频率3 Hz。记录电极置于动物右侧感觉皮质表面,参考电极插入左额皮下。信号以FA-92放大器(第二军医大学生理学教研室)放大,滤波带通100~1 000 Hz,平均200次,电脑采样并贮存信号。
, 百拇医药
1.4 运动诱发电位(MEP)检查 各组大鼠术前及术后3个月行MEP检查。动物俯卧于立体定位架上,用特制棘突夹固定C7和S2棘突以稳定脊柱。将一枚直径1 mm银球电极(阴极)置于右侧感觉运动皮质表面,另一枚EEG针电极(阳极)插入硬腭粘膜下作参考。经刺激仪和隔离器发出单个方波电脉冲刺激,强度50 mA,波宽0.1 ms,频率5 Hz,每次记录重复刺激50~100次。记录电极置于T12脊髓背侧硬膜表面,另一枚电极置于邻近脊旁肌作参考。局部以温石蜡油保护。大鼠颈部皮下置铜片作为接地电极。信号以FA-92放大器放大,滤波带通100~1 000 Hz,平均50次,储存于电脑以备后续打印分析。
1.5 统计学处理 实验结果采用Foxpro 3.0数据库软件录入实验数据,经计算机统计处理,结果以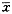 ±s表示。均值间差异采用t检验,各组间差异采用F检验,各组均数的比较采用方差分析(ANOVA)检验。
±s表示。均值间差异采用t检验,各组间差异采用F检验,各组均数的比较采用方差分析(ANOVA)检验。
, 百拇医药
2 结 果
2.1 基因细胞移植治疗大鼠SCI的电生理学表现
2.1.1 CSEP检查结果 所有大鼠受伤前均获得正常CSEP信号,包括一个负向波,平均潜伏期(1.74±0.06)ms,平均波幅(66.4±20.2)mV。受伤后各组动物CSEP信号均消失,而BDNF基因修饰细胞移植后3个月,A组中3只大鼠有信号恢复,但其波幅较伤前明显下降,潜伏期也明显延迟。另两组动物未见有信号恢复(表1)。
表 1 基因细胞移植对SCI大鼠CSEP的影响
Tab 1 CSEP in SCI rats treated with intraspinal
implantation of BDNF gene modified myoblast(n=10,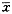 ±s) Group
±s) Group
, 百拇医药
Before
injury
Just after
injury
3 month after
injury
Amp
(U/mV)
Lan
(t/ms)
Amp
(U/mV)
, 百拇医药
Lan
(t/ms)
Amp
(U/mV)
Lan
(t/ms)
A
60.2±
18.5
1.77±
0.06……
14.7±
7.5**
, http://www.100md.com
1.82±
0.21*
B
65.7±
20.4
1.74±
0.08…………
C
73.3±22.7
1.72±
0.11…………
Amp: Amplitude; Lan: Latency; * P<0.05, ** P<0.01 vs before injury2.1.2 MEP检查结果 所有大鼠受伤前均获得正常MEP信号,典型的MEP信号包括3~4个负波组成的早期成分,依次记为N1,N2,N3和N4,较晚出现(10 ms以后)的一个负向波记为Nlate。由于其他波峰或者不够稳定,或者波幅太低,因此本研究中以N1为计量指标。考虑基线不稳定和刺激伪迹的影响,其波幅以负向波峰至相邻正向波峰距离计算,潜伏期以刺激伪迹开始至各波峰的时间计算。发现受伤前平均潜伏期(16.8±2.0)ms,平均波幅(27.2±11.4)mV。受伤后各组动物MEP信号均消失,而BDNF基因修饰细胞移植后3个月,A组中5只大鼠MEP信号早期成分有所恢复,但其波幅较伤前明显下降,潜伏期也明显延迟。另两组动物未见有信号恢复(表2)。
, 百拇医药
表 2 基因细胞移植对SCI大鼠MEP的影响
Tab 2 MEP in SCI rats treated with intraspinal
implantation of BDNF gene modified myoblast(n=10,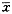 ±s) Group
±s) Group
Before
injury
Just after
injury
3 month after
, http://www.100md.com injury
Amp
(U/mV)
Lan
(t/ms)
Amp
(U/mV)
Lan
(t/ms)
Amp
(U/mV)
Lan
(t/ms)
, 百拇医药
A
31.2±
11.2
16.8±
2.0……
5.7±3.5**
21.5±
2.2*
B
24.5±
10.3
17.2±
, 百拇医药
2.1…………
C
25.8±12.0
16.3±
1.7…………
* P<0.05, ** P<0.01 vs before injury3 讨 论
近年来神经营养因子(neurotrophic Factors, NTFs)的发现为SCI的治疗带来了新的希望。NTFs是神经系统最重要的生物活性因子之一,其中BDNF多见于中枢神经组织,包括脑和脊髓。除了诱导神经突起定向生长,决定感觉和交感神经纤维生长方向等NGF所具有的效应外,它还具有运动神经元营养活性,能保护脊髓运动神经元在SCI后免于死亡[4]。但是,采用周围或脑室内给药的方法并不能使BDNF在损伤的脊髓节段发挥生理效应,必须建立新的途径来达到营养作用。通过基因转移来治疗SCI已经成为新的研究热点,也就是将某种神经营养因子基因以一定的方法转染给合适的受体细胞,再移植到脊髓损伤区,让其在体内表达并发挥效应,刺激脊髓再生。本研究即是将BDNF基因转染至作为受体细胞的成肌细胞,使之携带BDNF基因,移植入脊髓后受体细胞源源不断地分泌BNDF,从而发挥其神经营养作用。实验结果表明,基因细胞移植3个月后受伤脊髓的神经功能有显著改善,说明BDNF基因细胞移植入脊髓能够存活并发挥作用。判断和对照各种SCI治疗方法的效果,必须有一项客观、定量的评估手段。SEP技术已成功用于脊髓损伤诊断多年 [5] 。但是近年来有关研究证实,SEP不一定能完全反映SCI程度[5,6] ,理由是SEP信号主要经脊髓后索传导,而不是由脊髓前索和侧索上递。而支配肢体运动的锥体束主要分布在脊髓侧索和前索,在椎体爆裂骨折中受损机会更多,单纯依靠SEP检查显然不能满足需要。MEP是刺激中枢神经组织并在脊髓远端、外周神经或肌肉记录到的电信号,能直接反映脊髓下行传导束或外周运动神经的功能状态[7,8]。本研究发现,BDNF基因修饰细胞移植3个月后,部分大鼠CSEP和MEP信号恢复,但波幅减低,潜伏期延长。说明神经轴突已经再生并通过损伤断端,而基因细胞所分泌的BNDF促进了轴突的再生。通过后肢功能的检查,基因细胞移植组较对照组也有显著的改进。上述结果说明,BDNF基因转染成肌细胞移植入脊髓是成功的,结合HRP逆行示踪染色和神经元及神经纤维图像分析技术等病理学检查的阳性结果(另文报道),进一步证明基因治疗脊髓损伤是可行的。同时也说明,CSEP和MEP均可准确反映SCI后脊髓神经功能状态,也有助于在实验研究中客观、定量地分析各类治疗方法对促进神经功能恢复的效果。
, 百拇医药
本研究还发现,MEP伤后恢复出现率较CSEP更高,信号也更为明显。其中可能的解释有两种:(1)BDNF基因修饰细胞对运动轴突再生的促进作用强于对感觉轴突;(2)MEP信号较CSEP信号更为灵敏,可以测出更微弱的神经电传导。而后一点在我们以往的研究中已经得到证实。当然本实验的成功并不表明脊髓损伤的基因治疗马上可以进入临床,目前转基因技术治疗脊髓损伤仍然存在一些问题:(1)目的基因:目前的研究主要是将NTFs基因作为目的基因,但NTFs的作用只是单方面的,尚不能完全解决脊髓再生;(2)载体:目前无论是病毒还是非病毒技术,转基因的安全性和感染率都有待解决;(3)免疫原性:尽管中枢神经系统有一定的免疫豁免性,但仍然存在免疫排斥反应。解决这一问题的方法一是发展免疫隔离技术,二是开展自体细胞移植技术;(4)受体细胞在脊髓内长期存活和持续表达仍未完全解决。对上述问题,我们将在本实验研究成功的基础上,在细胞移植的技术和方法、基因表达的调控等方面进行大量的、更深入的研究,以期尽早过渡到临床,为脊髓损伤患者造福。
基金项目:国家自然科学基金资助项目(39600147)
, 百拇医药
作者简介:余科炜(1970-),男(汉族),博士,主治医师。
作者单位:路长林(基础医学部神经生物学教研室)
[参 考 文 献]
[1] Weidner N, Grill RJ, Tuszynski MH. Related articles elimination of basal lamina and the collagen "scar" after spinal cord injury fails to augment corticospinal tract regeneration [J]. Exp Neurol, 1999, 160(1):40-50.
[2] Tuszynski MH, Meyers G, Nakahara Y, et al. Fibroblast and Schwann cells genetically modified to produce neurotrophic factors induce robust neuritic growth after transplantation to the spinal cord [J]. Soc Neurosci Abstr, 1994, 20(1):10-15.
, 百拇医药
[3] 叶晓健,申准斌,冯 红. 逆转录病毒载体介导脑源性神经营养因子基因转染大鼠成肌细胞 [J]. 中国学术期刊文摘, 1999, 5(7):917-922.
[4] Jakeman LB, Wei P, Guan Z, et al. Related articles brain-derived neurotrophic factor stimulates hindlimb stepping and sprouting of cholinergic fibers after spinal cord injury [J]. Exp Neurol, 1998, 154(1):170-184.
[5] Restuccia D, Di Lazzaro V, Valeriani M, et al. Related articles spinal responses to median and tibial nerve stimulation and magnetic resonance imaging in intramedullary cord lesions [J]. Neurology, 1996, 46(6):1706-1714.
, http://www.100md.com
[6] Nashmi R, Imamura H, Tator CH, et al. Serial recording of somatosensory and myoelectric motor evoked potentials: role in assessing functional recovery after graded spinal cord injury in the rat [J]. J Neurotrau , 1997, 14(1):151-159.
[7] Di Lazzaro V, Oliviero A, Profice P, et al. The diagnostic value of motor evoked potentials [J]. Clin Neurophysiol, 1999, 110(7):1297-1307
[8] 孙天胜, 胥少汀. 实验性脊髓损伤的运动诱发电位检测价值 [J]. 中华外科杂志, 1991, 29(4):472-476.
[收稿日期] 2000-02-22
[修回日期] 2000-06-12, 百拇医药
单位:余科炜(武警上海总队医院骨科,上海201103);叶晓健(第二军医大学长征医院骨科,上海200003);冯红(第二军医大学长海医院药学部);曲伸(长海医院内分泌科);李家顺(第二军医大学长征医院骨科,上海200003)
关键词:脊髓损伤;基因修饰;成肌细胞;移植;电生理;神经营养因子,脑源性
第二军医大学学报000707 [摘要] 目的:采用神经电生理检查方法,观察逆转录病毒载体介导脑源性神经营养因子(BDNF)基因修饰成肌细胞对损伤脊髓的治疗作用。方法:30只SD大鼠在T9水平制成脊髓横断损伤模型,并随机分为基因细胞组(A组)、成肌细胞组(B组)及损伤对照组(C组),每组10只大鼠。术后3个月,采用皮质体感诱发电位(CSEP)和运动诱发电位(MEP)等电生理检测技术,观察轴突是否有再生及其神经功能恢复程度。结果:(1)A组中3只大鼠损伤3个月后出现CSEP波,5只出现MEP波,B,C组动物未发现电生理信号恢复; (2)重新出现的CSEP或MEP信号均较损伤前波幅减低,潜伏期延长。结论:BDNF基因修饰细胞脊髓内移植能有效促进损伤的脊髓神经部分传导功能恢复。
, 百拇医药
[中图分类号] R 651.205 [文献标识码] A
[文章编号] 0258-879X(2000)07-0621-04
Neurophysiological study on intraspinal implantation of genetically modified myoblast treating SCI in rats
YE Xiao-Jian LI Jia-Shun
(Department of Orthopaedics, Changzheng Hospital, Second Military Medical University, Shanghai 200003, China)
YU Ke-Wei
, 百拇医药
(Department of Othorpaedics, Shanghai Municipal Corps Hospital, 201103)
FENG Hong
(Department of Pharmacology, Changhai Hospital, Second Military Medical university)
QU Shen
(Department of Endocrine, Changhai Hospital)
LU Chang-Lin
(Department of Neurobiology, Department of Basic Medicine)
, 百拇医药
[ABSTRACT] Objective: To observe the value of gene therapy on SCI in vivo by transferring brain-derived neurotrophic factor (BDNF) to rat myoblast with retroviral vector using electrophysiological examination. Methods: Transection of spinal cord at the level of T9 were produced in 30 adult SD rats which were randomly divided into 3 groups (n=10): BDNF gene modified myoblast implantation (Group A), myoblast implantation (Group B) and without cell implantation as control (Group C). Three months after operation, whether the axon regenerated and how the neural function restored was observed by using cerebral somatosensory evoked potential (CSEP) and motor evoked potential (MEP). Results: (1) Thtee months after injury, 3 rats in Group A had CSEP signals and 5 rats had MEP signals, while no electrophysiological response was found in Group B or Group C. (2) The amplitudes of the recovered CSEP or MEP signals decreased and their latencies increased, comparing with those before injury. Conclusion: Treatment with genetically engineered myoblasts producing BDNF can accelerate recovery of traumatic spinal cord injury in adult rats.
, 百拇医药
[KEY WORDS] spinal cord injuries; genetically modified; myoblast; implantation; electrophysiology; neurotrophic factor, brain-derived
中枢神经系统(CNS)损伤后再生修复的研究一直是神经科学领域的前沿课题之一。过去认为,CNS损伤后神经元或轴突不能再生。但现代观点认为哺乳动物CNS损伤后神经元/轴突仍有再生潜力,并能形成新的突触联系,只是由于CNS内部微环境不适合,致使绝大部分轴突的再生努力归于失败,即所谓“夭折性再生(abortive regeneration)”[1]。其中神经营养因子或诱导因子不足是最重要的限制因素之一。由于血-脑屏障的影响,给予外源性神经营养因子的疗效不佳。而采用神经营养因子基因修饰细胞移植已被公认为最新、最有前途的治疗方法之一。此外,有关CNS损伤后神经功能损伤及恢复程度的判定,迫切需要有一种客观、定量的检测方法。本研究将脑源性营养因子(BDNF)基因修饰的成肌细胞移植到损伤脊髓内,探讨基因治疗脊髓损伤(SCI)的可行性,并采用包括体感诱发电位(somatosensory evoked potential, SEP)和运动诱发电位(motor evoked potential, MEP)在内的电生理检测技术验证其有效性,为将来基因治疗脊髓损伤应用于人类提供实验依据。
, 百拇医药
1 材料和方法
1.1 脊髓损伤模型与分组 30只成年SD大鼠,体质量(210±40)g,雌雄不限,由第二军医大学实验动物中心提供。按Tuszynski等[2]法制备大鼠脊髓横断伤模型。损伤水平位于T9。随机分为BDNF基因修饰成肌细胞组(A组)、成肌细胞组(B组)及损伤对照组(C组),每组10只大鼠。
1.2 BDNF基因修饰成肌细胞和成肌细胞的脊髓内移植 首先制备BDNF基因修饰的大鼠成肌细胞[3]。应用细胞悬液定向注射法分别注射基因细胞与成肌细胞至大鼠脊髓损伤区(悬液中细胞密度为2×104/μl)。损伤对照组无细胞移植。
1.3 皮质体感诱发电位(CSEP)检查 所有动物术前及术后3个月行CSEP检查。先分离动物左后肢坐骨神经,将其置于双极钩状银丝电极上,周围以温石蜡油保护。经Nihon Kohden 电刺激仪(日本)给予直流方波电脉冲刺激,强度50 mA,波宽0.1 ms,频率3 Hz。记录电极置于动物右侧感觉皮质表面,参考电极插入左额皮下。信号以FA-92放大器(第二军医大学生理学教研室)放大,滤波带通100~1 000 Hz,平均200次,电脑采样并贮存信号。
, 百拇医药
1.4 运动诱发电位(MEP)检查 各组大鼠术前及术后3个月行MEP检查。动物俯卧于立体定位架上,用特制棘突夹固定C7和S2棘突以稳定脊柱。将一枚直径1 mm银球电极(阴极)置于右侧感觉运动皮质表面,另一枚EEG针电极(阳极)插入硬腭粘膜下作参考。经刺激仪和隔离器发出单个方波电脉冲刺激,强度50 mA,波宽0.1 ms,频率5 Hz,每次记录重复刺激50~100次。记录电极置于T12脊髓背侧硬膜表面,另一枚电极置于邻近脊旁肌作参考。局部以温石蜡油保护。大鼠颈部皮下置铜片作为接地电极。信号以FA-92放大器放大,滤波带通100~1 000 Hz,平均50次,储存于电脑以备后续打印分析。
1.5 统计学处理 实验结果采用Foxpro 3.0数据库软件录入实验数据,经计算机统计处理,结果以
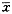 ±s表示。均值间差异采用t检验,各组间差异采用F检验,各组均数的比较采用方差分析(ANOVA)检验。
±s表示。均值间差异采用t检验,各组间差异采用F检验,各组均数的比较采用方差分析(ANOVA)检验。, 百拇医药
2 结 果
2.1 基因细胞移植治疗大鼠SCI的电生理学表现
2.1.1 CSEP检查结果 所有大鼠受伤前均获得正常CSEP信号,包括一个负向波,平均潜伏期(1.74±0.06)ms,平均波幅(66.4±20.2)mV。受伤后各组动物CSEP信号均消失,而BDNF基因修饰细胞移植后3个月,A组中3只大鼠有信号恢复,但其波幅较伤前明显下降,潜伏期也明显延迟。另两组动物未见有信号恢复(表1)。
表 1 基因细胞移植对SCI大鼠CSEP的影响
Tab 1 CSEP in SCI rats treated with intraspinal
implantation of BDNF gene modified myoblast(n=10,
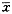 ±s) Group
±s) Group, 百拇医药
Before
injury
Just after
injury
3 month after
injury
Amp
(U/mV)
Lan
(t/ms)
Amp
(U/mV)
, 百拇医药
Lan
(t/ms)
Amp
(U/mV)
Lan
(t/ms)
A
60.2±
18.5
1.77±
0.06……
14.7±
7.5**
, http://www.100md.com
1.82±
0.21*
B
65.7±
20.4
1.74±
0.08…………
C
73.3±22.7
1.72±
0.11…………
Amp: Amplitude; Lan: Latency; * P<0.05, ** P<0.01 vs before injury2.1.2 MEP检查结果 所有大鼠受伤前均获得正常MEP信号,典型的MEP信号包括3~4个负波组成的早期成分,依次记为N1,N2,N3和N4,较晚出现(10 ms以后)的一个负向波记为Nlate。由于其他波峰或者不够稳定,或者波幅太低,因此本研究中以N1为计量指标。考虑基线不稳定和刺激伪迹的影响,其波幅以负向波峰至相邻正向波峰距离计算,潜伏期以刺激伪迹开始至各波峰的时间计算。发现受伤前平均潜伏期(16.8±2.0)ms,平均波幅(27.2±11.4)mV。受伤后各组动物MEP信号均消失,而BDNF基因修饰细胞移植后3个月,A组中5只大鼠MEP信号早期成分有所恢复,但其波幅较伤前明显下降,潜伏期也明显延迟。另两组动物未见有信号恢复(表2)。
, 百拇医药
表 2 基因细胞移植对SCI大鼠MEP的影响
Tab 2 MEP in SCI rats treated with intraspinal
implantation of BDNF gene modified myoblast(n=10,
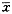 ±s) Group
±s) GroupBefore
injury
Just after
injury
3 month after
, http://www.100md.com injury
Amp
(U/mV)
Lan
(t/ms)
Amp
(U/mV)
Lan
(t/ms)
Amp
(U/mV)
Lan
(t/ms)
, 百拇医药
A
31.2±
11.2
16.8±
2.0……
5.7±3.5**
21.5±
2.2*
B
24.5±
10.3
17.2±
, 百拇医药
2.1…………
C
25.8±12.0
16.3±
1.7…………
* P<0.05, ** P<0.01 vs before injury3 讨 论
近年来神经营养因子(neurotrophic Factors, NTFs)的发现为SCI的治疗带来了新的希望。NTFs是神经系统最重要的生物活性因子之一,其中BDNF多见于中枢神经组织,包括脑和脊髓。除了诱导神经突起定向生长,决定感觉和交感神经纤维生长方向等NGF所具有的效应外,它还具有运动神经元营养活性,能保护脊髓运动神经元在SCI后免于死亡[4]。但是,采用周围或脑室内给药的方法并不能使BDNF在损伤的脊髓节段发挥生理效应,必须建立新的途径来达到营养作用。通过基因转移来治疗SCI已经成为新的研究热点,也就是将某种神经营养因子基因以一定的方法转染给合适的受体细胞,再移植到脊髓损伤区,让其在体内表达并发挥效应,刺激脊髓再生。本研究即是将BDNF基因转染至作为受体细胞的成肌细胞,使之携带BDNF基因,移植入脊髓后受体细胞源源不断地分泌BNDF,从而发挥其神经营养作用。实验结果表明,基因细胞移植3个月后受伤脊髓的神经功能有显著改善,说明BDNF基因细胞移植入脊髓能够存活并发挥作用。判断和对照各种SCI治疗方法的效果,必须有一项客观、定量的评估手段。SEP技术已成功用于脊髓损伤诊断多年 [5] 。但是近年来有关研究证实,SEP不一定能完全反映SCI程度[5,6] ,理由是SEP信号主要经脊髓后索传导,而不是由脊髓前索和侧索上递。而支配肢体运动的锥体束主要分布在脊髓侧索和前索,在椎体爆裂骨折中受损机会更多,单纯依靠SEP检查显然不能满足需要。MEP是刺激中枢神经组织并在脊髓远端、外周神经或肌肉记录到的电信号,能直接反映脊髓下行传导束或外周运动神经的功能状态[7,8]。本研究发现,BDNF基因修饰细胞移植3个月后,部分大鼠CSEP和MEP信号恢复,但波幅减低,潜伏期延长。说明神经轴突已经再生并通过损伤断端,而基因细胞所分泌的BNDF促进了轴突的再生。通过后肢功能的检查,基因细胞移植组较对照组也有显著的改进。上述结果说明,BDNF基因转染成肌细胞移植入脊髓是成功的,结合HRP逆行示踪染色和神经元及神经纤维图像分析技术等病理学检查的阳性结果(另文报道),进一步证明基因治疗脊髓损伤是可行的。同时也说明,CSEP和MEP均可准确反映SCI后脊髓神经功能状态,也有助于在实验研究中客观、定量地分析各类治疗方法对促进神经功能恢复的效果。
, 百拇医药
本研究还发现,MEP伤后恢复出现率较CSEP更高,信号也更为明显。其中可能的解释有两种:(1)BDNF基因修饰细胞对运动轴突再生的促进作用强于对感觉轴突;(2)MEP信号较CSEP信号更为灵敏,可以测出更微弱的神经电传导。而后一点在我们以往的研究中已经得到证实。当然本实验的成功并不表明脊髓损伤的基因治疗马上可以进入临床,目前转基因技术治疗脊髓损伤仍然存在一些问题:(1)目的基因:目前的研究主要是将NTFs基因作为目的基因,但NTFs的作用只是单方面的,尚不能完全解决脊髓再生;(2)载体:目前无论是病毒还是非病毒技术,转基因的安全性和感染率都有待解决;(3)免疫原性:尽管中枢神经系统有一定的免疫豁免性,但仍然存在免疫排斥反应。解决这一问题的方法一是发展免疫隔离技术,二是开展自体细胞移植技术;(4)受体细胞在脊髓内长期存活和持续表达仍未完全解决。对上述问题,我们将在本实验研究成功的基础上,在细胞移植的技术和方法、基因表达的调控等方面进行大量的、更深入的研究,以期尽早过渡到临床,为脊髓损伤患者造福。
基金项目:国家自然科学基金资助项目(39600147)
, 百拇医药
作者简介:余科炜(1970-),男(汉族),博士,主治医师。
作者单位:路长林(基础医学部神经生物学教研室)
[参 考 文 献]
[1] Weidner N, Grill RJ, Tuszynski MH. Related articles elimination of basal lamina and the collagen "scar" after spinal cord injury fails to augment corticospinal tract regeneration [J]. Exp Neurol, 1999, 160(1):40-50.
[2] Tuszynski MH, Meyers G, Nakahara Y, et al. Fibroblast and Schwann cells genetically modified to produce neurotrophic factors induce robust neuritic growth after transplantation to the spinal cord [J]. Soc Neurosci Abstr, 1994, 20(1):10-15.
, 百拇医药
[3] 叶晓健,申准斌,冯 红. 逆转录病毒载体介导脑源性神经营养因子基因转染大鼠成肌细胞 [J]. 中国学术期刊文摘, 1999, 5(7):917-922.
[4] Jakeman LB, Wei P, Guan Z, et al. Related articles brain-derived neurotrophic factor stimulates hindlimb stepping and sprouting of cholinergic fibers after spinal cord injury [J]. Exp Neurol, 1998, 154(1):170-184.
[5] Restuccia D, Di Lazzaro V, Valeriani M, et al. Related articles spinal responses to median and tibial nerve stimulation and magnetic resonance imaging in intramedullary cord lesions [J]. Neurology, 1996, 46(6):1706-1714.
, http://www.100md.com
[6] Nashmi R, Imamura H, Tator CH, et al. Serial recording of somatosensory and myoelectric motor evoked potentials: role in assessing functional recovery after graded spinal cord injury in the rat [J]. J Neurotrau , 1997, 14(1):151-159.
[7] Di Lazzaro V, Oliviero A, Profice P, et al. The diagnostic value of motor evoked potentials [J]. Clin Neurophysiol, 1999, 110(7):1297-1307
[8] 孙天胜, 胥少汀. 实验性脊髓损伤的运动诱发电位检测价值 [J]. 中华外科杂志, 1991, 29(4):472-476.
[收稿日期] 2000-02-22
[修回日期] 2000-06-12, 百拇医药