糖皮质激素诱导体外人嗜酸性粒细胞凋亡的研究
作者:赖克方 郭晓明 王长征 郭先健 钱桂生
单位:赖克方(广州呼吸疾病研究所 510120);郭晓明 王长征 郭先健 钱桂生(400037 重庆,第三军医大学新桥医院全军呼吸研究所)
关键词:
中华血液学杂志000716 嗜酸性粒细胞(Eos)是支气管哮喘等过敏性疾病的关键效应细胞,Eos浸润增加是这些疾病的病理特征。白细胞介素(IL)-5、粒-巨噬细胞集落刺激因子(GM-CSF)和IL-3是Eos的主要存活因子。糖皮质激素(GCS)是目前治疗Eos增多性炎症最有效的抗炎药物,用药后体内Eos迅速降低,其机制尚未完全清楚。我们采用体外细胞培养方法,观察了GCS和细胞因子对Eos凋亡的作用,以探讨GCS治疗哮喘的机制。
材料和方法
1 主要试剂 人重组(rh)IL-3、IL-5、GM-CSF由美国遗传研究所Meg O'Donell教授惠赠。Percoll分离液购自北京中山公司(Pharmacia公司产品),淋巴细胞分离液购自上海生化公司,fMLP、地塞米松(DM)为Sigma公司产品,原位细胞凋亡检测试剂盒为宝灵曼公司产品。
, 百拇医药
2 Eos分离方法 采用改良的Percoll分离液密度梯度分离Eos。抽取健康献血者外周静脉血50ml,枸橼酸钠(130mmol/L,pH 7.4)抗凝,将稀释血液加在淋巴细胞分离液上面(相对密度1.077),1000×g离心20min。取下层粒细胞和红细胞,加入NH4Cl溶液冰浴15min。400×g离心7min。Hanks液漂洗沉淀细胞。将10nmol/L fMLP与细胞悬液37℃孵育10min。将细胞悬液加于Percoll分离液上面,上层相对密度1.082,下层相对密度1.010。1000×g离心15min。收集界面细胞。分离后所得Eos 细胞活力和纯度>97%。
3 Eos培养 纯化的Eos悬浮于含体积分数为10%胎牛血清(FCS)的RPMI 1640培养基,置于96孔平底培养板,每孔细胞数2.0×105,总体积200μl。体积分数为5%CO2、37℃条件下培养。分别加入不同浓度的细胞因子[IL-5、IL-3、GM-CSF(0.1~100.0U/ml)和DM(10-10~10-6mol/L)],以不加入细胞因子或药物的培养孔作为对照,动态观察Eos活力和变化。Eos活力检测方法采用锥虫蓝(台盼蓝)拒染法,计算活细胞百分率。
, http://www.100md.com
4 原位细胞凋亡检测 参照试剂盒说明略加改进。将细胞置于含体积分数为0.3% H2O2、1g/L NaN3的溶液中封闭15min。用体积分数为0.1%的Triton X-100 4℃通透2min。加入由末端脱氧核苷酸转移酶(TdT)、脱氧三磷酸核苷(dNTP)和荧光素标记的脱氧三磷酸尿苷(dUTP)组成的混合物30μl,37℃反应60min。加入过氧化物酶(POD)连接的抗荧光素抗体30μl,37℃反应30min。加入50μl 0.5g/L DAB/体积分数为0.01% H202显色10min,苏木素复染,光镜下观察至少5个视野,计数200个细胞以上,计算阳性细胞百分率。
5 统计学处理 各组结果以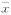 ±s表示,采用非配对资料t检验。
±s表示,采用非配对资料t检验。
结果
, http://www.100md.com
1 IL-3、IL-5、GM-CSF对Eos活力的影响 在缺乏细胞因子的条件下,体外培养的Eos活力迅速降低,第3天几乎全部死亡。细胞因子IL-3、IL-5或GM-CSF(10U/ml)与Eos共同培养时,可显著抑制Eos活力的下降,至第10天仍有相当部分Eos存活,其中IL-5可使50%的Eos存活10d以上。
不同浓度的细胞因子与Eos培养3d,IL-3、IL-5、GM-CSF对Eos的作用呈浓度依赖性,1U/ml IL-5可使50%的Eos存活,IL-5浓度为10U/ml时,其对Eos的作用达到最大。IL-3、GM-CSF浓度为10U/ml时,对Eos的作用尚未达到最大。
2 DM对Eos活力的影响 在加入细胞因子IL-5、IL-3、GM-CSF(1U/ml)的条件下,不同浓度的DM(10-10~10-4mol/L)与Eos共同培养,3d后观察Eos的活力。DM呈浓度依赖性抑制IL-5、IL-3、GM-CSF对Eos的作用(图1)。10-6mol/L DM可以显著抑制IL-5增强Eos活力的作用,抑制率达(90±4)%;10-8mol/L DM即可显著抑制IL-3、GM-CSF的作用(P<0.01)。DM抑制IL-5(1U/ml)延长Eos存活时间的作用呈时间依赖性,第2天开始Eos活力显著下降,DM组[(43±6)%]与对照组[(72±6)%]相比,差异显著(P<0.01)。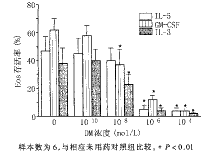
, 百拇医药
图1 DM对IL-5、GM-CSF、IL-3增强Eos活力作用的影响
Eos体外培养3d,观察DM(10-6mol/L)对不同浓度IL-5增强Eos活力作用的影响,发现随着IL-5浓度的增高,DM对Eos活力的抑制作用逐渐减弱,1000U/ml IL-5几乎完全抑制了DM的作用(表1)。
表1 DM(10-6mol/L)对不同浓度IL-5增强Eos活力
的影响(%,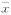 ±s) 组别
±s) 组别
样本
数
IL-5(U/ml)
, http://www.100md.com
1
10
100
1000
对照组
6
47±10
75±12
74±14
82±9
DM组
6
5±3#
, 百拇医药
21±5#
59±8*
69±10
注:与对照组相比,* P<0.05,#P<0.01
3 原位末端标记凋亡检测 为了进一步证实DM的促Eos凋亡作用,采用原位末端标记方法检测Eos凋亡。在IL-5(1U/ml)存在的条件下,DM(10-6mol/L)与Eos培养,检测细胞凋亡率。结果发现DM作用24,48h后,Eos凋亡率分别为(59±7)%、(87±6)%,与对照组[(22±5)%、(37±6)%]相比,差异有显著性(P<0.01)。
讨论
本研究结果表明,体外培养Eos存活时间很短,至第3天已接近全部死亡。IL-3、IL-5、GM-CSF可使Eos存活时间显著延长,并呈浓度依赖性。支气管哮喘时,支气管粘膜和外周血激活的淋巴细胞增加,表达IL-3、IL-5、GM-CSF mRNA和蛋白的细胞数显著增加[1,2],还有研究发现,支气管肺泡灌洗液(BALF)内IL-5、GM-CSF水平增加[3]。Simon等[4]最近对过敏性鼻炎合并鼻息肉患者鼻息肉组织研究表明,IL-5抑制了组织内Eos的凋亡。虽然尚无直接证据表明体内IL-3、IL-5、GM-CSF抑制Eos凋亡,但结合体外培养结果推测,这些细胞因子在体内同样延长Eos的存活时间,导致哮喘肺组织Eos增加。
, 百拇医药
本研究表明DM能够拮抗IL-3、IL-5、GM-CSF的作用,诱导Eos凋亡,这可能是GCS能够迅速降低体内Eos数量及有效治疗哮喘的一个重要机制。根据本实验的研究结果,相当于生理浓度(10-6mol/L)的DM即可显著抑制Eos的存活,但作用时间需要48h。我们认为除了体内和体外实验本身存在差别外,这与锥虫蓝检测Eos凋亡不够敏感有关。采用原位末端标记凋亡检测方法观察DM作用24h Eos的变化,发现50%以上的Eos发生凋亡,此时锥虫蓝检测Eos活力与对照组无明显差别。
本研究还表明,随着细胞因子IL-5浓度的增高,DM的促Eos凋亡作用逐渐减弱,高浓度的细胞因子显著抑制了DM的作用。某些Eos增高性疾病、少数严重支气管哮喘患者血清和BALF IL-5浓度高达22000fmol/L(1000pg/ml)[3]。由此推测,某些哮喘患者的皮质激素依赖可能与体内IL-5浓度显著增高有关。
基金项目:国家自然科学基金资助项目(39670337)
, 百拇医药
参 考 文 献
1,Ying S, Durham SR, Corrigan CJ, et al. Phenotype of cells expressing mRNA for Th2-type (interleukin 4 and interleukin 5) and Th-1type (interleukin 2 and interferon gama) cytokines in bronchoalveolar lavage and bronchial biopsies from atopic asthmatic and normal control subjects. Am J Respir Cell Mol Biol, 1995, 12: 477-487.
2,Lai CWKK, Ho AS, Chan CH, et al. Interleukin-5 messenger RNA expression in peripheral blood CD4+ cells in asthma. J Allergy Clin Immunol, 1996, 97: 1320-1328.
, http://www.100md.com
3,Virchow Jr JC, Kriegel C, Walker C, et al. Inflammatory determinants of asthma severity: mediator and cellular changes in bronchoalveolar lavage fluid of patients with severe asthma. J Allergy Clin Immunol, 1996, 98: 27-40.
4,Simon HU, Yousefi S, Schranz C, et al. Direct demonstration of delayed eosinophil apoptosis as a mechanism causing tissue eosinophilia. J Immunol, 1997, 158: 3902-3908.
(收稿日期:1999-04-09), http://www.100md.com
单位:赖克方(广州呼吸疾病研究所 510120);郭晓明 王长征 郭先健 钱桂生(400037 重庆,第三军医大学新桥医院全军呼吸研究所)
关键词:
中华血液学杂志000716 嗜酸性粒细胞(Eos)是支气管哮喘等过敏性疾病的关键效应细胞,Eos浸润增加是这些疾病的病理特征。白细胞介素(IL)-5、粒-巨噬细胞集落刺激因子(GM-CSF)和IL-3是Eos的主要存活因子。糖皮质激素(GCS)是目前治疗Eos增多性炎症最有效的抗炎药物,用药后体内Eos迅速降低,其机制尚未完全清楚。我们采用体外细胞培养方法,观察了GCS和细胞因子对Eos凋亡的作用,以探讨GCS治疗哮喘的机制。
材料和方法
1 主要试剂 人重组(rh)IL-3、IL-5、GM-CSF由美国遗传研究所Meg O'Donell教授惠赠。Percoll分离液购自北京中山公司(Pharmacia公司产品),淋巴细胞分离液购自上海生化公司,fMLP、地塞米松(DM)为Sigma公司产品,原位细胞凋亡检测试剂盒为宝灵曼公司产品。
, 百拇医药
2 Eos分离方法 采用改良的Percoll分离液密度梯度分离Eos。抽取健康献血者外周静脉血50ml,枸橼酸钠(130mmol/L,pH 7.4)抗凝,将稀释血液加在淋巴细胞分离液上面(相对密度1.077),1000×g离心20min。取下层粒细胞和红细胞,加入NH4Cl溶液冰浴15min。400×g离心7min。Hanks液漂洗沉淀细胞。将10nmol/L fMLP与细胞悬液37℃孵育10min。将细胞悬液加于Percoll分离液上面,上层相对密度1.082,下层相对密度1.010。1000×g离心15min。收集界面细胞。分离后所得Eos 细胞活力和纯度>97%。
3 Eos培养 纯化的Eos悬浮于含体积分数为10%胎牛血清(FCS)的RPMI 1640培养基,置于96孔平底培养板,每孔细胞数2.0×105,总体积200μl。体积分数为5%CO2、37℃条件下培养。分别加入不同浓度的细胞因子[IL-5、IL-3、GM-CSF(0.1~100.0U/ml)和DM(10-10~10-6mol/L)],以不加入细胞因子或药物的培养孔作为对照,动态观察Eos活力和变化。Eos活力检测方法采用锥虫蓝(台盼蓝)拒染法,计算活细胞百分率。
, http://www.100md.com
4 原位细胞凋亡检测 参照试剂盒说明略加改进。将细胞置于含体积分数为0.3% H2O2、1g/L NaN3的溶液中封闭15min。用体积分数为0.1%的Triton X-100 4℃通透2min。加入由末端脱氧核苷酸转移酶(TdT)、脱氧三磷酸核苷(dNTP)和荧光素标记的脱氧三磷酸尿苷(dUTP)组成的混合物30μl,37℃反应60min。加入过氧化物酶(POD)连接的抗荧光素抗体30μl,37℃反应30min。加入50μl 0.5g/L DAB/体积分数为0.01% H202显色10min,苏木素复染,光镜下观察至少5个视野,计数200个细胞以上,计算阳性细胞百分率。
5 统计学处理 各组结果以
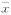 ±s表示,采用非配对资料t检验。
±s表示,采用非配对资料t检验。结果
, http://www.100md.com
1 IL-3、IL-5、GM-CSF对Eos活力的影响 在缺乏细胞因子的条件下,体外培养的Eos活力迅速降低,第3天几乎全部死亡。细胞因子IL-3、IL-5或GM-CSF(10U/ml)与Eos共同培养时,可显著抑制Eos活力的下降,至第10天仍有相当部分Eos存活,其中IL-5可使50%的Eos存活10d以上。
不同浓度的细胞因子与Eos培养3d,IL-3、IL-5、GM-CSF对Eos的作用呈浓度依赖性,1U/ml IL-5可使50%的Eos存活,IL-5浓度为10U/ml时,其对Eos的作用达到最大。IL-3、GM-CSF浓度为10U/ml时,对Eos的作用尚未达到最大。
2 DM对Eos活力的影响 在加入细胞因子IL-5、IL-3、GM-CSF(1U/ml)的条件下,不同浓度的DM(10-10~10-4mol/L)与Eos共同培养,3d后观察Eos的活力。DM呈浓度依赖性抑制IL-5、IL-3、GM-CSF对Eos的作用(图1)。10-6mol/L DM可以显著抑制IL-5增强Eos活力的作用,抑制率达(90±4)%;10-8mol/L DM即可显著抑制IL-3、GM-CSF的作用(P<0.01)。DM抑制IL-5(1U/ml)延长Eos存活时间的作用呈时间依赖性,第2天开始Eos活力显著下降,DM组[(43±6)%]与对照组[(72±6)%]相比,差异显著(P<0.01)。

, 百拇医药
图1 DM对IL-5、GM-CSF、IL-3增强Eos活力作用的影响
Eos体外培养3d,观察DM(10-6mol/L)对不同浓度IL-5增强Eos活力作用的影响,发现随着IL-5浓度的增高,DM对Eos活力的抑制作用逐渐减弱,1000U/ml IL-5几乎完全抑制了DM的作用(表1)。
表1 DM(10-6mol/L)对不同浓度IL-5增强Eos活力
的影响(%,
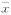 ±s) 组别
±s) 组别样本
数
IL-5(U/ml)
, http://www.100md.com
1
10
100
1000
对照组
6
47±10
75±12
74±14
82±9
DM组
6
5±3#
, 百拇医药
21±5#
59±8*
69±10
注:与对照组相比,* P<0.05,#P<0.01
3 原位末端标记凋亡检测 为了进一步证实DM的促Eos凋亡作用,采用原位末端标记方法检测Eos凋亡。在IL-5(1U/ml)存在的条件下,DM(10-6mol/L)与Eos培养,检测细胞凋亡率。结果发现DM作用24,48h后,Eos凋亡率分别为(59±7)%、(87±6)%,与对照组[(22±5)%、(37±6)%]相比,差异有显著性(P<0.01)。
讨论
本研究结果表明,体外培养Eos存活时间很短,至第3天已接近全部死亡。IL-3、IL-5、GM-CSF可使Eos存活时间显著延长,并呈浓度依赖性。支气管哮喘时,支气管粘膜和外周血激活的淋巴细胞增加,表达IL-3、IL-5、GM-CSF mRNA和蛋白的细胞数显著增加[1,2],还有研究发现,支气管肺泡灌洗液(BALF)内IL-5、GM-CSF水平增加[3]。Simon等[4]最近对过敏性鼻炎合并鼻息肉患者鼻息肉组织研究表明,IL-5抑制了组织内Eos的凋亡。虽然尚无直接证据表明体内IL-3、IL-5、GM-CSF抑制Eos凋亡,但结合体外培养结果推测,这些细胞因子在体内同样延长Eos的存活时间,导致哮喘肺组织Eos增加。
, 百拇医药
本研究表明DM能够拮抗IL-3、IL-5、GM-CSF的作用,诱导Eos凋亡,这可能是GCS能够迅速降低体内Eos数量及有效治疗哮喘的一个重要机制。根据本实验的研究结果,相当于生理浓度(10-6mol/L)的DM即可显著抑制Eos的存活,但作用时间需要48h。我们认为除了体内和体外实验本身存在差别外,这与锥虫蓝检测Eos凋亡不够敏感有关。采用原位末端标记凋亡检测方法观察DM作用24h Eos的变化,发现50%以上的Eos发生凋亡,此时锥虫蓝检测Eos活力与对照组无明显差别。
本研究还表明,随着细胞因子IL-5浓度的增高,DM的促Eos凋亡作用逐渐减弱,高浓度的细胞因子显著抑制了DM的作用。某些Eos增高性疾病、少数严重支气管哮喘患者血清和BALF IL-5浓度高达22000fmol/L(1000pg/ml)[3]。由此推测,某些哮喘患者的皮质激素依赖可能与体内IL-5浓度显著增高有关。
基金项目:国家自然科学基金资助项目(39670337)
, 百拇医药
参 考 文 献
1,Ying S, Durham SR, Corrigan CJ, et al. Phenotype of cells expressing mRNA for Th2-type (interleukin 4 and interleukin 5) and Th-1type (interleukin 2 and interferon gama) cytokines in bronchoalveolar lavage and bronchial biopsies from atopic asthmatic and normal control subjects. Am J Respir Cell Mol Biol, 1995, 12: 477-487.
2,Lai CWKK, Ho AS, Chan CH, et al. Interleukin-5 messenger RNA expression in peripheral blood CD4+ cells in asthma. J Allergy Clin Immunol, 1996, 97: 1320-1328.
, http://www.100md.com
3,Virchow Jr JC, Kriegel C, Walker C, et al. Inflammatory determinants of asthma severity: mediator and cellular changes in bronchoalveolar lavage fluid of patients with severe asthma. J Allergy Clin Immunol, 1996, 98: 27-40.
4,Simon HU, Yousefi S, Schranz C, et al. Direct demonstration of delayed eosinophil apoptosis as a mechanism causing tissue eosinophilia. J Immunol, 1997, 158: 3902-3908.
(收稿日期:1999-04-09), http://www.100md.com