实验性脑出血血肿周边及下丘脑SS与SSmRNA表达
作者:蒋晓江 琚亚非 李书林 许志强
单位:第三军医大学大坪医院脑三科,重庆 400042
关键词:生长抑素;脑出血
中国急救医学000809 [摘 要] 目的 研究脑出血时下丘脑及血肿周边脑组织SS、SSmRNA的变化,阐明SS、SSmRNA在脑出血过程中的作用及意义。方法 采用胶原酶加肝素联合注射致脑出血模型,分析出血后不同时相点SS活性及SSmRNA的表达。结果 脑出血后下丘脑、血肿周边脑组织SS含量明显升高,SSmRNA表达上调。结论 血肿周边及下丘脑SS含量升高是局部神经元SSmRNA表达上调使之合成SS增多的结果,是加重血肿周边神经元缺血、缺氧性损伤及下丘脑内分泌紊乱的重要因素之一。
[中图分类号] R 651.15 [文献标识码] A [文章编号] 1002-1949(2000)08-0464-03
, http://www.100md.com
Expression of SS and SSmRNA in perihemotoma and hypothalamus in experimental cerebral hemorrhage
JIANG Xiao-jiang, JU Ya-fei, LI Shu-lin, et al. Third Department of Cerebral Vascular Disease Hospital, Daping Hospital, Third Military Medical College, Chongqing 400042, China
[Abstract] Objective To explore the change of SS and SSmRNA in perihematoma and hypothalamus in experimental intracerebral hemorrhage.Methods We induced intracerebral hemorrhage in rats with infusing collagenase and heparin into the left caudate and examined SS and SmRNA reactions to hematoma at various stages using the method of RIA and HIS.Results SS and SSmRNA expression in perihematoma and hypothalamus were significantly increased.Conclusion SS activity and SSmRNA expression is involved in the pathophysiologic process of rats incracerebral hemorrhages.In addion,SS plays on role in the damage of CNS neruons and induces neuroendocrinological disorders in hypothalamus.
, 百拇医药
[Key words] Somatostatin mRNA; Cerebral hemorrhage
生长抑素(Somatostatin,SS)是一组广泛分布于中枢神经系统、周围神经系统及消化系统的多肽类物质,在体内具有抑制激素和消化液分泌、抑制神经元的活动、增强戊巴比妥的麻醉作用、调控机体免疫功能等抑制性介质的活性[1,2]。本研究通过测定脑出血后下丘脑、血肿周边脑组织SS活性及SSmRNA表达变化,从而阐明脑出血时SS的病理生理作用及意义。
1 材料与方法
1.1 实验动物及模型 Wistar大鼠,雄性,体重275±25 g,参照Rosenberg[3]及任泽光[4]等的方法加以改进,胶原酶加肝素联合注射建立脑出血动物模型,手术对照组不注入胶原酶及肝素。
, http://www.100md.com
1.2 动物观测时相点、测定部位 取出血前(Pre)、出血30 min(H30min)、3 h(H3h)、6 h(H6h)、12 h(H12h)、24 h(H24h)、48 h(H48h)、72 h(H72h)8个时相点,取下丘脑、血肿周边脑组织进行SS、SSmRNA测定。
1.3 SS活性测定 活杀大鼠后即刻取出脑组织入100℃生理盐水煮5 min,分离出下丘脑、血肿周边组织,置匀浆器(0.1 N HCl的匀浆液)匀浆,离心取上清液备测。SS活性测定用放射免疫法。其具体操作依药盒说明书进行。
1.4 SSmRNA表达测定 麻醉动物,开胸行主动脉插管,行多聚甲醛灌注后,取出全脑,行脱水,后固定、冰冻切片,用地高辛标记的SSmRNA探针与脑组织原位杂交,杂交采用漂浮法。
1.5 模型成功的评分判断 1级:将大鼠尾巴提起,瘫痪侧前肢回收屈曲于腹下,正常侧前肢向地面伸展;2级:除1级体征外,向瘫痪侧推大鼠时阻力较对侧明显降低;3级:除以上体征外,大鼠有向瘫痪侧旋转的行为。
, 百拇医药
1.6 统计学处理 所有数据均以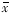 ±s表示,采用Microsoft Excel 7.0数理统计,组内自身对照和配对数据用配对t检验,组间比较采用方差分析t检验。采用MAS-1图像分析系统进行SSmRNA阳性细胞密度计量。对单位面积阳性细胞作t检验。
±s表示,采用Microsoft Excel 7.0数理统计,组内自身对照和配对数据用配对t检验,组间比较采用方差分析t检验。采用MAS-1图像分析系统进行SSmRNA阳性细胞密度计量。对单位面积阳性细胞作t检验。
2 结果
2.1 血肿周边脑组织SS活性变化 对照组:术后3~6 h SS有轻度升高趋向,12 h开始回落到术前水平,但均无显著差异。出血组:术后30 min及3 h虽有升高,但与对照组比较无差异,出血后6 h显著升高,于12~24 h达峰值,48 h后明显回落,详见表1。Tab1 SS activity(pg/mg) of perihematoma with ICH(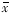 ±s,n=5)
±s,n=5)
, 百拇医药
Pre
H30min
H3h
H6h
H12h
H24h
H48h
H72h
Control
133.77±26.63
140.83±19.35
159.82±8.42
, http://www.100md.com
169.84±25.28
132.71±15.80
122.37±7.85
125.42±11.20
122.04±8.31
ICH
120.33±2.750
126.38±15.01
156.20±15.14c
227.97±23.20cd
247.94±21.66cf
, http://www.100md.com
253.31±27.78cf
189.84±21.42cf
148.41±30.76
a:P<0.05 b:P<0.01 c:P<0.001 compared with Pre; d:P<0.05 e:P<0.01 f:P<0.001 compared with control
2.2 下丘脑SS活性变化 对照组:术后3 h SS含量有明显升高,6 h降至术前水平。出血组:3 h SS虽比出血前有明显升高,但与对照组比较无显著差异,12~24 h达峰值,到72 h虽仍高于术前水平,但也无显著差异(见表2)。
Tab2 SS activity(pg/mg) of hypothalamus area with ICH(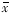 ±s,n=5)
±s,n=5)
, http://www.100md.com
Pre
H30min
H3h
H6h
H12h
H24h
H48h
H72h
Control
643.87±103.36
688.29±150.38
916.90±667.47a
, http://www.100md.com
667.17±106.26
713.8±555.66
626.01±106.31
584.67±72.84
664.60±146.39
ICH
607.89±120.67
800.99±192.32
969.93±142.02c
1245.59±219.54bd
, http://www.100md.com 1541.61±277.17cf
1523.74±389.71bf
1131.77±203.27bf
667.12±166.76
a:P<0.05 b:P<0.01 c:P<0.001 compared with Pre; d:P<0.05 e:P<0.01 f:P<0.001 compared with control
2.3 脑组织SSmRNA表达变化
2.3.1 下丘脑SSmRNA表达变化 对照组:术后3 h明显升高,随后降至正常。出血组:出血后3 h开始升高,并于12 h达峰值,然后开始下降(详见表3,图1)。
, 百拇医药
Tab3 SSmRNA expression of hypothalamus
areas (cells/mm3,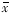 ±s,n=5)
±s,n=5)
Pre
H3h
H12h
H72h
Control
27.44±4.58
36.87±5.71a
30.39±6.96
, 百拇医药
34.34±8.76
ICH
30.29±5.95
73.36±10.80cf
120.97±97cf
74.98±13.28cf
a:P<0.05 b:P<0.01 c:P<0.001 compared with Pre;
d:P<0.05 e:P<0.01 f:P<0.001 compared with control
, http://www.100md.com
Photo l SSmRNA expression
surrouding hematoma at ICH 12 h×100
2.3.2 血肿周边脑组织SSmRNA表达变化 对照组:术后3 h明显升高,随后降至正常。出血组:出血后3 h开始升高,并于12 h达峰值,然后开始下降(详见表4,图2)
Tab4 SSmRNA expression of perihematoma
(cells/mm3,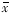 ±s,n=5)
±s,n=5)
Pre
H3h
, 百拇医药
H12h
H72h
Control
37.56±7.18
47.86±3.88a
38.70±9.72
38.89±8.09
ICH
39.99±7.17
59.30±6.62bd
83.651±7.77ce
, 百拇医药
50.06±10.75
a:P<0.05 b:P<0.01 c:P<0.001 compared with Pre;
d:P<0.05 e:P<0.01 f:P<0.001 compared with control
Photo 2 SSmRNA expression in
hypothalamus at ICH 12 h×100
3 讨论
中枢神经系统损伤时组织SS含量的变化,国内外文献对此报道不尽一致。Rosenberg[3]报道颅脑外伤和实验性脑缺血动物血浆及脑组织中SS含量明显升高,且随外伤严重程度和时间的延长而递增。缺血和颅脑外伤脑组织SS含量明显升高,且与脑组织H2O含量显著正相关。近期的研究表明SS可以作为一种调质,调节谷氨酸介导的CNS过度兴奋[5]。
, 百拇医药
本研究发现脑出血后下丘脑及血肿周边脑组织SS含量升高,并于出血后12~24 h达峰值,48 h后逐渐下降。同时,SS活性与脑出血血肿容量相关。用地高辛标记的SScDNA探针位杂交表明脑出血后下丘脑与血肿周边脑组织SSmRNA表达明显增强,其阳性细胞计数的PC值在出血后3 h明显增高,并在12 h达高峰,比较同部位SS活性与SSmRNA表达的PC值,两者明显相关,充分说明下丘脑及血肿周边脑组织SS活性升高是局部SS合成增强所致。
在机体内SS既可作为激素也可做为神经递质发挥作用[6],因此,对下丘脑及血肿周边脑组织SS活性增高的意义作以下推测:SS与SS受体(SSR)结合形成SSR-SS复合物,使抑制性亚型G蛋白(Gi蛋白)活化,后者与GTP结合抑制胸膜内腺苷酸环化酶的活性,使cAMP生成减少,导致神经元能量代谢障碍。由于cAMP具有促进SS转录的作用[7],cAMP的减少,使SSmRNA的表达减弱,可能是减轻神经元损伤的一种代偿机制。下丘脑SS活性增强,抑制下丘脑内分泌细胞由第二信使增高引起的激素分泌(近端效应),从而促发中枢神经系统内分泌紊乱,导致机体内环境的失衡。同时SS刺激抗利尿激素的分泌,从而导致肾小管对水的重吸收增多,尿量减少,加重血肿周边脑水肿。SS通过SSR与GK蛋白结合,使膜K+通道开放,膜趋极化从而抑制了神经细胞的活动,加重神经细胞功能障碍。SS-SSR复合物与Ge蛋白结合也抑制了细胞胞吐,导致下丘脑内分泌细胞众多激素的分泌抑制(远端效应)。SS通过调节血肿周边血管的张力,使血管扩张,从而加重出血区血液的渗出及脑细胞水肿。
, 百拇医药
[参考文献]
[1]Karalis K,Mastorakos G,Chrousos GP,et al.Somatostation analogs suppress the inflammatory reaction in vivo[J]. J Clin Invest,1994,93:2000.
[2]Karalis K,Mastorakos G,Hajme S,Roralcl L,et al.Somatostatin may participate in the autiinflammatory actions of glucoclrticoeds[J].Endocrinology,1995,136:4133.
[3]Rosenberg GB,Shelia Mun-Bryce,Mary Wesley,et al.Collagenase-induced intracerebral emrrhage in rats[J].Stroke,1990,21:801.
, 百拇医药
[4]任泽光,吴建中.大鼠脑出血模型[J].中华神经外科杂志,1993,9:205.
[5]Vezzani A,Rizzi M,Conti M,et al.Modulatory role of neuropepeides in seizures induceded in rats by seimulation of glueamate receptors[J].J Nuer,2000,130(4 SSuppl):1046S-8S.
[6]Mendelow AD.Mechamins of ischemic brain damage with intracerebralhemorrhage[J].Stroke,1993,24:I-115.
[7]Montminy M,Brindle P,Arias J,et al.Regulation of somatostatin gene transcription by cyclic adenosine monophosphate[J].Metabolism,1996,45(8 Suppl):4-7.
[收稿:1999-08-10,修回:1999-03-25], 百拇医药
单位:第三军医大学大坪医院脑三科,重庆 400042
关键词:生长抑素;脑出血
中国急救医学000809 [摘 要] 目的 研究脑出血时下丘脑及血肿周边脑组织SS、SSmRNA的变化,阐明SS、SSmRNA在脑出血过程中的作用及意义。方法 采用胶原酶加肝素联合注射致脑出血模型,分析出血后不同时相点SS活性及SSmRNA的表达。结果 脑出血后下丘脑、血肿周边脑组织SS含量明显升高,SSmRNA表达上调。结论 血肿周边及下丘脑SS含量升高是局部神经元SSmRNA表达上调使之合成SS增多的结果,是加重血肿周边神经元缺血、缺氧性损伤及下丘脑内分泌紊乱的重要因素之一。
[中图分类号] R 651.15 [文献标识码] A [文章编号] 1002-1949(2000)08-0464-03
, http://www.100md.com
Expression of SS and SSmRNA in perihemotoma and hypothalamus in experimental cerebral hemorrhage
JIANG Xiao-jiang, JU Ya-fei, LI Shu-lin, et al. Third Department of Cerebral Vascular Disease Hospital, Daping Hospital, Third Military Medical College, Chongqing 400042, China
[Abstract] Objective To explore the change of SS and SSmRNA in perihematoma and hypothalamus in experimental intracerebral hemorrhage.Methods We induced intracerebral hemorrhage in rats with infusing collagenase and heparin into the left caudate and examined SS and SmRNA reactions to hematoma at various stages using the method of RIA and HIS.Results SS and SSmRNA expression in perihematoma and hypothalamus were significantly increased.Conclusion SS activity and SSmRNA expression is involved in the pathophysiologic process of rats incracerebral hemorrhages.In addion,SS plays on role in the damage of CNS neruons and induces neuroendocrinological disorders in hypothalamus.
, 百拇医药
[Key words] Somatostatin mRNA; Cerebral hemorrhage
生长抑素(Somatostatin,SS)是一组广泛分布于中枢神经系统、周围神经系统及消化系统的多肽类物质,在体内具有抑制激素和消化液分泌、抑制神经元的活动、增强戊巴比妥的麻醉作用、调控机体免疫功能等抑制性介质的活性[1,2]。本研究通过测定脑出血后下丘脑、血肿周边脑组织SS活性及SSmRNA表达变化,从而阐明脑出血时SS的病理生理作用及意义。
1 材料与方法
1.1 实验动物及模型 Wistar大鼠,雄性,体重275±25 g,参照Rosenberg[3]及任泽光[4]等的方法加以改进,胶原酶加肝素联合注射建立脑出血动物模型,手术对照组不注入胶原酶及肝素。
, http://www.100md.com
1.2 动物观测时相点、测定部位 取出血前(Pre)、出血30 min(H30min)、3 h(H3h)、6 h(H6h)、12 h(H12h)、24 h(H24h)、48 h(H48h)、72 h(H72h)8个时相点,取下丘脑、血肿周边脑组织进行SS、SSmRNA测定。
1.3 SS活性测定 活杀大鼠后即刻取出脑组织入100℃生理盐水煮5 min,分离出下丘脑、血肿周边组织,置匀浆器(0.1 N HCl的匀浆液)匀浆,离心取上清液备测。SS活性测定用放射免疫法。其具体操作依药盒说明书进行。
1.4 SSmRNA表达测定 麻醉动物,开胸行主动脉插管,行多聚甲醛灌注后,取出全脑,行脱水,后固定、冰冻切片,用地高辛标记的SSmRNA探针与脑组织原位杂交,杂交采用漂浮法。
1.5 模型成功的评分判断 1级:将大鼠尾巴提起,瘫痪侧前肢回收屈曲于腹下,正常侧前肢向地面伸展;2级:除1级体征外,向瘫痪侧推大鼠时阻力较对侧明显降低;3级:除以上体征外,大鼠有向瘫痪侧旋转的行为。
, 百拇医药
1.6 统计学处理 所有数据均以
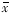 ±s表示,采用Microsoft Excel 7.0数理统计,组内自身对照和配对数据用配对t检验,组间比较采用方差分析t检验。采用MAS-1图像分析系统进行SSmRNA阳性细胞密度计量。对单位面积阳性细胞作t检验。
±s表示,采用Microsoft Excel 7.0数理统计,组内自身对照和配对数据用配对t检验,组间比较采用方差分析t检验。采用MAS-1图像分析系统进行SSmRNA阳性细胞密度计量。对单位面积阳性细胞作t检验。2 结果
2.1 血肿周边脑组织SS活性变化 对照组:术后3~6 h SS有轻度升高趋向,12 h开始回落到术前水平,但均无显著差异。出血组:术后30 min及3 h虽有升高,但与对照组比较无差异,出血后6 h显著升高,于12~24 h达峰值,48 h后明显回落,详见表1。Tab1 SS activity(pg/mg) of perihematoma with ICH(
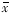 ±s,n=5)
±s,n=5), 百拇医药
Pre
H30min
H3h
H6h
H12h
H24h
H48h
H72h
Control
133.77±26.63
140.83±19.35
159.82±8.42
, http://www.100md.com
169.84±25.28
132.71±15.80
122.37±7.85
125.42±11.20
122.04±8.31
ICH
120.33±2.750
126.38±15.01
156.20±15.14c
227.97±23.20cd
247.94±21.66cf
, http://www.100md.com
253.31±27.78cf
189.84±21.42cf
148.41±30.76
a:P<0.05 b:P<0.01 c:P<0.001 compared with Pre; d:P<0.05 e:P<0.01 f:P<0.001 compared with control
2.2 下丘脑SS活性变化 对照组:术后3 h SS含量有明显升高,6 h降至术前水平。出血组:3 h SS虽比出血前有明显升高,但与对照组比较无显著差异,12~24 h达峰值,到72 h虽仍高于术前水平,但也无显著差异(见表2)。
Tab2 SS activity(pg/mg) of hypothalamus area with ICH(
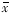 ±s,n=5)
±s,n=5), http://www.100md.com
Pre
H30min
H3h
H6h
H12h
H24h
H48h
H72h
Control
643.87±103.36
688.29±150.38
916.90±667.47a
, http://www.100md.com
667.17±106.26
713.8±555.66
626.01±106.31
584.67±72.84
664.60±146.39
ICH
607.89±120.67
800.99±192.32
969.93±142.02c
1245.59±219.54bd
, http://www.100md.com 1541.61±277.17cf
1523.74±389.71bf
1131.77±203.27bf
667.12±166.76
a:P<0.05 b:P<0.01 c:P<0.001 compared with Pre; d:P<0.05 e:P<0.01 f:P<0.001 compared with control
2.3 脑组织SSmRNA表达变化
2.3.1 下丘脑SSmRNA表达变化 对照组:术后3 h明显升高,随后降至正常。出血组:出血后3 h开始升高,并于12 h达峰值,然后开始下降(详见表3,图1)。
, 百拇医药
Tab3 SSmRNA expression of hypothalamus
areas (cells/mm3,
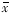 ±s,n=5)
±s,n=5)Pre
H3h
H12h
H72h
Control
27.44±4.58
36.87±5.71a
30.39±6.96
, 百拇医药
34.34±8.76
ICH
30.29±5.95
73.36±10.80cf
120.97±97cf
74.98±13.28cf
a:P<0.05 b:P<0.01 c:P<0.001 compared with Pre;
d:P<0.05 e:P<0.01 f:P<0.001 compared with control

, http://www.100md.com
Photo l SSmRNA expression
surrouding hematoma at ICH 12 h×100
2.3.2 血肿周边脑组织SSmRNA表达变化 对照组:术后3 h明显升高,随后降至正常。出血组:出血后3 h开始升高,并于12 h达峰值,然后开始下降(详见表4,图2)
Tab4 SSmRNA expression of perihematoma
(cells/mm3,
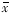 ±s,n=5)
±s,n=5)Pre
H3h
, 百拇医药
H12h
H72h
Control
37.56±7.18
47.86±3.88a
38.70±9.72
38.89±8.09
ICH
39.99±7.17
59.30±6.62bd
83.651±7.77ce
, 百拇医药
50.06±10.75
a:P<0.05 b:P<0.01 c:P<0.001 compared with Pre;
d:P<0.05 e:P<0.01 f:P<0.001 compared with control

Photo 2 SSmRNA expression in
hypothalamus at ICH 12 h×100
3 讨论
中枢神经系统损伤时组织SS含量的变化,国内外文献对此报道不尽一致。Rosenberg[3]报道颅脑外伤和实验性脑缺血动物血浆及脑组织中SS含量明显升高,且随外伤严重程度和时间的延长而递增。缺血和颅脑外伤脑组织SS含量明显升高,且与脑组织H2O含量显著正相关。近期的研究表明SS可以作为一种调质,调节谷氨酸介导的CNS过度兴奋[5]。
, 百拇医药
本研究发现脑出血后下丘脑及血肿周边脑组织SS含量升高,并于出血后12~24 h达峰值,48 h后逐渐下降。同时,SS活性与脑出血血肿容量相关。用地高辛标记的SScDNA探针位杂交表明脑出血后下丘脑与血肿周边脑组织SSmRNA表达明显增强,其阳性细胞计数的PC值在出血后3 h明显增高,并在12 h达高峰,比较同部位SS活性与SSmRNA表达的PC值,两者明显相关,充分说明下丘脑及血肿周边脑组织SS活性升高是局部SS合成增强所致。
在机体内SS既可作为激素也可做为神经递质发挥作用[6],因此,对下丘脑及血肿周边脑组织SS活性增高的意义作以下推测:SS与SS受体(SSR)结合形成SSR-SS复合物,使抑制性亚型G蛋白(Gi蛋白)活化,后者与GTP结合抑制胸膜内腺苷酸环化酶的活性,使cAMP生成减少,导致神经元能量代谢障碍。由于cAMP具有促进SS转录的作用[7],cAMP的减少,使SSmRNA的表达减弱,可能是减轻神经元损伤的一种代偿机制。下丘脑SS活性增强,抑制下丘脑内分泌细胞由第二信使增高引起的激素分泌(近端效应),从而促发中枢神经系统内分泌紊乱,导致机体内环境的失衡。同时SS刺激抗利尿激素的分泌,从而导致肾小管对水的重吸收增多,尿量减少,加重血肿周边脑水肿。SS通过SSR与GK蛋白结合,使膜K+通道开放,膜趋极化从而抑制了神经细胞的活动,加重神经细胞功能障碍。SS-SSR复合物与Ge蛋白结合也抑制了细胞胞吐,导致下丘脑内分泌细胞众多激素的分泌抑制(远端效应)。SS通过调节血肿周边血管的张力,使血管扩张,从而加重出血区血液的渗出及脑细胞水肿。
, 百拇医药
[参考文献]
[1]Karalis K,Mastorakos G,Chrousos GP,et al.Somatostation analogs suppress the inflammatory reaction in vivo[J]. J Clin Invest,1994,93:2000.
[2]Karalis K,Mastorakos G,Hajme S,Roralcl L,et al.Somatostatin may participate in the autiinflammatory actions of glucoclrticoeds[J].Endocrinology,1995,136:4133.
[3]Rosenberg GB,Shelia Mun-Bryce,Mary Wesley,et al.Collagenase-induced intracerebral emrrhage in rats[J].Stroke,1990,21:801.
, 百拇医药
[4]任泽光,吴建中.大鼠脑出血模型[J].中华神经外科杂志,1993,9:205.
[5]Vezzani A,Rizzi M,Conti M,et al.Modulatory role of neuropepeides in seizures induceded in rats by seimulation of glueamate receptors[J].J Nuer,2000,130(4 SSuppl):1046S-8S.
[6]Mendelow AD.Mechamins of ischemic brain damage with intracerebralhemorrhage[J].Stroke,1993,24:I-115.
[7]Montminy M,Brindle P,Arias J,et al.Regulation of somatostatin gene transcription by cyclic adenosine monophosphate[J].Metabolism,1996,45(8 Suppl):4-7.
[收稿:1999-08-10,修回:1999-03-25], 百拇医药