��ަ���NMDA�������������������������Ը�ǰ�Է���ԭ��ǰǿ����ԭmRNA�����Ӱ��
�Է���ԭ��ǰǿ����ԭmRNA�����Ӱ��*
���ݷ� лС�� ���Ļ� �����
ժ Ҫ Ŀ�� �۲춾ަ��(M)�������������������������Ը�ǰ�Է���ԭ(preproenkephalin,PPE)��ǰǿ����ԭ(preprodynorphin,PPD)mRNA�����Ӱ�졣���� ����������ת¼�ۺ�ø����Ӧ(RT-PCR)���Ԧ�-actin mRNAΪ�ڱ�����PPE��PPD mRNA�� ��� ���������������Ը�PPE������������������ȶ��������ӣ������������ע������ͪ������Ϸ�Ӧ����PPE����������ӣ����Ը��б仯�����ԡ����������������Ը�PPD������ﶼ�������������飬��Ƚ�Ϸ�Ӧʱ����PPD���������1 h�仯�����ԣ�2 hʱ���ӵ���ֵ��4 hʱ�Ը��������飬���Ը�ǿ���Ļ��������1 h��2 h��4 hʱ�����Լ��١���M������������ݹ�м��M1����pirenzepine�������������Ը�PPE��PPD�������Ͻ��1 h���в�ͬ�̶ȵ����ӣ���NMDA��������MK 801������, ������Ը���PPE����Ͻ����1 h�����Բ��죬������Ը�PPD�������Ͻ�����������ӣ�����NOS���Ƽ�L-N-�������������(L-NAME)�������������Ը�PPE�������Ͻ��1 h���в�ͬ�̶ȵ�����,������Ը�PPD�������仯�����ԡ�������Ը��Ц�-actin��������ڸ�������֮��û�в�𡣽��� M����������NMDA����������NOS���Ƽ�����Ƚ�Ϸ�Ӧʱ���ӣ�PPE ��PPD����������ӿ�����������Ч������Ƚ��֢״�Ļ���֮һ��
, http://www.100md.com
�ؼ��ʣ���� ��Ϸ�Ӧ ǰ�Է���ԭ ǰǿ����ԭ һ��������ø ��ަ������ NMDA����
�Է�����Դ��Ƭ���������������о���ʾ��Դ��Ƭ��ϵͳ�������ಡ��������Ӧ��������ʹ��Ӧ����Ӧ���ݿ˵ȡ���Դ��Ƭ����ǿ���ĺ��Է�����������������ܲ��������йأ�����������û�������Ϊֹ��Ȼ����������б�����������Դ�����ǿ���ĺ��Է������߷�Ӧ���ʺ�ǰǿ���ĺ�ǰ�Է���mRNA�ڲ�ͬ�����з����ı�[1]�������һ�����ע��ǿ���ĺ��Է��ľ�����ʹ���ã����ɿ��Ʋ�����Ƚ��֢״[2��3]���½���Simonia��[4]ͨ���ʰ�Ƭ����ȱʧ��С��֤ʵ�ʰ�Ƭ���������ʹ���ͱ�Ե�˶��ͦʰ�Ƭ���弤����U-50��488H����ʹ�����ЧӦ��ؼ����ã��Լ�������Ƚ��֢״�ı��Fukunaga��[5]������Ƚ��ʱ���Ե�ˮ����Χ������(cPAG)PPE mRNA���ӣ�ע���Է���ͬϵ�ﵽcPAG�ܼ��ٶ������Ծ������ˣ���Դ��ǿ���ĺ��Է��������ǵ������Խ�ϵİ�Ƭ����ʺͦ�֮���ƽ������������ͽ���з������á���ʵ�����о����ֶ�ަ��(M)��������[6]��NMDA��������[7]��NOS���Ƽ�[8]����������ͽ�Ϸ�Ӧ�����������ã��Ʋ����Ƕ�Ƭ�������Ź�ͬ�����û�����������û��M����������NMDA����������NOS���Ƽ�����������ͽ��ʱ����PPE��PPD mRNAӰ��ı��������IJ���RT-PCR���������������ͽ�ϴ�������Ը�PPE��PPD mRNA�ı���۲������Щ�����PPE��PPD mRNA�ı����Ӱ�졣
, http://www.100md.com
1 ���Ϻͷ���
1.1 �Լ� ���ϵ������һ��ҩ����Ʒ(����980401)������ͪ��MK 801��pirenzepine������ݹ�мL-N-Nitro-arginine methylester(L-NAME)��ϵSigma��˾��Ʒ����RNA��ȡ�Լ��У�RNA��ת¼�Լ��о�ΪPromega��˾��Ʒ��PCR�Լ��У���֬�ǣ�PCR Markerϵ������˾��Ʒ��DEPCϵFluka��˾��Ʒ�������Լ���Ϊ��������
1.2 ������ϴ��������� �� Sprague-Dawley�������Ϻ����������ṩ������(250��20)g����������[6]������Ƥ��ע�䣬����10 mg.kg-1(bid)������ÿ������10 mg.kg-1����d 6ĩ��ע��50 mg.kg-1��ȣ������������ģ�͡����鶯��Ϊ��������飬��ǻע������ͪ4 mg.kg-1�ɼ������֢״�����鶯��Ϊ��Ƚ���顣����ͪ�������֢״1 h��2 h��4 h�����Ĵ���ֱ�Ϊ���1 h�飬���2 h�飬���4 h�顣������ͪ����ǰ30 min��ǻע��MK 801(0.125 mg.kg-1)��M1��������pirenzepine(10 mg.kg-1)������ݹ�м�(0.5 mg.kg-1)��NOS���Ƽ�L-NAME(10 mg.kg-1)���������֢״1 h�����Ĵ���ΪMK801�����顢pirenzepine�����顢����ݹ�м�����L-NAME�����顣
, http://www.100md.com
1.3 ������� ���Ϻ����﹤�̹�˾�ϳɣ���������,�����������зֱ�Ϊ��PPE[9]���������5��GTC CAC CAT TGG TTC AGA AGG 3���������5��ACC GCA TAA AGC CTC CGT ATC 3��������723 bp��Ƭ�Ρ�PPD[10]����������5��CTG CCG ATC TTT GTT AGC CTC TG 3����������5�� ATC CAA GAT GCA GAA GGA GCC 3��������602 bp��Ƭ�Ρ���-actin[11]����������A��5��TCA TGA AGT GTG ACG TTG ACA TCC GTA AAG 3����������B��5��CCT AGA AGC ATT TGC GGT GCA CGA TGG AGG 3��������409 bp��Ƭ�Ρ�
1.4 ��RNA��ȡ �����ͷ������Ѹ�ٷ���ȡ��������Ը�Լ100 mg�����Լ���˵���������õ�RNA��������20 ��l��RNase��ˮ�ܽ⣬����ֹ��ȼƲⶨ��RNAŨ�ȣ�A260 nm/A280 nmΪ1.8��2.0�����ü�ȩ����������Ӿ������������ȡ��RNA��-70�汣�档
, http://www.100md.com
1.5 ��ת¼��Ӧ ȡ2 ��g RNA 65�����3 min���뷴Ӧ����Һ�������Ϊ20 ��l������Tris-HCl 10 mmol.L-1��pH 8.3��KCl 50 mmol.L-1��Triton X-100 0.1%��MgCl2 2.5 mmol.L-1��dNTPs 0.2 mmol.L-1��DTT 5 mmol.L-1��RNAø���Ƽ�20 U��AMV��ת¼ø23 U��oligo(dT) 0.5 ��g��42�淴Ӧ60 min��95�� 5 min��ֹ��Ӧ����ˮϡ����100 ��l��
1.6 PCR��Ӧ ȡ��ת¼��ӦҺ20 ��l���ֱ����PPE��PPD�ͦ�-actin�����PCR������PCR��ӦҺ�����Ϊ50 ��l������Tris-HCl 10 mmol.L-1��pH 8.3��KCl 50 mmol.L-1��Triton X-100 0.1%��MgCl2 1.5 mmol.L-1��dNTPs 0.2 mmol.L-1��DTT 5 mmol.L-1���ϡ����������50 pmol��95�����10 min����Taq DNA�ۺ�ø2.5 U���ٸ���ʯ����50 ��l��94�����3 min�����PCRѭ��(AMPLITRON��˾PCR��)������Ϊ��94�����30 s��59���˻�30 s��72������1 min�����35��ѭ����72��������10 min���ñ�ԡ�С�ȡ10 ��l PCR������1.5%����֬�������ϵ�Ӿ��5 V/cm��50 min�����Զ�������(FOTODYNE��˾)�۲����ա�
, ��Ĵҽҩ
2 ���
2.1 ���������������Ը�ǰ�Է���ԭmRNA�ı��� ��ȡ��RNA��ȩ����������Ӿ�Ͽ�����������28S��18S��������������֮��Ϊ2��1������RNA��������û�н��⣬����Ϊ��ת¼��Ӧ��ģ�塣��PPE������������Ƭ�γ�Լ700 bp������Ƶ�PPE����Ƭ�γ�723 bp��һ�¡�ͼ1��ͼ2��ʾ,���������ʱ������Ը�PPE���������������ӣ�����ͪ������1 h��2 h��4 h,������PPE�������������������������ӣ����Ը�PPE���������������û�����Բ��졣������ͪ����ǰ30 min��ǻ�ֱ�ע��M1��������pirenzepine(10 mg.kg-1)������ݹ�м�(0.5 mg.kg-1)��NOS���Ƽ�L-NAME(10 mg.kg-1)������Ը���PPE��������Ͻ��1 h���������ӣ�pirenzepine �����鼹����PPE�����������������������Ϊ����ݹ�м��L-NAME�����飬����ߴ����������ƣ����Ը��м���ݹ�м����PPE��������������Ϊ���ԣ����ΪL-NAME�顣MK 801(0.125 mg.kg-1)����������Ը���PPE��������Ͻ����1 h�����Բ��졣�����-actin������û�в���(ͼ1��ͼ2)��
, http://www.100md.com
Fig 1 Agrose gel electrophoresis of preproenkaphalin and
��-actin specific RT-PCR products in spinal cord
A: PCR marker; B: morphine dependence; C: control; D: morphine withdrawal 1 h;E:morphine withdrawal 2 h;F:morphine withdrawal 4 h;G:MK801 treatment;H: pirenzepine treatment; I: scopolamine pretreatment;J: L-NAME treatment.Upper: the specific product bands for proenkaphalin. Lower: the specific product bands for ��-actin.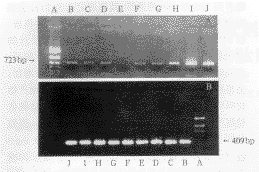
, http://www.100md.com
Fig 2 Agrose gel electrophoresis of proenkaphalin and
��-actin specific RT-PCR products in brain stem
A: PCR marker; B: morphine dependence; C: control; D: morphine withdrawal 1 h; E:morphine withdrawal 2 h; F: morphine withdrawal 4 h; G: MK 801 treatment; H: pirenzepine treatment; I: scopolamine treatment;J: L-NAME treatment.Upper: the specific product bands for proenkaphalin. Lower: the specific product bands for ��-actin.
, ��Ĵҽҩ
2.2 ���������������Ը�ǰǿ����ԭmRNA�ı��� ��PPD������������Ƭ�γ�Լ600 bp������Ƶ�PPD����Ƭ�γ�602 bp��һ�¡�ͼ3��ʾ, ���������ʱ������Ը�PPD����������٣�����ͪ����1 h,������Ը�PPD�����������Լ��٣�����2 h��4 h��,������PPD����������������������ӣ����Ը���PPD��������������������١� ������ͪ����ǰ30 min��ǻע��pirenzepine(10 mg.kg-1)������ݹ�м�(0.5 mg.kg-1)��MK 801(0.125 mg.kg-1)������Ը���PPD��������Ͻ��1 h���������ӣ�pirenzepine������PPD��������������Ϊ������L-NAME(10 mg.kg-1)����������PPD��������Ͻ����1 h�����Բ��죬�Ը�PPD��������Ͻ����1 h���١������-actin������û�в���(ͼ1��ͼ2)��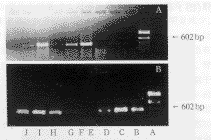
, ��Ĵҽҩ
Fig 3 Agrose gel electrophoresis of prodynorphin specific
RT-PCR products in spinal cord and brainstern
A: PCR marker; B: morphine dependence; C: control; D: morphine withdrawal 1 h; E: morphine withdrawal 2 h; F: morphine withdrawal 4 h; G: MK 801 treatment; H: pirenzepine treatment; I: scopolamine treatment;J: L-NAME treatment.Upper: the specific product bands for prodynorphin in spinal cord. Lower: the specific product bands for prodynorphin in brain stem.
, ��Ĵҽҩ
3 ����
�밢Ƭ����ʺͦĽ�ϵ���Դ��Ƭ��Ϊǿ���ĺ��Է��ġ��б���������Դ�������Դ��Ƭ����ǿ���ĺ��Է��ĵ����߷�Ӧ���ʺ�mRNA�����仯��ע����Щ��Ƭ�IJ���������ʹ���ã����ɿ��Ʋ�����Ƚ��֢״����ʵ�鷢��������Դ���������Ը�PPE�������������������ӣ���������Ը�PPD������ﶼ�����������������������ע������ͪ������Ϸ�Ӧ1 h����PPE����������ӣ�2 h��PPD����������ӣ����Ը���PPE�������仯�����ԣ�PPD����������Լ��١�������Ը��ǽ鵼���������������Ҫ��λ�������Է��ĺ����Է��IJ�����ע�������С�����Ծ��Ӧ������ע��D-Ala,D-Leu�Է���(DADLE)(60 ��g.kg-1)���ƺ����������ߵĽ��֢״[2]��Dyn A(1-13)����ע�������ע�������ʪ��ҡ��,�����κ���ë,��������ע��û��Ч��,�������ƺ����������ߵĽ��֢״[3]�������Simonia��[4]ͨ���ʰ�Ƭ����ȱʧ��С��֤ʵ�ʰ�Ƭ���������ʹ���ͱ�Ե�˶��ͦʰ�Ƭ���弤����U-50 488H����ʹ�����ЧӦ��ؼ�����,���Ҳ�����Ƚ��֢״�ı���б���Ӧ�÷���RNA����֤ʵ�İ�Ƭ���������ȵĽ���ЧӦ�ͽ�Ϸ�Ӧ[13]����ˣ�������Դ���Է��ĺ�ǿ���ĵĻ��������ڿ�����ȵĽ��֢״������ġ�
, http://www.100md.com
������ʾM1��������pirenzepine�ͼ���ݹ�м�����������Ը�PPE�����PPD�������Ͻ��1 h���в�ͬ�̶ȵ����ӣ��б�������ע��С����ǿ���ĺ��Է�����ʹ������Эͬ����[14]����ˣ�M������Ϻ�����Ը�����Դ��PPE��PPD���ӿ����ǵ����������������ư�Ƭ���֢״�Ļ���֮һ[6]���б�������ע��ǿ�����������IJ�������������ͨ��NMDA���������ã���Դ��ǿ���Ŀ���ͨ��ͻ��ǰ�ٽ��˷�����������ͷţ���NMDA��������������ֹǿ������̱�����ã����Ҽ���ǿ���IJ����ĵ���������֯ѧ�ı�[12]�����ķ���NMDA��������MK801������, ������Ը���PPE����Ͻ���������Բ��죬��������Ը�PPD�������Ͻ�����������ӣ������ʾNMDA������ǿ����֮����ܴ����Ż�����ڵĻ��ơ��ڱ�����ʾ������MK 801����Ƚ��֢״��һ�������ã�����������NMDA���������յ���Դ��ǿ���ĵı�����������Կ��ư�Ƭ�����Ч�����û��ơ�����NOS���Ƽ�L-NAME�������������Ը�PPE�������Ͻ�����в�ͬ�̶ȵ�����,������Ը�PPD�������仯�����ԡ�M����������NMDA����������NO��ø���Ƽ�����Ƚ��֢״������������[8],���Ƕ�PPE��PPD���������ڵĻ����Բ����������PPE��PPD�Ļ������������[15��16]��PPE�������ж���cAMP���Ԫ����PPD��������AP-1�Ľ��Ԫ������M���塢NMDA������ϸ������Ϣ����;����cAMP��PKC��Ca2+ż��������б�Ҫ̽������Ƚ��ʱM����������NMDA����������NOS���Ƽ���PPE��PPD���������ز���Ļ��ơ�
, http://www.100md.com
*�㽭ʡҽѧ��ѧ����������No 98A093
����飺���ݷң�34�꣬�����о�Ա��1987���ҵ�ں��ݴ�ѧ����ϵ����Ҫ���·�������ѧ���о���
�������62�꣬�о�Ա����Ҫ����ҩ�������Ļ��ƺͷ��ε��о�
���ݷ�(�㽭ʡ���в�ѭ����ݹ����ҩ�о���.�����䶾�о����ģ����� 315010)
лС��(�㽭ʡ���в�ѭ����ݹ����ҩ�о���.�����䶾�о����ģ����� 315010)
���Ļ�(�㽭ʡ���в�ѭ����ݹ����ҩ�о���.�����䶾�о����ģ����� 315010)
�����(�㽭ʡ���в�ѭ����ݹ����ҩ�о���.�����䶾�о����ģ����� 315010)
, ��Ĵҽҩ
�����
1��Uhl GR, Ryan JP, Schwartz JP.Morphine alters preproenkephalin gene expression.Brain Res��1988;459:391��7
2��Bhargava HN. Opioid-like action of methionine-enkephalin in inhibiting morphine abstinence syndrome. Eur J Pharmacol, 1977;41:81��4
3��Takemori AE, Loh HH, Lee NM. Supression of dynorphin A (1��13) of the expression of opiate withdrawal and tolerance in mice. Eur J Pharmacol, 1992;221:223��6
, ��Ĵҽҩ
4��Simonin F, Valverde O, Smadja C et al. Disruption of the kappa-opioid receptor gene in mice enhances sensitivity to chemical visceral pain, impairs pharmacological actions of the selective kappa-agonist U-50,488H and attenuates morphine withdrawal. EMBO J, 1998;17:886��97
5��Fukunaga Y, Inoue N, Miyamoto M et al. Effects of peptidase inhibitors,[D-Ala2,Mek5]-enkephaminamide and antiserum to methionine-enkaphalin microinjected into the caudal periaqueductal gray on morphine withdrawal in rats. Jpn J Pharmacol,1998;78:455��61
, http://www.100md.com
6�������,���Ļ�,�Ÿ�ǿ��.ѡ���Զ�ަ��������������������ܺ�������ʵ���о�.�л�ҽѧ��־,1997;77:130��3
7��Thorat SN, Barjavel M, Matwyshyn GA��Bhargava HN. Comparative effects of N-monomethyl-L-arginine and MK801 on the abstinence syndrome in morphine-dependent mice. Brain Res, 1994;642:153��9
8�����Ļ����� ����лС�� et al.���������������Ը�һ�����������ͺ�ø��������.�й�ҩ����������־, 1999;8(2):95��7
9��Rosen H, Douglass J, Herbert E. Isolation and charactrization of the rat proenkephalin gene. J Biol Chem��1984;259:14309��13
, ��Ĵҽҩ
10��Douglass J, Mcmurray CT, Garrett JE et al. Characterization of the rat prodynorphin gene. Mol Endocrinol, 1989;3:2070��8
11��Tokunaga K, Taniguchi H, Yoda K et al. Nucleotide sequence of a full-length cDNA for mouse cytoskeletal beta-actin mRNA. Nucleic Acids Res,1986;14:2829��33
12��Bakshi R, Ni RX, Faden AI. N-methyl-D-aspartate(NMDA) and opioid receptors mediate dynorphin-induced spinal cord injury: behavioral and histological studies. Brain Res�� 1992;580:255��64
, ��Ĵҽҩ
13��Suzuki T, Ikeda H, Tsuji M et al. Antisense oligodeoxynucleotide to �� receptors attenuates morphine dependence in mice.Life Science,1997;61:165��70
14�������죬��������Ԭ ع et al.2��15 Hz����̼���ʹ���弹����ͬʱ�ͷż����ĺ�ǿ����A.����ҽ�ƴ�ѧѧ����1992��24��807��9
15��Comb M, Mermod N, Hyman SE et al.Proteins bound at adjacent DNA elements act synergistically to regulate human proenkaphalin cAMP inducible transcription. EMBO J, 1988;7:3793��805
16��Civelli O, Douglass J, Goldstein A et al. Sequence and expression of the rat prodynorphin gene. Proc Natl Acad Sci USA��1985;82;4291��429, ��Ĵҽҩ(�Է���ԭ��ǰǿ����ԭmRNA�����Ӱ��*)
���ݷ� лС�� ���Ļ� �����
ժ Ҫ Ŀ�� �۲춾ަ��(M)�������������������������Ը�ǰ�Է���ԭ(preproenkephalin,PPE)��ǰǿ����ԭ(preprodynorphin,PPD)mRNA�����Ӱ�졣���� ����������ת¼�ۺ�ø����Ӧ(RT-PCR)���Ԧ�-actin mRNAΪ�ڱ�����PPE��PPD mRNA�� ��� ���������������Ը�PPE������������������ȶ��������ӣ������������ע������ͪ������Ϸ�Ӧ����PPE����������ӣ����Ը��б仯�����ԡ����������������Ը�PPD������ﶼ�������������飬��Ƚ�Ϸ�Ӧʱ����PPD���������1 h�仯�����ԣ�2 hʱ���ӵ���ֵ��4 hʱ�Ը��������飬���Ը�ǿ���Ļ��������1 h��2 h��4 hʱ�����Լ��١���M������������ݹ�м��M1����pirenzepine�������������Ը�PPE��PPD�������Ͻ��1 h���в�ͬ�̶ȵ����ӣ���NMDA��������MK 801������, ������Ը���PPE����Ͻ����1 h�����Բ��죬������Ը�PPD�������Ͻ�����������ӣ�����NOS���Ƽ�L-N-�������������(L-NAME)�������������Ը�PPE�������Ͻ��1 h���в�ͬ�̶ȵ�����,������Ը�PPD�������仯�����ԡ�������Ը��Ц�-actin��������ڸ�������֮��û�в�𡣽��� M����������NMDA����������NOS���Ƽ�����Ƚ�Ϸ�Ӧʱ���ӣ�PPE ��PPD����������ӿ�����������Ч������Ƚ��֢״�Ļ���֮һ��
, http://www.100md.com
�ؼ��ʣ���� ��Ϸ�Ӧ ǰ�Է���ԭ ǰǿ����ԭ һ��������ø ��ަ������ NMDA����
�Է�����Դ��Ƭ���������������о���ʾ��Դ��Ƭ��ϵͳ�������ಡ��������Ӧ��������ʹ��Ӧ����Ӧ���ݿ˵ȡ���Դ��Ƭ����ǿ���ĺ��Է�����������������ܲ��������йأ�����������û�������Ϊֹ��Ȼ����������б�����������Դ�����ǿ���ĺ��Է������߷�Ӧ���ʺ�ǰǿ���ĺ�ǰ�Է���mRNA�ڲ�ͬ�����з����ı�[1]�������һ�����ע��ǿ���ĺ��Է��ľ�����ʹ���ã����ɿ��Ʋ�����Ƚ��֢״[2��3]���½���Simonia��[4]ͨ���ʰ�Ƭ����ȱʧ��С��֤ʵ�ʰ�Ƭ���������ʹ���ͱ�Ե�˶��ͦʰ�Ƭ���弤����U-50��488H����ʹ�����ЧӦ��ؼ����ã��Լ�������Ƚ��֢״�ı��Fukunaga��[5]������Ƚ��ʱ���Ե�ˮ����Χ������(cPAG)PPE mRNA���ӣ�ע���Է���ͬϵ�ﵽcPAG�ܼ��ٶ������Ծ������ˣ���Դ��ǿ���ĺ��Է��������ǵ������Խ�ϵİ�Ƭ����ʺͦ�֮���ƽ������������ͽ���з������á���ʵ�����о����ֶ�ަ��(M)��������[6]��NMDA��������[7]��NOS���Ƽ�[8]����������ͽ�Ϸ�Ӧ�����������ã��Ʋ����Ƕ�Ƭ�������Ź�ͬ�����û�����������û��M����������NMDA����������NOS���Ƽ�����������ͽ��ʱ����PPE��PPD mRNAӰ��ı��������IJ���RT-PCR���������������ͽ�ϴ�������Ը�PPE��PPD mRNA�ı���۲������Щ�����PPE��PPD mRNA�ı����Ӱ�졣
, http://www.100md.com
1 ���Ϻͷ���
1.1 �Լ� ���ϵ������һ��ҩ����Ʒ(����980401)������ͪ��MK 801��pirenzepine������ݹ�мL-N-Nitro-arginine methylester(L-NAME)��ϵSigma��˾��Ʒ����RNA��ȡ�Լ��У�RNA��ת¼�Լ��о�ΪPromega��˾��Ʒ��PCR�Լ��У���֬�ǣ�PCR Markerϵ������˾��Ʒ��DEPCϵFluka��˾��Ʒ�������Լ���Ϊ��������
1.2 ������ϴ��������� �� Sprague-Dawley�������Ϻ����������ṩ������(250��20)g����������[6]������Ƥ��ע�䣬����10 mg.kg-1(bid)������ÿ������10 mg.kg-1����d 6ĩ��ע��50 mg.kg-1��ȣ������������ģ�͡����鶯��Ϊ��������飬��ǻע������ͪ4 mg.kg-1�ɼ������֢״�����鶯��Ϊ��Ƚ���顣����ͪ�������֢״1 h��2 h��4 h�����Ĵ���ֱ�Ϊ���1 h�飬���2 h�飬���4 h�顣������ͪ����ǰ30 min��ǻע��MK 801(0.125 mg.kg-1)��M1��������pirenzepine(10 mg.kg-1)������ݹ�м�(0.5 mg.kg-1)��NOS���Ƽ�L-NAME(10 mg.kg-1)���������֢״1 h�����Ĵ���ΪMK801�����顢pirenzepine�����顢����ݹ�м�����L-NAME�����顣
, http://www.100md.com
1.3 ������� ���Ϻ����﹤�̹�˾�ϳɣ���������,�����������зֱ�Ϊ��PPE[9]���������5��GTC CAC CAT TGG TTC AGA AGG 3���������5��ACC GCA TAA AGC CTC CGT ATC 3��������723 bp��Ƭ�Ρ�PPD[10]����������5��CTG CCG ATC TTT GTT AGC CTC TG 3����������5�� ATC CAA GAT GCA GAA GGA GCC 3��������602 bp��Ƭ�Ρ���-actin[11]����������A��5��TCA TGA AGT GTG ACG TTG ACA TCC GTA AAG 3����������B��5��CCT AGA AGC ATT TGC GGT GCA CGA TGG AGG 3��������409 bp��Ƭ�Ρ�
1.4 ��RNA��ȡ �����ͷ������Ѹ�ٷ���ȡ��������Ը�Լ100 mg�����Լ���˵���������õ�RNA��������20 ��l��RNase��ˮ�ܽ⣬����ֹ��ȼƲⶨ��RNAŨ�ȣ�A260 nm/A280 nmΪ1.8��2.0�����ü�ȩ����������Ӿ������������ȡ��RNA��-70�汣�档
, http://www.100md.com
1.5 ��ת¼��Ӧ ȡ2 ��g RNA 65�����3 min���뷴Ӧ����Һ�������Ϊ20 ��l������Tris-HCl 10 mmol.L-1��pH 8.3��KCl 50 mmol.L-1��Triton X-100 0.1%��MgCl2 2.5 mmol.L-1��dNTPs 0.2 mmol.L-1��DTT 5 mmol.L-1��RNAø���Ƽ�20 U��AMV��ת¼ø23 U��oligo(dT) 0.5 ��g��42�淴Ӧ60 min��95�� 5 min��ֹ��Ӧ����ˮϡ����100 ��l��
1.6 PCR��Ӧ ȡ��ת¼��ӦҺ20 ��l���ֱ����PPE��PPD�ͦ�-actin�����PCR������PCR��ӦҺ�����Ϊ50 ��l������Tris-HCl 10 mmol.L-1��pH 8.3��KCl 50 mmol.L-1��Triton X-100 0.1%��MgCl2 1.5 mmol.L-1��dNTPs 0.2 mmol.L-1��DTT 5 mmol.L-1���ϡ����������50 pmol��95�����10 min����Taq DNA�ۺ�ø2.5 U���ٸ���ʯ����50 ��l��94�����3 min�����PCRѭ��(AMPLITRON��˾PCR��)������Ϊ��94�����30 s��59���˻�30 s��72������1 min�����35��ѭ����72��������10 min���ñ�ԡ�С�ȡ10 ��l PCR������1.5%����֬�������ϵ�Ӿ��5 V/cm��50 min�����Զ�������(FOTODYNE��˾)�۲����ա�
, ��Ĵҽҩ
2 ���
2.1 ���������������Ը�ǰ�Է���ԭmRNA�ı��� ��ȡ��RNA��ȩ����������Ӿ�Ͽ�����������28S��18S��������������֮��Ϊ2��1������RNA��������û�н��⣬����Ϊ��ת¼��Ӧ��ģ�塣��PPE������������Ƭ�γ�Լ700 bp������Ƶ�PPE����Ƭ�γ�723 bp��һ�¡�ͼ1��ͼ2��ʾ,���������ʱ������Ը�PPE���������������ӣ�����ͪ������1 h��2 h��4 h,������PPE�������������������������ӣ����Ը�PPE���������������û�����Բ��졣������ͪ����ǰ30 min��ǻ�ֱ�ע��M1��������pirenzepine(10 mg.kg-1)������ݹ�м�(0.5 mg.kg-1)��NOS���Ƽ�L-NAME(10 mg.kg-1)������Ը���PPE��������Ͻ��1 h���������ӣ�pirenzepine �����鼹����PPE�����������������������Ϊ����ݹ�м��L-NAME�����飬����ߴ����������ƣ����Ը��м���ݹ�м����PPE��������������Ϊ���ԣ����ΪL-NAME�顣MK 801(0.125 mg.kg-1)����������Ը���PPE��������Ͻ����1 h�����Բ��졣�����-actin������û�в���(ͼ1��ͼ2)��

, http://www.100md.com
Fig 1 Agrose gel electrophoresis of preproenkaphalin and
��-actin specific RT-PCR products in spinal cord
A: PCR marker; B: morphine dependence; C: control; D: morphine withdrawal 1 h;E:morphine withdrawal 2 h;F:morphine withdrawal 4 h;G:MK801 treatment;H: pirenzepine treatment; I: scopolamine pretreatment;J: L-NAME treatment.Upper: the specific product bands for proenkaphalin. Lower: the specific product bands for ��-actin.

, http://www.100md.com
Fig 2 Agrose gel electrophoresis of proenkaphalin and
��-actin specific RT-PCR products in brain stem
A: PCR marker; B: morphine dependence; C: control; D: morphine withdrawal 1 h; E:morphine withdrawal 2 h; F: morphine withdrawal 4 h; G: MK 801 treatment; H: pirenzepine treatment; I: scopolamine treatment;J: L-NAME treatment.Upper: the specific product bands for proenkaphalin. Lower: the specific product bands for ��-actin.
, ��Ĵҽҩ
2.2 ���������������Ը�ǰǿ����ԭmRNA�ı��� ��PPD������������Ƭ�γ�Լ600 bp������Ƶ�PPD����Ƭ�γ�602 bp��һ�¡�ͼ3��ʾ, ���������ʱ������Ը�PPD����������٣�����ͪ����1 h,������Ը�PPD�����������Լ��٣�����2 h��4 h��,������PPD����������������������ӣ����Ը���PPD��������������������١� ������ͪ����ǰ30 min��ǻע��pirenzepine(10 mg.kg-1)������ݹ�м�(0.5 mg.kg-1)��MK 801(0.125 mg.kg-1)������Ը���PPD��������Ͻ��1 h���������ӣ�pirenzepine������PPD��������������Ϊ������L-NAME(10 mg.kg-1)����������PPD��������Ͻ����1 h�����Բ��죬�Ը�PPD��������Ͻ����1 h���١������-actin������û�в���(ͼ1��ͼ2)��

, ��Ĵҽҩ
Fig 3 Agrose gel electrophoresis of prodynorphin specific
RT-PCR products in spinal cord and brainstern
A: PCR marker; B: morphine dependence; C: control; D: morphine withdrawal 1 h; E: morphine withdrawal 2 h; F: morphine withdrawal 4 h; G: MK 801 treatment; H: pirenzepine treatment; I: scopolamine treatment;J: L-NAME treatment.Upper: the specific product bands for prodynorphin in spinal cord. Lower: the specific product bands for prodynorphin in brain stem.
, ��Ĵҽҩ
3 ����
�밢Ƭ����ʺͦĽ�ϵ���Դ��Ƭ��Ϊǿ���ĺ��Է��ġ��б���������Դ�������Դ��Ƭ����ǿ���ĺ��Է��ĵ����߷�Ӧ���ʺ�mRNA�����仯��ע����Щ��Ƭ�IJ���������ʹ���ã����ɿ��Ʋ�����Ƚ��֢״����ʵ�鷢��������Դ���������Ը�PPE�������������������ӣ���������Ը�PPD������ﶼ�����������������������ע������ͪ������Ϸ�Ӧ1 h����PPE����������ӣ�2 h��PPD����������ӣ����Ը���PPE�������仯�����ԣ�PPD����������Լ��١�������Ը��ǽ鵼���������������Ҫ��λ�������Է��ĺ����Է��IJ�����ע�������С�����Ծ��Ӧ������ע��D-Ala,D-Leu�Է���(DADLE)(60 ��g.kg-1)���ƺ����������ߵĽ��֢״[2]��Dyn A(1-13)����ע�������ע�������ʪ��ҡ��,�����κ���ë,��������ע��û��Ч��,�������ƺ����������ߵĽ��֢״[3]�������Simonia��[4]ͨ���ʰ�Ƭ����ȱʧ��С��֤ʵ�ʰ�Ƭ���������ʹ���ͱ�Ե�˶��ͦʰ�Ƭ���弤����U-50 488H����ʹ�����ЧӦ��ؼ�����,���Ҳ�����Ƚ��֢״�ı���б���Ӧ�÷���RNA����֤ʵ�İ�Ƭ���������ȵĽ���ЧӦ�ͽ�Ϸ�Ӧ[13]����ˣ�������Դ���Է��ĺ�ǿ���ĵĻ��������ڿ�����ȵĽ��֢״������ġ�
, http://www.100md.com
������ʾM1��������pirenzepine�ͼ���ݹ�м�����������Ը�PPE�����PPD�������Ͻ��1 h���в�ͬ�̶ȵ����ӣ��б�������ע��С����ǿ���ĺ��Է�����ʹ������Эͬ����[14]����ˣ�M������Ϻ�����Ը�����Դ��PPE��PPD���ӿ����ǵ����������������ư�Ƭ���֢״�Ļ���֮һ[6]���б�������ע��ǿ�����������IJ�������������ͨ��NMDA���������ã���Դ��ǿ���Ŀ���ͨ��ͻ��ǰ�ٽ��˷�����������ͷţ���NMDA��������������ֹǿ������̱�����ã����Ҽ���ǿ���IJ����ĵ���������֯ѧ�ı�[12]�����ķ���NMDA��������MK801������, ������Ը���PPE����Ͻ���������Բ��죬��������Ը�PPD�������Ͻ�����������ӣ������ʾNMDA������ǿ����֮����ܴ����Ż�����ڵĻ��ơ��ڱ�����ʾ������MK 801����Ƚ��֢״��һ�������ã�����������NMDA���������յ���Դ��ǿ���ĵı�����������Կ��ư�Ƭ�����Ч�����û��ơ�����NOS���Ƽ�L-NAME�������������Ը�PPE�������Ͻ�����в�ͬ�̶ȵ�����,������Ը�PPD�������仯�����ԡ�M����������NMDA����������NO��ø���Ƽ�����Ƚ��֢״������������[8],���Ƕ�PPE��PPD���������ڵĻ����Բ����������PPE��PPD�Ļ������������[15��16]��PPE�������ж���cAMP���Ԫ����PPD��������AP-1�Ľ��Ԫ������M���塢NMDA������ϸ������Ϣ����;����cAMP��PKC��Ca2+ż��������б�Ҫ̽������Ƚ��ʱM����������NMDA����������NOS���Ƽ���PPE��PPD���������ز���Ļ��ơ�
, http://www.100md.com
*�㽭ʡҽѧ��ѧ����������No 98A093
����飺���ݷң�34�꣬�����о�Ա��1987���ҵ�ں��ݴ�ѧ����ϵ����Ҫ���·�������ѧ���о���
�������62�꣬�о�Ա����Ҫ����ҩ�������Ļ��ƺͷ��ε��о�
���ݷ�(�㽭ʡ���в�ѭ����ݹ����ҩ�о���.�����䶾�о����ģ����� 315010)
лС��(�㽭ʡ���в�ѭ����ݹ����ҩ�о���.�����䶾�о����ģ����� 315010)
���Ļ�(�㽭ʡ���в�ѭ����ݹ����ҩ�о���.�����䶾�о����ģ����� 315010)
�����(�㽭ʡ���в�ѭ����ݹ����ҩ�о���.�����䶾�о����ģ����� 315010)
, ��Ĵҽҩ
�����
1��Uhl GR, Ryan JP, Schwartz JP.Morphine alters preproenkephalin gene expression.Brain Res��1988;459:391��7
2��Bhargava HN. Opioid-like action of methionine-enkephalin in inhibiting morphine abstinence syndrome. Eur J Pharmacol, 1977;41:81��4
3��Takemori AE, Loh HH, Lee NM. Supression of dynorphin A (1��13) of the expression of opiate withdrawal and tolerance in mice. Eur J Pharmacol, 1992;221:223��6
, ��Ĵҽҩ
4��Simonin F, Valverde O, Smadja C et al. Disruption of the kappa-opioid receptor gene in mice enhances sensitivity to chemical visceral pain, impairs pharmacological actions of the selective kappa-agonist U-50,488H and attenuates morphine withdrawal. EMBO J, 1998;17:886��97
5��Fukunaga Y, Inoue N, Miyamoto M et al. Effects of peptidase inhibitors,[D-Ala2,Mek5]-enkephaminamide and antiserum to methionine-enkaphalin microinjected into the caudal periaqueductal gray on morphine withdrawal in rats. Jpn J Pharmacol,1998;78:455��61
, http://www.100md.com
6�������,���Ļ�,�Ÿ�ǿ��.ѡ���Զ�ަ��������������������ܺ�������ʵ���о�.�л�ҽѧ��־,1997;77:130��3
7��Thorat SN, Barjavel M, Matwyshyn GA��Bhargava HN. Comparative effects of N-monomethyl-L-arginine and MK801 on the abstinence syndrome in morphine-dependent mice. Brain Res, 1994;642:153��9
8�����Ļ����� ����лС�� et al.���������������Ը�һ�����������ͺ�ø��������.�й�ҩ����������־, 1999;8(2):95��7
9��Rosen H, Douglass J, Herbert E. Isolation and charactrization of the rat proenkephalin gene. J Biol Chem��1984;259:14309��13
, ��Ĵҽҩ
10��Douglass J, Mcmurray CT, Garrett JE et al. Characterization of the rat prodynorphin gene. Mol Endocrinol, 1989;3:2070��8
11��Tokunaga K, Taniguchi H, Yoda K et al. Nucleotide sequence of a full-length cDNA for mouse cytoskeletal beta-actin mRNA. Nucleic Acids Res,1986;14:2829��33
12��Bakshi R, Ni RX, Faden AI. N-methyl-D-aspartate(NMDA) and opioid receptors mediate dynorphin-induced spinal cord injury: behavioral and histological studies. Brain Res�� 1992;580:255��64
, ��Ĵҽҩ
13��Suzuki T, Ikeda H, Tsuji M et al. Antisense oligodeoxynucleotide to �� receptors attenuates morphine dependence in mice.Life Science,1997;61:165��70
14�������죬��������Ԭ ع et al.2��15 Hz����̼���ʹ���弹����ͬʱ�ͷż����ĺ�ǿ����A.����ҽ�ƴ�ѧѧ����1992��24��807��9
15��Comb M, Mermod N, Hyman SE et al.Proteins bound at adjacent DNA elements act synergistically to regulate human proenkaphalin cAMP inducible transcription. EMBO J, 1988;7:3793��805
16��Civelli O, Douglass J, Goldstein A et al. Sequence and expression of the rat prodynorphin gene. Proc Natl Acad Sci USA��1985;82;4291��429, ��Ĵҽҩ(�Է���ԭ��ǰǿ����ԭmRNA�����Ӱ��*)