应用无支架离心管培养技术构建组织工程化关节软骨
作者:杨志明 王跃 解慧琪 钟亚玲 杨振琳 孙爱民 李胜富
单位:杨志明、解慧琪(610041成都,华西医科大学附属第一医院骨科);李胜富(移植免疫室);孙爱民(华西医科大学基础医学院);王跃、钟亚玲、杨振琳(四川省人民医院骨科)
关键词:软骨;关节;组织学;生物医学工程;细胞培养
中华骨科杂志000903 【摘要】目的探索应用离心管培养技术进行体外构建组织工程化关节软骨组织的可行性,并研究其结构和功能。方法分离培养人胚胎关节表层软骨细胞,在无支架材料条件下,用离心管培养技术构建关节软骨,通过组织学、生物化学和逆转录-聚合酶链反应(RT-PCR)技术,对离心管内构建的软骨组织进行形态学和细胞功能状态研究。结果在体外培养第2周时,组织切片可见软骨样组织结构;第3周时软骨发育趋于成熟,经阿新蓝染色基质丰富;第16周时,组织形态无明显变化,未见钙化。DNA含量在体外培养第2周时达最高峰,其硫酸化糖胺多糖(GAG)含量在第4周时达最高峰,维持至第8周。GAG与DNA含量之比于第8周时达最高峰。RT-PCR检测结果显示,体外培养至第16周时,Ⅱ型胶原蛋白mRNA呈阳性表达,其扩增片段为160bp,与正常人的胚胎关节软骨一致。结论在无支架材料条件下,采用离心管培养技术培养的人胚胎关节表面软骨细胞可以构建组织工程化关节软骨,而且接近正常关节软骨的形态和功能。
, 百拇医药
Construction of tissue engineered articular cartilage without scaffold materials by centrifuge tube culture technique
YANG ZhimingXIE Huiqi WANG Yue,et al.
(Department of Orthopaedic Surgery, the First University Hospital, West China University of Medical Sciences,Chengdu 610041, China)
【Abstract】Objective To explore the feasibility of tissue engineered articular cartilage constructed by the technique of centrifuge tube culture and study its structure and function. Methods Chondrocytes were separated from human embryonic articular cartilage and cultured after centrifugation without any scaffold materials. The cellular morphological and functional characteristics were observed after cultured in centrifuge tube by histological, biochemical and RT- PCR technique. Results The articular cartilage constructed by the technique of centrifuge tube culture was hyaline cartilage. The histological observation showed that cartilage- like tissue was formed at the 2nd week after culture, and mature articular cartilage was formed at the 3rd week. No calcification was observed until the 16th week. The DNA contents achieved peak value at the 2nd week, the GAG contents was highest at the 4th week, and the high mRNA expression of type Ⅱ collagen similar to natural human embryonic articular cartilage was occurred until at the 16th week. Conclusion The method of centrifuge tube culture can be used as a constructing technique of tissue engineered cartilage without scaffold material.
, http://www.100md.com
【Key words】Cartilage,articular; Histology; Biomedical engineering; Cell culture
从动物关节内获取软骨细胞是构建组织工程化关节软骨的主要方法,与可降解的生物支架材料联合培养,形成组织工程化关节软骨,其中可降解生物材料为软骨细胞停泊、生长、发育、发挥细胞功能提供支架[1]。Kato等[2]和颜炜群等[3]先后报告了用离心管培养形成生长板软骨的技术,但在无支架材料条件下,用离心管培养技术构建组织工程化关节软骨尚少有报道。为此,我们探索用人胚胎关节软骨细胞,在无支架条件下,体外构建组织工程化关节软骨的组织学表现及功能状态。
材料与方法
一、主要实验仪器、材料、试剂
实验仪器包括721-A分光光度计(上海市仪器厂)、RF-5000荧光分光光度计(岛津公司)、PTC-200循环扩增仪(MJ Research公司)、J2-HS高速冷冻离心机(BECKMAN公司)、2F-A型紫外透射分析仪(上海长明光学电子仪器厂)。实验材料有木瓜蛋白酶(E.Merck公司)和阿新蓝(dimethylmethyleneblue,DMMB)(Aldrich公司)。Ⅱ型胶原、Hoechst33258、CalfThymusDNA和硫酸软骨素A等试剂均购自Sigma公司。
, http://www.100md.com
二、软骨细胞培养
采用无菌技术切取因外伤自然流产的5月龄胎儿的肱骨头、股骨头和股骨髁关节面表层软骨,剪切成1mm×1mm×1mm大小。用质量分数为0.25%的胰蛋白酶37℃消化30min,再以质量分数为0.2%的Ⅱ型胶原酶继续消化4~6h,收集细胞悬液,1200r/min离心6min,弃上清液,Hank液洗涤一次,所收集细胞用血细胞计数板计数。取原代软骨细胞,用质量分数为10%的小牛血清DMEM培养液制备成细胞悬液。按照Kato法,每管含5×106个软骨细胞,将软骨细胞悬液移入15mlFalcon塑料离心管内,再加入DMEM培养液至5ml,其中含质量分数为10%的小牛血清、青霉素100u/ml、链霉素100μg/ml,pH值7.4,1500r/min离心5min,使软骨细胞在离心管内形成小团状,然后放置于37℃、体积分数为5%的CO2、饱和湿度下培养。5d后第一次换液,以后每隔2d换液一次,培养至第16周,对各项指标进行检测。
, 百拇医药 三、观察指标
(一)DNA和GAG含量测定:采用Hoechst33258荧光法测定软骨细胞的DNA含量[4]。以Calf Thymus DNA作为标准品绘制标准曲线,比较测定结果。采用DMMB分光光度法测定离心管所培养软骨组织的硫酸化糖胺多糖(glycosaminoglycan,GAG)含量[5]。以硫酸软骨素A作为标准品,比较测定结果。
(二)Ⅱ型胶原蛋白mRNA检测:以人Ⅱ型前胶原蛋白mRNA的cDNA序列为靶序列,由中国军事医学科学院生物工程研究所合成如下4条引物。
引物1:5-TGGAAGAGTGGAGACTACTGG-3’
引物2:5-GTGTACGTGAACCAGCTAAAGC-3’
引物3:5-GACGCCATGAAGGTTTTCTGC-3
, http://www.100md.com
引物4:5-CATAGCTGAAATGGAAGCCACC-3'
引物1、2的扩增片段为419bp,引物3、4在引物1、2扩增的419bp片段内巢式扩增为160bp片段。取体外培养16周的离心管培养的软骨组织和正常人胚胎关节面表层软骨各0.5g,制成细胞悬液,提取细胞总RNA,取5μl对倍稀释成10、20和40μl。进行两步逆转录-聚合酶链反应(RT-PCR)法检测Ⅱ型胶原mRNA表达,以出现160bp的特异性条带为阳性,并经ACCI限制性内切酶37℃作用12h,进行酶切证实[6]。
(三)组织学检查:取离心管培养的软骨组织块,固定、包埋、切片,然后行HE染色,观察细胞和组织结构;阿新蓝染色,观察基质中硫酸化GAG的形成;钙染色,观察软骨组织有无钙化。
四、统计学处理方法
所有数据用PEMS医用统计程序包进行秩和检验,KW法总体比较,计算P值。
, 百拇医药
结果
一、大体观察
软骨细胞悬液经离心后,在离心管底部形成一小的细胞团,直径约1mm。3d后细胞小团的体积开始逐渐增大,至第3周时,直径达8mm,外观透明、帽状,类似软骨组织(图1);至第16周,体积增大不明显。
图1 离心管培养第3周时的软骨外观
二、组织学观察
体外培养至第2周时,组织切片可观察到软骨组织样结构。至第3周时,软骨结构发育趋于成熟,HE染色见软骨细胞呈圆形,位于软骨陷窝内,表层组织内细胞密度较大,由表层至深层,细胞数量逐渐减少,软骨囊增大,排列欠规整(图2);阿新蓝染色可见基质蓝染,软骨陷窝清楚,陷窝周围有着色较深的软骨囊,囊间基质着色较浅(图3)。第3~16周,经离心管培养的软骨细胞保持软骨组织基本结构。第4、8、12和16周分别行钙染色,均未见软骨组织钙化现象。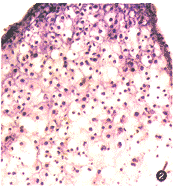
, 百拇医药
图2 离心管培养第3周,细胞呈圆形,位于软骨陷窝内,表层细胞密度较大,深层细胞密度减少,软骨囊增大,排列欠规整HE染色×100
图3 离心管培养第3周,软骨基质呈蓝色,软骨囊、软骨陷窝清晰可见AB染色×400
三、DNA和GAG含量测定
在细胞接种后第1周,经离心管培养的软骨细胞DNA含量增加不明显;第2周迅速增加达最高峰;第2~4周维持在较高水平;第4周以后逐渐下降;第12~16周维持在较低水平。
在细胞接种后第4周,GAG含量达高峰,并维持在较高水平;至第8周后下降;第12~16周期间维持在较低水平。但在第8周以前GAG与DNA含量之比(GAG/DNA)呈持续上升,至第8周时达高峰;第8~12周期间GAG/DNA含量比下降;第12~16周下降速度减缓(表1)。
, 百拇医药
表1 在不同检测时间经离心管培养的软骨细胞的DNA和GAG含量(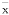 ±s,μg/tube) 观察
±s,μg/tube) 观察
指标
n
检测时间(周)
0
1
2
4
8
12
16
, http://www.100md.com
DNA
3
1.841±0.158
2.274±0.065
4.093±0.436
3.988±0.256
3.280±0.258
2.577±0.257
2.451±0.295
GAG
3
10.667±2.750
, http://www.100md.com
55.000±6.614
318.333±25.658
671.667±30.139
631.667±29.297
413.333±41.633
385.000±91.788
GAG/DNA
3
5.794
24.186
77.775
, 百拇医药 168.422
192.581
160.393
157.079
注:秩和检验P<0.01
四、Ⅱ型胶原蛋白mRNA的表达
体外离心管培养16周的软骨细胞经RT-PCR检测显示,Ⅱ型胶原蛋白mRNA的阳性扩增片段为160bp,经ACCI限制性内切酶酶切证实,此阳性扩增片段为特异性扩增片段。将经体外离心管培养16周的软骨进行对倍稀释后所产生的扩增片段与正常人胚胎关节软骨进行比较,其表达浓度基本一致(图4)。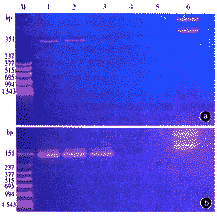
MPCRMarker1~4Ⅱ型胶原mRNA对倍稀释
, 百拇医药
电泳带,阳性条带为160bp5蒸馏水
对照6阳性条带经ACCI酶切为
46bp和114bp两条带
图4 Ⅱ型胶原mRNART-PCR结果
a离心管培养的软骨细胞Ⅱ型胶原mRNA的RT-PCR结果
b正常人胚胎关节面表层软骨细胞Ⅱ型胶原mRNA的RT-PCR结果
讨论
Kato等[2]分离培养的新西兰兔的生长板软骨细胞在体外构建出的软骨组织具有生长板软骨的特点,在体外培养至24d时,软骨基质内出现钙化。颜炜群等[3]采用生长板软骨细胞进行培养也获得相同结果。生长板软骨与关节软骨虽同属透明软骨,但它们之间在结构和功能上有所差别。生长板最终将骨化成骨,而关节软骨不发生骨化。钙化是软骨骨化的过渡环节。在本实验中,我们观察到体外培养的软骨细胞至第16周时仍无钙化,表明用无支架离心管培养法构建的关节软骨组织具有与细胞来源相似的特性。因此可以认为,以修复关节软骨为目标的组织工程化软骨的构建应采用关节面表层的软骨细胞。
, 百拇医药
Buckwalter等[7]认为,天然软骨在发育初期的细胞密度最高,随着软骨发育的成熟,其细胞密度也逐渐下降。Vacanti等[8]在软骨组织工程学研究中也观察到,在软骨发育早期的细胞密度较大,以后细胞密度下降,维持在接近正常软骨细胞密度的水平。笔者发现,在体外培养至第3周时,组织学观察显示,软骨细胞密度较第16周时增加;同时,DNA和GAG含量亦维持在较高水平。表明用离心管培养技术构建的软骨,其细胞密度的变化与生化检测结果相一致。
本实验结果显示,GAG与DNA含量变化不同步,GAG含量的高峰出现在第4周,较DNA峰值滞后。而GAG与DNA含量比则在第8周达高峰。基质中GAG/DNA的动态变化,反映了软骨合成代谢的活性,其峰值代表软骨细胞合成代谢的高峰。从理论上讲,在细胞合成代谢较旺盛的阶段,应是软骨基质的成熟时期,此时软骨功能的活性也较强。由此可见,用无支架离心管培养构建的关节软骨有两个高峰,即软骨增殖高峰和软骨基质形成高峰。因此,在修复关节软骨缺损的选材时机上应考虑到这一点,移植时机以培养第2~8周为宜。关于修复取材的具体时间是以细胞增殖高峰还是以基质合成高峰为最佳,尚有待于进一步的体内实验予以证实。
, 百拇医药
软骨细胞在体内具有高分化特性,可分泌软骨组织特有的Ⅱ型胶原。但在体外培养时,软骨细胞表型不稳定,容易丧失其高分化状态,被称为软骨细胞的去分化(dedifferentiation)现象。我们采用RT-PCR方法检测Ⅱ型胶原蛋白mRNA,发现经离心管法培养的软骨细胞在体外培养至第16周时仍可高度表达Ⅱ型胶原蛋白mRNA,表明该培养方法能使体外长期培养的软骨细胞保持表型稳定。据此可推测,离心管软骨培养法构建组织工程化关节软骨是可行的。
国家科技部国家重点基础研究发展规划项目(973)资助课题(G1999054308)
国家自然科学基金重点资助项目(39830100)
参考文献
1,杨志明 主编.组织工程基础与临床.第1版.成都:四川科学技术出版社,2000.2-3.
, http://www.100md.com
2,Kato Y Iwamoto M, Koike T, et al. Terminal differentiation and calcification in rabbit chondrocyte cultures grown in centrifuge tubes: regulation by transforming growth factor-β and serum factors. Proc Natl Acad Sci USA, 1988, 85:9552-9556.
3,颜炜群,佟明华,宇莉,等.培养软骨细胞再形成生长板软骨组织的研究.实验生物学报,1994,27:193-196.
4,Kim YJ, Sah RL, Doong JY, et al. Fluorometric assay of DNA in cartilage explants using Hoechst 33258. Anal Biochem,1988, 174:168-176.
, http://www.100md.com
5,Farndale RW, Buttle DJ, Barrett AJ. Improved quantitation and discrimination of sulphated glycosaminoglycans by use of dimethylmethylene blue. Biochem Biophys Acta, 1986, 883:173-177.
6,姜泊,张亚历,周殿元,主编.分子生物学常用实验方法.北京:人民军医出版社,1992.112-124.
7,Buckwalter JA, Mankin HJ. Articular cartilage. Part I: tissue design and chondrocyte-matrix interaction. J Bone Joint Surg(Am), 1997,79:600-610.
8,Vacanti CA, Vacanti JP. Bone and cartilage reconstruction. In:Lanza R, Langer R, Click W, eds. Principle of tissue engineering. New York:RG Landes Company,1997.619-628.
(收稿日期:2000-06-12), http://www.100md.com
单位:杨志明、解慧琪(610041成都,华西医科大学附属第一医院骨科);李胜富(移植免疫室);孙爱民(华西医科大学基础医学院);王跃、钟亚玲、杨振琳(四川省人民医院骨科)
关键词:软骨;关节;组织学;生物医学工程;细胞培养
中华骨科杂志000903 【摘要】目的探索应用离心管培养技术进行体外构建组织工程化关节软骨组织的可行性,并研究其结构和功能。方法分离培养人胚胎关节表层软骨细胞,在无支架材料条件下,用离心管培养技术构建关节软骨,通过组织学、生物化学和逆转录-聚合酶链反应(RT-PCR)技术,对离心管内构建的软骨组织进行形态学和细胞功能状态研究。结果在体外培养第2周时,组织切片可见软骨样组织结构;第3周时软骨发育趋于成熟,经阿新蓝染色基质丰富;第16周时,组织形态无明显变化,未见钙化。DNA含量在体外培养第2周时达最高峰,其硫酸化糖胺多糖(GAG)含量在第4周时达最高峰,维持至第8周。GAG与DNA含量之比于第8周时达最高峰。RT-PCR检测结果显示,体外培养至第16周时,Ⅱ型胶原蛋白mRNA呈阳性表达,其扩增片段为160bp,与正常人的胚胎关节软骨一致。结论在无支架材料条件下,采用离心管培养技术培养的人胚胎关节表面软骨细胞可以构建组织工程化关节软骨,而且接近正常关节软骨的形态和功能。
, 百拇医药
Construction of tissue engineered articular cartilage without scaffold materials by centrifuge tube culture technique
YANG ZhimingXIE Huiqi WANG Yue,et al.
(Department of Orthopaedic Surgery, the First University Hospital, West China University of Medical Sciences,Chengdu 610041, China)
【Abstract】Objective To explore the feasibility of tissue engineered articular cartilage constructed by the technique of centrifuge tube culture and study its structure and function. Methods Chondrocytes were separated from human embryonic articular cartilage and cultured after centrifugation without any scaffold materials. The cellular morphological and functional characteristics were observed after cultured in centrifuge tube by histological, biochemical and RT- PCR technique. Results The articular cartilage constructed by the technique of centrifuge tube culture was hyaline cartilage. The histological observation showed that cartilage- like tissue was formed at the 2nd week after culture, and mature articular cartilage was formed at the 3rd week. No calcification was observed until the 16th week. The DNA contents achieved peak value at the 2nd week, the GAG contents was highest at the 4th week, and the high mRNA expression of type Ⅱ collagen similar to natural human embryonic articular cartilage was occurred until at the 16th week. Conclusion The method of centrifuge tube culture can be used as a constructing technique of tissue engineered cartilage without scaffold material.
, http://www.100md.com
【Key words】Cartilage,articular; Histology; Biomedical engineering; Cell culture
从动物关节内获取软骨细胞是构建组织工程化关节软骨的主要方法,与可降解的生物支架材料联合培养,形成组织工程化关节软骨,其中可降解生物材料为软骨细胞停泊、生长、发育、发挥细胞功能提供支架[1]。Kato等[2]和颜炜群等[3]先后报告了用离心管培养形成生长板软骨的技术,但在无支架材料条件下,用离心管培养技术构建组织工程化关节软骨尚少有报道。为此,我们探索用人胚胎关节软骨细胞,在无支架条件下,体外构建组织工程化关节软骨的组织学表现及功能状态。
材料与方法
一、主要实验仪器、材料、试剂
实验仪器包括721-A分光光度计(上海市仪器厂)、RF-5000荧光分光光度计(岛津公司)、PTC-200循环扩增仪(MJ Research公司)、J2-HS高速冷冻离心机(BECKMAN公司)、2F-A型紫外透射分析仪(上海长明光学电子仪器厂)。实验材料有木瓜蛋白酶(E.Merck公司)和阿新蓝(dimethylmethyleneblue,DMMB)(Aldrich公司)。Ⅱ型胶原、Hoechst33258、CalfThymusDNA和硫酸软骨素A等试剂均购自Sigma公司。
, http://www.100md.com
二、软骨细胞培养
采用无菌技术切取因外伤自然流产的5月龄胎儿的肱骨头、股骨头和股骨髁关节面表层软骨,剪切成1mm×1mm×1mm大小。用质量分数为0.25%的胰蛋白酶37℃消化30min,再以质量分数为0.2%的Ⅱ型胶原酶继续消化4~6h,收集细胞悬液,1200r/min离心6min,弃上清液,Hank液洗涤一次,所收集细胞用血细胞计数板计数。取原代软骨细胞,用质量分数为10%的小牛血清DMEM培养液制备成细胞悬液。按照Kato法,每管含5×106个软骨细胞,将软骨细胞悬液移入15mlFalcon塑料离心管内,再加入DMEM培养液至5ml,其中含质量分数为10%的小牛血清、青霉素100u/ml、链霉素100μg/ml,pH值7.4,1500r/min离心5min,使软骨细胞在离心管内形成小团状,然后放置于37℃、体积分数为5%的CO2、饱和湿度下培养。5d后第一次换液,以后每隔2d换液一次,培养至第16周,对各项指标进行检测。
, 百拇医药 三、观察指标
(一)DNA和GAG含量测定:采用Hoechst33258荧光法测定软骨细胞的DNA含量[4]。以Calf Thymus DNA作为标准品绘制标准曲线,比较测定结果。采用DMMB分光光度法测定离心管所培养软骨组织的硫酸化糖胺多糖(glycosaminoglycan,GAG)含量[5]。以硫酸软骨素A作为标准品,比较测定结果。
(二)Ⅱ型胶原蛋白mRNA检测:以人Ⅱ型前胶原蛋白mRNA的cDNA序列为靶序列,由中国军事医学科学院生物工程研究所合成如下4条引物。
引物1:5-TGGAAGAGTGGAGACTACTGG-3’
引物2:5-GTGTACGTGAACCAGCTAAAGC-3’
引物3:5-GACGCCATGAAGGTTTTCTGC-3
, http://www.100md.com
引物4:5-CATAGCTGAAATGGAAGCCACC-3'
引物1、2的扩增片段为419bp,引物3、4在引物1、2扩增的419bp片段内巢式扩增为160bp片段。取体外培养16周的离心管培养的软骨组织和正常人胚胎关节面表层软骨各0.5g,制成细胞悬液,提取细胞总RNA,取5μl对倍稀释成10、20和40μl。进行两步逆转录-聚合酶链反应(RT-PCR)法检测Ⅱ型胶原mRNA表达,以出现160bp的特异性条带为阳性,并经ACCI限制性内切酶37℃作用12h,进行酶切证实[6]。
(三)组织学检查:取离心管培养的软骨组织块,固定、包埋、切片,然后行HE染色,观察细胞和组织结构;阿新蓝染色,观察基质中硫酸化GAG的形成;钙染色,观察软骨组织有无钙化。
四、统计学处理方法
所有数据用PEMS医用统计程序包进行秩和检验,KW法总体比较,计算P值。
, 百拇医药
结果
一、大体观察
软骨细胞悬液经离心后,在离心管底部形成一小的细胞团,直径约1mm。3d后细胞小团的体积开始逐渐增大,至第3周时,直径达8mm,外观透明、帽状,类似软骨组织(图1);至第16周,体积增大不明显。

图1 离心管培养第3周时的软骨外观
二、组织学观察
体外培养至第2周时,组织切片可观察到软骨组织样结构。至第3周时,软骨结构发育趋于成熟,HE染色见软骨细胞呈圆形,位于软骨陷窝内,表层组织内细胞密度较大,由表层至深层,细胞数量逐渐减少,软骨囊增大,排列欠规整(图2);阿新蓝染色可见基质蓝染,软骨陷窝清楚,陷窝周围有着色较深的软骨囊,囊间基质着色较浅(图3)。第3~16周,经离心管培养的软骨细胞保持软骨组织基本结构。第4、8、12和16周分别行钙染色,均未见软骨组织钙化现象。

, 百拇医药
图2 离心管培养第3周,细胞呈圆形,位于软骨陷窝内,表层细胞密度较大,深层细胞密度减少,软骨囊增大,排列欠规整HE染色×100

图3 离心管培养第3周,软骨基质呈蓝色,软骨囊、软骨陷窝清晰可见AB染色×400
三、DNA和GAG含量测定
在细胞接种后第1周,经离心管培养的软骨细胞DNA含量增加不明显;第2周迅速增加达最高峰;第2~4周维持在较高水平;第4周以后逐渐下降;第12~16周维持在较低水平。
在细胞接种后第4周,GAG含量达高峰,并维持在较高水平;至第8周后下降;第12~16周期间维持在较低水平。但在第8周以前GAG与DNA含量之比(GAG/DNA)呈持续上升,至第8周时达高峰;第8~12周期间GAG/DNA含量比下降;第12~16周下降速度减缓(表1)。
, 百拇医药
表1 在不同检测时间经离心管培养的软骨细胞的DNA和GAG含量(
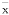 ±s,μg/tube) 观察
±s,μg/tube) 观察指标
n
检测时间(周)
0
1
2
4
8
12
16
, http://www.100md.com
DNA
3
1.841±0.158
2.274±0.065
4.093±0.436
3.988±0.256
3.280±0.258
2.577±0.257
2.451±0.295
GAG
3
10.667±2.750
, http://www.100md.com
55.000±6.614
318.333±25.658
671.667±30.139
631.667±29.297
413.333±41.633
385.000±91.788
GAG/DNA
3
5.794
24.186
77.775
, 百拇医药 168.422
192.581
160.393
157.079
注:秩和检验P<0.01
四、Ⅱ型胶原蛋白mRNA的表达
体外离心管培养16周的软骨细胞经RT-PCR检测显示,Ⅱ型胶原蛋白mRNA的阳性扩增片段为160bp,经ACCI限制性内切酶酶切证实,此阳性扩增片段为特异性扩增片段。将经体外离心管培养16周的软骨进行对倍稀释后所产生的扩增片段与正常人胚胎关节软骨进行比较,其表达浓度基本一致(图4)。

MPCRMarker1~4Ⅱ型胶原mRNA对倍稀释
, 百拇医药
电泳带,阳性条带为160bp5蒸馏水
对照6阳性条带经ACCI酶切为
46bp和114bp两条带
图4 Ⅱ型胶原mRNART-PCR结果
a离心管培养的软骨细胞Ⅱ型胶原mRNA的RT-PCR结果
b正常人胚胎关节面表层软骨细胞Ⅱ型胶原mRNA的RT-PCR结果
讨论
Kato等[2]分离培养的新西兰兔的生长板软骨细胞在体外构建出的软骨组织具有生长板软骨的特点,在体外培养至24d时,软骨基质内出现钙化。颜炜群等[3]采用生长板软骨细胞进行培养也获得相同结果。生长板软骨与关节软骨虽同属透明软骨,但它们之间在结构和功能上有所差别。生长板最终将骨化成骨,而关节软骨不发生骨化。钙化是软骨骨化的过渡环节。在本实验中,我们观察到体外培养的软骨细胞至第16周时仍无钙化,表明用无支架离心管培养法构建的关节软骨组织具有与细胞来源相似的特性。因此可以认为,以修复关节软骨为目标的组织工程化软骨的构建应采用关节面表层的软骨细胞。
, 百拇医药
Buckwalter等[7]认为,天然软骨在发育初期的细胞密度最高,随着软骨发育的成熟,其细胞密度也逐渐下降。Vacanti等[8]在软骨组织工程学研究中也观察到,在软骨发育早期的细胞密度较大,以后细胞密度下降,维持在接近正常软骨细胞密度的水平。笔者发现,在体外培养至第3周时,组织学观察显示,软骨细胞密度较第16周时增加;同时,DNA和GAG含量亦维持在较高水平。表明用离心管培养技术构建的软骨,其细胞密度的变化与生化检测结果相一致。
本实验结果显示,GAG与DNA含量变化不同步,GAG含量的高峰出现在第4周,较DNA峰值滞后。而GAG与DNA含量比则在第8周达高峰。基质中GAG/DNA的动态变化,反映了软骨合成代谢的活性,其峰值代表软骨细胞合成代谢的高峰。从理论上讲,在细胞合成代谢较旺盛的阶段,应是软骨基质的成熟时期,此时软骨功能的活性也较强。由此可见,用无支架离心管培养构建的关节软骨有两个高峰,即软骨增殖高峰和软骨基质形成高峰。因此,在修复关节软骨缺损的选材时机上应考虑到这一点,移植时机以培养第2~8周为宜。关于修复取材的具体时间是以细胞增殖高峰还是以基质合成高峰为最佳,尚有待于进一步的体内实验予以证实。
, 百拇医药
软骨细胞在体内具有高分化特性,可分泌软骨组织特有的Ⅱ型胶原。但在体外培养时,软骨细胞表型不稳定,容易丧失其高分化状态,被称为软骨细胞的去分化(dedifferentiation)现象。我们采用RT-PCR方法检测Ⅱ型胶原蛋白mRNA,发现经离心管法培养的软骨细胞在体外培养至第16周时仍可高度表达Ⅱ型胶原蛋白mRNA,表明该培养方法能使体外长期培养的软骨细胞保持表型稳定。据此可推测,离心管软骨培养法构建组织工程化关节软骨是可行的。
国家科技部国家重点基础研究发展规划项目(973)资助课题(G1999054308)
国家自然科学基金重点资助项目(39830100)
参考文献
1,杨志明 主编.组织工程基础与临床.第1版.成都:四川科学技术出版社,2000.2-3.
, http://www.100md.com
2,Kato Y Iwamoto M, Koike T, et al. Terminal differentiation and calcification in rabbit chondrocyte cultures grown in centrifuge tubes: regulation by transforming growth factor-β and serum factors. Proc Natl Acad Sci USA, 1988, 85:9552-9556.
3,颜炜群,佟明华,宇莉,等.培养软骨细胞再形成生长板软骨组织的研究.实验生物学报,1994,27:193-196.
4,Kim YJ, Sah RL, Doong JY, et al. Fluorometric assay of DNA in cartilage explants using Hoechst 33258. Anal Biochem,1988, 174:168-176.
, http://www.100md.com
5,Farndale RW, Buttle DJ, Barrett AJ. Improved quantitation and discrimination of sulphated glycosaminoglycans by use of dimethylmethylene blue. Biochem Biophys Acta, 1986, 883:173-177.
6,姜泊,张亚历,周殿元,主编.分子生物学常用实验方法.北京:人民军医出版社,1992.112-124.
7,Buckwalter JA, Mankin HJ. Articular cartilage. Part I: tissue design and chondrocyte-matrix interaction. J Bone Joint Surg(Am), 1997,79:600-610.
8,Vacanti CA, Vacanti JP. Bone and cartilage reconstruction. In:Lanza R, Langer R, Click W, eds. Principle of tissue engineering. New York:RG Landes Company,1997.619-628.
(收稿日期:2000-06-12), http://www.100md.com