KATP 在腺苷降低去窦弓神经大鼠血压波动性中的作用
作者:沈甫明 苏定冯
单位:沈甫明(第二军医大学基础医学部药理学教研室, 上海 200433);苏定冯(第二军医大学基础医学部药理学教研室, 上海 200433)
关键词:去窦弓神经;血压波动性;ATP敏感钾通道;腺苷
第二军医大学学报001011 [摘要] 目的:利用计算机化清醒自由活 动大鼠血流动力学监测技术,分析ATP敏感钾通道(KATP)在腺苷降低去窦弓神经(SAD) 大鼠血压波动性(BPV)中的作用。方法:观察腺苷、腺苷A1受体选择 性激动剂N6-环戊基腺苷(CPA)、A2受体选择性激动剂5′-N-环丙基-酰氨羰基腺苷( CPCA)、 KATP选择性拮抗剂格列本脲、以及格列本脲阻断KATP后CPCA对SAD大 鼠BPV的影响。结果:腺苷和CPCA能显著降低SAD大鼠的BPV,CPA对此 并无影响;格列本脲可降低SAD大鼠的BPV,并可阻断CPCA降SAD大鼠BPV的作用。结 论:KATP状态对于SAD大鼠高BPV的形成具有重要意义。
, http://www.100md.com
[中图分类号]R 96 [文献标识码] A
[文章编号] 0258-879X(2000)10-0938-03
Role of KATP on the reduction of blood pressure variability caused by aden osine in sinoaortic denervated rats
SHEN Fu-Ming, SU Ding-Feng
(Department of Pharmacology, Department of Basic Me dicine, Second Military Medical University, Shanghai 200433, China)
[ABSTRACT] Objective: To determine the effect of KATP o n the reduction of blood pressure variability (BPV) caused by adenosine in consc ious, freely moving sinoaortic denervated (SAD) rats. Methods: Using computerized analytic system of blood pressure (BP), five groups treated with a denosine, adenosine A1-receptor agonist N6-cyclopentyladenosine (CPA), A 2-receptor agonist 5′-N-cyclopropyl-carboxamido-adenosine (CPCA), ATP-sen sitive K+ channel (KATP) blocker glibenclamide, and CPCA with the KA TP-blocked by glibenclamide in advance were used. BP, heart period (HP) and B PV were analyzed. Results: Both adenosine and CPCA significantly decreased BPV in SAD rats, but CPA had no influence on it. Glibenclamide marked ly reduced BPV in SAD rats as well, furthermore, it might antagonize the effect of CPCA on BPV by blocking KATP. Conclusion: KATP pl ays an important role in the development of high BPV in SAD rats.
, 百拇医药
[KEY WORDS] sinoaortic denervated; blood pressure variability; ATP-s ensitive potassium channel; adenosine
去窦弓神经(SAD)大鼠是指去除双侧颈动脉窦和主动脉弓神经传入的大鼠,具有24 h平 均动脉压正常而血压波动性(BPV)明显升高的特点。本室以往工作证明SAD大鼠的这一单纯 性BPV升高可致器官损伤[1]。腺苷是ATP代谢的产物,存在于机体的每一个细胞内 。激动腺苷受体可导致BP和BPV降低,在用新福林抵消腺苷的降压效应后,BPV仍保持在单独 给予腺苷的水平[2]。腺苷受体存在3种亚型(A1,A2,A3),其中A2又可 进一步分为A2a 和A2b亚型。激动A1受体主要在心脏引起负性变时、变力和 变传导效应,而激动A2受体则主要引起外周血管扩张[3]。研究表明腺苷A2受 体降低外周血管阻力的作用与KATP状态[4]、NO途径以及环一磷酸腺苷(cAM P)浓度有关。本研究目的在于明确腺苷A1和A2受体在降低SAD大鼠BPV中的作用,并分 析KATP状态对其的影响。
, 百拇医药
1 材料和方法
1.1 试剂 腺苷、CPA和CPCA均为Sigma公司产品,临用时以生理盐水配制成所需 的浓度。格列本脲为Sigma公司产品,临用时先以1 ml 0.1 mol/L的NaOH溶解,接着在超声 条件下加5%葡萄糖至5 mg/ml。
1.2 实验动物 雄性SD大鼠,体质量270~330 g, 由上海SIPPR-BK公司提供。依 Krieger[5]所确立的方法制作SAD大鼠模型。术后1个月行腹主动脉(BP监测)和股 静脉(给药)插管。实验前16 h将动物连接至计算机化清醒自由活动大鼠血流动力学监测装 置,以2~3 μg/kg新福林iv,使大鼠血压升高6.78 kPa, 若心率减慢少于20次/min则认为 SAD成功。
1.3 方法 模型成功的大鼠于次日上午8:00开始采集数据。实验组共分5组。
, 百拇医药
1.3.1 腺苷、CPA和CPCA组 该3组实验于8:00~9:00静脉恒速 给予2 ml/(kg*h)的生理盐水,于9:00~10:00静脉分别给予腺苷、CPA或CPCA,剂量分别 为 347.8,0.7,0.8 μg/(kg*min)[容量均为2 ml/(kg*h)]。分别采集这两个阶段的 数据。
1.3.2 格列本脲组 第一阶段同1.3.1,于9:00~9:05给予格列本脲20 mg/kg, iv ,第二阶段的数据从给予格列本脲后15 min开始采集,即采集9:20~10:20 时间段的数 据。
1.3.3 格列本脲+CPCA组 同1.3.2,但从9:20开始静脉恒速给予0.8 μg/(kg*m in)的CPCA。
1.4 实验数据采集 每一个60 min的实验阶段被等分为两个30 min的时间段,本 实验所有数据均来自后30 min时间段。收缩压(SBP)、舒张压(DBP)和心动周期(HP)为 每搏采样基础上该30 min内的平均值,收缩压波动性(SBPV)和舒张压波动性(DBPV)为每 搏采样基础上该30 min内SBP和DBP的标准差。
, 百拇医药
1.5 统计学处理 数据以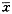 ±s表示,组内以配对t检验判断显著 性,组间以t检验判断显著性。
±s表示,组内以配对t检验判断显著 性,组间以t检验判断显著性。
2 结 果
2.1 腺苷、CPA和CPCA对SAD大鼠BP,HP和BPV的影响 腺苷、CPA和CPCA均可显著 降低SAD大鼠的BP(P<0.01),并延长其HP(P<0.01),以CPA延长HP的作用最 为明显(表1)。腺苷及CPCA均可显著降低SAD大鼠SBPV和DBPV (P<0.01)。CPA 0.7 μg /(kg*min) 可降低SBP和DBP达CPCA同等程度,但CPA对SBPV和DBPV并无显著影响(P>0 .05, 图1)。
2.2 格列本脲和格列本脲+CPCA对SAD大鼠BP,HP和BPV的影 响 格列本脲能明显升高SAD大鼠的SBP和DBP(P<0.01),但其对HP并无显著影 响(P>0.05)。格列本脲阻断KATP后再给予CPCA,此时SBP与生理盐水比较仍显著 升高(P<0.05),但与单独给予格列本脲组比较明显下降(P<0.05); 对DBP而言,无论与生理盐水或是与单独给予格列本脲组比较均呈显著下降(P<0.01) ;HP则无明显变化(P>0.05, 表2)。 虽然格列本脲显著升高SAD大鼠的SBP和DBP,但它 使SBPV 和DBPV明显下降(P<0.01)。格列本脲阻断KATP后再给予CPCA,此时SBPV 和 DBPV仍明显下降(P<0.01),其下降幅度与单独给予格列本脲时相似(图2)。
, 百拇医药
表 1 腺苷、CPA和CPCA对SAD大鼠BP和HP的影响
Tab 1 Effect of adenosine, CPA and
CPCA on BP and HP in SAD rats(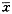 ±s) Group
±s) Group
n
SBP(p/kPa)
DBP
(p/kPa)
HP
(t/ms)
, 百拇医药 Control
7
18.93±
0.85
12.80 ±
1.20
148±
12.3
Adenosi ne
7
14.93±
1.43**
9.07±
, 百拇医药
2. 12**
158±
14.2**
Control
8
19.73±
1.01
13.07±
0.95
146±
15.5
CPA
, http://www.100md.com
8
14.93±
1.31**
8.80±
0.59**
331±
32.5**
Control
9
19.20±
1.05
12.67±
, 百拇医药
0.64
148±
10.4
CPCA
9
16.00±
1.32**
8.13±
1.03**
172±
19.5**
**P<0.01 vs control group
, 百拇医药
图 1 腺苷、CP A和CPCA对SAD大鼠BPV的影响
Fig 1 Effect of adenosine, CPA and
CPCA on BPV in SAD rats
NS: Control; Ado: Adenosine; ** P <0.01 vs NS
表 2 格列本脲和格列本脲+CPCA
对SAD大鼠BP和HP的影响
Tab 2 Effect of glibenclamide and glibenclamide
+CPCA on BP and HP in SAD rats (n=7,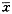 ±s) Group
±s) Group
, http://www.100md.com
SBP(p/kPa)
DBP
(p/kPa)
HP
(t/ms)
Control
19.07±0.69
12.13±0.73
153±17.9
Gli
21.73±1.28**
15.47±1.23**
, http://www.100md.com
163±15.9
Control
18.80±0.93
11.73±0.68
154±12.7
Gli+CPCA
19.73±1.41*△
10.67±0.64**△△
161±17.0
Gli: Glibenclamide; * P<0.05, ** P<0.01 vs control group;
, 百拇医药
△ P<0.05, △△ P< 0.01 vs Gli group
图 2 格列本脲和格列本脲
+CPCA对SAD大鼠BPV的影响
Fig 2 Effect of glibenclamide and glibenclamide
+ CPCA on BPV in SAD rats
NS: Control; Gli: Glibenclamide; ** P<0.01 vs NS
3 讨 论
, 百拇医药
BPV是指BP在一定时间内的波动程度,是随动态血流动力学监测技术而出现的研 究心血管活动的指标。研究表明BPV升高可致器官损伤[1]。SAD大鼠具有BPV明显升 高而24 h平均动脉压不变的特点,是研究BPV的有效模型。SAD后BPV的升高涉及神经和体液 两大调节机制中的众多因素,因而其形成机制复杂。但可以肯定的一点是,致BPV升高的最 直接因素是外周总阻力(total peripheral resistance, TPR)的经常性改变。要降低BPV, 必须减轻或消除TPR的波动。
我们的实验发现,腺苷确实能降低SAD大鼠的BPV,这与Jacob等[2]的报道结果一致 。腺苷A1受体存在于心肌细胞,激动时产生负性变时、变力和变传导作用,导致心率减慢 和血压下降。从其受体的分布情况和功能分析,并不具备减轻或消除TPR的能力。本实验中C PA虽降低BP至与腺苷相似程度,但并无降BPV的作用证实了这一点。腺苷A2受体几乎分布 于所有的阻力血管,激动时可致血管舒张,其舒张血管的机制与促进KATP开放、以及 NO和cAMP形成增加有关。“腺苷假说”[3]认为当局部组织由于某种原因致血流不 足或阻力升高发生缺O2时,腺苷的形成就增加,并作用于该部位的腺苷受体使血管扩张和 血流代偿性增加,即腺苷具有保持局部组织O2供需平衡和稳定血管阻力的作用 。Trapani等[6]认为SAD后大鼠局部血管床的阻力处于不稳定状态, 这些局部血管床阻力的不稳定导致了TPR的波动,SAD大鼠BPV的升高可能源于此。本研究中 当用CPCA激动A2受体,使BP下降至与腺苷同等程度时,BPV也明显降低。因此,我们认为 无 论是腺苷还是CPCA,它们降低BPV作用与其降低外周血管阻力并维持局部血管床阻力稳定有 关。Mubagwa等[3] 和Satio等[4] 研究表明,KATP开放在腺苷及腺 苷A2受体激动剂降低BP的过程中具有重要作用,如果说CPCA降BPV的过程中KATP的 开放也具有重要作用,那么KATP特异性阻断剂格列本脲降BPV的作用则与之矛盾。我 们的研究中还发现当用格列本脲阻断KATP后,进一步的CPCA滴注并不能加大BPV下降 的幅度,因而推测此时BPV的下降仍来自于KATP的关闭。由于腺苷A2受体介导 的降 低BP或BPV作用存在多种可能的机制,因此无法确定KATP开放在其中的作用,进一步 的研究尚在进行中。
, 百拇医药
研究结果表明,腺苷经A2受体介导其降低SAD大鼠BPV的作用,格列本脲阻断KATP可 取消腺苷A2受体激动剂CPCA降低SAD大鼠BPV的作用。
[基金项目]国家自然科学基金资助项目(39670831).
[作者简介]沈甫明(1967-),男(汉族),硕士,助教.
[参 考 文 献]
[1] 龚 侃, 刘建国, 程 勇, 等. 血压波动性增高引起的器官损伤[J ].第二军医大学学报,1997,18(5):462-464.
[2] Jacob HJ, Alper RH, Brody MJ. Lability of arterial pressure after ba roreceptor denervation is not pressure dependent [J]. Hypertension,1989,14(5) :501-510.
, 百拇医药
[3] Mubagwa K, Mullane K, Flameng W. Role of adenosine in the heart and circulation [J]. Cardiovasc Res,1996,32(5):797-813.
[4] Saito K, Sakai K. Potentiating effects of nicorandil on the adenosin e A2 receptor-mediated vasodepression in rats: potential role for KATP channels [J]. Fundam Clin Pharmacol,1998,12(2):143-151.
[5] Krieger EM. Neurogenic hypertension in the rats [J]. Circ Res,1964 ,15(3):511-521.
[6] Trapani AJ, Barron KW, Brody MJ. Analysis of hemodynamic variability after sinoaortic denervation in the conscious rat [J]. Am J Physiol,1986,251 (20):R1163-1169.
[收稿日期] 2000-05-12
[修回日期] 2000-07-17, 百拇医药
单位:沈甫明(第二军医大学基础医学部药理学教研室, 上海 200433);苏定冯(第二军医大学基础医学部药理学教研室, 上海 200433)
关键词:去窦弓神经;血压波动性;ATP敏感钾通道;腺苷
第二军医大学学报001011 [摘要] 目的:利用计算机化清醒自由活 动大鼠血流动力学监测技术,分析ATP敏感钾通道(KATP)在腺苷降低去窦弓神经(SAD) 大鼠血压波动性(BPV)中的作用。方法:观察腺苷、腺苷A1受体选择 性激动剂N6-环戊基腺苷(CPA)、A2受体选择性激动剂5′-N-环丙基-酰氨羰基腺苷( CPCA)、 KATP选择性拮抗剂格列本脲、以及格列本脲阻断KATP后CPCA对SAD大 鼠BPV的影响。结果:腺苷和CPCA能显著降低SAD大鼠的BPV,CPA对此 并无影响;格列本脲可降低SAD大鼠的BPV,并可阻断CPCA降SAD大鼠BPV的作用。结 论:KATP状态对于SAD大鼠高BPV的形成具有重要意义。
, http://www.100md.com
[中图分类号]R 96 [文献标识码] A
[文章编号] 0258-879X(2000)10-0938-03
Role of KATP on the reduction of blood pressure variability caused by aden osine in sinoaortic denervated rats
SHEN Fu-Ming, SU Ding-Feng
(Department of Pharmacology, Department of Basic Me dicine, Second Military Medical University, Shanghai 200433, China)
[ABSTRACT] Objective: To determine the effect of KATP o n the reduction of blood pressure variability (BPV) caused by adenosine in consc ious, freely moving sinoaortic denervated (SAD) rats. Methods: Using computerized analytic system of blood pressure (BP), five groups treated with a denosine, adenosine A1-receptor agonist N6-cyclopentyladenosine (CPA), A 2-receptor agonist 5′-N-cyclopropyl-carboxamido-adenosine (CPCA), ATP-sen sitive K+ channel (KATP) blocker glibenclamide, and CPCA with the KA TP-blocked by glibenclamide in advance were used. BP, heart period (HP) and B PV were analyzed. Results: Both adenosine and CPCA significantly decreased BPV in SAD rats, but CPA had no influence on it. Glibenclamide marked ly reduced BPV in SAD rats as well, furthermore, it might antagonize the effect of CPCA on BPV by blocking KATP. Conclusion: KATP pl ays an important role in the development of high BPV in SAD rats.
, 百拇医药
[KEY WORDS] sinoaortic denervated; blood pressure variability; ATP-s ensitive potassium channel; adenosine
去窦弓神经(SAD)大鼠是指去除双侧颈动脉窦和主动脉弓神经传入的大鼠,具有24 h平 均动脉压正常而血压波动性(BPV)明显升高的特点。本室以往工作证明SAD大鼠的这一单纯 性BPV升高可致器官损伤[1]。腺苷是ATP代谢的产物,存在于机体的每一个细胞内 。激动腺苷受体可导致BP和BPV降低,在用新福林抵消腺苷的降压效应后,BPV仍保持在单独 给予腺苷的水平[2]。腺苷受体存在3种亚型(A1,A2,A3),其中A2又可 进一步分为A2a 和A2b亚型。激动A1受体主要在心脏引起负性变时、变力和 变传导效应,而激动A2受体则主要引起外周血管扩张[3]。研究表明腺苷A2受 体降低外周血管阻力的作用与KATP状态[4]、NO途径以及环一磷酸腺苷(cAM P)浓度有关。本研究目的在于明确腺苷A1和A2受体在降低SAD大鼠BPV中的作用,并分 析KATP状态对其的影响。
, 百拇医药
1 材料和方法
1.1 试剂 腺苷、CPA和CPCA均为Sigma公司产品,临用时以生理盐水配制成所需 的浓度。格列本脲为Sigma公司产品,临用时先以1 ml 0.1 mol/L的NaOH溶解,接着在超声 条件下加5%葡萄糖至5 mg/ml。
1.2 实验动物 雄性SD大鼠,体质量270~330 g, 由上海SIPPR-BK公司提供。依 Krieger[5]所确立的方法制作SAD大鼠模型。术后1个月行腹主动脉(BP监测)和股 静脉(给药)插管。实验前16 h将动物连接至计算机化清醒自由活动大鼠血流动力学监测装 置,以2~3 μg/kg新福林iv,使大鼠血压升高6.78 kPa, 若心率减慢少于20次/min则认为 SAD成功。
1.3 方法 模型成功的大鼠于次日上午8:00开始采集数据。实验组共分5组。
, 百拇医药
1.3.1 腺苷、CPA和CPCA组 该3组实验于8:00~9:00静脉恒速 给予2 ml/(kg*h)的生理盐水,于9:00~10:00静脉分别给予腺苷、CPA或CPCA,剂量分别 为 347.8,0.7,0.8 μg/(kg*min)[容量均为2 ml/(kg*h)]。分别采集这两个阶段的 数据。
1.3.2 格列本脲组 第一阶段同1.3.1,于9:00~9:05给予格列本脲20 mg/kg, iv ,第二阶段的数据从给予格列本脲后15 min开始采集,即采集9:20~10:20 时间段的数 据。
1.3.3 格列本脲+CPCA组 同1.3.2,但从9:20开始静脉恒速给予0.8 μg/(kg*m in)的CPCA。
1.4 实验数据采集 每一个60 min的实验阶段被等分为两个30 min的时间段,本 实验所有数据均来自后30 min时间段。收缩压(SBP)、舒张压(DBP)和心动周期(HP)为 每搏采样基础上该30 min内的平均值,收缩压波动性(SBPV)和舒张压波动性(DBPV)为每 搏采样基础上该30 min内SBP和DBP的标准差。
, 百拇医药
1.5 统计学处理 数据以
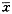 ±s表示,组内以配对t检验判断显著 性,组间以t检验判断显著性。
±s表示,组内以配对t检验判断显著 性,组间以t检验判断显著性。2 结 果
2.1 腺苷、CPA和CPCA对SAD大鼠BP,HP和BPV的影响 腺苷、CPA和CPCA均可显著 降低SAD大鼠的BP(P<0.01),并延长其HP(P<0.01),以CPA延长HP的作用最 为明显(表1)。腺苷及CPCA均可显著降低SAD大鼠SBPV和DBPV (P<0.01)。CPA 0.7 μg /(kg*min) 可降低SBP和DBP达CPCA同等程度,但CPA对SBPV和DBPV并无显著影响(P>0 .05, 图1)。
2.2 格列本脲和格列本脲+CPCA对SAD大鼠BP,HP和BPV的影 响 格列本脲能明显升高SAD大鼠的SBP和DBP(P<0.01),但其对HP并无显著影 响(P>0.05)。格列本脲阻断KATP后再给予CPCA,此时SBP与生理盐水比较仍显著 升高(P<0.05),但与单独给予格列本脲组比较明显下降(P<0.05); 对DBP而言,无论与生理盐水或是与单独给予格列本脲组比较均呈显著下降(P<0.01) ;HP则无明显变化(P>0.05, 表2)。 虽然格列本脲显著升高SAD大鼠的SBP和DBP,但它 使SBPV 和DBPV明显下降(P<0.01)。格列本脲阻断KATP后再给予CPCA,此时SBPV 和 DBPV仍明显下降(P<0.01),其下降幅度与单独给予格列本脲时相似(图2)。
, 百拇医药
表 1 腺苷、CPA和CPCA对SAD大鼠BP和HP的影响
Tab 1 Effect of adenosine, CPA and
CPCA on BP and HP in SAD rats(
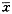 ±s) Group
±s) Groupn
SBP(p/kPa)
DBP
(p/kPa)
HP
(t/ms)
, 百拇医药 Control
7
18.93±
0.85
12.80 ±
1.20
148±
12.3
Adenosi ne
7
14.93±
1.43**
9.07±
, 百拇医药
2. 12**
158±
14.2**
Control
8
19.73±
1.01
13.07±
0.95
146±
15.5
CPA
, http://www.100md.com
8
14.93±
1.31**
8.80±
0.59**
331±
32.5**
Control
9
19.20±
1.05
12.67±
, 百拇医药
0.64
148±
10.4
CPCA
9
16.00±
1.32**
8.13±
1.03**
172±
19.5**
**P<0.01 vs control group

, 百拇医药
图 1 腺苷、CP A和CPCA对SAD大鼠BPV的影响
Fig 1 Effect of adenosine, CPA and
CPCA on BPV in SAD rats
NS: Control; Ado: Adenosine; ** P <0.01 vs NS
表 2 格列本脲和格列本脲+CPCA
对SAD大鼠BP和HP的影响
Tab 2 Effect of glibenclamide and glibenclamide
+CPCA on BP and HP in SAD rats (n=7,
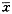 ±s) Group
±s) Group, http://www.100md.com
SBP(p/kPa)
DBP
(p/kPa)
HP
(t/ms)
Control
19.07±0.69
12.13±0.73
153±17.9
Gli
21.73±1.28**
15.47±1.23**
, http://www.100md.com
163±15.9
Control
18.80±0.93
11.73±0.68
154±12.7
Gli+CPCA
19.73±1.41*△
10.67±0.64**△△
161±17.0
Gli: Glibenclamide; * P<0.05, ** P<0.01 vs control group;
, 百拇医药
△ P<0.05, △△ P< 0.01 vs Gli group

图 2 格列本脲和格列本脲
+CPCA对SAD大鼠BPV的影响
Fig 2 Effect of glibenclamide and glibenclamide
+ CPCA on BPV in SAD rats
NS: Control; Gli: Glibenclamide; ** P<0.01 vs NS
3 讨 论
, 百拇医药
BPV是指BP在一定时间内的波动程度,是随动态血流动力学监测技术而出现的研 究心血管活动的指标。研究表明BPV升高可致器官损伤[1]。SAD大鼠具有BPV明显升 高而24 h平均动脉压不变的特点,是研究BPV的有效模型。SAD后BPV的升高涉及神经和体液 两大调节机制中的众多因素,因而其形成机制复杂。但可以肯定的一点是,致BPV升高的最 直接因素是外周总阻力(total peripheral resistance, TPR)的经常性改变。要降低BPV, 必须减轻或消除TPR的波动。
我们的实验发现,腺苷确实能降低SAD大鼠的BPV,这与Jacob等[2]的报道结果一致 。腺苷A1受体存在于心肌细胞,激动时产生负性变时、变力和变传导作用,导致心率减慢 和血压下降。从其受体的分布情况和功能分析,并不具备减轻或消除TPR的能力。本实验中C PA虽降低BP至与腺苷相似程度,但并无降BPV的作用证实了这一点。腺苷A2受体几乎分布 于所有的阻力血管,激动时可致血管舒张,其舒张血管的机制与促进KATP开放、以及 NO和cAMP形成增加有关。“腺苷假说”[3]认为当局部组织由于某种原因致血流不 足或阻力升高发生缺O2时,腺苷的形成就增加,并作用于该部位的腺苷受体使血管扩张和 血流代偿性增加,即腺苷具有保持局部组织O2供需平衡和稳定血管阻力的作用 。Trapani等[6]认为SAD后大鼠局部血管床的阻力处于不稳定状态, 这些局部血管床阻力的不稳定导致了TPR的波动,SAD大鼠BPV的升高可能源于此。本研究中 当用CPCA激动A2受体,使BP下降至与腺苷同等程度时,BPV也明显降低。因此,我们认为 无 论是腺苷还是CPCA,它们降低BPV作用与其降低外周血管阻力并维持局部血管床阻力稳定有 关。Mubagwa等[3] 和Satio等[4] 研究表明,KATP开放在腺苷及腺 苷A2受体激动剂降低BP的过程中具有重要作用,如果说CPCA降BPV的过程中KATP的 开放也具有重要作用,那么KATP特异性阻断剂格列本脲降BPV的作用则与之矛盾。我 们的研究中还发现当用格列本脲阻断KATP后,进一步的CPCA滴注并不能加大BPV下降 的幅度,因而推测此时BPV的下降仍来自于KATP的关闭。由于腺苷A2受体介导 的降 低BP或BPV作用存在多种可能的机制,因此无法确定KATP开放在其中的作用,进一步 的研究尚在进行中。
, 百拇医药
研究结果表明,腺苷经A2受体介导其降低SAD大鼠BPV的作用,格列本脲阻断KATP可 取消腺苷A2受体激动剂CPCA降低SAD大鼠BPV的作用。
[基金项目]国家自然科学基金资助项目(39670831).
[作者简介]沈甫明(1967-),男(汉族),硕士,助教.
[参 考 文 献]
[1] 龚 侃, 刘建国, 程 勇, 等. 血压波动性增高引起的器官损伤[J ].第二军医大学学报,1997,18(5):462-464.
[2] Jacob HJ, Alper RH, Brody MJ. Lability of arterial pressure after ba roreceptor denervation is not pressure dependent [J]. Hypertension,1989,14(5) :501-510.
, 百拇医药
[3] Mubagwa K, Mullane K, Flameng W. Role of adenosine in the heart and circulation [J]. Cardiovasc Res,1996,32(5):797-813.
[4] Saito K, Sakai K. Potentiating effects of nicorandil on the adenosin e A2 receptor-mediated vasodepression in rats: potential role for KATP channels [J]. Fundam Clin Pharmacol,1998,12(2):143-151.
[5] Krieger EM. Neurogenic hypertension in the rats [J]. Circ Res,1964 ,15(3):511-521.
[6] Trapani AJ, Barron KW, Brody MJ. Analysis of hemodynamic variability after sinoaortic denervation in the conscious rat [J]. Am J Physiol,1986,251 (20):R1163-1169.
[收稿日期] 2000-05-12
[修回日期] 2000-07-17, 百拇医药