母血中胎儿有核红细胞的分离及无创性产前基因诊断研究
作者:谢建生 龙桂芳
单位:530021 南宁, 广西医科大学第一附属医院儿科
关键词:胎儿细胞;产前诊断;母血循环
中华血液学杂志001002
【摘要】 目的 从母血循环中分离、富集、鉴定和提取胎儿有核红细胞,建立遗传病无创性产前基因诊断方法。方法 取25名妊娠8~36周的孕妇静脉血,加载在细胞分离液Histopaque 1.077上分离单个核细胞(MNC);用包被CD71抗体的Dynabeads M-450 CD71免疫磁珠或包被CD45抗体的Dynabeads M-450 CD45免疫磁珠富集MNC中的胎儿有核红细胞; anti-ζ-biotin或anti-γ-biotin珠蛋白链抗体和Fast Red显色反应识别富集的有核红细胞。在倒置显微镜下刮取5例重型β地中海贫血(地贫)高危胎儿的有核红细胞进行巢式聚合酶链反应(PCR),扩增产物经DNA逆向斑点杂交法阐明地贫基因突变类型。结果 25名孕妇外周血中均发现与anti-ζ-biotin 或anti-γ-biotin珠蛋白链呈阳性反应的胎儿有核红细胞。5例重型β地贫高危胎儿中,有3例所刮取的母血胎儿有核红细胞能成功进行巢式PCR,并鉴定基因突变类型。结论 Histopaque 1.077单一密度梯度离心分离MNC,结合抗CD71免疫磁珠阳性富集或CD45免疫磁珠阴性富集法,能有效富集母血循环中的胎儿有核红细胞。应用巢式PCR能对20个左右的胎儿有核红细胞DNA进行扩增,使遗传病的无创性产前基因诊断成为可能。
, http://www.100md.com
Separation and enrichment of fetal nucleated red blood cells from maternal blood for non-invasive prenatal gene diagnosis
XIE Jiansheng LONG Guifang
(Department of Pediatrics, First Affiliated Hospital, Guangxi Medical University, Nanning 530021, China)
【Abstract】 Objective In order to develop a non-invasive technique for prenatal gene diagnosis. Methods Peripheral blood mononuclear cells (MNCs)were separated by single density gradient Histopaque 1.077 from 25 pregnant women with gestations between 8~36 weeks. The fetal nucleated red blood cells (NRBCs)were enriched from the MNCs by positive selection using Dynabeads M-450 CD71 or negative selection using Dynabeads M-450 CD45. The enriched NRBCs were identified by anti-γ-biotin or anti-ζ-biotin antibodies. Globin gene of NRBCs from fetuses with risk of β-thalassemia major were amplified with nested PCR followed by reverse dot blot hybridization for gene diagnosis. Results NRBCs stained by anti-γ-biotin or anti-ζ-biotin antibodies could be found in the peripheral blood samples of the 25 pregnant women. Three out of 5 fetuses with risk of β-thalassemia major were successfully diagnosed using these NRBCs. Conclusion Fetal NRBCs in maternal circulation can be isolated and enriched by single gradient density Histopaque 1.077 followed by magnetic activated cell sorting. Nested PCR can amplify DNA for gene diagnosis from no less than 20 NRBCs.
, 百拇医药
【Key words】 Fetal cell; Prenatal diagnosis; Maternal circulation
1893年,Schmorl等[1]在死于子痫(eclampsia)的孕妇肺循环血中观察到滋养细胞(trophoblast),孕妇血中的HbF细胞比例增高,新生儿血型不合溶血病等,这些皆提示母血循环中存在胎儿细胞。1969年Walknowska等[2]首次报道在怀男性胎儿孕妇的外周血淋巴细胞中查出46,XY染色体核型。现在已经明确,母血循环中的胎儿细胞有四类,即有核红细胞(nucleated red blood cell, NRBC)[3]、淋巴细胞[4]、粒细胞[5]和滋养细胞[6]。因孕妇产后胎儿淋巴细胞在母血循环中可存留27年之久[7],因此不能区别母血中的胎儿淋巴细胞是本次妊娠还是既往妊娠的结果;滋养细胞体积太大,常常滞留在肺循环中,体循环很难发现[8];胎儿粒细胞和母血粒细胞不易识别,显然胎儿淋巴细胞、粒细胞和滋养细胞不宜作为无创性产前诊断的首选靶细胞。NRBC具有下列优势:①寿命较短,在产后妇女外周血中不会长期存留,本次妊娠发现的NRBC与既往妊娠无关;②有细胞核DNA可供遗传学分析;③细胞膜有转铁蛋白受体(transferrin receptor,CD71)和Glycophorin A受体,细胞浆有胚胎及胎儿血红蛋白或珠蛋白链(HbF,γ、ε、ζ肽链),有利于细胞的鉴别和分离,因此NRBC是进行无创性产前基因诊断的首选靶细胞。
, http://www.100md.com
对象和方法
1 研究对象 25名妊娠妇女为门诊进行遗传咨询、孕期保健检查者,妊娠8~36周。其中有5例及其丈夫均为地中海贫血(地贫)杂合子,绒毛活检和经腹壁羊膜腔穿刺取羊水在抽取静脉血后进行。
2 外周血单个核细胞(MNC)的分离 取孕妇静脉血4~20 ml,EDTA抗凝,用磷酸盐缓冲液(PBS,pH 7.4)按1∶1稀释。在15 ml Falcon离心管内,加入细胞分离液Histopaque 1.077(Sigma公司产品)5 ml,沿着离心管壁缓慢加入稀释孕妇血10 ml ,使血液覆盖在Histopaque 1.077上。以400×g室温离心30 min。吸取位于血浆和Histopaque 1.077之间的MNC,经用含5mmol/L EDTA和含体积分数为0.5%的BSA的PBS缓冲液洗涤1次后,以每107个细胞加80μl PBS缓冲液(pH 7.4)的比例制成MNC细胞悬液,此细胞悬液包含淋巴细胞、胎儿NRBC、血小板等。
, 百拇医药
3 免疫磁珠富集胎儿NRBC
3.1 阳性富集法: 抗CD71抗体能特异性识别NRBC细胞膜表面的转铁蛋白受体。将包被有CD71抗体的Dynabeads M-450 CD71免疫磁珠(挪威Dynal公司产品)以每个靶细胞4个磁珠的比例加入MNC细胞悬液中,在4℃冰箱中孵育45min后将磁珠标记的MNC细胞悬液放入Dynal MPC磁性柱内,静置2min,这样被磁珠标记的有核细胞被吸附,吸掉未被吸附的细胞。将磁珠标记的有核细胞经PBS洗涤后,以适当比例悬浮于PBS缓冲液中。
3.2 阴性富集法: 胎儿NRBC无CD45受体,将包被有CD45抗体的Dynabeads M-450 CD45免疫磁珠(挪威Dynal公司产品)与MNC细胞悬液孵育后,淋巴细胞等免疫磁珠阳性细胞被吸附在Dynal MPC磁性柱内,留在液相中的NRBCs因而得以富集。实验步骤同上述。
, 百拇医药
4 待检细胞的预处理 将免疫磁珠阳性或阴性富集所得的待检细胞用体积分数为4%的甲醛(稀释于PBS缓冲液中)固定30min,离心除去甲醛。用预冷至-20℃稀释丙酮(丙酮∶水=1∶1)1ml处理细胞2min。离心除去稀释丙酮,用预冷至-20℃的纯丙酮处理细胞5min。离心去掉纯丙酮后,再次用预冷至-20℃的稀释丙酮(丙酮∶水=1∶1)处理细胞2min。
5 单克隆抗体免疫标记细胞
5.1 封闭细胞内的非特异性结合位点: 将待检细胞悬浮于200μl 封闭(blocking)液(体积分数为0.5%的BSA磷酸盐缓冲液)中,室温孵育20min,目的在于封闭细胞上的非特异性结合位点。
5.2 特异性抗体标记胎儿NRBC: 将结合有生物素(biotin)的抗-ζ或抗-γ珠蛋白链抗体(anti-ζ-biotin或anti-γ-biotin)3μl(浓度250g/ml,Sigma公司产品)加入上述含待检细胞的封闭液中,室温孵育1h,特异性抗体即与胎儿NRBC内的ζ或γ珠蛋白链结合。离心除去封闭液,用PBS缓冲液洗涤细胞2次,以除去未结合的抗体。
, 百拇医药
5.3 显色反应:将经anti-ζ-biotin或anti-γ-biotin抗体标记的细胞悬浮于200μl PBS缓冲液中,加入1μl碱性磷酸酶-链抗生物素球蛋白(Alkaline Phosphatase-Streptavidin,AP-Streptavidin ,美国ZYMED Laboratories公司产品),室温孵育30 min,AP-Streptavidin即与抗体标记细胞上的biotin牢牢结合。经PBS缓冲液洗涤细胞2次后,悬浮于Fast Red TR/Napthol AS-MX(Sigma公司产品)Tris 缓冲液中,室温孵育1h,抗体标记细胞上的碱性磷酸酶催化底物Fast Red TR/Napthol AS-MX发生化学反应,anti-ζ-biotin或anti-γ-biotin抗体标记细胞被染成红色。用PBS缓冲液洗涤细胞2次后,将细胞悬浮在适量PBS缓冲液中,用细胞离心仪以700r/min离心4min将细胞涂布到载玻片上。
6 无创性产前基因诊断 将5例地贫杂合子孕妇细胞涂片在倒置显微镜(Axiovert 135,德国Zeiss公司)下,寻找胎儿NRBC。通过显微镜配置的显微操作仪,用玻璃纤维针将20个左右的胎儿NRBC刮到内含5μl 1×PCR缓冲液的Eppendorf管内,加入60μg蛋白酶K(Promega公司产品),50℃消化20min,最后95℃ 5min灭活蛋白酶K。巢式PCR由两次扩增反应组成,所用引物序列见表1,2,扩增部位和PCR片段长度见图1。胎儿NRBC消化产物作为第1次PCR的模板;取3~5μl 第1次PCR产物作为第2次PCR的模板。巢式PCR液组成:10×PCR 缓冲液5 μl,25mmol/L MgCl2 4 μl,2mmol/L dNTPs 5 μl,Taq 聚合酶 (PE公司,热启动酶) 1.5U,1 pmol/μl的PCR引物各2.5 μl,加入模板后用注射用水补足至总体积50 μl 。PCR条件:95℃ 12 min使聚合酶热启动,然后依次95℃ 30s、55℃ 45s、72℃ 45s,共30个循环,最后72℃ 10 min。胎儿NRBC经巢式PCR后得到两段DNA扩增带,按文献[9]用逆向斑点杂交鉴定基因突变。
, 百拇医药
表1 第1次PCR引物序列 引物名称
引物序列
P7
5′-TCCTAAGCCAGTGCCAGAAG-3′
S3
5′-TCCCATAGACTCACCCTGAA-3′
C3
5′-GTGTACACATATTGACCAAA-3′
B4
5′-CACTGACCTCCCACATTCCCTTTT-3′
表2 第2次PCR引物序列 引物名称
, 百拇医药
引物序列
China 1
5′ biotin-GTACGGCTGTCATCACTTAGACCTCA-3′
China 2
5′ biotin-TGCAGCTTGTCACAGTGCAGCTCACT-3′
China 3
5′ biotin-GTGTACACATATTGACCAAA-3′
China 4
5′ biotin-AGCACACAGACCAGCACGTT-3′
, 百拇医药
图1 巢式PCR引物在β基因中的位置及扩增片段长度示意图
结果
25名孕妇采血时的妊娠周数、采血量、免疫磁珠富集法、所用抗珠蛋白抗体和显微镜下观察到的胎儿NRBC数见表3。
表3 25例母血标本中发现的胎儿有核红细胞数 例号
妊娠
周数
采血量
(ml)
免疫磁珠
富集法
抗珠蛋白
, 百拇医药
抗体
NRBCs
1
8
6
阳性富集
γ
8
2
11
8
阳性富集
γ
13
, 百拇医药
3
9
5
阳性富集
γ
7
4
18
8
阳性富集
γ
10
5
22
, 百拇医药
7
阳性富集
γ
5
6
13
5
阳性富集
γ
5
7
13
5
阳性富集
, 百拇医药
γ
6
8
8
15
阳性富集
γ
26
9
35
17
阳性富集
γ
34
, http://www.100md.com
10
8
20
阳性富集
γ
45
11
8
10
阳性富集
γ
13
12
8
, http://www.100md.com
8
阳性富集
γ
10
13
14
4
阴性富集
γ
5
14
20
4
阴性富集
, 百拇医药
γ
6
15
16
16
阴性富集
γ
20
16
22
17
阴性富集
γ
20
, 百拇医药
17
36
12
阴性富集
γ
18
18
25
10
阴性富集
ζ
51
19
12
, 百拇医药
10
阴性富集
ζ
48
20
12
20
阴性富集
ζ
62
21
14
20
阴性富集
, 百拇医药
ζ
22
22
12
20
阴性富集
ζ
44
23
20
20
阳性+ 阴性富集
ζ
17+53
, 百拇医药
24
36
14
阳性+ 阴性富集
ζ
6+15
25
34
16
阳性+ 阴性富集
ζ
10+13
例1~例12母血标本经Histopaque 1.077离心分离的MNC层由抗CD71免疫磁珠阳性富集法收集CD71受体阳性细胞,再用anti-γ-biotin抗体标记其中的NRBC。在显微镜下观察,可发现被Fast Red染成红色的NRBC,其中不少细胞仍被CD71免疫磁珠吸附(图2)。从图2中可以看到,有些淋巴细胞也存在CD71受体,能被抗CD71免疫磁珠吸附。在未被抗CD71免疫磁珠吸附的MNC层中,也能找到NRBC,说明抗CD71免疫磁珠不能完全富集MNC层中所有的NRBC。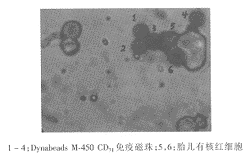
, 百拇医药
图2 Dynabeads M-450 CD71免疫磁珠NRBC阳性富集法
(Fast Red 显色反应,×100)
例13~例22的MNC层采用抗CD45免疫磁珠阴性富集法收集CD45受体阴性细胞。CD45受体阴性细胞中的NRBC,用anti-ζ-biotin或anti-γ-biotin抗体标记,结合Fast Red染色在显微镜下识别(图3)。抗CD45免疫磁珠也不能吸附所有的淋巴细胞,显微镜下观察到,经抗CD45免疫磁珠耗竭后的MNC中,仍有大量的淋巴细胞。
图3 Dynabeads M-450 CD45免疫磁珠NRBC阴性富集法
, 百拇医药
(Fast Red 显色反应,×100)
为了比较抗CD71阳性富集法和抗CD45阴性富集法收集NRBC的多寡,把例23~例25的MNC层平均分为两部分,一部分MNC采用抗CD71阳性富集法收集NRBC,另一部分采用抗CD45阴性富集法收集NRBC。结果显示抗CD45阴性富集法收集的NRBC细胞多于抗CD71阳性富集法。
例8~例12的胎儿为重型β地中海贫血高危儿,因此在倒置显微镜下将母血标本中的NRBC刮到Eppendorf管中进行巢式PCR,例8~例10成功得到PCR产物,PCR扩增图谱见图4。例11,例12 PCR失败。例8~例10的PCR产物经逆向斑点杂交法检测出胎儿基因型(表4),与绒毛或羊水细胞DNA的基因诊断结果一致。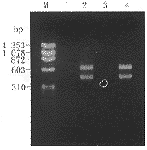
, http://www.100md.com
M:Φ174/Hae Ⅲ Markers;1,3:第1次PCR结果,无肉眼可见的扩增片段;2,4:第2次PCR结果,可见602bp和423bp扩增带
图4 巢式PCR扩增图谱
表4 3例胎儿有核红细胞基因诊断结果 例号
孕妇基因型
丈夫基因型
NRBCs基因诊断
8
41-42(-CTTT)杂合子
17(A→T)杂合子
17(A→T)杂合子
, http://www.100md.com
9
17(A→T)杂合子
IVS-Ⅱ-654(C→T)杂合子
17(A→T)杂合子
10
41-42(-CTTT)杂合子
17(A→T)杂合子
41-42(-CTTT) /17(A→T)
讨论 母血循环中胎儿细胞与母血细胞的比率约为1∶(105~108)[1],故要利用母血循环中的胎儿细胞作基因诊断,必须先对母血中的胎儿细胞进行分离和富集。目前,胎儿细胞的分离和富集技术有:密度梯度离心法; 红细胞溶解法; 荧光素激活细胞分类法(fluorescent activated cell sorting); 磁激活细胞分类法(magnetic activated cell sorting)和混合法:上述方法混合使用。
, http://www.100md.com
密度梯度离心法分离母血中的MNC,可采用三重密度梯度[10]和双重密度梯度[11]。我们用新生儿脐血和脾脏切除术后的β地贫/HbE双重杂合子外周血(两者均含有大量的NRBC)作预实验时发现,三重密度梯度离心法能把血细胞分为四层,即上层为淋巴细胞,中层主要为NRBC,下层主要为粒细胞,底层为成熟红细胞。双重密度梯度离心法仅能把血细胞分为MNC层、粒细胞层和成熟红细胞层,不能形成NRBC层。因为孕妇血中的NRBC十分稀少,10~20 ml的孕妇血经三重密度梯度离心分离后,很难形成肉眼可见的NRBC层。我们选用单一密度梯度离心法分离母血细胞,所形成的MNC层十分容易提取,比较经济实用。
转铁蛋白受体(CD71)是一种细胞膜表面糖蛋白,这种受体在NRBC膜上高度表达,所以可以利用包被抗CD71单克隆抗体的免疫磁珠,俘获母血MNC层中的胎儿NRBC。由于有些激活的淋巴细胞也有CD71表达,故Dynabead M-450 CD71在俘获NRBC的同时,也俘获激活的淋巴细胞。
, 百拇医药
白细胞膜有CD45抗原表达,而红系细胞则无此抗原,包被抗CD45单克隆抗体的免疫磁珠通过耗竭母血MNC层中的淋巴细胞,从而富集胎儿NRBC。我们的结果显示这种方法富集胎儿NRBC产量比用Dynabead M-450 CD71阳性富集法高。
不管是通过免疫磁珠阳性法或是阴性法富集母血胎儿NRBC,都不可避免地被母亲细胞污染。因此还必须对富集的胎儿细胞加以识别。人类从胚胎期发育过渡到胎儿期的过程中,有规律地按序出现两种类型的血红蛋白:早期的胚胎血红蛋白,即Hb Gower Ⅰ(ζ2ε2)、Hb Gower Ⅱ(α2γ2)、Hb Portland(ζ2γ2);妊娠中晚期的胎儿血红蛋白,即HbF(α2γ2)。根据血红蛋白的发育规律,我们应用anti-ζ和anti-γ抗体,完成对胎儿NRBC的鉴别。除了我们使用的免疫细胞化学法鉴定胚胎或胎儿特异血红蛋白外,可供选择的技术有Y探针荧光原位杂交法、PCR扩增Y染色体DNA序列、比较父方-母方和胎儿细胞的HLA差异等。
, http://www.100md.com
获取胎儿细胞进行产前诊断的主要途径有绒毛活检、羊膜腔穿刺和脐静脉穿刺三种。然而这些胎儿组织取样技术,尤其是绒毛活检对胎儿的潜在危险不能不加以考虑。由于孕妇外周血中存在胎儿细胞,并能从母血中分离提取胎儿NRBC,无创性产前基因诊断前景喜人。进行地贫无创性产前诊断,难度在于怎样把显微镜下发现的胎儿NRBC通过显微操作技术一个个刮入PCR缓冲液里。为了确保不被邻近的母血淋巴细胞污染,显微操作提取NRBC要注意以下几点:①制作细胞涂片的NRBC悬液浓度要适宜,以使细胞涂片中的细胞排列不至于太密集;②尽量选择远离淋巴细胞的NRBC;③把NRBC周围的母血淋巴细胞刮除干净后,再提取NRBC。只要能够收集20个左右的胎儿NRBC,通过巢式PCR,一般能够得到扩增产物,便于后续的基因诊断。
参 考 文 献
1,Martin WL, durrant LG, Liu DTY. No-invasive fetal cell isolation from maternal blood. Br J Obstet Gynaecol,1998, 105:576-583.
, 百拇医药
2,Walknowska J, Conte FA, Grumback MM. Practical and theoretical implications of fetal/maternal lymphocyte transfer. Lancet, 1969,1:1119-1122.
3,Bianchi DW, Flint AF, Pizzimenti MF,et al. Isolation of fetal DNA from nucleated erythrocyes in maternal blood. Proc Natl Acad Sci U S A,1990,87:3279-3283.
4,Herzenberg LA, Bianchi DW,Schroder J,et al. Fetal cells in the blood of pregnent women: detection and enrichment by fluorescence-activated cell sorting. Proc Natl Acad Sci U S A,1979,76:1453-1455.
, 百拇医药
5,Wessman M, Ylinen K, Knuutila S. Fetal granulocytes in maternal venous blood detected by in situ hybridization. Prenat Diagn, 1992,12:993-1000.
6,Goodfellow CF, Taylor PV. Extraction and identification of trophoblast cells circulating in peripheral blood during pregnancy. Br J Obstet Gynaecol,1982, 89:65-68.
7,Bianchi DW, Zickwolf GK, Weil GJ,et al. Male fetal progenitor cells persist in maternal blood for as long as 27 years postpartum. Proc Natl Acad Sci U S A, 1996, 93:705-708.
, 百拇医药
8,Adinolfi M. Non- or minimally invasive prenatal diagnostic tests on maternal blood samples or transcervical cells. Prenat Diagn, 1995, 15:889-896.
9,Cai SP, Wall J, Dan YW, et al. Reverse dot blot probes for the screening of β thalassemia mutations in Asians and American Blacks. Hum Mut, 1994, 3:59-63.
10,Ganshirt-Ahlert D, Borjesson-Stoll R, Burschyk M, et al. Detection of fetal trisomies 21 and 18 from maternal blood using triple gradient and magnetic cell sorting. Am J Reprod Immunol, 1993,30:194-201.
11,Sekizawa A, Kimura T, Sasaki M,et al. Prenatal diagnosis of Duchenne muscular dystrophy using a single fetal nucleated erthrocyte in maternal blood. Neurology, 1996,5:1350-1353.
(收稿日期:1999-10-26), http://www.100md.com
单位:530021 南宁, 广西医科大学第一附属医院儿科
关键词:胎儿细胞;产前诊断;母血循环
中华血液学杂志001002
【摘要】 目的 从母血循环中分离、富集、鉴定和提取胎儿有核红细胞,建立遗传病无创性产前基因诊断方法。方法 取25名妊娠8~36周的孕妇静脉血,加载在细胞分离液Histopaque 1.077上分离单个核细胞(MNC);用包被CD71抗体的Dynabeads M-450 CD71免疫磁珠或包被CD45抗体的Dynabeads M-450 CD45免疫磁珠富集MNC中的胎儿有核红细胞; anti-ζ-biotin或anti-γ-biotin珠蛋白链抗体和Fast Red显色反应识别富集的有核红细胞。在倒置显微镜下刮取5例重型β地中海贫血(地贫)高危胎儿的有核红细胞进行巢式聚合酶链反应(PCR),扩增产物经DNA逆向斑点杂交法阐明地贫基因突变类型。结果 25名孕妇外周血中均发现与anti-ζ-biotin 或anti-γ-biotin珠蛋白链呈阳性反应的胎儿有核红细胞。5例重型β地贫高危胎儿中,有3例所刮取的母血胎儿有核红细胞能成功进行巢式PCR,并鉴定基因突变类型。结论 Histopaque 1.077单一密度梯度离心分离MNC,结合抗CD71免疫磁珠阳性富集或CD45免疫磁珠阴性富集法,能有效富集母血循环中的胎儿有核红细胞。应用巢式PCR能对20个左右的胎儿有核红细胞DNA进行扩增,使遗传病的无创性产前基因诊断成为可能。
, http://www.100md.com
Separation and enrichment of fetal nucleated red blood cells from maternal blood for non-invasive prenatal gene diagnosis
XIE Jiansheng LONG Guifang
(Department of Pediatrics, First Affiliated Hospital, Guangxi Medical University, Nanning 530021, China)
【Abstract】 Objective In order to develop a non-invasive technique for prenatal gene diagnosis. Methods Peripheral blood mononuclear cells (MNCs)were separated by single density gradient Histopaque 1.077 from 25 pregnant women with gestations between 8~36 weeks. The fetal nucleated red blood cells (NRBCs)were enriched from the MNCs by positive selection using Dynabeads M-450 CD71 or negative selection using Dynabeads M-450 CD45. The enriched NRBCs were identified by anti-γ-biotin or anti-ζ-biotin antibodies. Globin gene of NRBCs from fetuses with risk of β-thalassemia major were amplified with nested PCR followed by reverse dot blot hybridization for gene diagnosis. Results NRBCs stained by anti-γ-biotin or anti-ζ-biotin antibodies could be found in the peripheral blood samples of the 25 pregnant women. Three out of 5 fetuses with risk of β-thalassemia major were successfully diagnosed using these NRBCs. Conclusion Fetal NRBCs in maternal circulation can be isolated and enriched by single gradient density Histopaque 1.077 followed by magnetic activated cell sorting. Nested PCR can amplify DNA for gene diagnosis from no less than 20 NRBCs.
, 百拇医药
【Key words】 Fetal cell; Prenatal diagnosis; Maternal circulation
1893年,Schmorl等[1]在死于子痫(eclampsia)的孕妇肺循环血中观察到滋养细胞(trophoblast),孕妇血中的HbF细胞比例增高,新生儿血型不合溶血病等,这些皆提示母血循环中存在胎儿细胞。1969年Walknowska等[2]首次报道在怀男性胎儿孕妇的外周血淋巴细胞中查出46,XY染色体核型。现在已经明确,母血循环中的胎儿细胞有四类,即有核红细胞(nucleated red blood cell, NRBC)[3]、淋巴细胞[4]、粒细胞[5]和滋养细胞[6]。因孕妇产后胎儿淋巴细胞在母血循环中可存留27年之久[7],因此不能区别母血中的胎儿淋巴细胞是本次妊娠还是既往妊娠的结果;滋养细胞体积太大,常常滞留在肺循环中,体循环很难发现[8];胎儿粒细胞和母血粒细胞不易识别,显然胎儿淋巴细胞、粒细胞和滋养细胞不宜作为无创性产前诊断的首选靶细胞。NRBC具有下列优势:①寿命较短,在产后妇女外周血中不会长期存留,本次妊娠发现的NRBC与既往妊娠无关;②有细胞核DNA可供遗传学分析;③细胞膜有转铁蛋白受体(transferrin receptor,CD71)和Glycophorin A受体,细胞浆有胚胎及胎儿血红蛋白或珠蛋白链(HbF,γ、ε、ζ肽链),有利于细胞的鉴别和分离,因此NRBC是进行无创性产前基因诊断的首选靶细胞。
, http://www.100md.com
对象和方法
1 研究对象 25名妊娠妇女为门诊进行遗传咨询、孕期保健检查者,妊娠8~36周。其中有5例及其丈夫均为地中海贫血(地贫)杂合子,绒毛活检和经腹壁羊膜腔穿刺取羊水在抽取静脉血后进行。
2 外周血单个核细胞(MNC)的分离 取孕妇静脉血4~20 ml,EDTA抗凝,用磷酸盐缓冲液(PBS,pH 7.4)按1∶1稀释。在15 ml Falcon离心管内,加入细胞分离液Histopaque 1.077(Sigma公司产品)5 ml,沿着离心管壁缓慢加入稀释孕妇血10 ml ,使血液覆盖在Histopaque 1.077上。以400×g室温离心30 min。吸取位于血浆和Histopaque 1.077之间的MNC,经用含5mmol/L EDTA和含体积分数为0.5%的BSA的PBS缓冲液洗涤1次后,以每107个细胞加80μl PBS缓冲液(pH 7.4)的比例制成MNC细胞悬液,此细胞悬液包含淋巴细胞、胎儿NRBC、血小板等。
, 百拇医药
3 免疫磁珠富集胎儿NRBC
3.1 阳性富集法: 抗CD71抗体能特异性识别NRBC细胞膜表面的转铁蛋白受体。将包被有CD71抗体的Dynabeads M-450 CD71免疫磁珠(挪威Dynal公司产品)以每个靶细胞4个磁珠的比例加入MNC细胞悬液中,在4℃冰箱中孵育45min后将磁珠标记的MNC细胞悬液放入Dynal MPC磁性柱内,静置2min,这样被磁珠标记的有核细胞被吸附,吸掉未被吸附的细胞。将磁珠标记的有核细胞经PBS洗涤后,以适当比例悬浮于PBS缓冲液中。
3.2 阴性富集法: 胎儿NRBC无CD45受体,将包被有CD45抗体的Dynabeads M-450 CD45免疫磁珠(挪威Dynal公司产品)与MNC细胞悬液孵育后,淋巴细胞等免疫磁珠阳性细胞被吸附在Dynal MPC磁性柱内,留在液相中的NRBCs因而得以富集。实验步骤同上述。
, 百拇医药
4 待检细胞的预处理 将免疫磁珠阳性或阴性富集所得的待检细胞用体积分数为4%的甲醛(稀释于PBS缓冲液中)固定30min,离心除去甲醛。用预冷至-20℃稀释丙酮(丙酮∶水=1∶1)1ml处理细胞2min。离心除去稀释丙酮,用预冷至-20℃的纯丙酮处理细胞5min。离心去掉纯丙酮后,再次用预冷至-20℃的稀释丙酮(丙酮∶水=1∶1)处理细胞2min。
5 单克隆抗体免疫标记细胞
5.1 封闭细胞内的非特异性结合位点: 将待检细胞悬浮于200μl 封闭(blocking)液(体积分数为0.5%的BSA磷酸盐缓冲液)中,室温孵育20min,目的在于封闭细胞上的非特异性结合位点。
5.2 特异性抗体标记胎儿NRBC: 将结合有生物素(biotin)的抗-ζ或抗-γ珠蛋白链抗体(anti-ζ-biotin或anti-γ-biotin)3μl(浓度250g/ml,Sigma公司产品)加入上述含待检细胞的封闭液中,室温孵育1h,特异性抗体即与胎儿NRBC内的ζ或γ珠蛋白链结合。离心除去封闭液,用PBS缓冲液洗涤细胞2次,以除去未结合的抗体。
, 百拇医药
5.3 显色反应:将经anti-ζ-biotin或anti-γ-biotin抗体标记的细胞悬浮于200μl PBS缓冲液中,加入1μl碱性磷酸酶-链抗生物素球蛋白(Alkaline Phosphatase-Streptavidin,AP-Streptavidin ,美国ZYMED Laboratories公司产品),室温孵育30 min,AP-Streptavidin即与抗体标记细胞上的biotin牢牢结合。经PBS缓冲液洗涤细胞2次后,悬浮于Fast Red TR/Napthol AS-MX(Sigma公司产品)Tris 缓冲液中,室温孵育1h,抗体标记细胞上的碱性磷酸酶催化底物Fast Red TR/Napthol AS-MX发生化学反应,anti-ζ-biotin或anti-γ-biotin抗体标记细胞被染成红色。用PBS缓冲液洗涤细胞2次后,将细胞悬浮在适量PBS缓冲液中,用细胞离心仪以700r/min离心4min将细胞涂布到载玻片上。
6 无创性产前基因诊断 将5例地贫杂合子孕妇细胞涂片在倒置显微镜(Axiovert 135,德国Zeiss公司)下,寻找胎儿NRBC。通过显微镜配置的显微操作仪,用玻璃纤维针将20个左右的胎儿NRBC刮到内含5μl 1×PCR缓冲液的Eppendorf管内,加入60μg蛋白酶K(Promega公司产品),50℃消化20min,最后95℃ 5min灭活蛋白酶K。巢式PCR由两次扩增反应组成,所用引物序列见表1,2,扩增部位和PCR片段长度见图1。胎儿NRBC消化产物作为第1次PCR的模板;取3~5μl 第1次PCR产物作为第2次PCR的模板。巢式PCR液组成:10×PCR 缓冲液5 μl,25mmol/L MgCl2 4 μl,2mmol/L dNTPs 5 μl,Taq 聚合酶 (PE公司,热启动酶) 1.5U,1 pmol/μl的PCR引物各2.5 μl,加入模板后用注射用水补足至总体积50 μl 。PCR条件:95℃ 12 min使聚合酶热启动,然后依次95℃ 30s、55℃ 45s、72℃ 45s,共30个循环,最后72℃ 10 min。胎儿NRBC经巢式PCR后得到两段DNA扩增带,按文献[9]用逆向斑点杂交鉴定基因突变。
, 百拇医药
表1 第1次PCR引物序列 引物名称
引物序列
P7
5′-TCCTAAGCCAGTGCCAGAAG-3′
S3
5′-TCCCATAGACTCACCCTGAA-3′
C3
5′-GTGTACACATATTGACCAAA-3′
B4
5′-CACTGACCTCCCACATTCCCTTTT-3′
表2 第2次PCR引物序列 引物名称
, 百拇医药
引物序列
China 1
5′ biotin-GTACGGCTGTCATCACTTAGACCTCA-3′
China 2
5′ biotin-TGCAGCTTGTCACAGTGCAGCTCACT-3′
China 3
5′ biotin-GTGTACACATATTGACCAAA-3′
China 4
5′ biotin-AGCACACAGACCAGCACGTT-3′

, 百拇医药
图1 巢式PCR引物在β基因中的位置及扩增片段长度示意图
结果
25名孕妇采血时的妊娠周数、采血量、免疫磁珠富集法、所用抗珠蛋白抗体和显微镜下观察到的胎儿NRBC数见表3。
表3 25例母血标本中发现的胎儿有核红细胞数 例号
妊娠
周数
采血量
(ml)
免疫磁珠
富集法
抗珠蛋白
, 百拇医药
抗体
NRBCs
1
8
6
阳性富集
γ
8
2
11
8
阳性富集
γ
13
, 百拇医药
3
9
5
阳性富集
γ
7
4
18
8
阳性富集
γ
10
5
22
, 百拇医药
7
阳性富集
γ
5
6
13
5
阳性富集
γ
5
7
13
5
阳性富集
, 百拇医药
γ
6
8
8
15
阳性富集
γ
26
9
35
17
阳性富集
γ
34
, http://www.100md.com
10
8
20
阳性富集
γ
45
11
8
10
阳性富集
γ
13
12
8
, http://www.100md.com
8
阳性富集
γ
10
13
14
4
阴性富集
γ
5
14
20
4
阴性富集
, 百拇医药
γ
6
15
16
16
阴性富集
γ
20
16
22
17
阴性富集
γ
20
, 百拇医药
17
36
12
阴性富集
γ
18
18
25
10
阴性富集
ζ
51
19
12
, 百拇医药
10
阴性富集
ζ
48
20
12
20
阴性富集
ζ
62
21
14
20
阴性富集
, 百拇医药
ζ
22
22
12
20
阴性富集
ζ
44
23
20
20
阳性+ 阴性富集
ζ
17+53
, 百拇医药
24
36
14
阳性+ 阴性富集
ζ
6+15
25
34
16
阳性+ 阴性富集
ζ
10+13
例1~例12母血标本经Histopaque 1.077离心分离的MNC层由抗CD71免疫磁珠阳性富集法收集CD71受体阳性细胞,再用anti-γ-biotin抗体标记其中的NRBC。在显微镜下观察,可发现被Fast Red染成红色的NRBC,其中不少细胞仍被CD71免疫磁珠吸附(图2)。从图2中可以看到,有些淋巴细胞也存在CD71受体,能被抗CD71免疫磁珠吸附。在未被抗CD71免疫磁珠吸附的MNC层中,也能找到NRBC,说明抗CD71免疫磁珠不能完全富集MNC层中所有的NRBC。

, 百拇医药
图2 Dynabeads M-450 CD71免疫磁珠NRBC阳性富集法
(Fast Red 显色反应,×100)
例13~例22的MNC层采用抗CD45免疫磁珠阴性富集法收集CD45受体阴性细胞。CD45受体阴性细胞中的NRBC,用anti-ζ-biotin或anti-γ-biotin抗体标记,结合Fast Red染色在显微镜下识别(图3)。抗CD45免疫磁珠也不能吸附所有的淋巴细胞,显微镜下观察到,经抗CD45免疫磁珠耗竭后的MNC中,仍有大量的淋巴细胞。

图3 Dynabeads M-450 CD45免疫磁珠NRBC阴性富集法
, 百拇医药
(Fast Red 显色反应,×100)
为了比较抗CD71阳性富集法和抗CD45阴性富集法收集NRBC的多寡,把例23~例25的MNC层平均分为两部分,一部分MNC采用抗CD71阳性富集法收集NRBC,另一部分采用抗CD45阴性富集法收集NRBC。结果显示抗CD45阴性富集法收集的NRBC细胞多于抗CD71阳性富集法。
例8~例12的胎儿为重型β地中海贫血高危儿,因此在倒置显微镜下将母血标本中的NRBC刮到Eppendorf管中进行巢式PCR,例8~例10成功得到PCR产物,PCR扩增图谱见图4。例11,例12 PCR失败。例8~例10的PCR产物经逆向斑点杂交法检测出胎儿基因型(表4),与绒毛或羊水细胞DNA的基因诊断结果一致。

, http://www.100md.com
M:Φ174/Hae Ⅲ Markers;1,3:第1次PCR结果,无肉眼可见的扩增片段;2,4:第2次PCR结果,可见602bp和423bp扩增带
图4 巢式PCR扩增图谱
表4 3例胎儿有核红细胞基因诊断结果 例号
孕妇基因型
丈夫基因型
NRBCs基因诊断
8
41-42(-CTTT)杂合子
17(A→T)杂合子
17(A→T)杂合子
, http://www.100md.com
9
17(A→T)杂合子
IVS-Ⅱ-654(C→T)杂合子
17(A→T)杂合子
10
41-42(-CTTT)杂合子
17(A→T)杂合子
41-42(-CTTT) /17(A→T)
讨论 母血循环中胎儿细胞与母血细胞的比率约为1∶(105~108)[1],故要利用母血循环中的胎儿细胞作基因诊断,必须先对母血中的胎儿细胞进行分离和富集。目前,胎儿细胞的分离和富集技术有:密度梯度离心法; 红细胞溶解法; 荧光素激活细胞分类法(fluorescent activated cell sorting); 磁激活细胞分类法(magnetic activated cell sorting)和混合法:上述方法混合使用。
, http://www.100md.com
密度梯度离心法分离母血中的MNC,可采用三重密度梯度[10]和双重密度梯度[11]。我们用新生儿脐血和脾脏切除术后的β地贫/HbE双重杂合子外周血(两者均含有大量的NRBC)作预实验时发现,三重密度梯度离心法能把血细胞分为四层,即上层为淋巴细胞,中层主要为NRBC,下层主要为粒细胞,底层为成熟红细胞。双重密度梯度离心法仅能把血细胞分为MNC层、粒细胞层和成熟红细胞层,不能形成NRBC层。因为孕妇血中的NRBC十分稀少,10~20 ml的孕妇血经三重密度梯度离心分离后,很难形成肉眼可见的NRBC层。我们选用单一密度梯度离心法分离母血细胞,所形成的MNC层十分容易提取,比较经济实用。
转铁蛋白受体(CD71)是一种细胞膜表面糖蛋白,这种受体在NRBC膜上高度表达,所以可以利用包被抗CD71单克隆抗体的免疫磁珠,俘获母血MNC层中的胎儿NRBC。由于有些激活的淋巴细胞也有CD71表达,故Dynabead M-450 CD71在俘获NRBC的同时,也俘获激活的淋巴细胞。
, 百拇医药
白细胞膜有CD45抗原表达,而红系细胞则无此抗原,包被抗CD45单克隆抗体的免疫磁珠通过耗竭母血MNC层中的淋巴细胞,从而富集胎儿NRBC。我们的结果显示这种方法富集胎儿NRBC产量比用Dynabead M-450 CD71阳性富集法高。
不管是通过免疫磁珠阳性法或是阴性法富集母血胎儿NRBC,都不可避免地被母亲细胞污染。因此还必须对富集的胎儿细胞加以识别。人类从胚胎期发育过渡到胎儿期的过程中,有规律地按序出现两种类型的血红蛋白:早期的胚胎血红蛋白,即Hb Gower Ⅰ(ζ2ε2)、Hb Gower Ⅱ(α2γ2)、Hb Portland(ζ2γ2);妊娠中晚期的胎儿血红蛋白,即HbF(α2γ2)。根据血红蛋白的发育规律,我们应用anti-ζ和anti-γ抗体,完成对胎儿NRBC的鉴别。除了我们使用的免疫细胞化学法鉴定胚胎或胎儿特异血红蛋白外,可供选择的技术有Y探针荧光原位杂交法、PCR扩增Y染色体DNA序列、比较父方-母方和胎儿细胞的HLA差异等。
, http://www.100md.com
获取胎儿细胞进行产前诊断的主要途径有绒毛活检、羊膜腔穿刺和脐静脉穿刺三种。然而这些胎儿组织取样技术,尤其是绒毛活检对胎儿的潜在危险不能不加以考虑。由于孕妇外周血中存在胎儿细胞,并能从母血中分离提取胎儿NRBC,无创性产前基因诊断前景喜人。进行地贫无创性产前诊断,难度在于怎样把显微镜下发现的胎儿NRBC通过显微操作技术一个个刮入PCR缓冲液里。为了确保不被邻近的母血淋巴细胞污染,显微操作提取NRBC要注意以下几点:①制作细胞涂片的NRBC悬液浓度要适宜,以使细胞涂片中的细胞排列不至于太密集;②尽量选择远离淋巴细胞的NRBC;③把NRBC周围的母血淋巴细胞刮除干净后,再提取NRBC。只要能够收集20个左右的胎儿NRBC,通过巢式PCR,一般能够得到扩增产物,便于后续的基因诊断。
参 考 文 献
1,Martin WL, durrant LG, Liu DTY. No-invasive fetal cell isolation from maternal blood. Br J Obstet Gynaecol,1998, 105:576-583.
, 百拇医药
2,Walknowska J, Conte FA, Grumback MM. Practical and theoretical implications of fetal/maternal lymphocyte transfer. Lancet, 1969,1:1119-1122.
3,Bianchi DW, Flint AF, Pizzimenti MF,et al. Isolation of fetal DNA from nucleated erythrocyes in maternal blood. Proc Natl Acad Sci U S A,1990,87:3279-3283.
4,Herzenberg LA, Bianchi DW,Schroder J,et al. Fetal cells in the blood of pregnent women: detection and enrichment by fluorescence-activated cell sorting. Proc Natl Acad Sci U S A,1979,76:1453-1455.
, 百拇医药
5,Wessman M, Ylinen K, Knuutila S. Fetal granulocytes in maternal venous blood detected by in situ hybridization. Prenat Diagn, 1992,12:993-1000.
6,Goodfellow CF, Taylor PV. Extraction and identification of trophoblast cells circulating in peripheral blood during pregnancy. Br J Obstet Gynaecol,1982, 89:65-68.
7,Bianchi DW, Zickwolf GK, Weil GJ,et al. Male fetal progenitor cells persist in maternal blood for as long as 27 years postpartum. Proc Natl Acad Sci U S A, 1996, 93:705-708.
, 百拇医药
8,Adinolfi M. Non- or minimally invasive prenatal diagnostic tests on maternal blood samples or transcervical cells. Prenat Diagn, 1995, 15:889-896.
9,Cai SP, Wall J, Dan YW, et al. Reverse dot blot probes for the screening of β thalassemia mutations in Asians and American Blacks. Hum Mut, 1994, 3:59-63.
10,Ganshirt-Ahlert D, Borjesson-Stoll R, Burschyk M, et al. Detection of fetal trisomies 21 and 18 from maternal blood using triple gradient and magnetic cell sorting. Am J Reprod Immunol, 1993,30:194-201.
11,Sekizawa A, Kimura T, Sasaki M,et al. Prenatal diagnosis of Duchenne muscular dystrophy using a single fetal nucleated erthrocyte in maternal blood. Neurology, 1996,5:1350-1353.
(收稿日期:1999-10-26), http://www.100md.com