己酮可可碱保护内毒素诱导急性肺损伤的实验研究
作者:何新华 李春盛 桂陪春 杨红
单位:何新华 李春盛 桂陪春(北京军区总医院,100700);杨红(中国医学科学院 中国协和医科大学基础研究所病理生理研究室)
关键词:己酮可可碱;急性肺损伤;NO;iNOS;ET
中国急救医学001003 [摘 要] 目的 探讨急性肺损伤的治疗方法。方法 建立大鼠急性肺损伤模型,随机分成3组,筛选药物己酮可可碱治疗,检测支气管肺泡灌洗液中性白细胞及巨噬细胞比例和肺通透指数,肺组织湿重/干重,肺血管通透性,一氧化氮(NO)、诱生性一氧化氮合成酶(iNOS)、内皮素(ET)测定和肺组织大体、病理观察。结果 治疗组与内毒素组比较,中性白细胞比例下降,肺通透指数减低,肺血管通透性下降,NO、iNOS、ET明显下降,肺组织大体明显改善,病理观察损伤肺组织修复;与生理盐水组差异不明显。结论 己酮可可碱能有效防治由内毒素诱导的急性肺损伤。
, 百拇医药
[中图分类号] R 563;R 36 [文献标识码] A [文章编号] 1002-1949(2000)10-0573-03
Experimental study on the protective effect of pentoxifylline in Lipopolysacharide-induced acute lung injury
HE Xin-hua
(Dept.of Emergency,General Hospital of Beijing Military Command,Beijing 100700, China)
LI Chun-sheng
(Dept.of Emergency,General Hospital of Beijing Military Command,Beijing 100700, China)
, http://www.100md.com
GUI Pei-chun,et al
(Dept.of Emergency,General Hospital of Beijing Military Command,Beijing 100700, China)
[Abstract] Objective To explore a therapeutic method for acute lung injury.Methods Wistar rat models of Lipopolysacharide(LPS)-induced acute lung injury(ALI) were randomly divided into the model group(group A),the pentoxifylline group (group B)and the saline solution group (group C).The ratio of the neutrophile and the macrophage in the bronchoalveolar lavage fluid (BALF) and lung permeability index (LPI) were observed.The lung wet weight/dry weight and the pulmonary microvascular permeability index (PMPI)were also analyzed respectively.The serum Nitric oxide (NO),Endothelium(ET)levels and the lung inducible NO,ET levels and the lung inducible nitric oxide synthnase (iNOS)activity were analyzed.The surface and histological appearance of lung were observed under microscope and electromicroscope.Results There were more obvious changes in ratio of the neutrophile and the macrophage,LPT,lung wet weight/dry weight,PMPI,NO,ET,iNOS activity and the surface and histological appearance of lung in group B than that in group A,and there were no significantly difference in group B and in group C.Conclusion It suggests pentoxifylline can obvious improve the Lipopolysacharide-induced ALI.
, http://www.100md.com
[Key words] Pentoxifylline; Acute lung injury; NO; iNOS; ET
己酮可可碱(PTX)作为血管活性药物用于治疗血管功能不全性疾病。近年发现它能抑制中性粒细胞、单核细胞聚集,保护血管内皮细胞而用于炎症性疾病的治疗,但机制不明确。本实验旨在探讨PTX对急性肺损伤的保护作用,进而了解治疗急性肺损伤的可行性及机制。
1 材料与方法
1.1 动物 实验用雄性Wistar大鼠(101只)由中国医学科学院动物所提供,体重200~350克,3%戊巴比妥(30 mg/kg)腹腔注射麻醉。内毒素组(A组):舌下静脉注射LPS(5 mg/kg)(Sigma提供),2小时后采集标本。治疗组(B组):注射LPS前1小时舌下静脉注射1%PTX(10 mg/kg),余同内毒素组。生理盐水组(C组):舌下静脉注射生理盐水,2小时后采集标本。
, 百拇医药
1.2 检测指标及方法 ①实验结束(2小时后)采集样本后,活杀动物,切开大鼠气管,经气管插入12号针头行肺泡灌洗,每次1 ml,总量为5 ml,记录收集的肺泡灌洗液量。显微镜下计数肺泡灌洗液中细胞总数及中性粒细胞及巨噬细胞数并计算所占百分比[1]。蛋白含量测定按Lowry法进行。2 000 r/min离心回收肺泡灌洗液15分钟,取上清液(或血浆1:30稀释液)50 μl,加入2 ml试剂C(0.2 N NaOH:4%Na2CO3:1%CuSO4:2%酒石酸钠=50:50:1:1)室温静置10分钟,加入1 N酚试剂100 μl摇匀,30分钟后,722型分光光度计比色(波长700 nm),将各样品OD值与标准曲线对比后,计算蛋白含量并以大鼠肺泡灌洗液上清液蛋白含量比血浆蛋白含量得到肺通透指数(LPI)。②肺血管通透性的测定:所有动物均预先股静脉注射Evans蓝(50 mg/kg体重),余方法同前。实验结束,取出肺脏,观察蓝染情况,剪去周围结缔组织,将肺浸泡于甲酰胺溶液中(甲酰胺溶液用量按20 ml/100 g动物体重计算),并放置在45~50℃温箱中温育72小时,取出肺组织,离心甲酰胺浸泡液,取上清液,722型分光光度计(波长620 nm)比色,根据标准曲线算出Evans蓝含量。以Evans含量多少表示通透性大小。③肺组织湿重/干重测定[2]:实验结束,开胸取出肺脏,称湿重后,置烤箱(80℃,20小时)烤至恒重,称干重,然后计算肺组织湿重干重之比。④大鼠血中NO含量:按北京邦定公司提供的试剂操作说明进行。⑤肺组织iNOS活性测定[3]:注射LPS后2小时处死大鼠,迅速取出一定量的肺组织,按1:5(W/V)比例加入预冷的Buffer A,在冰浴中匀浆器匀浆,4℃,20 000 g离心30分钟,收集上清液即为NOS提取液,置-20℃保存。采用Lowry法测定NOS提取液蛋白含量。取不同蛋白浓度的NOS提取液50 μl,加入50 μl反应缓冲液(内含0.2 μ Ci3H-精氨酸)于37℃水浴中反应15分钟,用2 ml预冷的Buffer C终止反应,再经0.5~0.7 ml Dowex 50 w×8(Na+型,Sigma 提供)的阳离子交换树脂层析柱分离反应液中游离的3H-精氨酸和新生成的3H-胍氨酸。上样前层析柱先用1 ml终止Buffer C平衡,上样后收集2 ml流出液和2 ml蒸馏水洗脱液,收集样品混匀后取出1 ml于闪烁杯中,加入甲苯-Triton X-100闪烁液7 ml,在液体闪烁计数仪上测定样本的放射性活性。⑥血管内皮素测定:按北方化学试剂公司提供的试剂说明操作。⑦肺组织学检查:每组各取4只大鼠肺组织少许,相关处理后普通光学显微镜和透射电镜观察。
, http://www.100md.com
1.3 数据处理 数据以平均值±标准差(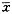 ±s)表示,组间差异性比较用t检验,以P<0.05表示有统计学意义。
±s)表示,组间差异性比较用t检验,以P<0.05表示有统计学意义。
2 结果
2.1 BALF中性粒细胞及巨噬细胞比例、LPI(10-3)、肺泡通透性(Evan氏蓝含量μg/ml)和肺组织湿重/干重比较见表1。
表1 BALF中性粒细胞及巨噬细胞比例、LPI、PMPI和肺组织干重/湿重比较
RATIO
LPI(10-3)
PMPI(μg/ml)
, 百拇医药
WET W./DRY W.
A
49.21±8.52*(n=6)
4.78±1.90**
6.08±0.73**(n=6)
4.47±0.14*(n=11)
B
32.44±9.16#(n=5)
1.51±0.67#
3.14±1.11#(n=5)
, 百拇医药
4.23±0.13#(n=6)
C
23.29±9.8(n=6)
1.09±0.28
2.70±0.78(n=6)
4.18±0.28(n=11)
A组与B组比较:*P<0.05,**P<0.01;B组与C组比较:#P>0.05
2.2 血清NO含量测定(μmol/L)、肺组织iNOS活性(pmol/mg*min)、血清内皮素(pg/ml)见表2。
表2 肺血清及肺组织NO、iNOS和ET比较
, 百拇医药
NO(μmol/L)
iNOS(pmol/mg*min)
ET(pg/ml)
A
3.12±0.88**(n=6)
109.87±50.28**(n=6)
647.95±185.24*(n=12)
B
0.93±0.36*(n=7)
53.47±16.54#(n=6)
, http://www.100md.com
585.29±135.56#(n=7)
C
2.10±0.34(n=6)
37.25±12.10(n=7)
359.55±128.54(n=9)
A组与B组比较:*P<0.05,**P<0.01;B组与C组比较:#P>0.05
2.3 肺组织学变化 注射LPS后大鼠肺血管内巳有中性粒细胞滞留、聚集。随时间延长,滞留、聚集现象更加明显,并有向毛细血管外移行增多趋势。给LPS后1小时,肺组织水肿,肺泡隔稍增厚,有少量血液成分渗出,肺泡内有中性粒细胞渗出。给LPS后2小时,肺泡内渗出增多,主要是血浆蛋白形成透明膜,肺泡隔增厚,内有中性粒细胞及红细胞渗出。B组大体标本观察到肺脏充血、水肿减轻,普通显微镜下可见肺血管内中性粒细胞滞留减少,肺充血及肺间质水肿减轻。电镜下A组可见肺泡隔间质水肿,毛细血管内皮肿胀,Ⅱ型上皮细胞板层体排空;B组上述现象减轻,肺损伤血管内皮修复;C组改变不明显。
, http://www.100md.com
3 讨论
3.1 肺损伤模型评价 Wistar大白鼠舌下静脉注射内毒素后,观察到大鼠呼吸加快、窘迫,其肺泡灌洗液中中性粒细胞及巨噬细胞比例和LPI、肺组织的湿重/干重比、肺泡通透性及肺组织大体及光学和电子显微镜观察,达到急性肺损伤的诊断标准[4],可以作为急性肺损伤动物模型用于实验研究。
早期应用PTX减轻了肺内白细胞聚集,减少肺血管蛋白渗出,有效防止了肺水肿形成。与笔者既往实验结果相似[5]。说明PTX能够保护肺脏免受致伤因素的影响,防止肺损伤的发生。
3.2 PTX对大鼠血清内皮素(ET)的影响 研究人员发现内皮细胞是信号感受器和传感器,能够协调众多生物活性分子,以维持内环境的稳定。本实验内毒素组ET明显高于正常,导致其增高的原因可能与LPS作为一种致病因素,直接损伤内皮细胞,改变其表型以及LPS激活中性粒细胞向内皮细胞粘附和聚集双重作用使ET合成、分泌增加而肺脏清除能力降低有关。血清ET升高后也可刺激中性粒细胞向内皮细胞粘附和聚集,增加中性粒细胞和肺泡巨噬细胞产生超氧阴离子的能力,从而导致肺微血管内皮细胞通透性增加,促进肺水肿的发生。而Rene等[6]亦认为LPS能直接损伤血管内皮。实验中观察到PTX组中性粒细胞及巨噬细胞比例则明显下降,病理观察血管内皮损伤后开始修复和肺间质水肿减轻、肺泡渗出减少,因而说明PTX在阻断LPS对血管内皮的损伤及ET分泌与释放方面起到了作用。
, 百拇医药
3.3 PTX对大鼠血清NO和肺组织iNOS活性的影响 实验发现,LPS致急性肺损伤组血清NO和肺组织iNOS活性均显著升高。NO作为一种新型的细胞信使分子,参与机体心血管、免疫和神经系统的生理和病理调节[7]。具有松弛血管平滑肌,抑制血小板聚集粘附和抑制白细胞粘附,影响神经传导,具有神经毒性、细胞毒性和免疫调节作用。其作用机理:①NO与细胞浆可溶性鸟苷酸环化酶(GC)活化中心上的Heme基因结合,使之活化,造成细胞内cGMP升高,而产生血管平滑肌松弛作用,抑制血小板聚集和粘附及神经传导等生理功能。②高浓度NO(通常由iNOS产生),不仅通过激活GC产生作用,还可能通过与细胞中含铁硫中心的酶结合,使之失活。③NO与超氧阴离子结合生成另一种强氧化自由基-过氧化亚硝基化合物,而产生细胞毒性作用,造成组织损伤、细胞坏死。NOS作为NO生成关键的限速因子,对其生物学功能的发挥起重要作用。正常生理条件下,肺血管内皮细胞NOS基因表达量低,而在IL-1、TNF等炎症介质刺激下可产生iNOS,iNOS诱导产生和释放包括NO在内的多种有害的炎性介质,从而影响白细胞、血小板、巨噬细胞及平滑肌细胞的功能,促使全身炎症反应进一步发展。文献报道,LPS激活内皮细胞释放的炎性介质还包括PAF、PGI2、IL-8、LTB4、氧自由基等。提示LPS可以激活血管内皮细胞以外的多种细胞包括单核细胞、中性粒细胞、血小板[8]等,释放多种炎性介质[9]。PTX具有降低中性粒细胞和巨噬细胞的粘附,减少肺内中性粒细胞和巨噬细胞的聚集。而且通过增强中性粒细胞内cAMP水平,减少氧自由基的产生,从而减少肺血管内皮的损害[10]。与此同时,PTX能下调TNF-α mRNA的表达,抑制TNF-α的产生与活性[11]。因而PTX通过上述两方面的作用,使血管内皮细胞NOS基因的表达,从而iNOS产生减少,导致产生和释放NO在内的多种有害的炎症介质减少,保护了肺组织,阻止了肺损伤的形成和发展。实验结果证明PTX的上述作用。
, 百拇医药
在内毒素诱导的急性肺损伤模型中,LPS激活单核细胞、中性粒细胞和血管内皮细胞,释放多种炎性介质如ET、NO、iNOS等,后者反过来可加重上述细胞的损害,形成一种恶性循环。而PTX能明显阻断单核细胞、中性粒细胞和血管内皮细胞的激活,预防和防止肺损伤的发生和发展。
[参考文献]
[1]Blythe S,England D,Esser B,et al.IgE antibody mediated inflammation of rat lung histologic and bronchoalveolar lavage assessment[J].Am Rev Respir Dis,1986,134:1246.
[2]Ono S,Westcott JY,Chang SW,et al.Endotoxin priming followed by high altitude causes pulmonary edema in rats[J].J Appl Physio,1993,74(4):1534.
, 百拇医药
[3]Pou S,Pou WS,Bredt DS,et al.Generation of superoxide by purified brain nitric oxide synthase[J].J Biol Chem,1992,267:24173-24176.
[4]冯新为.病理生理学[M].人民出版社,1993.269-273.
[5]何新华,周玉淑,黄席珍,等.己酮可可碱治疗急性胰腺炎合并急性肺损伤的实验研究[J].中华创伤杂志,1998,14(8):288-230.
[6]Rene G,James K,Alan H,et al.Synergistic hemodynamic effects of low-dose endotoxin and acute lung injury[J].Am J Respir Crit Care Med,1998,157:1919-1926.
, 百拇医药
[7]Kubes P,Suzuki M,Granger DN,et al.Nitric Oxide:an endogenous modulator of leukocyte adhension[J].Proc Natl Acad Sci,1991,88:46-51.
[8]Vander Meer TJ,Menconi MJ,Larkin VA,et al.Acute lung injury in endotoxiemic pigs:role of leuktriene B4[J].J Appl Physiol,1995,78(3):1121-31.
[9]Palace GP,Del Vecchio PJ,Horgan MJ,et al.Release of tumor necrosis factor after pulmonary artery occlusion and reperfusion[J].Am Rev Respir Dis,1993,147(1):143-7.
[10]彭应香,邓伟吾,黄绍光,等.己酮可可碱在胰腺炎并发急性肺损伤中的作用[J].中华结核和呼吸杂志,1994,17:106-108.
[11]Bernard C,Baenier P,Esposito B,et al.Prntoxifylline inhibits tumor necrosis factor synthesis in the arterial wall[J].J Cardiovascular Pharmac,1995,25(Suppl 2):S30-S33.
[收稿:1999-11-08], http://www.100md.com
单位:何新华 李春盛 桂陪春(北京军区总医院,100700);杨红(中国医学科学院 中国协和医科大学基础研究所病理生理研究室)
关键词:己酮可可碱;急性肺损伤;NO;iNOS;ET
中国急救医学001003 [摘 要] 目的 探讨急性肺损伤的治疗方法。方法 建立大鼠急性肺损伤模型,随机分成3组,筛选药物己酮可可碱治疗,检测支气管肺泡灌洗液中性白细胞及巨噬细胞比例和肺通透指数,肺组织湿重/干重,肺血管通透性,一氧化氮(NO)、诱生性一氧化氮合成酶(iNOS)、内皮素(ET)测定和肺组织大体、病理观察。结果 治疗组与内毒素组比较,中性白细胞比例下降,肺通透指数减低,肺血管通透性下降,NO、iNOS、ET明显下降,肺组织大体明显改善,病理观察损伤肺组织修复;与生理盐水组差异不明显。结论 己酮可可碱能有效防治由内毒素诱导的急性肺损伤。
, 百拇医药
[中图分类号] R 563;R 36 [文献标识码] A [文章编号] 1002-1949(2000)10-0573-03
Experimental study on the protective effect of pentoxifylline in Lipopolysacharide-induced acute lung injury
HE Xin-hua
(Dept.of Emergency,General Hospital of Beijing Military Command,Beijing 100700, China)
LI Chun-sheng
(Dept.of Emergency,General Hospital of Beijing Military Command,Beijing 100700, China)
, http://www.100md.com
GUI Pei-chun,et al
(Dept.of Emergency,General Hospital of Beijing Military Command,Beijing 100700, China)
[Abstract] Objective To explore a therapeutic method for acute lung injury.Methods Wistar rat models of Lipopolysacharide(LPS)-induced acute lung injury(ALI) were randomly divided into the model group(group A),the pentoxifylline group (group B)and the saline solution group (group C).The ratio of the neutrophile and the macrophage in the bronchoalveolar lavage fluid (BALF) and lung permeability index (LPI) were observed.The lung wet weight/dry weight and the pulmonary microvascular permeability index (PMPI)were also analyzed respectively.The serum Nitric oxide (NO),Endothelium(ET)levels and the lung inducible NO,ET levels and the lung inducible nitric oxide synthnase (iNOS)activity were analyzed.The surface and histological appearance of lung were observed under microscope and electromicroscope.Results There were more obvious changes in ratio of the neutrophile and the macrophage,LPT,lung wet weight/dry weight,PMPI,NO,ET,iNOS activity and the surface and histological appearance of lung in group B than that in group A,and there were no significantly difference in group B and in group C.Conclusion It suggests pentoxifylline can obvious improve the Lipopolysacharide-induced ALI.
, http://www.100md.com
[Key words] Pentoxifylline; Acute lung injury; NO; iNOS; ET
己酮可可碱(PTX)作为血管活性药物用于治疗血管功能不全性疾病。近年发现它能抑制中性粒细胞、单核细胞聚集,保护血管内皮细胞而用于炎症性疾病的治疗,但机制不明确。本实验旨在探讨PTX对急性肺损伤的保护作用,进而了解治疗急性肺损伤的可行性及机制。
1 材料与方法
1.1 动物 实验用雄性Wistar大鼠(101只)由中国医学科学院动物所提供,体重200~350克,3%戊巴比妥(30 mg/kg)腹腔注射麻醉。内毒素组(A组):舌下静脉注射LPS(5 mg/kg)(Sigma提供),2小时后采集标本。治疗组(B组):注射LPS前1小时舌下静脉注射1%PTX(10 mg/kg),余同内毒素组。生理盐水组(C组):舌下静脉注射生理盐水,2小时后采集标本。
, 百拇医药
1.2 检测指标及方法 ①实验结束(2小时后)采集样本后,活杀动物,切开大鼠气管,经气管插入12号针头行肺泡灌洗,每次1 ml,总量为5 ml,记录收集的肺泡灌洗液量。显微镜下计数肺泡灌洗液中细胞总数及中性粒细胞及巨噬细胞数并计算所占百分比[1]。蛋白含量测定按Lowry法进行。2 000 r/min离心回收肺泡灌洗液15分钟,取上清液(或血浆1:30稀释液)50 μl,加入2 ml试剂C(0.2 N NaOH:4%Na2CO3:1%CuSO4:2%酒石酸钠=50:50:1:1)室温静置10分钟,加入1 N酚试剂100 μl摇匀,30分钟后,722型分光光度计比色(波长700 nm),将各样品OD值与标准曲线对比后,计算蛋白含量并以大鼠肺泡灌洗液上清液蛋白含量比血浆蛋白含量得到肺通透指数(LPI)。②肺血管通透性的测定:所有动物均预先股静脉注射Evans蓝(50 mg/kg体重),余方法同前。实验结束,取出肺脏,观察蓝染情况,剪去周围结缔组织,将肺浸泡于甲酰胺溶液中(甲酰胺溶液用量按20 ml/100 g动物体重计算),并放置在45~50℃温箱中温育72小时,取出肺组织,离心甲酰胺浸泡液,取上清液,722型分光光度计(波长620 nm)比色,根据标准曲线算出Evans蓝含量。以Evans含量多少表示通透性大小。③肺组织湿重/干重测定[2]:实验结束,开胸取出肺脏,称湿重后,置烤箱(80℃,20小时)烤至恒重,称干重,然后计算肺组织湿重干重之比。④大鼠血中NO含量:按北京邦定公司提供的试剂操作说明进行。⑤肺组织iNOS活性测定[3]:注射LPS后2小时处死大鼠,迅速取出一定量的肺组织,按1:5(W/V)比例加入预冷的Buffer A,在冰浴中匀浆器匀浆,4℃,20 000 g离心30分钟,收集上清液即为NOS提取液,置-20℃保存。采用Lowry法测定NOS提取液蛋白含量。取不同蛋白浓度的NOS提取液50 μl,加入50 μl反应缓冲液(内含0.2 μ Ci3H-精氨酸)于37℃水浴中反应15分钟,用2 ml预冷的Buffer C终止反应,再经0.5~0.7 ml Dowex 50 w×8(Na+型,Sigma 提供)的阳离子交换树脂层析柱分离反应液中游离的3H-精氨酸和新生成的3H-胍氨酸。上样前层析柱先用1 ml终止Buffer C平衡,上样后收集2 ml流出液和2 ml蒸馏水洗脱液,收集样品混匀后取出1 ml于闪烁杯中,加入甲苯-Triton X-100闪烁液7 ml,在液体闪烁计数仪上测定样本的放射性活性。⑥血管内皮素测定:按北方化学试剂公司提供的试剂说明操作。⑦肺组织学检查:每组各取4只大鼠肺组织少许,相关处理后普通光学显微镜和透射电镜观察。
, http://www.100md.com
1.3 数据处理 数据以平均值±标准差(
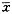 ±s)表示,组间差异性比较用t检验,以P<0.05表示有统计学意义。
±s)表示,组间差异性比较用t检验,以P<0.05表示有统计学意义。2 结果
2.1 BALF中性粒细胞及巨噬细胞比例、LPI(10-3)、肺泡通透性(Evan氏蓝含量μg/ml)和肺组织湿重/干重比较见表1。
表1 BALF中性粒细胞及巨噬细胞比例、LPI、PMPI和肺组织干重/湿重比较
RATIO
LPI(10-3)
PMPI(μg/ml)
, 百拇医药
WET W./DRY W.
A
49.21±8.52*(n=6)
4.78±1.90**
6.08±0.73**(n=6)
4.47±0.14*(n=11)
B
32.44±9.16#(n=5)
1.51±0.67#
3.14±1.11#(n=5)
, 百拇医药
4.23±0.13#(n=6)
C
23.29±9.8(n=6)
1.09±0.28
2.70±0.78(n=6)
4.18±0.28(n=11)
A组与B组比较:*P<0.05,**P<0.01;B组与C组比较:#P>0.05
2.2 血清NO含量测定(μmol/L)、肺组织iNOS活性(pmol/mg*min)、血清内皮素(pg/ml)见表2。
表2 肺血清及肺组织NO、iNOS和ET比较
, 百拇医药
NO(μmol/L)
iNOS(pmol/mg*min)
ET(pg/ml)
A
3.12±0.88**(n=6)
109.87±50.28**(n=6)
647.95±185.24*(n=12)
B
0.93±0.36*(n=7)
53.47±16.54#(n=6)
, http://www.100md.com
585.29±135.56#(n=7)
C
2.10±0.34(n=6)
37.25±12.10(n=7)
359.55±128.54(n=9)
A组与B组比较:*P<0.05,**P<0.01;B组与C组比较:#P>0.05
2.3 肺组织学变化 注射LPS后大鼠肺血管内巳有中性粒细胞滞留、聚集。随时间延长,滞留、聚集现象更加明显,并有向毛细血管外移行增多趋势。给LPS后1小时,肺组织水肿,肺泡隔稍增厚,有少量血液成分渗出,肺泡内有中性粒细胞渗出。给LPS后2小时,肺泡内渗出增多,主要是血浆蛋白形成透明膜,肺泡隔增厚,内有中性粒细胞及红细胞渗出。B组大体标本观察到肺脏充血、水肿减轻,普通显微镜下可见肺血管内中性粒细胞滞留减少,肺充血及肺间质水肿减轻。电镜下A组可见肺泡隔间质水肿,毛细血管内皮肿胀,Ⅱ型上皮细胞板层体排空;B组上述现象减轻,肺损伤血管内皮修复;C组改变不明显。
, http://www.100md.com
3 讨论
3.1 肺损伤模型评价 Wistar大白鼠舌下静脉注射内毒素后,观察到大鼠呼吸加快、窘迫,其肺泡灌洗液中中性粒细胞及巨噬细胞比例和LPI、肺组织的湿重/干重比、肺泡通透性及肺组织大体及光学和电子显微镜观察,达到急性肺损伤的诊断标准[4],可以作为急性肺损伤动物模型用于实验研究。
早期应用PTX减轻了肺内白细胞聚集,减少肺血管蛋白渗出,有效防止了肺水肿形成。与笔者既往实验结果相似[5]。说明PTX能够保护肺脏免受致伤因素的影响,防止肺损伤的发生。
3.2 PTX对大鼠血清内皮素(ET)的影响 研究人员发现内皮细胞是信号感受器和传感器,能够协调众多生物活性分子,以维持内环境的稳定。本实验内毒素组ET明显高于正常,导致其增高的原因可能与LPS作为一种致病因素,直接损伤内皮细胞,改变其表型以及LPS激活中性粒细胞向内皮细胞粘附和聚集双重作用使ET合成、分泌增加而肺脏清除能力降低有关。血清ET升高后也可刺激中性粒细胞向内皮细胞粘附和聚集,增加中性粒细胞和肺泡巨噬细胞产生超氧阴离子的能力,从而导致肺微血管内皮细胞通透性增加,促进肺水肿的发生。而Rene等[6]亦认为LPS能直接损伤血管内皮。实验中观察到PTX组中性粒细胞及巨噬细胞比例则明显下降,病理观察血管内皮损伤后开始修复和肺间质水肿减轻、肺泡渗出减少,因而说明PTX在阻断LPS对血管内皮的损伤及ET分泌与释放方面起到了作用。
, 百拇医药
3.3 PTX对大鼠血清NO和肺组织iNOS活性的影响 实验发现,LPS致急性肺损伤组血清NO和肺组织iNOS活性均显著升高。NO作为一种新型的细胞信使分子,参与机体心血管、免疫和神经系统的生理和病理调节[7]。具有松弛血管平滑肌,抑制血小板聚集粘附和抑制白细胞粘附,影响神经传导,具有神经毒性、细胞毒性和免疫调节作用。其作用机理:①NO与细胞浆可溶性鸟苷酸环化酶(GC)活化中心上的Heme基因结合,使之活化,造成细胞内cGMP升高,而产生血管平滑肌松弛作用,抑制血小板聚集和粘附及神经传导等生理功能。②高浓度NO(通常由iNOS产生),不仅通过激活GC产生作用,还可能通过与细胞中含铁硫中心的酶结合,使之失活。③NO与超氧阴离子结合生成另一种强氧化自由基-过氧化亚硝基化合物,而产生细胞毒性作用,造成组织损伤、细胞坏死。NOS作为NO生成关键的限速因子,对其生物学功能的发挥起重要作用。正常生理条件下,肺血管内皮细胞NOS基因表达量低,而在IL-1、TNF等炎症介质刺激下可产生iNOS,iNOS诱导产生和释放包括NO在内的多种有害的炎性介质,从而影响白细胞、血小板、巨噬细胞及平滑肌细胞的功能,促使全身炎症反应进一步发展。文献报道,LPS激活内皮细胞释放的炎性介质还包括PAF、PGI2、IL-8、LTB4、氧自由基等。提示LPS可以激活血管内皮细胞以外的多种细胞包括单核细胞、中性粒细胞、血小板[8]等,释放多种炎性介质[9]。PTX具有降低中性粒细胞和巨噬细胞的粘附,减少肺内中性粒细胞和巨噬细胞的聚集。而且通过增强中性粒细胞内cAMP水平,减少氧自由基的产生,从而减少肺血管内皮的损害[10]。与此同时,PTX能下调TNF-α mRNA的表达,抑制TNF-α的产生与活性[11]。因而PTX通过上述两方面的作用,使血管内皮细胞NOS基因的表达,从而iNOS产生减少,导致产生和释放NO在内的多种有害的炎症介质减少,保护了肺组织,阻止了肺损伤的形成和发展。实验结果证明PTX的上述作用。
, 百拇医药
在内毒素诱导的急性肺损伤模型中,LPS激活单核细胞、中性粒细胞和血管内皮细胞,释放多种炎性介质如ET、NO、iNOS等,后者反过来可加重上述细胞的损害,形成一种恶性循环。而PTX能明显阻断单核细胞、中性粒细胞和血管内皮细胞的激活,预防和防止肺损伤的发生和发展。
[参考文献]
[1]Blythe S,England D,Esser B,et al.IgE antibody mediated inflammation of rat lung histologic and bronchoalveolar lavage assessment[J].Am Rev Respir Dis,1986,134:1246.
[2]Ono S,Westcott JY,Chang SW,et al.Endotoxin priming followed by high altitude causes pulmonary edema in rats[J].J Appl Physio,1993,74(4):1534.
, 百拇医药
[3]Pou S,Pou WS,Bredt DS,et al.Generation of superoxide by purified brain nitric oxide synthase[J].J Biol Chem,1992,267:24173-24176.
[4]冯新为.病理生理学[M].人民出版社,1993.269-273.
[5]何新华,周玉淑,黄席珍,等.己酮可可碱治疗急性胰腺炎合并急性肺损伤的实验研究[J].中华创伤杂志,1998,14(8):288-230.
[6]Rene G,James K,Alan H,et al.Synergistic hemodynamic effects of low-dose endotoxin and acute lung injury[J].Am J Respir Crit Care Med,1998,157:1919-1926.
, 百拇医药
[7]Kubes P,Suzuki M,Granger DN,et al.Nitric Oxide:an endogenous modulator of leukocyte adhension[J].Proc Natl Acad Sci,1991,88:46-51.
[8]Vander Meer TJ,Menconi MJ,Larkin VA,et al.Acute lung injury in endotoxiemic pigs:role of leuktriene B4[J].J Appl Physiol,1995,78(3):1121-31.
[9]Palace GP,Del Vecchio PJ,Horgan MJ,et al.Release of tumor necrosis factor after pulmonary artery occlusion and reperfusion[J].Am Rev Respir Dis,1993,147(1):143-7.
[10]彭应香,邓伟吾,黄绍光,等.己酮可可碱在胰腺炎并发急性肺损伤中的作用[J].中华结核和呼吸杂志,1994,17:106-108.
[11]Bernard C,Baenier P,Esposito B,et al.Prntoxifylline inhibits tumor necrosis factor synthesis in the arterial wall[J].J Cardiovascular Pharmac,1995,25(Suppl 2):S30-S33.
[收稿:1999-11-08], http://www.100md.com