不同生长形态绿脓杆菌胞外粘液多糖的含量及其意义
不同生长形态绿脓杆菌胞外粘液多糖的含量及其意义
丛延广 刘俊康 袁泽涛 邓国宏 徐启旺
摘 要: 目的 探讨不同形态绿脓杆菌胞外粘多糖的含量及其对体外培养的肺癌细胞粘附能力的影响。方法 在分离一株形态对培养温度敏感的绿脓杆菌基础上,提取潜生体与繁殖体的胞外粘液多糖,以干重比评价二者粘液多糖的含量;并测定其对体外培养细胞粘附的影响。结果 潜生体胞外粘液多糖含量显著增加(P<0.01),同时其对体外培养细胞的粘附率也显著提高(P<0.01)。结论 绿脓杆菌繁殖体转变为潜生体后,其胞外粘液多糖含量及其粘附能力均有显著性提高。对绿脓杆菌潜生体的研究有助于对绿脓杆菌致病性的深入认识。
关键词:绿脓杆菌;潜生体;繁殖体
, 百拇医药
细菌在其不同生长阶段具有多形性特点,比较特殊的是纤丝状形态变化。细菌形成纤丝状菌体可由多种因素导致,Jensen等[1]认为纤丝体是由于细菌受外界环境的影响不能正常分裂而形成的,是细菌对自然环境某些条件的适应性变化。本实验室在生物波理论的研究过程中,根据变形杆菌纤丝状菌体在原条件下无明显增殖,代谢缓慢,具有多个核质,能在适当条件下断裂形成多个繁殖体等特点,称其为潜生体(Cryptic growth cell,CGC)[2]。
本实验在分离得到1株对培养温度敏感的绿脓杆菌基础上,对绿脓杆菌潜生体与繁殖体胞外粘液多糖的含量及其粘附能力进行了比较,以深入认识绿脓杆菌潜生体与致病性有关的生物学性质。
1 材料与方法
1.1 绿脓杆菌菌株 本室分离,血清8型,该菌的形态具有温度敏感性,即在37°C培养时细菌呈短杆状即繁殖体,而在低于25°C培养时呈纤丝状即潜生体。
, 百拇医药
1.2 绿脓杆菌选择鉴定培养基(DPA)
主要配方为蛋白胨20 g/L,硫酸钾10 g/L,氯化钾1.4 g/L,甘油9g/L,toween-20 20 g/L,硫酸铁0.05 g/L,琼脂15 g/L。
1.3 肺巨细胞癌细胞株(PG细胞)
北京医科大学建株,引自重庆医科大学病生教研室,以标准方法传代。
1.4 细菌培养及定量方法
将菌苔点种于DPA平板上,于25°C培养过夜即获得潜生体,于37°C培养过夜即获得繁殖体,以生理盐水稀释成细菌悬液。经十倍系列稀释后,进行菌落记数,以获得菌悬液的数量浓度。
1.5 胞外粘液多糖的分离及测定
, http://www.100md.com
参考陆森泉[3]方法进行提取,最后沉淀以双蒸水溶解,在4°C双蒸水中透析。取透析后剩下的物质加入已称好的称量瓶中,于100°C烤箱中烤至恒重,将前后称量的结果相减即得到粘液多糖的干重。同时分别称量潜生体和繁殖体干重,以粘液多糖与潜生体及繁殖体的干重比评价二者胞外粘液多糖的产量。
1.6 粘附实验
参考Simpson[4]的方法进行,记数30个细胞粘附的细菌数,计算粘附率(cfu/cell)。
1.7 数据处理
采用EZSTAT2统计软件处理数据。
2 结果
2.1 绿脓杆菌潜生体与繁殖体形态
, 百拇医药
见图1、2。
2.2 胞外粘液多糖含量测定结果
结果见表1。
2.3 潜生体与繁殖体对体外培养的PG细胞粘附实验结果
结果见表2。
图1 绿脓杆菌潜生体形态 (革兰氏染色×1 000)
Fig 1 Morphology of cryptic growth cells withGram stain (×1 000)
, 百拇医药
图2 绿脓杆菌繁殖体形态 (革兰氏染色×1 000)
Fig 2 Morphology of vegetative cells withGram stain (×1 000)
表1 潜生体与繁殖体胞外粘液多糖含量测定结果(X±s)
Tab 1 The mucoexopolysaccharide(MEPS) content ofvegetative cell and cryptic growth cell(X±s)
Growth forms
Content of MEPS(mg/mg cell)
Vegetative cell
, http://www.100md.com
0.084±0.002
Cryptic growth cell
0.514±0.060*
*:P<0.01 vs vegetative cell group
表2 潜生体与繁殖体对体外培养的PG细胞粘附率比较(X±s)
Tab 2 The adhesion rate of vegetative cell and cryptic growth cell to cultured lung cancer cells in vitro(X±s)
Growth forms
The adherence rate(cfu/cell)
, http://www.100md.com
Vegetative cell
3.78±0.544
Cryptic growth cell
12.6 ±2.10*
*:P<0.01 vs vegetative cell group
结果表明该绿脓杆菌潜生体多聚集在一起粘附于细胞表面,使粘附率显著提高,见图3。而繁殖体多以单个细菌散在地粘附于细胞上,粘附率较低,见图4。
图3 绿脓杆菌潜生体对体外培养的PG细胞的粘附 (瑞氏染色×1 000)
, http://www.100md.com
Fig 3 Adhesion of cryptic growth cells to PG cells in vitro (Wright stain×1 000)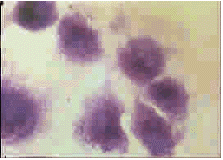
图4 绿脓杆菌繁殖体对体外培养的PG细胞的粘附 (瑞氏染色×1 000)
Fig 4 Adhesion of vegetative cells to PG cells in vitro (Wright stain×1 000)
3 讨论
细菌在生长过程中表现多形性,如得到广泛研究的变形杆菌迁徙生长现象中的丝状体[5]。多种因素可导致潜生体的形成,其长度可以是一般菌体的几倍乃至几十倍。绿脓杆菌潜生体的研究较少,一个重要原因是难以获得潜生体稳定的纯培养。而作为一个临床上重要的机会致病菌,绿脓杆菌潜生体的研究显得更有意义。
, http://www.100md.com
本研究在分离得到一株形态对培养温度敏感的绿脓杆菌基础上,实验发现潜生体胞外粘液多糖的含量显著高于繁殖体。粘液多糖具有多种重要的生物学性质,如抵抗吞噬细胞的吞噬和抗菌药物的损伤作用,也是细菌的粘附因子之一,粘液多糖的增多会对潜生体有关的生物学性质产生重要影响。
粘液型绿脓杆菌在组织表面的粘附主要受胞外粘液多糖的影响(非粘液型则主要受菌毛的控制)。Hata等[6]对绿脓杆菌感染的呼吸道表面的扫描电镜观察显示,非粘液型绿脓杆菌多以单个菌体粘附在细胞表面,粘液型绿脓杆菌则主要以微菌落群的形式粘附。因此,粘液型菌株的粘附能力显著高于非粘液型菌株。这个结论与本实验结果可以相互应证,即产生大量粘液多糖的潜生体对PG细胞的粘附率显著高于繁殖体。粘液多糖对潜生体粘附能力的提高起到非常重要的作用,同时潜生体较大的个体也是重要的因素之一,因为个体较大,与细胞的接触面积增大,相互作用的机率也显著提高,从而有利于它粘附在细胞表面,也有利于相互聚集在一起。绿脓杆菌粘液多糖主要成分是藻酸盐,由D-甘露糖醛酸,L-古洛糖醛酸组成,多聚物中较多的羟基和羧基能促进细菌间的聚集。由粘附照片也可以看出,繁殖体散在地粘附于PG细胞表面,而潜生体则聚集在一起粘附于细胞表面,这就显著增加了细菌粘附的数量和质量。聚集在一起的菌体构成稳定的群体结构,这种群体结构的适应能力明显提高,能抵抗不利因素的影响。McCoy等[7]研究表明,表面生长的细菌在其生物膜的形成过程中,伴随着潜生体的大量产生,这些潜生体使生物膜构成一个立体的交叉网络结构,使其在表面的存在更牢固。生物膜在细菌致病过程中起到非常重要的作用[8]。
, 百拇医药
藻酸盐不仅仅是绿脓杆菌重要的毒力因子,更广泛地应用于食品、制药及化工等领域。因此,有关藻酸盐合成的分子生物学及生物化学研究引起人们极大的兴趣[9]。多种环境因素能影响藻酸盐的生成,有文献报道某些绿脓杆菌藻酸盐的产生受到温度的影响,文章认为是由于生成藻酸盐的酶类或调控多肽的最适温度发生了漂移[10]。潜生体的形成涉及多基因多产物,是一个复杂过程,在此过程中,也可能产生藻酸盐的基因或其表达同时发生变化,导致细菌藻酸盐的产生量发生改变。对于本株绿脓杆菌藻酸盐的增减,究竟是环境温度直接或间接作用,抑或与形态改变有关尚不清楚。但迄今无文献报道绿脓杆菌在藻酸盐产生改变的同时,有形态上的变化,说明本实验发现的是一个独特现象。
Alm[11]认为绿脓杆菌能根据宿主环境的变化,调控它两个重要的毒力因子――4型菌毛和藻酸盐的表达。本实验结果表明,部分绿脓杆菌还能随温度条件的变化,改变其自身的形态,同时改变藻酸盐的产量。作为细菌生命活动过程中的另一种细胞形式,潜生体是适应某种环境条件形成的特殊类型细胞。该现象的研究,对绿脓杆菌致病过程的认识有重要意义,值得进一步探讨。
, 百拇医药
作者简介:丛延广(1973-),男,辽宁省盘锦市人,硕士,助教,主要从事细菌潜生体变化及其致病性方面的研究,发表论文5篇。电话:(023)68752190
丛延广(第三军医大学生物波研究中心,重庆 400038)
刘俊康(第三军医大学生物波研究中心,重庆 400038)
袁泽涛(第三军医大学生物波研究中心,重庆 400038)
邓国宏(第三军医大学生物波研究中心,重庆 400038)
徐启旺(第三军医大学生物波研究中心,重庆 400038)
参考文献:
[1] Jensen R H, Woolfolk C A. Formation of filaments by Pseudomonas putida[J]. Appl Environ Microbiol,1985,50(2):364-372.
, 百拇医药
[2] 邓国宏,高强国,王 源,等.绿脓杆菌水中生存的非周期性变化观察[J].第三军医大学学报,1997,19(3):197-199.
[3] 陆森泉,尹 秀,褚佩英.绿脓杆菌胞外粘液多糖的实验研究[J].中国人兽共患病杂志,1996,12(5):9-11.
[4] Simpson D A, Ramphal R, Lory S. Genetic analysis of Pseudomonas aeruginosa adherence: distinct genetic loci control attachment to epithelial cells and mucins[J]. Infect Immun,1992,60(9):3 771-3 780.
[5] Falkinham Ⅲ J O, Hoffman P S. Unique developmental charcteristics of the swarm and short cells of Proteus vulgaris and Proteus mirabilis[J]. J Bcteriol,1984,158(3):1 037-1 040.
, 百拇医药
[6] Hata J S, Fick R B. Airway adherence of Pseudomonas aeruginosa: mucoexopolysaccharide binding to human and bovine airway proteins[J]. J Lab Clin Med,1991,117(5):410-422.
[7] McCoy W F, Bryers J D, Robbins J, et al. Observations of fouling biofilm formation[J]. Can J Microbiol,1981,27(9):910-917.
[8] Khardori N, Yassien M. Biofilms in device-related infections[J]. J Ind Microbiol,1995,15(3):141-147.
, 百拇医药
[9] Baynham P J, Brown A L, Hall L L, et al. Pseudomonas aeruginosa AlgZ, a ribbon-helix-helixDNA-binding protein, is essential for alginate synthesis and algD transcriptional activation[J]. Mol Microbiol,1999,33(5):1 069-1 080.
[10] Gordberg J B , Ohman D E. Cloning and expression in Pseudomonas aeruginosa of a gene involved in the prodution of alginate[J]. J bacteriol,1984,158(3):1 115-1 121.
[11] Alm R A, Mattick J S. Genes involved in the biogenesis and function of type-4 fimbriae in Pseudomonas aeruginosa[J]. Gene,1997,192(1):89-98., http://www.100md.com
丛延广 刘俊康 袁泽涛 邓国宏 徐启旺
摘 要: 目的 探讨不同形态绿脓杆菌胞外粘多糖的含量及其对体外培养的肺癌细胞粘附能力的影响。方法 在分离一株形态对培养温度敏感的绿脓杆菌基础上,提取潜生体与繁殖体的胞外粘液多糖,以干重比评价二者粘液多糖的含量;并测定其对体外培养细胞粘附的影响。结果 潜生体胞外粘液多糖含量显著增加(P<0.01),同时其对体外培养细胞的粘附率也显著提高(P<0.01)。结论 绿脓杆菌繁殖体转变为潜生体后,其胞外粘液多糖含量及其粘附能力均有显著性提高。对绿脓杆菌潜生体的研究有助于对绿脓杆菌致病性的深入认识。
关键词:绿脓杆菌;潜生体;繁殖体
, 百拇医药
细菌在其不同生长阶段具有多形性特点,比较特殊的是纤丝状形态变化。细菌形成纤丝状菌体可由多种因素导致,Jensen等[1]认为纤丝体是由于细菌受外界环境的影响不能正常分裂而形成的,是细菌对自然环境某些条件的适应性变化。本实验室在生物波理论的研究过程中,根据变形杆菌纤丝状菌体在原条件下无明显增殖,代谢缓慢,具有多个核质,能在适当条件下断裂形成多个繁殖体等特点,称其为潜生体(Cryptic growth cell,CGC)[2]。
本实验在分离得到1株对培养温度敏感的绿脓杆菌基础上,对绿脓杆菌潜生体与繁殖体胞外粘液多糖的含量及其粘附能力进行了比较,以深入认识绿脓杆菌潜生体与致病性有关的生物学性质。
1 材料与方法
1.1 绿脓杆菌菌株 本室分离,血清8型,该菌的形态具有温度敏感性,即在37°C培养时细菌呈短杆状即繁殖体,而在低于25°C培养时呈纤丝状即潜生体。
, 百拇医药
1.2 绿脓杆菌选择鉴定培养基(DPA)
主要配方为蛋白胨20 g/L,硫酸钾10 g/L,氯化钾1.4 g/L,甘油9g/L,toween-20 20 g/L,硫酸铁0.05 g/L,琼脂15 g/L。
1.3 肺巨细胞癌细胞株(PG细胞)
北京医科大学建株,引自重庆医科大学病生教研室,以标准方法传代。
1.4 细菌培养及定量方法
将菌苔点种于DPA平板上,于25°C培养过夜即获得潜生体,于37°C培养过夜即获得繁殖体,以生理盐水稀释成细菌悬液。经十倍系列稀释后,进行菌落记数,以获得菌悬液的数量浓度。
1.5 胞外粘液多糖的分离及测定
, http://www.100md.com
参考陆森泉[3]方法进行提取,最后沉淀以双蒸水溶解,在4°C双蒸水中透析。取透析后剩下的物质加入已称好的称量瓶中,于100°C烤箱中烤至恒重,将前后称量的结果相减即得到粘液多糖的干重。同时分别称量潜生体和繁殖体干重,以粘液多糖与潜生体及繁殖体的干重比评价二者胞外粘液多糖的产量。
1.6 粘附实验
参考Simpson[4]的方法进行,记数30个细胞粘附的细菌数,计算粘附率(cfu/cell)。
1.7 数据处理
采用EZSTAT2统计软件处理数据。
2 结果
2.1 绿脓杆菌潜生体与繁殖体形态
, 百拇医药
见图1、2。
2.2 胞外粘液多糖含量测定结果
结果见表1。
2.3 潜生体与繁殖体对体外培养的PG细胞粘附实验结果
结果见表2。

图1 绿脓杆菌潜生体形态 (革兰氏染色×1 000)
Fig 1 Morphology of cryptic growth cells withGram stain (×1 000)

, 百拇医药
图2 绿脓杆菌繁殖体形态 (革兰氏染色×1 000)
Fig 2 Morphology of vegetative cells withGram stain (×1 000)
表1 潜生体与繁殖体胞外粘液多糖含量测定结果(X±s)
Tab 1 The mucoexopolysaccharide(MEPS) content ofvegetative cell and cryptic growth cell(X±s)
Growth forms
Content of MEPS(mg/mg cell)
Vegetative cell
, http://www.100md.com
0.084±0.002
Cryptic growth cell
0.514±0.060*
*:P<0.01 vs vegetative cell group
表2 潜生体与繁殖体对体外培养的PG细胞粘附率比较(X±s)
Tab 2 The adhesion rate of vegetative cell and cryptic growth cell to cultured lung cancer cells in vitro(X±s)
Growth forms
The adherence rate(cfu/cell)
, http://www.100md.com
Vegetative cell
3.78±0.544
Cryptic growth cell
12.6 ±2.10*
*:P<0.01 vs vegetative cell group
结果表明该绿脓杆菌潜生体多聚集在一起粘附于细胞表面,使粘附率显著提高,见图3。而繁殖体多以单个细菌散在地粘附于细胞上,粘附率较低,见图4。

图3 绿脓杆菌潜生体对体外培养的PG细胞的粘附 (瑞氏染色×1 000)
, http://www.100md.com
Fig 3 Adhesion of cryptic growth cells to PG cells in vitro (Wright stain×1 000)

图4 绿脓杆菌繁殖体对体外培养的PG细胞的粘附 (瑞氏染色×1 000)
Fig 4 Adhesion of vegetative cells to PG cells in vitro (Wright stain×1 000)
3 讨论
细菌在生长过程中表现多形性,如得到广泛研究的变形杆菌迁徙生长现象中的丝状体[5]。多种因素可导致潜生体的形成,其长度可以是一般菌体的几倍乃至几十倍。绿脓杆菌潜生体的研究较少,一个重要原因是难以获得潜生体稳定的纯培养。而作为一个临床上重要的机会致病菌,绿脓杆菌潜生体的研究显得更有意义。
, http://www.100md.com
本研究在分离得到一株形态对培养温度敏感的绿脓杆菌基础上,实验发现潜生体胞外粘液多糖的含量显著高于繁殖体。粘液多糖具有多种重要的生物学性质,如抵抗吞噬细胞的吞噬和抗菌药物的损伤作用,也是细菌的粘附因子之一,粘液多糖的增多会对潜生体有关的生物学性质产生重要影响。
粘液型绿脓杆菌在组织表面的粘附主要受胞外粘液多糖的影响(非粘液型则主要受菌毛的控制)。Hata等[6]对绿脓杆菌感染的呼吸道表面的扫描电镜观察显示,非粘液型绿脓杆菌多以单个菌体粘附在细胞表面,粘液型绿脓杆菌则主要以微菌落群的形式粘附。因此,粘液型菌株的粘附能力显著高于非粘液型菌株。这个结论与本实验结果可以相互应证,即产生大量粘液多糖的潜生体对PG细胞的粘附率显著高于繁殖体。粘液多糖对潜生体粘附能力的提高起到非常重要的作用,同时潜生体较大的个体也是重要的因素之一,因为个体较大,与细胞的接触面积增大,相互作用的机率也显著提高,从而有利于它粘附在细胞表面,也有利于相互聚集在一起。绿脓杆菌粘液多糖主要成分是藻酸盐,由D-甘露糖醛酸,L-古洛糖醛酸组成,多聚物中较多的羟基和羧基能促进细菌间的聚集。由粘附照片也可以看出,繁殖体散在地粘附于PG细胞表面,而潜生体则聚集在一起粘附于细胞表面,这就显著增加了细菌粘附的数量和质量。聚集在一起的菌体构成稳定的群体结构,这种群体结构的适应能力明显提高,能抵抗不利因素的影响。McCoy等[7]研究表明,表面生长的细菌在其生物膜的形成过程中,伴随着潜生体的大量产生,这些潜生体使生物膜构成一个立体的交叉网络结构,使其在表面的存在更牢固。生物膜在细菌致病过程中起到非常重要的作用[8]。
, 百拇医药
藻酸盐不仅仅是绿脓杆菌重要的毒力因子,更广泛地应用于食品、制药及化工等领域。因此,有关藻酸盐合成的分子生物学及生物化学研究引起人们极大的兴趣[9]。多种环境因素能影响藻酸盐的生成,有文献报道某些绿脓杆菌藻酸盐的产生受到温度的影响,文章认为是由于生成藻酸盐的酶类或调控多肽的最适温度发生了漂移[10]。潜生体的形成涉及多基因多产物,是一个复杂过程,在此过程中,也可能产生藻酸盐的基因或其表达同时发生变化,导致细菌藻酸盐的产生量发生改变。对于本株绿脓杆菌藻酸盐的增减,究竟是环境温度直接或间接作用,抑或与形态改变有关尚不清楚。但迄今无文献报道绿脓杆菌在藻酸盐产生改变的同时,有形态上的变化,说明本实验发现的是一个独特现象。
Alm[11]认为绿脓杆菌能根据宿主环境的变化,调控它两个重要的毒力因子――4型菌毛和藻酸盐的表达。本实验结果表明,部分绿脓杆菌还能随温度条件的变化,改变其自身的形态,同时改变藻酸盐的产量。作为细菌生命活动过程中的另一种细胞形式,潜生体是适应某种环境条件形成的特殊类型细胞。该现象的研究,对绿脓杆菌致病过程的认识有重要意义,值得进一步探讨。
, 百拇医药
作者简介:丛延广(1973-),男,辽宁省盘锦市人,硕士,助教,主要从事细菌潜生体变化及其致病性方面的研究,发表论文5篇。电话:(023)68752190
丛延广(第三军医大学生物波研究中心,重庆 400038)
刘俊康(第三军医大学生物波研究中心,重庆 400038)
袁泽涛(第三军医大学生物波研究中心,重庆 400038)
邓国宏(第三军医大学生物波研究中心,重庆 400038)
徐启旺(第三军医大学生物波研究中心,重庆 400038)
参考文献:
[1] Jensen R H, Woolfolk C A. Formation of filaments by Pseudomonas putida[J]. Appl Environ Microbiol,1985,50(2):364-372.
, 百拇医药
[2] 邓国宏,高强国,王 源,等.绿脓杆菌水中生存的非周期性变化观察[J].第三军医大学学报,1997,19(3):197-199.
[3] 陆森泉,尹 秀,褚佩英.绿脓杆菌胞外粘液多糖的实验研究[J].中国人兽共患病杂志,1996,12(5):9-11.
[4] Simpson D A, Ramphal R, Lory S. Genetic analysis of Pseudomonas aeruginosa adherence: distinct genetic loci control attachment to epithelial cells and mucins[J]. Infect Immun,1992,60(9):3 771-3 780.
[5] Falkinham Ⅲ J O, Hoffman P S. Unique developmental charcteristics of the swarm and short cells of Proteus vulgaris and Proteus mirabilis[J]. J Bcteriol,1984,158(3):1 037-1 040.
, 百拇医药
[6] Hata J S, Fick R B. Airway adherence of Pseudomonas aeruginosa: mucoexopolysaccharide binding to human and bovine airway proteins[J]. J Lab Clin Med,1991,117(5):410-422.
[7] McCoy W F, Bryers J D, Robbins J, et al. Observations of fouling biofilm formation[J]. Can J Microbiol,1981,27(9):910-917.
[8] Khardori N, Yassien M. Biofilms in device-related infections[J]. J Ind Microbiol,1995,15(3):141-147.
, 百拇医药
[9] Baynham P J, Brown A L, Hall L L, et al. Pseudomonas aeruginosa AlgZ, a ribbon-helix-helixDNA-binding protein, is essential for alginate synthesis and algD transcriptional activation[J]. Mol Microbiol,1999,33(5):1 069-1 080.
[10] Gordberg J B , Ohman D E. Cloning and expression in Pseudomonas aeruginosa of a gene involved in the prodution of alginate[J]. J bacteriol,1984,158(3):1 115-1 121.
[11] Alm R A, Mattick J S. Genes involved in the biogenesis and function of type-4 fimbriae in Pseudomonas aeruginosa[J]. Gene,1997,192(1):89-98., http://www.100md.com