重组人粒细胞集落刺激因子在小儿急性白血病治疗中的应用
作者:夏焱 方建培 薛红漫 陈纯 钟凤仪 李文益
单位:中山医科大学孙逸仙纪念医院儿科 510120
关键词:粒细胞集落刺激因子;急性白血病;化疗
广东医学001102 【摘要】 目的 观察分析重组人粒细胞集落刺激因子(rhG-CSF)对小儿急性白血病化疗后粒细胞减少症的治疗效果和对感染的防治效果。方法 对急性白血病患儿,以化疗后外周血白细胞(WBC)<1.0×109/L和(或)中性粒细胞绝对值(ANC)<0.5×109/L为标准,分为接受rhG-CSF治疗的治疗组(110例次)和对照组(29例次),比较两组间粒细胞恢复的程度和时间,以及感染发生率的差异。结果 rhG-CSF治疗化疗后粒细胞减少症,有效率达95.5%,治疗组外周血WBC及ANC恢复的数值和时间明显优于对照组(P<0.05),且感染的发生率明显低于对照组(P<0.05)。结论 rhG-CSF可明显缩短化疗后粒细胞减少的持续时间,对感染有重要的防治作用,化疗后WBC低下时应及时应用rhG-CSF。
, 百拇医药
近年来,随着联合强化疗的应用,小儿急性白血病的缓解率及长期存活率已有明显的提高。大剂量强化疗导致骨髓抑制是白血病根治的必经阶段,但在提高疗效的同时也带来了治疗的严重副作用。由于患儿处于骨髓抑制期,粒细胞减少或缺乏,极易合并严重的甚至是致死性的感染,这是造成患儿早期死亡的重要原因。因此,如何克服粒细胞减少是一个令人关注的问题。随着重组人粒细胞集落刺激因子(rhG-CSF)的临床应用,普遍认为它可以帮助化疗后粒细胞减少症的恢复,现将我科近年的应用效果报道如下。
1 资料与方法
1.1 一般资料 治疗组:1996~1999年在我科确诊并接受化疗的急性白血病患儿44例,年龄1岁1个月至13岁,其中急性淋巴细胞性白血病(ALL)39例,急性非淋巴细胞性白血病(ANLL)5例,共接受rhG-CSF治疗110例次。对照组:同期急性白血病患儿17例,未接受rhG-CSF治疗,年龄2岁1个月至12岁,其中ALL 15例,ANLL 2例 ,共29例次。rhG-CSF治疗前两组患儿外周血白细胞(WBC)<1.0×109/L和(或)中性粒细胞绝对值(ANC)<0.5×109/L,两组差异无统计学意义(P>0.05)。
, 百拇医药
1.2 药品 吉粒芬(国产)75 μg/支,惠尔血(进口)75 μg/支或150 μg/支,格拉诺赛特(进口),75 μg/支或250 μg/支。
1.3 rhG-CSF的用法 化疗后连续2 d外周血WBC<1.0×109/L和(或)ANC<0.5×109/L,则开始予rhG-CSF治疗,4~6 μg/(kg.d)皮下注射,至WBC>3.0×109/L和(或)ANC>1.5×109/L,3~7 d为一疗程,个别病例因骨髓抑制严重,加大剂量至10 μg/(kg.d),延长治疗时间为10~12 d,治疗组同时予常规支持治疗,而对照组则仅予常规支持治疗。常规支持治疗包括入层流床或隔离病房,予肠道口服抗生素,输注静脉用丙种球蛋白及成份输血等。
1.4 观察指标 每日或隔日查血常规计算中性粒细胞绝对值,rhG-CSF治疗期间查肝肾功能,部分病例查心电图,以观察rhG-CSF治疗的副作用。
, 百拇医药
1.5 化疗方案 急淋方案:采用新华88方案及全国协作组方案。急非淋方案:采用HAD、HOP、DA、HDArc-C方案。
1.6 统计学方法 分组比较配对资料t检验及χ2检验。
2 结果
2.1 用rhG-CSF治疗对白细胞的作用 以治疗后2周外周血WBC达到4.0×109/L或WBC从低于1.0×109/L升至4.0×109/L以上为有效,结果有效105例次,无效5例次,有效率达95.5%。用药后外周血WBC较用药前明显升高(见表1),差异有统计学意义(P<0.05),且治疗组外周血WBC及ANC恢复的数值和时间(见表1、表2)明显优于对照组(P<0.05)。WBC恢复时间最短2 d,停药后部分病例WBC有不同程度下降,但均在4.0×109/L以上,个别病例WBC>10.0×109/L,但是未发现幼稚细胞。
, 百拇医药
表1 rhG-CSF治疗急性白血病化疗后粒细胞
减少症WBC及ANC的变化(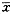 ±s)×109/L
±s)×109/L
治疗组(105例次)
对照组(29例次)
WBC
?ANC
WBC
?ANC
用药前
1.05±0.44
, http://www.100md.com
0.24±0.12
1.03±0.54
0.26±0.14
用药后
2 d
2.05±0.48
0.48±0.25
1.27±0.78
0.28±0.19
4 d
3.37±1.25*
1.60±0.82*
, http://www.100md.com
1.91±1.05#
0.37±0.24#
6 d
4.10±2.34*
2.27±1.12*
2.19±1.77#
0.71±0.52#
10 d
5.61±3.81*
2.87±1.68*
, 百拇医药
3.26±2.62#
1.10±0.86#
15 d
5.78±3.12*
3.20±2.63*
3.89±2.1#
2.01±1.12#
治疗组中同用药前比 *P<0.05, 治疗组与对照组比 #P<0.05
2.2 用rhG-CSF治疗 治疗组感染率明显降低,与对照组相比,差异有统计学意义(P<0.05)(见表2),感染的类型按发生率高低依次为:原因不明的发热、上呼吸道感染、口腔炎、支气管肺炎、泌尿系感染、小儿肠炎及败血症,两组的感染类型无明显差异。
, http://www.100md.com
2.3 rhG-CSF治疗对血小板和血红蛋白的影响 治疗组中血小板(PLT)和血红蛋白(Hb)数值的恢复与WBC数的升高无明显相关,两组中输注血小板或浓缩红细胞的次数的差异无统计学意义(P>0.05)(见表2)。
表2 rhG-CSF对患儿白细胞恢复、感染及输血影响的比较
例次数
WBC<1.0×109/L
的天数
感染的发生率
(%)
输注血小板或浓
缩红细胞的次数
, 百拇医药
治疗组
105
3.3±2.1
47.6(50/105)
2.3±1.1
对照组
29
7.5±3.1
86.2(25/29)
2.1±1.2
P值
<0.05
, http://www.100md.com <0.05
>0.05
2.4 国产制剂与进口制剂效果的比较 国产制剂吉粒芬与进口制剂惠尔血、格拉诺赛特的用量和用法相同,国产组与进口组用药前后外周血WBC数变化的差异无统计学意义(P>0.05),有效率相似。表3 国产组与进口组用药前后外周血
WBC数的变化(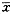 ±s)×109/L
±s)×109/L
例次数
用药前
用药后(6 d)
有效率(%)
国产组
, http://www.100md.com
38
1.07±0.49
4.11±0.88
94.7(2/38)
进口组
67
1.12±0.37
4.68±1.03
95.5(3/67)
P值
>0.05
>0.05
, 百拇医药
>0.05
2.5 副作用 治疗组2例患儿用药后出现发热,体温37~38℃,持续1~2 d;2例出现双下肢疼痛,持续1 d;1例出现双下肢斑丘疹,持续3 d,未发现与rhG-CSF相关的肝肾功能异常。3 讨论
急性白血病联合强化疗后常常导致骨髓抑制,中性粒细胞减少,使患儿极易合并严重的感染而导致治疗的失败或是延迟规则的化疗。rhG-CSF能促进造血干、祖细胞向中性粒细胞分化和增殖,促进成熟的粒细胞向外周血释放,加强粒细胞的趋化、吞噬功能[1],可缩短化疗后的骨髓抑制期,降低感染率,提高患儿对化疗的耐受性,保证强化疗的顺利实施,从而提高白血病的治愈率及长期存活率[2]。
本组观察结果显示,使用rhG-CSF治疗化疗后粒细胞减少症,取得较好疗效,有效率达95.5%,治疗组外周血WBC及ANC恢复的数值和时间明显优于对照组(P<0.05),说明rhG-CSF可明显缩短化疗后粒细胞减少的持续时间,与国外报道相符[3];并且治疗组感染的发生率明显低于对照组(P<0.05),说明rhG-CSF的应用对感染有重要的防治作用。因此,化疗后WBC低下时应及时使用rhG-CSF,可减少感染的发生率,减轻感染的严重程度,降低死亡率,减少住院天数及总的治疗费用,并为下一疗程的及时实施和规则化疗提供条件。
, http://www.100md.com
G-CSF主要作用于粒系干、祖细胞,对血小板及血红蛋白的恢复没有影响[1],在治疗组中我们观察到PLT和HB数值的恢复与WBC数的升高无明显相关,两组中输注血小板或浓缩红细胞的次数的差异无统计学意义(P>0.05),这与有关文献报道在使用rhG-CSF时可见到血小板迅速恢复、可减少输血量的结果不同[4,5];还有待进一步研究。
急性白血病应用rhG-CSF是否会促进白血病细胞的增殖是一个令人关注的问题,目前还存在不同意见,特别是在ANLL的治疗方面。有文献报道体外实验证明G-CSF有刺激髓性白血病细胞增殖的作用,并有抑制细胞程序性死亡、导致白血病细胞的持续存活以及对化疗药物产生抗性[6,7];但也报道认为G-CSF不促进白血病细胞的增殖,并可使白血病细胞进入S期,提高化疗的敏感性[3],近期报道多认为在AML的患者中使用rhG-CSF是安全的,与复发无明显相关,还可作为逆转白血病耐药的手段之一来提高缓解率[4]。本研究追踪观察使用过rhG-CSF的39例ALL患儿,复发率与对照组无明显差异;治疗组中5例AML患儿,1例复发(M1),1例耐药(M2),而对照组2例中有1例复发(M5)。因病例数太少,很难判断复发与使用rhG-CSF是否相关。
, 百拇医药
总之,rhG-CSF能有效地促进化疗后粒细胞的恢复,降低感染率且毒副作用少,总的治疗费用降低,使规则化疗能够顺利完成,是急性白血病联合绐化疗的重要辅助治疗手段。
参考文献
1,Lord BI, Bronchud MH, Owens S, et al. The kinetics of humangranulopoiesis following treatment with granulocyte colony-stimulating facotr in vivo. Proc Natl Acad Sci USA, 1989, 86: 9499
2,Chen SH, Liang DC, Liu HC. High-dose cytrabine-containing chemotherapy with or without granulocyte colony-stimulating facotr for children with acute leukemia. Am J Hematol, 1998, 58:20
, 百拇医药
3,Ohno R, Tomoraga M, Kobayashi T, et al. Effect of granulocyte colony-stimulating factor after intensive induction therapy in relapsed or refractory acute leukemia. N Engl J Med, 1990, 323: 871
4,陆爱东,殷慧君,张乐萍.粒细胞集落刺激因子在儿童急性髓性白血病治疗中的应用.临床儿科杂志,1998,16(5):296
5,卢元,庞秀英,佟琳茹,等.G-CSF在白血病骨髓抑制期的应用.中国小儿血液,1998,3(4):156
6,Terpstra W, Lowenberg B. Application of myeloid growth factors in the treatment of acute myeloid leukemia. Leukemia, 1997, 11:315
7,Loten J. Hematopoietic cytokines in hibitor apoptosis induced by transforming growth factor B-1 and caner chemotherapy compounds in myeloid leukemic cell. Blood, 1992, 80: 1750
(收稿日期:2000-08-22), 百拇医药
单位:中山医科大学孙逸仙纪念医院儿科 510120
关键词:粒细胞集落刺激因子;急性白血病;化疗
广东医学001102 【摘要】 目的 观察分析重组人粒细胞集落刺激因子(rhG-CSF)对小儿急性白血病化疗后粒细胞减少症的治疗效果和对感染的防治效果。方法 对急性白血病患儿,以化疗后外周血白细胞(WBC)<1.0×109/L和(或)中性粒细胞绝对值(ANC)<0.5×109/L为标准,分为接受rhG-CSF治疗的治疗组(110例次)和对照组(29例次),比较两组间粒细胞恢复的程度和时间,以及感染发生率的差异。结果 rhG-CSF治疗化疗后粒细胞减少症,有效率达95.5%,治疗组外周血WBC及ANC恢复的数值和时间明显优于对照组(P<0.05),且感染的发生率明显低于对照组(P<0.05)。结论 rhG-CSF可明显缩短化疗后粒细胞减少的持续时间,对感染有重要的防治作用,化疗后WBC低下时应及时应用rhG-CSF。
, 百拇医药
近年来,随着联合强化疗的应用,小儿急性白血病的缓解率及长期存活率已有明显的提高。大剂量强化疗导致骨髓抑制是白血病根治的必经阶段,但在提高疗效的同时也带来了治疗的严重副作用。由于患儿处于骨髓抑制期,粒细胞减少或缺乏,极易合并严重的甚至是致死性的感染,这是造成患儿早期死亡的重要原因。因此,如何克服粒细胞减少是一个令人关注的问题。随着重组人粒细胞集落刺激因子(rhG-CSF)的临床应用,普遍认为它可以帮助化疗后粒细胞减少症的恢复,现将我科近年的应用效果报道如下。
1 资料与方法
1.1 一般资料 治疗组:1996~1999年在我科确诊并接受化疗的急性白血病患儿44例,年龄1岁1个月至13岁,其中急性淋巴细胞性白血病(ALL)39例,急性非淋巴细胞性白血病(ANLL)5例,共接受rhG-CSF治疗110例次。对照组:同期急性白血病患儿17例,未接受rhG-CSF治疗,年龄2岁1个月至12岁,其中ALL 15例,ANLL 2例 ,共29例次。rhG-CSF治疗前两组患儿外周血白细胞(WBC)<1.0×109/L和(或)中性粒细胞绝对值(ANC)<0.5×109/L,两组差异无统计学意义(P>0.05)。
, 百拇医药
1.2 药品 吉粒芬(国产)75 μg/支,惠尔血(进口)75 μg/支或150 μg/支,格拉诺赛特(进口),75 μg/支或250 μg/支。
1.3 rhG-CSF的用法 化疗后连续2 d外周血WBC<1.0×109/L和(或)ANC<0.5×109/L,则开始予rhG-CSF治疗,4~6 μg/(kg.d)皮下注射,至WBC>3.0×109/L和(或)ANC>1.5×109/L,3~7 d为一疗程,个别病例因骨髓抑制严重,加大剂量至10 μg/(kg.d),延长治疗时间为10~12 d,治疗组同时予常规支持治疗,而对照组则仅予常规支持治疗。常规支持治疗包括入层流床或隔离病房,予肠道口服抗生素,输注静脉用丙种球蛋白及成份输血等。
1.4 观察指标 每日或隔日查血常规计算中性粒细胞绝对值,rhG-CSF治疗期间查肝肾功能,部分病例查心电图,以观察rhG-CSF治疗的副作用。
, 百拇医药
1.5 化疗方案 急淋方案:采用新华88方案及全国协作组方案。急非淋方案:采用HAD、HOP、DA、HDArc-C方案。
1.6 统计学方法 分组比较配对资料t检验及χ2检验。
2 结果
2.1 用rhG-CSF治疗对白细胞的作用 以治疗后2周外周血WBC达到4.0×109/L或WBC从低于1.0×109/L升至4.0×109/L以上为有效,结果有效105例次,无效5例次,有效率达95.5%。用药后外周血WBC较用药前明显升高(见表1),差异有统计学意义(P<0.05),且治疗组外周血WBC及ANC恢复的数值和时间(见表1、表2)明显优于对照组(P<0.05)。WBC恢复时间最短2 d,停药后部分病例WBC有不同程度下降,但均在4.0×109/L以上,个别病例WBC>10.0×109/L,但是未发现幼稚细胞。
, 百拇医药
表1 rhG-CSF治疗急性白血病化疗后粒细胞
减少症WBC及ANC的变化(
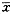 ±s)×109/L
±s)×109/L治疗组(105例次)
对照组(29例次)
WBC
?ANC
WBC
?ANC
用药前
1.05±0.44
, http://www.100md.com
0.24±0.12
1.03±0.54
0.26±0.14
用药后
2 d
2.05±0.48
0.48±0.25
1.27±0.78
0.28±0.19
4 d
3.37±1.25*
1.60±0.82*
, http://www.100md.com
1.91±1.05#
0.37±0.24#
6 d
4.10±2.34*
2.27±1.12*
2.19±1.77#
0.71±0.52#
10 d
5.61±3.81*
2.87±1.68*
, 百拇医药
3.26±2.62#
1.10±0.86#
15 d
5.78±3.12*
3.20±2.63*
3.89±2.1#
2.01±1.12#
治疗组中同用药前比 *P<0.05, 治疗组与对照组比 #P<0.05
2.2 用rhG-CSF治疗 治疗组感染率明显降低,与对照组相比,差异有统计学意义(P<0.05)(见表2),感染的类型按发生率高低依次为:原因不明的发热、上呼吸道感染、口腔炎、支气管肺炎、泌尿系感染、小儿肠炎及败血症,两组的感染类型无明显差异。
, http://www.100md.com
2.3 rhG-CSF治疗对血小板和血红蛋白的影响 治疗组中血小板(PLT)和血红蛋白(Hb)数值的恢复与WBC数的升高无明显相关,两组中输注血小板或浓缩红细胞的次数的差异无统计学意义(P>0.05)(见表2)。
表2 rhG-CSF对患儿白细胞恢复、感染及输血影响的比较
例次数
WBC<1.0×109/L
的天数
感染的发生率
(%)
输注血小板或浓
缩红细胞的次数
, 百拇医药
治疗组
105
3.3±2.1
47.6(50/105)
2.3±1.1
对照组
29
7.5±3.1
86.2(25/29)
2.1±1.2
P值
<0.05
, http://www.100md.com <0.05
>0.05
2.4 国产制剂与进口制剂效果的比较 国产制剂吉粒芬与进口制剂惠尔血、格拉诺赛特的用量和用法相同,国产组与进口组用药前后外周血WBC数变化的差异无统计学意义(P>0.05),有效率相似。表3 国产组与进口组用药前后外周血
WBC数的变化(
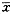 ±s)×109/L
±s)×109/L例次数
用药前
用药后(6 d)
有效率(%)
国产组
, http://www.100md.com
38
1.07±0.49
4.11±0.88
94.7(2/38)
进口组
67
1.12±0.37
4.68±1.03
95.5(3/67)
P值
>0.05
>0.05
, 百拇医药
>0.05
2.5 副作用 治疗组2例患儿用药后出现发热,体温37~38℃,持续1~2 d;2例出现双下肢疼痛,持续1 d;1例出现双下肢斑丘疹,持续3 d,未发现与rhG-CSF相关的肝肾功能异常。3 讨论
急性白血病联合强化疗后常常导致骨髓抑制,中性粒细胞减少,使患儿极易合并严重的感染而导致治疗的失败或是延迟规则的化疗。rhG-CSF能促进造血干、祖细胞向中性粒细胞分化和增殖,促进成熟的粒细胞向外周血释放,加强粒细胞的趋化、吞噬功能[1],可缩短化疗后的骨髓抑制期,降低感染率,提高患儿对化疗的耐受性,保证强化疗的顺利实施,从而提高白血病的治愈率及长期存活率[2]。
本组观察结果显示,使用rhG-CSF治疗化疗后粒细胞减少症,取得较好疗效,有效率达95.5%,治疗组外周血WBC及ANC恢复的数值和时间明显优于对照组(P<0.05),说明rhG-CSF可明显缩短化疗后粒细胞减少的持续时间,与国外报道相符[3];并且治疗组感染的发生率明显低于对照组(P<0.05),说明rhG-CSF的应用对感染有重要的防治作用。因此,化疗后WBC低下时应及时使用rhG-CSF,可减少感染的发生率,减轻感染的严重程度,降低死亡率,减少住院天数及总的治疗费用,并为下一疗程的及时实施和规则化疗提供条件。
, http://www.100md.com
G-CSF主要作用于粒系干、祖细胞,对血小板及血红蛋白的恢复没有影响[1],在治疗组中我们观察到PLT和HB数值的恢复与WBC数的升高无明显相关,两组中输注血小板或浓缩红细胞的次数的差异无统计学意义(P>0.05),这与有关文献报道在使用rhG-CSF时可见到血小板迅速恢复、可减少输血量的结果不同[4,5];还有待进一步研究。
急性白血病应用rhG-CSF是否会促进白血病细胞的增殖是一个令人关注的问题,目前还存在不同意见,特别是在ANLL的治疗方面。有文献报道体外实验证明G-CSF有刺激髓性白血病细胞增殖的作用,并有抑制细胞程序性死亡、导致白血病细胞的持续存活以及对化疗药物产生抗性[6,7];但也报道认为G-CSF不促进白血病细胞的增殖,并可使白血病细胞进入S期,提高化疗的敏感性[3],近期报道多认为在AML的患者中使用rhG-CSF是安全的,与复发无明显相关,还可作为逆转白血病耐药的手段之一来提高缓解率[4]。本研究追踪观察使用过rhG-CSF的39例ALL患儿,复发率与对照组无明显差异;治疗组中5例AML患儿,1例复发(M1),1例耐药(M2),而对照组2例中有1例复发(M5)。因病例数太少,很难判断复发与使用rhG-CSF是否相关。
, 百拇医药
总之,rhG-CSF能有效地促进化疗后粒细胞的恢复,降低感染率且毒副作用少,总的治疗费用降低,使规则化疗能够顺利完成,是急性白血病联合绐化疗的重要辅助治疗手段。
参考文献
1,Lord BI, Bronchud MH, Owens S, et al. The kinetics of humangranulopoiesis following treatment with granulocyte colony-stimulating facotr in vivo. Proc Natl Acad Sci USA, 1989, 86: 9499
2,Chen SH, Liang DC, Liu HC. High-dose cytrabine-containing chemotherapy with or without granulocyte colony-stimulating facotr for children with acute leukemia. Am J Hematol, 1998, 58:20
, 百拇医药
3,Ohno R, Tomoraga M, Kobayashi T, et al. Effect of granulocyte colony-stimulating factor after intensive induction therapy in relapsed or refractory acute leukemia. N Engl J Med, 1990, 323: 871
4,陆爱东,殷慧君,张乐萍.粒细胞集落刺激因子在儿童急性髓性白血病治疗中的应用.临床儿科杂志,1998,16(5):296
5,卢元,庞秀英,佟琳茹,等.G-CSF在白血病骨髓抑制期的应用.中国小儿血液,1998,3(4):156
6,Terpstra W, Lowenberg B. Application of myeloid growth factors in the treatment of acute myeloid leukemia. Leukemia, 1997, 11:315
7,Loten J. Hematopoietic cytokines in hibitor apoptosis induced by transforming growth factor B-1 and caner chemotherapy compounds in myeloid leukemic cell. Blood, 1992, 80: 1750
(收稿日期:2000-08-22), 百拇医药