Ⅱ型糖尿病合并高血压患者氧化损伤及抗氧化酶活性的研究
作者:刘和俊,汪太平,李芹,史学功
单位:安徽医科大学附属医院心内科 230022
关键词:非胰岛素依赖型糖尿病;高血压;氧化损伤
高血压杂志990312
目的:评价氧化损伤及抗氧化酶活性对Ⅱ型糖尿病(NIDDM)及其伴发高血压(HT)的影响。方法与结果:采用鲁米诺依赖的中性粒细胞化学发光法,对136例NIDDM患者(其中 70例不伴有HT,66例伴有HT)及30例年龄匹配的健康对照者,检测其外周血中性粒细胞产生氧自由基(OFR)的水平。采用化学定量法,测定其血浆脂质过氧化终末产物-丙二醛(MDA)的浓度及抗氧化酶-超氧化物歧化酶(SOD)、谷胱甘肽过氧化物酶(GSHPx)的活性。NIDDM伴发HT组,其PMN-CL 峰值、积分和吞噬指数均明显高于NIDDM不伴HT组及健康对照组;血浆MDA浓度较后两组也明显升高(P均<0.01); NIDDM组及NIDDM伴发HT组的血浆SOD和GSHPx活性较正常对照组均明显降低(P均<0.01);但与NIDDM组相比,NIDDM伴发HT组的血浆SOD和GSHPx活性其差异无显著性(P均>0.05);PMN-CL峰值与MDA呈明显正相关(r=0.7486,Y=159.8X+132.2,P<0.01,n=66),与SOD活性呈明显负相关(r=-0.6471,Y=-2.6X+1127.4,P<0.05,n=66)。结论:NIDDM患者体内已存在着氧化损伤,而在NIDDM伴发 HT时氧化损伤进一步加重,提示氧化损伤对NIDDM患者HT的发生发展可能有着病因学意义。
, 百拇医药
要点:NIDDM及NIDDM合并高血压患者血浆MDA增加,SOD和GSHPx活性降低。多形核白细胞氧自由基产生增加,这种氧化损伤在NIDDM及其合并高血压的发生和发展上有意义。
中图分类号:R587.1;R544.1;R331.1;Q505 文献标识码:A
文章编号:1006-2866(1999)02-0228-02
Oxidative Stress Is Present in NIDDM and Further Enchaned by Hypertension
LIU Hejun,WANG Taiping,LI Qin,SHI Xungong
(Cardiovascular Department of Affiliated Hospital of Anhui Medical Univeresity,Hefei,230022)
, 百拇医药
ABSTRACT Aim:Oxidative stress is believed to play an important role in the development of hypertension associates with diabetes mellitus in animal models.To test this hypothesis in humans,we determined to evaluate the markers of polymorphonuclear leukocyte oxygen free radical( OFR)production,lipid peroxidation and defenses against oxidative stress in NIDDM patients with and without hypertension.Methods and Results:A convenient and senstive method for estimation of neutrophil OFR production was assayed by polymorphonuclear leukocyte chemiluminescence(PMN-CL).We have measured the parameters of PMN-CL,the plasma malondialdehyde(MDA) concentration,the plasma activities of superoxide dismutase(SOD) and glulathione peroxidase(GSHPx) in 136 NIDDM patients( 70 without hypertension and 66 with hypertension) and 30 age-matched healthy subjects.Patients with hypertension showed significantly increased PMN-CL parameters as peak value(974.8±357.7 mV),integration(149368±74761 mV.s) ,and phagocytic index(0.298±0.131 mV.mm-3) compared to diabetics without hypertension(572.3±106.8 mV,79038±24137 mV and 0.213±0.079 mV.mm-3 ) and healthy controls(275.9±65.2 mV,36631±9442 mV.s,and 0.078±0.045 mV.mm-3).(P<0.01,respectively).The plasma MDA concentration(4.87±0.13 nmol.ml-1) increased in patients with hypertension compared with that in diabetics without hypertension(4.18±0.21 nmol.ml-1) and healthy controls(3.42±0.29 nmol.ml-1),(P<0.01,respectively).The PMN-CL peak value correlated best with plasma MDA concentration (r=0.7486,P<0.01,n=66) and negatively correlated with the plasma activity of SOD (r=-0.6471,P<0.05,n=66).Conclusion:These data confirm that the oxidative stress was significant in NIDDM patients and was enchaned in diabetic patients with hypertension.
, http://www.100md.com
Key Words: non-insulin dependent diabetes mellitus(NIDDM); hypertension; oxidative stress
糖尿病和高血压是相互关联的疾病,是动脉硬化的独立危险因素,两病合并时会加速心血管病、脑卒中、肾病及视网膜病变的发生及进展[1]。动物实验业已表明,氧化损伤对糖尿病引发高血压起着重要作用[2,3],但在人体的研究,目前尚鲜见报道。本文采用鲁米诺(Luminol,化学名为氨基苯二酰一肼)依赖的中性粒细胞化学发光(Polymorphonuclear chemiluminescence,PMN-CL)法[4],对伴或不伴高血压(HT)的Ⅱ型糖尿病(NIDDM)患者外周血中性粒细胞产生的氧自由基( OFR)水平进行检测,采用化学定量法对血浆过氧化脂质终末产物-丙二醛(MDA) 浓度及抗氧化酶活性进行检测,旨在评价氧化损伤及抗氧化酶活性对NIDDM及其伴发HT的影响。
, 百拇医药
MATERIALS AND METHODS
1 对象
1.1 正常对照组:体检身体健康者30例,其中男性21例,女性9例,年龄55.0±9.5岁。
1.2 NIDDM组:70例,根据1990年WHO暂行标准作出诊断,其中男性49例,女性21例,年龄57.5±12.8岁。
1.3 NIDDM伴发HT组:66例,NIDDM诊断标准同上,HT诊断按1978年WHO标准,HT发生于罹患NIDDM之后,其中男性46例,女性20例,年龄59.7±14.2岁。
所有检测对象在检测前2周内均未服用自由基清除剂或抗氧化剂,并除外感染现象。
2 方法:
, 百拇医药
2.1 采血:抽取静脉血(肝素抗凝)2毫升,取 0.1 毫升用于检测中性粒细胞化学发光(PMN-CL)各参数,余下血样行2 000转/分钟离心10分钟,取出血浆用于测定MDA,SOD,GSHPx。
2.2 PMN-CL参数检测:取肝素抗凝的静脉血0.1 ml,加入0.7 ml pH值为7.8的 Hank's液中,在37℃孵育20分钟,加浓度为1×10-3mol/L的鲁米诺液(Luminol,Sigma产品)0.1 ml,再孵育15 min,上机检测本底值,加2.5 g/L酵母多糖(Zymosan A,Sigma产品)0.1 ml,每150 s测量1次,每次测量时间为6 s,共测20次。测量仪器为SHG-1型生物化学发光仪,自动温控在37±0.5℃,最后得出每例的峰值、积分。并测算出每例的吞噬指数(峰值/PMN数/103),反映单个PMN的吞噬功能。
2.3 血浆MDA,SOD,GSHPx测定:均采用化学法测定,试剂盒由南京建成试剂厂提供,按说明书进行操作。
, http://www.100md.com
3 统计学处理: 所有数据以 ±s表示,组间比较用SAS软件方差分析q检验,并用直线相关分析判定有关指标间的关系。
±s表示,组间比较用SAS软件方差分析q检验,并用直线相关分析判定有关指标间的关系。
RESULTS
1 PMN-CL参数水平及血浆MDA浓度:由附表可见,NIDDM伴发HT患者PMN-CL峰值、积分、吞噬指数及血浆MDA水平,较NIDDM组及正常组明显升高(P均<0.01)。且NIDDM组的上述指标较正常对照组亦明显升高(P均<0.01)。
2 血浆SOD和GSHPx活性:由表1可见,与正常对照组相比,NIDDM组及NIDDM伴发HT组的血浆SOD和GSHPx活性均明显降低(P均<0.01)。与NIDDM组相比,NIDDM 伴发HT组的血浆SOD和GSHPx活性其差异却无显著性(P均>0.05)。
, http://www.100md.com
表1 正常对照组、NIDDM组和NIDDM伴发HT组氧化损伤指标及抗氧化酶活性比较 ±s
±s
正常对照组
(n=30)
NIDDM组
(n=70)
NIDDM+HT组
(n=66)
PMN-CL峰值(mV)
275.9±65.2
572.3±106.8*
, http://www.100md.com
974.8±357.7*+
PMN-CL积分(mV.s)
36631±9442
79038±24137*
149368±74761*+
吞噬指数(mV/103PMN)
0.078±0.045
0.213±0.079*
0.298±0.131*+
, http://www.100md.com
MDA(nmol/ml)
3.42±0.29
4.18±0.21*
4.87±0.13*+
SOD(nU/ml)
110.6±9.0
97.2±6.3*
94.4±5.7*
GSHPx(nU/0.1ml)
98.7±10.4
, 百拇医药
89.7±9.2*
88.1±7.3*
注:与正常组相比,*P<0.01;与NIDDM组相比,+P<0.01。
3 NIDDM伴发HT患者PMN-CL峰值与血浆MDA浓度及SOD活性的相关分析:PMN-CL峰值与血浆MDA浓度呈正相关(r=0.7486,Y=159.8X+132.2,P<0.01,n=66),见附图1,与血浆SOD活性呈负相关(r=-0.6471,Y=-2.6X+1127.4,P<0.05,n=66),见附图2。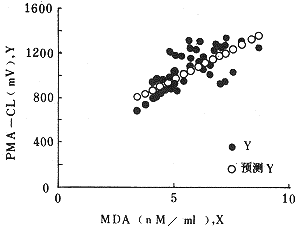
图1 PMN-CL峰值与MDA浓度关系
Fig 1 Correlation between PMN-CL peak value and MDA concentration
, http://www.100md.com
图2 PMN-CL峰值与SOD活性关系
Fig 2 Correlation between PMN-CL peak value and activity of SOD
DISCUSSION
NIDDM患者的血管内皮功能异常是其主要的特征之一,并且为糖尿病血管并发症的主要原因,异常的血管内皮细胞,表现出合成血管舒张因子减少和释放缩血管因子及促凝因子增加,从而促进HT和动脉硬化的发生[5]。但导致动脉内皮细胞诸多功能改变的始动因素却不甚明了。Tsao PS等在鼠的动物实验中发现,糖尿病伴发HT时,血管内皮吸附血中单核细胞的能力明显增强,该特点与血中过氧化产物增多及单核细胞的趋化蛋白-1的过度表达有关[6]。Napoli C等认为糖尿病时发生的糖基化LDL诱发氧自由基(OFR)的生成增多,进而对LDL进行氧化修饰,并降低乙酰水解酶的活性,从而加速糖尿病伴发HT和动脉硬化进程[7]。
, 百拇医药
本研究显示NIDDM及其伴发HT患者较健康对照组的PMN-CL各参数、血浆MDA浓度均明显升高,且NIDDM伴发HT组较NIDDM组的上述指标仍明显升高;血浆SOD及GSHPx活性在NIDDM及其伴发HT组均明显降低,而该两组之间比较,其差异无显著性。PMN-CL参数升高表明PMN吞噬功能加强,并使OFR产生增加[8]。研究表明,NIDDM患者体内OFR水平升高,抗氧化能力下降,故使氧化损伤业已存在;而NIDDM伴发HT患者,尽管抗氧化能力较NIDDM患者无明显下降,但由于OFR的进一步增加,故比后者更易遭受氧化损伤,其结果可能导致内皮细胞的前列环素及NO的活性下降,使外周血管阻力增加,进而血压升高;另外,血浆MDA的进一步升高,表明体内过氧化脂质增多,加速动脉硬化的进程。因此,我们认为氧化损伤参与了NIDDM患者伴发HT的过程,并可能具有病因学意义;提示有效的抗氧化治疗,对于防止或延缓NIDDM血管并发症或有裨益。
REFERENCES
, 百拇医药
1 Giugliano D,Ceriello A,Paolisso G,et al.Diabetes mellitus,hypertension,and cardiovascular disease:which role for oxidative stress?[J] Melabolism 1995;44(3):363-8
2 Heygate KM,Lawrence IG,Bennett MA,et al.Impaired endothelium-dependent relaxation in isolated resistance arteries of spontaneously diabetic rats[J] Br J Pharmacol 1995;116(8):3251-9
3 Pieper GM,Langenstroer P,Gross GJ.Hydroxyl radicals mediate injury to endothelium-dependent relaxation in diabetes rat[J] Mol Cell Biochem 1993;26;122(2):139-45
, 百拇医药
4 Van Dyke K.Cellular chemiluminescence[M] .Vol 1.Boca Raton,CRC Press 1987,3-22
5 Tribe RM,Poston L.Oxidative stress and lipids in diabetes: a role in endothelium vasodilator dysfuntion?[J] Vasc Med 1996;1(3):195-206
6 Tsao PS,Niebeauer J,Buitrago R,et al.Interaction of diabetes and hypertension on determinants of endothelial adhesiveness[J] Arterioscler Thromb Vasc Biol 1998;18(6):947-53
7 Napoli C,Triggiani M,Palumbo G,et al.Glycosylation enhances oxygen radical-induced modifications and decreases acetylhydrolase activity of human low density lipoprotein[J] Basic Res Cardiol 1997;92(2):96-105
8 Delamaire M,Maugendre D,Moreno M,et al.Impaired leucocyte functions in diabetes patients[J] Diabet Med 1997;14(1):29-34
收稿日期:1999-01-10, http://www.100md.com
单位:安徽医科大学附属医院心内科 230022
关键词:非胰岛素依赖型糖尿病;高血压;氧化损伤
高血压杂志990312
目的:评价氧化损伤及抗氧化酶活性对Ⅱ型糖尿病(NIDDM)及其伴发高血压(HT)的影响。方法与结果:采用鲁米诺依赖的中性粒细胞化学发光法,对136例NIDDM患者(其中 70例不伴有HT,66例伴有HT)及30例年龄匹配的健康对照者,检测其外周血中性粒细胞产生氧自由基(OFR)的水平。采用化学定量法,测定其血浆脂质过氧化终末产物-丙二醛(MDA)的浓度及抗氧化酶-超氧化物歧化酶(SOD)、谷胱甘肽过氧化物酶(GSHPx)的活性。NIDDM伴发HT组,其PMN-CL 峰值、积分和吞噬指数均明显高于NIDDM不伴HT组及健康对照组;血浆MDA浓度较后两组也明显升高(P均<0.01); NIDDM组及NIDDM伴发HT组的血浆SOD和GSHPx活性较正常对照组均明显降低(P均<0.01);但与NIDDM组相比,NIDDM伴发HT组的血浆SOD和GSHPx活性其差异无显著性(P均>0.05);PMN-CL峰值与MDA呈明显正相关(r=0.7486,Y=159.8X+132.2,P<0.01,n=66),与SOD活性呈明显负相关(r=-0.6471,Y=-2.6X+1127.4,P<0.05,n=66)。结论:NIDDM患者体内已存在着氧化损伤,而在NIDDM伴发 HT时氧化损伤进一步加重,提示氧化损伤对NIDDM患者HT的发生发展可能有着病因学意义。
, 百拇医药
要点:NIDDM及NIDDM合并高血压患者血浆MDA增加,SOD和GSHPx活性降低。多形核白细胞氧自由基产生增加,这种氧化损伤在NIDDM及其合并高血压的发生和发展上有意义。
中图分类号:R587.1;R544.1;R331.1;Q505 文献标识码:A
文章编号:1006-2866(1999)02-0228-02
Oxidative Stress Is Present in NIDDM and Further Enchaned by Hypertension
LIU Hejun,WANG Taiping,LI Qin,SHI Xungong
(Cardiovascular Department of Affiliated Hospital of Anhui Medical Univeresity,Hefei,230022)
, 百拇医药
ABSTRACT Aim:Oxidative stress is believed to play an important role in the development of hypertension associates with diabetes mellitus in animal models.To test this hypothesis in humans,we determined to evaluate the markers of polymorphonuclear leukocyte oxygen free radical( OFR)production,lipid peroxidation and defenses against oxidative stress in NIDDM patients with and without hypertension.Methods and Results:A convenient and senstive method for estimation of neutrophil OFR production was assayed by polymorphonuclear leukocyte chemiluminescence(PMN-CL).We have measured the parameters of PMN-CL,the plasma malondialdehyde(MDA) concentration,the plasma activities of superoxide dismutase(SOD) and glulathione peroxidase(GSHPx) in 136 NIDDM patients( 70 without hypertension and 66 with hypertension) and 30 age-matched healthy subjects.Patients with hypertension showed significantly increased PMN-CL parameters as peak value(974.8±357.7 mV),integration(149368±74761 mV.s) ,and phagocytic index(0.298±0.131 mV.mm-3) compared to diabetics without hypertension(572.3±106.8 mV,79038±24137 mV and 0.213±0.079 mV.mm-3 ) and healthy controls(275.9±65.2 mV,36631±9442 mV.s,and 0.078±0.045 mV.mm-3).(P<0.01,respectively).The plasma MDA concentration(4.87±0.13 nmol.ml-1) increased in patients with hypertension compared with that in diabetics without hypertension(4.18±0.21 nmol.ml-1) and healthy controls(3.42±0.29 nmol.ml-1),(P<0.01,respectively).The PMN-CL peak value correlated best with plasma MDA concentration (r=0.7486,P<0.01,n=66) and negatively correlated with the plasma activity of SOD (r=-0.6471,P<0.05,n=66).Conclusion:These data confirm that the oxidative stress was significant in NIDDM patients and was enchaned in diabetic patients with hypertension.
, http://www.100md.com
Key Words: non-insulin dependent diabetes mellitus(NIDDM); hypertension; oxidative stress
糖尿病和高血压是相互关联的疾病,是动脉硬化的独立危险因素,两病合并时会加速心血管病、脑卒中、肾病及视网膜病变的发生及进展[1]。动物实验业已表明,氧化损伤对糖尿病引发高血压起着重要作用[2,3],但在人体的研究,目前尚鲜见报道。本文采用鲁米诺(Luminol,化学名为氨基苯二酰一肼)依赖的中性粒细胞化学发光(Polymorphonuclear chemiluminescence,PMN-CL)法[4],对伴或不伴高血压(HT)的Ⅱ型糖尿病(NIDDM)患者外周血中性粒细胞产生的氧自由基( OFR)水平进行检测,采用化学定量法对血浆过氧化脂质终末产物-丙二醛(MDA) 浓度及抗氧化酶活性进行检测,旨在评价氧化损伤及抗氧化酶活性对NIDDM及其伴发HT的影响。
, 百拇医药
MATERIALS AND METHODS
1 对象
1.1 正常对照组:体检身体健康者30例,其中男性21例,女性9例,年龄55.0±9.5岁。
1.2 NIDDM组:70例,根据1990年WHO暂行标准作出诊断,其中男性49例,女性21例,年龄57.5±12.8岁。
1.3 NIDDM伴发HT组:66例,NIDDM诊断标准同上,HT诊断按1978年WHO标准,HT发生于罹患NIDDM之后,其中男性46例,女性20例,年龄59.7±14.2岁。
所有检测对象在检测前2周内均未服用自由基清除剂或抗氧化剂,并除外感染现象。
2 方法:
, 百拇医药
2.1 采血:抽取静脉血(肝素抗凝)2毫升,取 0.1 毫升用于检测中性粒细胞化学发光(PMN-CL)各参数,余下血样行2 000转/分钟离心10分钟,取出血浆用于测定MDA,SOD,GSHPx。
2.2 PMN-CL参数检测:取肝素抗凝的静脉血0.1 ml,加入0.7 ml pH值为7.8的 Hank's液中,在37℃孵育20分钟,加浓度为1×10-3mol/L的鲁米诺液(Luminol,Sigma产品)0.1 ml,再孵育15 min,上机检测本底值,加2.5 g/L酵母多糖(Zymosan A,Sigma产品)0.1 ml,每150 s测量1次,每次测量时间为6 s,共测20次。测量仪器为SHG-1型生物化学发光仪,自动温控在37±0.5℃,最后得出每例的峰值、积分。并测算出每例的吞噬指数(峰值/PMN数/103),反映单个PMN的吞噬功能。
2.3 血浆MDA,SOD,GSHPx测定:均采用化学法测定,试剂盒由南京建成试剂厂提供,按说明书进行操作。
, http://www.100md.com
3 统计学处理: 所有数据以
 ±s表示,组间比较用SAS软件方差分析q检验,并用直线相关分析判定有关指标间的关系。
±s表示,组间比较用SAS软件方差分析q检验,并用直线相关分析判定有关指标间的关系。RESULTS
1 PMN-CL参数水平及血浆MDA浓度:由附表可见,NIDDM伴发HT患者PMN-CL峰值、积分、吞噬指数及血浆MDA水平,较NIDDM组及正常组明显升高(P均<0.01)。且NIDDM组的上述指标较正常对照组亦明显升高(P均<0.01)。
2 血浆SOD和GSHPx活性:由表1可见,与正常对照组相比,NIDDM组及NIDDM伴发HT组的血浆SOD和GSHPx活性均明显降低(P均<0.01)。与NIDDM组相比,NIDDM 伴发HT组的血浆SOD和GSHPx活性其差异却无显著性(P均>0.05)。
, http://www.100md.com
表1 正常对照组、NIDDM组和NIDDM伴发HT组氧化损伤指标及抗氧化酶活性比较
 ±s
±s正常对照组
(n=30)
NIDDM组
(n=70)
NIDDM+HT组
(n=66)
PMN-CL峰值(mV)
275.9±65.2
572.3±106.8*
, http://www.100md.com
974.8±357.7*+
PMN-CL积分(mV.s)
36631±9442
79038±24137*
149368±74761*+
吞噬指数(mV/103PMN)
0.078±0.045
0.213±0.079*
0.298±0.131*+
, http://www.100md.com
MDA(nmol/ml)
3.42±0.29
4.18±0.21*
4.87±0.13*+
SOD(nU/ml)
110.6±9.0
97.2±6.3*
94.4±5.7*
GSHPx(nU/0.1ml)
98.7±10.4
, 百拇医药
89.7±9.2*
88.1±7.3*
注:与正常组相比,*P<0.01;与NIDDM组相比,+P<0.01。
3 NIDDM伴发HT患者PMN-CL峰值与血浆MDA浓度及SOD活性的相关分析:PMN-CL峰值与血浆MDA浓度呈正相关(r=0.7486,Y=159.8X+132.2,P<0.01,n=66),见附图1,与血浆SOD活性呈负相关(r=-0.6471,Y=-2.6X+1127.4,P<0.05,n=66),见附图2。

图1 PMN-CL峰值与MDA浓度关系
Fig 1 Correlation between PMN-CL peak value and MDA concentration

, http://www.100md.com
图2 PMN-CL峰值与SOD活性关系
Fig 2 Correlation between PMN-CL peak value and activity of SOD
DISCUSSION
NIDDM患者的血管内皮功能异常是其主要的特征之一,并且为糖尿病血管并发症的主要原因,异常的血管内皮细胞,表现出合成血管舒张因子减少和释放缩血管因子及促凝因子增加,从而促进HT和动脉硬化的发生[5]。但导致动脉内皮细胞诸多功能改变的始动因素却不甚明了。Tsao PS等在鼠的动物实验中发现,糖尿病伴发HT时,血管内皮吸附血中单核细胞的能力明显增强,该特点与血中过氧化产物增多及单核细胞的趋化蛋白-1的过度表达有关[6]。Napoli C等认为糖尿病时发生的糖基化LDL诱发氧自由基(OFR)的生成增多,进而对LDL进行氧化修饰,并降低乙酰水解酶的活性,从而加速糖尿病伴发HT和动脉硬化进程[7]。
, 百拇医药
本研究显示NIDDM及其伴发HT患者较健康对照组的PMN-CL各参数、血浆MDA浓度均明显升高,且NIDDM伴发HT组较NIDDM组的上述指标仍明显升高;血浆SOD及GSHPx活性在NIDDM及其伴发HT组均明显降低,而该两组之间比较,其差异无显著性。PMN-CL参数升高表明PMN吞噬功能加强,并使OFR产生增加[8]。研究表明,NIDDM患者体内OFR水平升高,抗氧化能力下降,故使氧化损伤业已存在;而NIDDM伴发HT患者,尽管抗氧化能力较NIDDM患者无明显下降,但由于OFR的进一步增加,故比后者更易遭受氧化损伤,其结果可能导致内皮细胞的前列环素及NO的活性下降,使外周血管阻力增加,进而血压升高;另外,血浆MDA的进一步升高,表明体内过氧化脂质增多,加速动脉硬化的进程。因此,我们认为氧化损伤参与了NIDDM患者伴发HT的过程,并可能具有病因学意义;提示有效的抗氧化治疗,对于防止或延缓NIDDM血管并发症或有裨益。
REFERENCES
, 百拇医药
1 Giugliano D,Ceriello A,Paolisso G,et al.Diabetes mellitus,hypertension,and cardiovascular disease:which role for oxidative stress?[J] Melabolism 1995;44(3):363-8
2 Heygate KM,Lawrence IG,Bennett MA,et al.Impaired endothelium-dependent relaxation in isolated resistance arteries of spontaneously diabetic rats[J] Br J Pharmacol 1995;116(8):3251-9
3 Pieper GM,Langenstroer P,Gross GJ.Hydroxyl radicals mediate injury to endothelium-dependent relaxation in diabetes rat[J] Mol Cell Biochem 1993;26;122(2):139-45
, 百拇医药
4 Van Dyke K.Cellular chemiluminescence[M] .Vol 1.Boca Raton,CRC Press 1987,3-22
5 Tribe RM,Poston L.Oxidative stress and lipids in diabetes: a role in endothelium vasodilator dysfuntion?[J] Vasc Med 1996;1(3):195-206
6 Tsao PS,Niebeauer J,Buitrago R,et al.Interaction of diabetes and hypertension on determinants of endothelial adhesiveness[J] Arterioscler Thromb Vasc Biol 1998;18(6):947-53
7 Napoli C,Triggiani M,Palumbo G,et al.Glycosylation enhances oxygen radical-induced modifications and decreases acetylhydrolase activity of human low density lipoprotein[J] Basic Res Cardiol 1997;92(2):96-105
8 Delamaire M,Maugendre D,Moreno M,et al.Impaired leucocyte functions in diabetes patients[J] Diabet Med 1997;14(1):29-34
收稿日期:1999-01-10, http://www.100md.com