小杯法测定艾司唑仑片溶出度的实验研究
作者:吴延晖 邵广洲 冯涌
单位:吴延晖 邵广洲 冯涌(中国人民解放军第464医院 天津 300381)
关键词:
药物分析杂志000322 艾司唑仑(Estazolam)又名三唑氯安定,是苯二氮 类衍生物[1],70年代由日本武田药厂创制,临床作为镇静催眠药广泛应用,但在临床应用中疗效不一,有关其质控指标之一的溶出度测定在英国药典1993年版、美国药典Ⅹ 版及中国药典1995年版均未收载。由于艾司唑仑在水中几乎不溶,且每片剂量很小,每片标示量为1 mg,为了进一步控制其质量,按照中国药典小杯法进行了艾司唑仑片的溶出度实验,并且对3个厂家9个批号的产品进行了体外溶出度检查,实验结果表明,该法简便快速,结果准确。
类衍生物[1],70年代由日本武田药厂创制,临床作为镇静催眠药广泛应用,但在临床应用中疗效不一,有关其质控指标之一的溶出度测定在英国药典1993年版、美国药典Ⅹ 版及中国药典1995年版均未收载。由于艾司唑仑在水中几乎不溶,且每片剂量很小,每片标示量为1 mg,为了进一步控制其质量,按照中国药典小杯法进行了艾司唑仑片的溶出度实验,并且对3个厂家9个批号的产品进行了体外溶出度检查,实验结果表明,该法简便快速,结果准确。
, 百拇医药
1 仪器与试药
ZRS-4智能溶出仪,小杯法装置(天津大学无线电厂);岛津UV-2201紫外分光光度计。
艾司唑仑片每片1 mg;天津A药厂,批号:981001(A1);981101(A2);981203(A3);湖北B药厂,批号:980407(B1);980701(B2);980804(B3);981001(B4);北京C药厂,批号:980701(C1);980702(C2)。
37%盐酸(天津市化学试剂三厂)。
2 含量测定[2]
取本品30片,精密称定,研细,精密称取适量(约相当于艾司唑仑10 mg),置100 mL量瓶中,加盐酸溶液(9→1 000)(以下简称盐酸溶液)60 mL,充分振摇,使艾司唑仑溶解,用盐酸溶液稀释至刻度,摇匀,滤过;弃去初滤液,精密量取续滤液5 mL,置50 mL量瓶中,用盐酸溶液稀释至刻度,摇匀,照分光光度法(附录ⅥA),在(271±2) nm的波长处测定吸收度,按C16H11ClN4的吸收系数E1%1cm为358计算即得。计算结果见表1。
, 百拇医药
表1 艾司唑仑片含量测定结果 样品
平均片重/g
标示量 %
A1
0.05740
92.13
A2
0.06105
98.89
A3
0.06141
102.3
, 百拇医药 B1
0.08124
90.66
B2
0.08418
92.64
B3
0.08273
99.06
B4
0.07898
92.19
C1
, 百拇医药
0.06819
94.88
C2
0.06654
92.40
3 溶出度测定
3.1 溶剂的选择 根据艾司唑仑溶解特性,进行了5种不同的pH缓冲液的筛选[3],并考虑到中国药典95版含量均匀度、含量测定均以盐酸溶液为溶剂,按C16H11ClN4的吸收系数(E1%1cm)为358计算,故认为本品溶出度的测定以盐酸溶液为溶出溶剂[4]。
3.2 溶出转速的选择 以脱气后的盐酸溶液250 mL为溶出溶剂,转速分别选择50,60,75 r.min-1进行实验,每一操作容器内投1片,经30 min取样,在271 nm波长处测定吸收度,并同时以盐酸溶液为空白,计算出溶出量,结果表明:50 r.min-1溶出速率较慢、溶出量偏低;而75 r.min-1溶出速率较快、溶出量偏高,故转速选择为60 r.min-1。
, http://www.100md.com
4 方法的确定
4.1 溶出曲线 用选定的溶出溶剂分别对B4批号的艾司唑仑片进行5次30个数据的实验,考核该产品溶出均一性,绘制溶出曲线(见图1)。取艾司唑仑片按照溶出度测定法(中国药典95版附录66页第三法)以脱气后的盐酸溶液250 mL为溶剂,每一操作容器内投入1片,60 r.min-1,分别在15,30,45,60 min时取样3 mL,以滤纸过滤,取续滤液照分光光度法(中国药典95版附录18页Ⅳ法)271 nm处测吸收度计算出溶出量,结果见表2。
4.2 样品测定 根据以上实验结果,取本品1片,照溶出度测定法(中国药典95版二部附录66页第三法)以脱气后的盐酸溶液250 mL为溶剂,转速为60 r.min-1,经20 min时取样,其他操作同前测定方法,对3个厂家的9个批号的样品进行检验,按C16H11ClN4的吸收系数(E1%1cm)为358计算出每片的溶出量,限度为标示量的75%。结果见表3。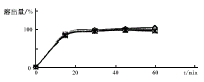
, http://www.100md.com
图1 B4艾司唑仑片溶出度曲线
表2 艾司唑仑片溶出曲线结果(%)
溶出时间/min
15
30
45
60
1
85.78
94.91
95.90
92.88
, 百拇医药 2
82.81
94.04
97.30
93.58
3
87.93
96.26
99.05
99.39
4
86.30
95.09
, http://www.100md.com
96.72
96.95
5
88.11
97.54
100.7
103.1
X/%
86.19
95.57
97.93
97.18
RSD/%
, 百拇医药
2.48
1.42
1.97
4.35
表3 9批样品30 min溶出结果(%) 批号
溶出量
RSD
最大值
最小值
平均值
/%
A1
94.79
, http://www.100md.com
88.32
91.10
2.62
A2
98.46
88.28
93.46
3.92
A3
97.37
91.80
93.98
2.37
, 百拇医药
B1
99.86
84.13
92.00
6.28
B2
98.53
84.72
89.89
5.60
B3
91.48
78.55
, http://www.100md.com
87.18
5.37
B4
98.78
88.69
93.84
4.86
C1
68.44
57.18
64.95
4.86
C2
, 百拇医药
61.45
51.16
55.24
6.51
5 数据处理
提取参数:根据威布尔分布建立了溶出百分率与时间的函数关系,从中提取T50(释放50%所需时间),Td(释放63.2%所需时间),m(释放曲线形状参数,即曲线斜率)3个参数,结果见表4。
表4 9个不同批号样品溶出参数(n=6) 批号
T50/min
Td/min
, 百拇医药
m
A1
15.63
20.88
1.264
A2
9.43
13.51
1.017
A3
5.80
9.60
0.726
, http://www.100md.com
B1
8.88
11.30
1.514
B2
4.50
8.08
0.625
B3
9.97
14.76
0.934
B4
, 百拇医药
2.80
5.72
0.512
C1
33.17
44.03
1.293
C2
36.01
49.38
1.159
6 讨论
6.1 本实验9批样品其含量均在标示量90%~110%范围之内,崩解时限均未超过15 min,均匀度检查均符合中国药典95版规定。
, http://www.100md.com
6.2 对溶出参数Td、T50和m的方差分析结果表明,不同厂家及同一厂家不同批号之间的艾司唑仑片的溶出度及Td、T50和m均有显著差异,这可能是造成临床疗效不一的原因之一,艾司唑仑片有必要作溶出度检查,以控制其质量。
6.3 实验中所用滤纸对本品有一定的吸附作用,所以取样前应至少用10 mL样品溶出液充分饱和,此时的吸收值保持恒定。
6.4 艾司唑仑为几乎不溶于水的药物,通过试验表明,拟定的溶出度测定法能有效地控制产品质量,建议今后药典中在制定艾司唑仑及其同类精神药的溶出度限度以20 min时溶出的百分率不低于标示量的75%,以此来控制产品质量,保证临床疗效。
6.5 从北京C药厂复核数据分析,该厂产品由于压片工艺等原因,溶出度明显低于A、B药厂,说明该方法是可以反映和控制质量情况的。
, 百拇医药
冯涌:天津医科大学药学院毕业实习生
参考文献
1,竺心影.药理学.第三版,北京:人民卫生出版社,1995.138
2,中国药典.1995.二部:88
3,袁和亮.杨鹏晖,李光平等.米非司酮片溶出速率的研究.中国药科大学学报,1993,24(3):212
4,左志辉.卡比马唑片溶出度方法的选择.天津药学,1994,6(4):52
(本文于1999年7月12日收到), 百拇医药
单位:吴延晖 邵广洲 冯涌(中国人民解放军第464医院 天津 300381)
关键词:
药物分析杂志000322 艾司唑仑(Estazolam)又名三唑氯安定,是苯二氮
 类衍生物[1],70年代由日本武田药厂创制,临床作为镇静催眠药广泛应用,但在临床应用中疗效不一,有关其质控指标之一的溶出度测定在英国药典1993年版、美国药典Ⅹ 版及中国药典1995年版均未收载。由于艾司唑仑在水中几乎不溶,且每片剂量很小,每片标示量为1 mg,为了进一步控制其质量,按照中国药典小杯法进行了艾司唑仑片的溶出度实验,并且对3个厂家9个批号的产品进行了体外溶出度检查,实验结果表明,该法简便快速,结果准确。
类衍生物[1],70年代由日本武田药厂创制,临床作为镇静催眠药广泛应用,但在临床应用中疗效不一,有关其质控指标之一的溶出度测定在英国药典1993年版、美国药典Ⅹ 版及中国药典1995年版均未收载。由于艾司唑仑在水中几乎不溶,且每片剂量很小,每片标示量为1 mg,为了进一步控制其质量,按照中国药典小杯法进行了艾司唑仑片的溶出度实验,并且对3个厂家9个批号的产品进行了体外溶出度检查,实验结果表明,该法简便快速,结果准确。, 百拇医药
1 仪器与试药
ZRS-4智能溶出仪,小杯法装置(天津大学无线电厂);岛津UV-2201紫外分光光度计。
艾司唑仑片每片1 mg;天津A药厂,批号:981001(A1);981101(A2);981203(A3);湖北B药厂,批号:980407(B1);980701(B2);980804(B3);981001(B4);北京C药厂,批号:980701(C1);980702(C2)。
37%盐酸(天津市化学试剂三厂)。
2 含量测定[2]
取本品30片,精密称定,研细,精密称取适量(约相当于艾司唑仑10 mg),置100 mL量瓶中,加盐酸溶液(9→1 000)(以下简称盐酸溶液)60 mL,充分振摇,使艾司唑仑溶解,用盐酸溶液稀释至刻度,摇匀,滤过;弃去初滤液,精密量取续滤液5 mL,置50 mL量瓶中,用盐酸溶液稀释至刻度,摇匀,照分光光度法(附录ⅥA),在(271±2) nm的波长处测定吸收度,按C16H11ClN4的吸收系数E1%1cm为358计算即得。计算结果见表1。
, 百拇医药
表1 艾司唑仑片含量测定结果 样品
平均片重/g
标示量 %
A1
0.05740
92.13
A2
0.06105
98.89
A3
0.06141
102.3
, 百拇医药 B1
0.08124
90.66
B2
0.08418
92.64
B3
0.08273
99.06
B4
0.07898
92.19
C1
, 百拇医药
0.06819
94.88
C2
0.06654
92.40
3 溶出度测定
3.1 溶剂的选择 根据艾司唑仑溶解特性,进行了5种不同的pH缓冲液的筛选[3],并考虑到中国药典95版含量均匀度、含量测定均以盐酸溶液为溶剂,按C16H11ClN4的吸收系数(E1%1cm)为358计算,故认为本品溶出度的测定以盐酸溶液为溶出溶剂[4]。
3.2 溶出转速的选择 以脱气后的盐酸溶液250 mL为溶出溶剂,转速分别选择50,60,75 r.min-1进行实验,每一操作容器内投1片,经30 min取样,在271 nm波长处测定吸收度,并同时以盐酸溶液为空白,计算出溶出量,结果表明:50 r.min-1溶出速率较慢、溶出量偏低;而75 r.min-1溶出速率较快、溶出量偏高,故转速选择为60 r.min-1。
, http://www.100md.com
4 方法的确定
4.1 溶出曲线 用选定的溶出溶剂分别对B4批号的艾司唑仑片进行5次30个数据的实验,考核该产品溶出均一性,绘制溶出曲线(见图1)。取艾司唑仑片按照溶出度测定法(中国药典95版附录66页第三法)以脱气后的盐酸溶液250 mL为溶剂,每一操作容器内投入1片,60 r.min-1,分别在15,30,45,60 min时取样3 mL,以滤纸过滤,取续滤液照分光光度法(中国药典95版附录18页Ⅳ法)271 nm处测吸收度计算出溶出量,结果见表2。
4.2 样品测定 根据以上实验结果,取本品1片,照溶出度测定法(中国药典95版二部附录66页第三法)以脱气后的盐酸溶液250 mL为溶剂,转速为60 r.min-1,经20 min时取样,其他操作同前测定方法,对3个厂家的9个批号的样品进行检验,按C16H11ClN4的吸收系数(E1%1cm)为358计算出每片的溶出量,限度为标示量的75%。结果见表3。

, http://www.100md.com
图1 B4艾司唑仑片溶出度曲线
表2 艾司唑仑片溶出曲线结果(%)
溶出时间/min
15
30
45
60
1
85.78
94.91
95.90
92.88
, 百拇医药 2
82.81
94.04
97.30
93.58
3
87.93
96.26
99.05
99.39
4
86.30
95.09
, http://www.100md.com
96.72
96.95
5
88.11
97.54
100.7
103.1
X/%
86.19
95.57
97.93
97.18
RSD/%
, 百拇医药
2.48
1.42
1.97
4.35
表3 9批样品30 min溶出结果(%) 批号
溶出量
RSD
最大值
最小值
平均值
/%
A1
94.79
, http://www.100md.com
88.32
91.10
2.62
A2
98.46
88.28
93.46
3.92
A3
97.37
91.80
93.98
2.37
, 百拇医药
B1
99.86
84.13
92.00
6.28
B2
98.53
84.72
89.89
5.60
B3
91.48
78.55
, http://www.100md.com
87.18
5.37
B4
98.78
88.69
93.84
4.86
C1
68.44
57.18
64.95
4.86
C2
, 百拇医药
61.45
51.16
55.24
6.51
5 数据处理
提取参数:根据威布尔分布建立了溶出百分率与时间的函数关系,从中提取T50(释放50%所需时间),Td(释放63.2%所需时间),m(释放曲线形状参数,即曲线斜率)3个参数,结果见表4。
表4 9个不同批号样品溶出参数(n=6) 批号
T50/min
Td/min
, 百拇医药
m
A1
15.63
20.88
1.264
A2
9.43
13.51
1.017
A3
5.80
9.60
0.726
, http://www.100md.com
B1
8.88
11.30
1.514
B2
4.50
8.08
0.625
B3
9.97
14.76
0.934
B4
, 百拇医药
2.80
5.72
0.512
C1
33.17
44.03
1.293
C2
36.01
49.38
1.159
6 讨论
6.1 本实验9批样品其含量均在标示量90%~110%范围之内,崩解时限均未超过15 min,均匀度检查均符合中国药典95版规定。
, http://www.100md.com
6.2 对溶出参数Td、T50和m的方差分析结果表明,不同厂家及同一厂家不同批号之间的艾司唑仑片的溶出度及Td、T50和m均有显著差异,这可能是造成临床疗效不一的原因之一,艾司唑仑片有必要作溶出度检查,以控制其质量。
6.3 实验中所用滤纸对本品有一定的吸附作用,所以取样前应至少用10 mL样品溶出液充分饱和,此时的吸收值保持恒定。
6.4 艾司唑仑为几乎不溶于水的药物,通过试验表明,拟定的溶出度测定法能有效地控制产品质量,建议今后药典中在制定艾司唑仑及其同类精神药的溶出度限度以20 min时溶出的百分率不低于标示量的75%,以此来控制产品质量,保证临床疗效。
6.5 从北京C药厂复核数据分析,该厂产品由于压片工艺等原因,溶出度明显低于A、B药厂,说明该方法是可以反映和控制质量情况的。
, 百拇医药
冯涌:天津医科大学药学院毕业实习生
参考文献
1,竺心影.药理学.第三版,北京:人民卫生出版社,1995.138
2,中国药典.1995.二部:88
3,袁和亮.杨鹏晖,李光平等.米非司酮片溶出速率的研究.中国药科大学学报,1993,24(3):212
4,左志辉.卡比马唑片溶出度方法的选择.天津药学,1994,6(4):52
(本文于1999年7月12日收到), 百拇医药